Страница:
Со способностью к образованию самостоятельных минералов отчасти связаны наши обыденные представления о редкости или распространенности элементов. Эти представления часто не соответствуют фактическому соотношению кларков. Содержание галлия в земной коре в 300 раз больше, чем ртути. Но минералы галлия очень редки, а главный минерал ртути – киноварь – встречается во многих местах. Люди давно обратили на него внимание и научились извлекать из него всем хорошо известную металлическую ртуть.
Имея в виду силикатный состав земной коры, ее часто сравнивают со шлаком, который образуется при плавке руды. Эта аналогия очень условна. Земная кора не просто легкая силикатная масса, отделившаяся от более тяжелых компонентов при расплавлении. В отличие от шлака, земная кора имеет кристаллическое строение. Основная масса (более 80 %) твердой оболочки Земли сложена силикатами главных элементов: алюминия, железа, кальция, магния, калия и натрия. Примерно 12 % массы коры составляет кварц (SiO2). Силикатный состав и кристаллическое строение вещества земной коры играют особую роль в дифференциации элементов с малыми кларками. При этом сказываются уже не особенности строения ядер, а электронных оболочек атомов.
Образование любых соединений, в том числе минералов, определенным образом регламентируется химическими свойствами элементов, из которых образуются эти соединения. Химические же свойства элементов обусловлены строением их электронных оболочек (энергетических уровней), главным образом внешней. Как известно, у атома на внешнем уровне может быть от одного до восьми электронов. Атомы всех элементов, кроме благородных газов, имеют незавершенные уровни и стремятся к их завершению. Это и осуществляется при образовании химических соединений. Имеется несколько типов химической связи. В минералах, из которых состоит земная кора, наиболее распространены сложные комбинации ионной и ковалентной связи.
Строение энергетических уровней определяет не только химические свойства элементов, но и размер их атомов. Вокруг ядра имеется объем, внутрь которого другой атом не может проникнуть при химической реакции. Объем оценивается величиной радиуса, измеряемого нанометрами – миллиардными долями метра (10-9 м).
Подавляющая часть массы земной коры имеет кристаллическое строение. Кристаллы состоят из бесконечно повторяющихся в определенном порядке атомов или ионов. Хотя связь химических элементов в породообразующих минералах сложная, ковалентно-ионная, известный норвежский геохимик В.М. Гольдшмидт предложил эту связь рассматривать как чисто ионную. Согласно концепции этого ученого, в кристаллохимических структурах ионы ведут себя как жесткие сферы (твердые шары). Поэтому радиус каждого конкретного иона рассматривается как постоянная величина.
Главная особенность ионов в кристаллохимических структурах заключается в том, что радиусы отрицательно заряженных ионов (анионов) значительно больше радиусов положительно заряженных ионов (катионов). Представим себе анионы в виде крупных шаров, а катионы – в виде мелких. Тогда моделью кристаллического вещества с ионным типом связи будет пространство, заполненное плотно прилегающими большими шарами – анионами, между которыми должны размещаться мелкие шарики – катионы. Поразительная картина обнаруживается при пересчете химического состава земной коры на атомные объемы, исходя из взглядов Гольдшмидта о ионных радиусах: ионы кислорода занимают более 91 % объема. Земная кора оказывается состоящей из сплошного каркаса анионов кислорода, в пустотах которого располагаются мелкие катионы кремния и других элементов. По представлениям Гольдшмидта, этот каркас играет роль своеобразного геохимического фильтра, способствующего дифференциации химических элементов по величине их ионов.
То обстоятельство, что породообразующие минералы состоят из ограниченного количества химических элементов, не означает простоты их кристаллохимического строения. Структуры силикатов очень разнообразны. Их основу составляют группировки из четырех анионов кислорода, окружающих катион кремния. Четыре отрицательные валентности такого кремнекислородного тетраэдра уравновешиваются дополнительными катионами или используются для комбинирования в кольца, цепочки, ленты, слои и трехмерные группы. Катионы, уравновешивающие отрицательный заряд этих групп, имеют вполне определенную величину радиуса. Следовательно, если существует конкретная кристаллохимическая структура, то в нее могут войти не любые элементы, а лишь те, ионы которых имеют соответствующую величину радиуса.
Образование распространенных минералов сопровождается: своего рода сортировкой рассеянных элементов. Для пояснения этого процесса обратимся к распространенному минералу – полевому шпату. Его кристаллохимическая структура образована группировками, состоящими из трех катионов кремния и одного алюминия, каждый из которых связан с четырьмя анионами кислорода. Группировка в целом представляет собой комплексный анион, который имеет восемь ионов кислорода, три – кремния и один – алюминия. Это создает один отрицательный заряд, который уравновешивается одновалентным катионом калия. В итоге существует трехмерная структура, состав которой отвечает формуле: К[АlSi308]. Величина радиуса иона калия составляет 0,133 нм. Его место в структуре может занять только катион с близкой величиной радиуса. Таковым является двухвалентный катион бария, радиус которого равен 0,134 нм. Барий значительно менее распространен, чем калий. Обычно он присутствует в виде незначительной примеси в полевых шпатах. Только в особых случаях создается его значительная концентрация и образуется редкий минерал цельзиан (бариевый полевой шпат), имеющий формулу Ba[Al2Si208]. Подчеркнем, что главное условие вхождения бария в структуру полевых шпатов – величина ионного: радиуса, а не валентность.
Аналогичным образом в распространенных минералах и горных породах избирательно задерживаются химические элементы, концентрация которых не так велика, чтобы они могли образовывать самостоятельные минералы. Взаимное замещение ионов в кристаллической структуре благодаря близости их радиусов называется изоморфизмом. Это явление было установлено еще в начале прошлого века, но его значение для глобальной дифференциации рассеянных химических элементов получило оценку только в текущем столетии.
Различные химические свойства элементов с низкими кларками, неодинаковая их способность к образованию минералов и непостоянное содержание позволяют заключить, что в земной коре имеются различные формы нахождения рассеянных элементов.
Относительно грубодисперсные проявления рассеяния характеризуются микрообразованиями химических соединений рассеянных элементов. К ним относятся мельчайшие включения акцессорных минералов, содержащиеся в таком незначительном количестве, что не оказывают влияния ни на состав, ни на свойства горных пород. В такой форме часто присутствуют циркон Zr[Si04], рутил ТiO2, апатит Са5[РО4]3F хромит Fe[Cr204], присутствие которых обусловливает примесь соответственно циркония, титана, фосфора, фтора, хрома. В некоторых минералах находятся соединения, обособившиеся от основной массы при понижении температуры (так называемые структуры распада твердого раствора). Примером служит эмульсионная вкрапленность халькопирита (CuFeS2) и станнина (Cu2FeSnS4) в сфалерите (ZnS), мелкие выделения минералов серебра в галените (PbS). Часть элементов-примесей содержится в маточных растворах, сохранившихся в микропустотах минералов.
Проявление рассеяния на наиболее высокодисперсном, атомарном уровне фиксируется в виде перераспределения изолированных атомов и ионов. Если величина их радиусов соответствует параметрам кристаллохимической структуры породообразующих минералов, то атомы могут войти в структуры по законам изоморфизма, как это рассмотрено выше. Наряду с этим в минералах постоянно присутствуют элементы-примеси, не имеющие никакой связи с изоморфизмом. Установлено, что в кварце постоянно присутствуют свинец, цинк, некоторые другие металлы. Невозможно предполагать их изоморфное вхождение в структуру кварца, образованную комбинацией ионов кремния и кислорода. В этом случае элементы-примеси частично сорбированы на поверхности ультрамикроскопических трещин и других дефектов реальных кристаллов. Содержание этой формы довольно значительно и достигает 10–20 % общего количества рассеянных металлов, находящихся в породообразующих силикатах. Наконец, небольшое количество атомов беспорядочно рассеяно в кристаллических структурах минералов.
В итоге проведенного обзора можно констатировать следующие формы нахождения рассеянных элементов в кристаллическом веществе земной коры.
Микроминералогические формы – элементы:
• входящие в акцессорные минералы;
• содержащиеся в микроскопических выделениях в результате распада твердых растворов;
• находящиеся во включениях остаточных растворов.
Неминералогические формы – элементы:
• сорбированные поверхностью дефектов реальных кристаллов;
• входящие в структуру минерала-носителя по законам изоморфизма;
• находящиеся в структуре минерала-носителя в неупорядоченном состоянии.
Минералы, которые мы обычно воспринимаем как природные химические соединения, вместе с тем являются носителями рассеянных элементов. По этому поводу В.И. Вернадский указывал, что за элементами, учитываемыми химическими формулами минералов, находятся мириады рассеянных атомов. Земная кора в целом выступает перед нами как глобальный геохимический фильтр, в котором происходила сортировка и перераспределение атомов химических элементов.
Геохимическая неоднородность земной коры
Контрольные вопросы
Задания для самостоятельной работы
Глава II
Кларки Мирового океана
Имея в виду силикатный состав земной коры, ее часто сравнивают со шлаком, который образуется при плавке руды. Эта аналогия очень условна. Земная кора не просто легкая силикатная масса, отделившаяся от более тяжелых компонентов при расплавлении. В отличие от шлака, земная кора имеет кристаллическое строение. Основная масса (более 80 %) твердой оболочки Земли сложена силикатами главных элементов: алюминия, железа, кальция, магния, калия и натрия. Примерно 12 % массы коры составляет кварц (SiO2). Силикатный состав и кристаллическое строение вещества земной коры играют особую роль в дифференциации элементов с малыми кларками. При этом сказываются уже не особенности строения ядер, а электронных оболочек атомов.
Образование любых соединений, в том числе минералов, определенным образом регламентируется химическими свойствами элементов, из которых образуются эти соединения. Химические же свойства элементов обусловлены строением их электронных оболочек (энергетических уровней), главным образом внешней. Как известно, у атома на внешнем уровне может быть от одного до восьми электронов. Атомы всех элементов, кроме благородных газов, имеют незавершенные уровни и стремятся к их завершению. Это и осуществляется при образовании химических соединений. Имеется несколько типов химической связи. В минералах, из которых состоит земная кора, наиболее распространены сложные комбинации ионной и ковалентной связи.
Строение энергетических уровней определяет не только химические свойства элементов, но и размер их атомов. Вокруг ядра имеется объем, внутрь которого другой атом не может проникнуть при химической реакции. Объем оценивается величиной радиуса, измеряемого нанометрами – миллиардными долями метра (10-9 м).
Подавляющая часть массы земной коры имеет кристаллическое строение. Кристаллы состоят из бесконечно повторяющихся в определенном порядке атомов или ионов. Хотя связь химических элементов в породообразующих минералах сложная, ковалентно-ионная, известный норвежский геохимик В.М. Гольдшмидт предложил эту связь рассматривать как чисто ионную. Согласно концепции этого ученого, в кристаллохимических структурах ионы ведут себя как жесткие сферы (твердые шары). Поэтому радиус каждого конкретного иона рассматривается как постоянная величина.
Главная особенность ионов в кристаллохимических структурах заключается в том, что радиусы отрицательно заряженных ионов (анионов) значительно больше радиусов положительно заряженных ионов (катионов). Представим себе анионы в виде крупных шаров, а катионы – в виде мелких. Тогда моделью кристаллического вещества с ионным типом связи будет пространство, заполненное плотно прилегающими большими шарами – анионами, между которыми должны размещаться мелкие шарики – катионы. Поразительная картина обнаруживается при пересчете химического состава земной коры на атомные объемы, исходя из взглядов Гольдшмидта о ионных радиусах: ионы кислорода занимают более 91 % объема. Земная кора оказывается состоящей из сплошного каркаса анионов кислорода, в пустотах которого располагаются мелкие катионы кремния и других элементов. По представлениям Гольдшмидта, этот каркас играет роль своеобразного геохимического фильтра, способствующего дифференциации химических элементов по величине их ионов.
То обстоятельство, что породообразующие минералы состоят из ограниченного количества химических элементов, не означает простоты их кристаллохимического строения. Структуры силикатов очень разнообразны. Их основу составляют группировки из четырех анионов кислорода, окружающих катион кремния. Четыре отрицательные валентности такого кремнекислородного тетраэдра уравновешиваются дополнительными катионами или используются для комбинирования в кольца, цепочки, ленты, слои и трехмерные группы. Катионы, уравновешивающие отрицательный заряд этих групп, имеют вполне определенную величину радиуса. Следовательно, если существует конкретная кристаллохимическая структура, то в нее могут войти не любые элементы, а лишь те, ионы которых имеют соответствующую величину радиуса.
Образование распространенных минералов сопровождается: своего рода сортировкой рассеянных элементов. Для пояснения этого процесса обратимся к распространенному минералу – полевому шпату. Его кристаллохимическая структура образована группировками, состоящими из трех катионов кремния и одного алюминия, каждый из которых связан с четырьмя анионами кислорода. Группировка в целом представляет собой комплексный анион, который имеет восемь ионов кислорода, три – кремния и один – алюминия. Это создает один отрицательный заряд, который уравновешивается одновалентным катионом калия. В итоге существует трехмерная структура, состав которой отвечает формуле: К[АlSi308]. Величина радиуса иона калия составляет 0,133 нм. Его место в структуре может занять только катион с близкой величиной радиуса. Таковым является двухвалентный катион бария, радиус которого равен 0,134 нм. Барий значительно менее распространен, чем калий. Обычно он присутствует в виде незначительной примеси в полевых шпатах. Только в особых случаях создается его значительная концентрация и образуется редкий минерал цельзиан (бариевый полевой шпат), имеющий формулу Ba[Al2Si208]. Подчеркнем, что главное условие вхождения бария в структуру полевых шпатов – величина ионного: радиуса, а не валентность.
Аналогичным образом в распространенных минералах и горных породах избирательно задерживаются химические элементы, концентрация которых не так велика, чтобы они могли образовывать самостоятельные минералы. Взаимное замещение ионов в кристаллической структуре благодаря близости их радиусов называется изоморфизмом. Это явление было установлено еще в начале прошлого века, но его значение для глобальной дифференциации рассеянных химических элементов получило оценку только в текущем столетии.
Различные химические свойства элементов с низкими кларками, неодинаковая их способность к образованию минералов и непостоянное содержание позволяют заключить, что в земной коре имеются различные формы нахождения рассеянных элементов.
Относительно грубодисперсные проявления рассеяния характеризуются микрообразованиями химических соединений рассеянных элементов. К ним относятся мельчайшие включения акцессорных минералов, содержащиеся в таком незначительном количестве, что не оказывают влияния ни на состав, ни на свойства горных пород. В такой форме часто присутствуют циркон Zr[Si04], рутил ТiO2, апатит Са5[РО4]3F хромит Fe[Cr204], присутствие которых обусловливает примесь соответственно циркония, титана, фосфора, фтора, хрома. В некоторых минералах находятся соединения, обособившиеся от основной массы при понижении температуры (так называемые структуры распада твердого раствора). Примером служит эмульсионная вкрапленность халькопирита (CuFeS2) и станнина (Cu2FeSnS4) в сфалерите (ZnS), мелкие выделения минералов серебра в галените (PbS). Часть элементов-примесей содержится в маточных растворах, сохранившихся в микропустотах минералов.
Проявление рассеяния на наиболее высокодисперсном, атомарном уровне фиксируется в виде перераспределения изолированных атомов и ионов. Если величина их радиусов соответствует параметрам кристаллохимической структуры породообразующих минералов, то атомы могут войти в структуры по законам изоморфизма, как это рассмотрено выше. Наряду с этим в минералах постоянно присутствуют элементы-примеси, не имеющие никакой связи с изоморфизмом. Установлено, что в кварце постоянно присутствуют свинец, цинк, некоторые другие металлы. Невозможно предполагать их изоморфное вхождение в структуру кварца, образованную комбинацией ионов кремния и кислорода. В этом случае элементы-примеси частично сорбированы на поверхности ультрамикроскопических трещин и других дефектов реальных кристаллов. Содержание этой формы довольно значительно и достигает 10–20 % общего количества рассеянных металлов, находящихся в породообразующих силикатах. Наконец, небольшое количество атомов беспорядочно рассеяно в кристаллических структурах минералов.
В итоге проведенного обзора можно констатировать следующие формы нахождения рассеянных элементов в кристаллическом веществе земной коры.
Микроминералогические формы – элементы:
• входящие в акцессорные минералы;
• содержащиеся в микроскопических выделениях в результате распада твердых растворов;
• находящиеся во включениях остаточных растворов.
Неминералогические формы – элементы:
• сорбированные поверхностью дефектов реальных кристаллов;
• входящие в структуру минерала-носителя по законам изоморфизма;
• находящиеся в структуре минерала-носителя в неупорядоченном состоянии.
Минералы, которые мы обычно воспринимаем как природные химические соединения, вместе с тем являются носителями рассеянных элементов. По этому поводу В.И. Вернадский указывал, что за элементами, учитываемыми химическими формулами минералов, находятся мириады рассеянных атомов. Земная кора в целом выступает перед нами как глобальный геохимический фильтр, в котором происходила сортировка и перераспределение атомов химических элементов.
Геохимическая неоднородность земной коры
Химические элементы находятся в земной коре в двух главных состояниях. Первое отвечает прочному связыванию атомов в кристаллические структуры с определенным соотношением их образующих химических элементов. Второе состояние характеризуется разреженным, но повсеместным распространением рассеянных атомов в кристаллическом веществе. Важной геохимической особенностью земной коры является то, что, независимо от состояния, распределение химических элементов в пространстве очень непостоянно.
Главные химические элементы образуют минералы, слагающие горные породы. Последние сложено сочетаются в тектонических структурах земной коры. Смена типов горных пород сопровождается изменением концентрации главных элементов. Не менее сильным колебаниям подвержена величина концентрации элементов с низкими кларками. Сочетание всех ранее рассмотренных форм нахождения рассеянных элементов сильно меняется в зависимости от многих факторов. Соответственно меняется суммарное содержание элементов в разных участках земной коры. Поэтому для объективной оценки распределения их концентраций в пространстве необходимы методы математической статистики.
Прежде всего, необходимо выяснить закон распределения содержаний. Как отмечалось выше, большое количество независимых причин вызывает варьирование содержания элемента в разных пробах. Когда распределение величины определяется достаточно большим числом примерно равнодействующих и взаимно независимых причин, то распределение подчиняется так называемому нормальному закону Гаусса. Его графическим выражением является кривая с симметричными ветвями по обе стороны максимальной ординаты. При нормальном распределении наиболее вероятным значением служит среднее арифметическое (х), которое совпадает с наиболее часто встречающимися значениями (модой). Растянутость симметричной кривой по оси абсцисс, т. е. разброс значений в большую и меньшую стороны от моды, характеризуется средним квадратичным отклонением, которое обозначается о.
Нормальное распределение может также проявляться не для численного значения содержания элемента, а для его логарифма. Это называется логарифмически нормальным (логнормальным) законом распределения. В этом случае мода совпадает со средним геометрическим, а разброс значений характеризуется логарифмом о.
В 1940 г. Н.К. Разумовский чисто эмпирически обнаружил, что содержание металлов в рудах соответствует логарифмически нормальному распределению. Л. Х. Аренс в 1954 г., обработав обширный материал, независимо от Разумовского, установил, что распределение рассеянных элементов в магматических породах приближается к логарифмически нормальному закону. Многочисленные факты указывают на то, что распределение элементов с высокими кларками обычно подчиняется нормальному закону, а рассеянных – логнормальному (рис. 4). Этим еще раз подчеркивается принципиальное различие главных и рассеянных элементов.
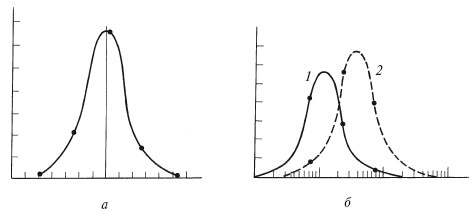
Рис. 4. Распределение концентраций химических элементов:
а – нормальное распределение Al2O3 в ледниковых глинах Норвегии; б – логарифмически-нормальное распределение никеля в четвертичных отложениях Хибин (1) и Мончетундры (2)
Хотя нормальный и логнормальный – наиболее распространенные законы распределения химических элементов в земной коре, встречаются случаи и более сложных функций. Обычно это связано со взаимным наложением нескольких природных процессов.
Среднее содержание химического элемента представляет собой норму, так называемый геохимический фон для данного типа пород в определенном районе. Отклонения от среднего значения в большую сторону указывают на тенденцию к аккумуляции элемента, а в меньшую – на усиление его рассеяния. Используя статистическую обработку массовых аналитических данных, во-первых, можно обнаружить участки повышенных концентраций и ореолы рассеяния месторождений; во-вторых, статистический анализ дает возможность установить закономерные изменения величины геохимического фона в пространстве и выявить геохимические провинции. В пределах этих провинций горные породы одного типа обладают выдержанными статистическими параметрами, в первую очередь величиной среднего содержания одного, или нескольких рассеянных элементов. Однотипные породы разных геохимических провинций могут различаться величиной среднего содержания некоторых рассеянных элементов в несколько раз. При этом химический состав этих пород, определяемый содержанием главных элементов, остается одинаковым или имеет очень слабые отличия. Например, в гранитах разных провинций, имеющих практически одинаковое количество кремния, алюминия, железа, концентрация олова, свинца, молибдена, урана может различаться в 2–3 раза. Это еще раз указывает на принципиальное различие элементов с высокими и низкими кларками.
Кларк – это интегрированная величина, характеризующая общий уровень концентрации элемента. В реальных объектах встречаются постоянные отклонения от этой величины как в сторону меньших, так и больших значений. Аккумуляции некоторых необходимых для промышленности элементов (например, металлов) могут быть такими, что их экономически выгодно и технически возможно разрабатывать. В этом случае мы имеем дело с месторождениями руд.
Способностью создавать очень высокие концентрации на небольших участках обладают только рассеянные элементы. Если максимальная степень концентрации металлов с высоким кларком (более 1 %) может достигать 10–20, то для металлов с низким кларком эта величина обычно составляет несколько сотен или даже тысяч. Степень концентрации рассеянных металлов в рудах промышленных месторождений может быть охарактеризована следующими показателями:
Марганец, медь, цинк, ванадий, ниобий…… n·100
Свинец, никель, литий, олово, вольфрам,
бериллий, уран, хром……………………………….. n·100—1000
Золото, молибден, кобальт……………………….. n·1000—10000
Ртуть, сурьма……………………………………………. n·10000—100000
В месторождениях сосредоточены громадные количества металлов. По состоянию на 1976 г. общемировые запасы руд (без данных для СССР и социалистических стран) составляли (в млн т): меди – 465; цинка – 214; свинца – 135; никеля – 96; молибдена – 8,4; олова– 6,7; кобальта – 4,0; сурьмы – 1,6; ртути – 0,4. В связи с этим возникает вопрос: не сконцентрирована ли основная масса металлов в месторождениях руд?
Чтобы ответить на этот вопрос, необходимо оценить массу этих металлов, находящихся в земной коре или хотя бы в ее верхней части, в «гранитном» слое.
Приведенные в табл. 3 данные свидетельствуют о том, что только в километровом слое верхней части земной коры континентов содержатся такие количества металлов в рассеянном состоянии, по сравнению с которыми их массы, сконцентрированные в месторождениях руд, составляют тысячные доли процента.
Таблица 3
Соотношение масс рассеянных металлов и их рудных концентраций
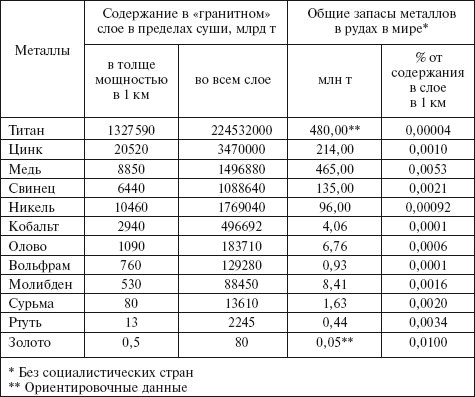
Следовательно, основная масса металлов с низкими кларками находится в рассеянном состоянии, а в месторождениях руд сконцентрирована лишь ничтожно малая часть их массы.
Участки высоких (рудных) концентраций связаны с окружающими горными породами постепенными переходами. Рудные тела находятся как бы в чехле постепенно убывающей концентрации металлов. Такие образования получили название ореолов рассеяния. Первичные, так называемые сингенетические рудные ореолы возникают одновременно с рудными телами и в результате одних и тех же процессов. Они имеют разнообразную конфигурацию в зависимости от геологического строения, состава вмещающих пород и условий рудообразования (рис. 5).
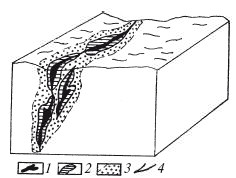
Рис. 5. Эндогенные ореолы рассеяния металлов вокруг рудных тел:
1 – рудные тела; 2 – внутренняя часть ореола с повышенной концентрацией металлов; 3 – наружная часть ореола с ослабленной концентрацией; 4 – тектонические нарушения
В рудах наряду с одним или несколькими главными рудообразующими элементами присутствуют сопутствующие элементы, концентрация которых также повышена, хотя и не так сильно, как главных. Элементы-спутники часто образуют изоморфные замещения главных. Например, в цинковых рудах постоянно содержится кадмий, в меньшем количестве – индий, галлий, германий. В медно-никелевых рудах присутствует значительная примесь кобальта, в меньшем количестве – селена и теллура. Все эти сопутствующие элементы также рассеиваются вокруг рудных тел. Обладая неодинаковой геохимической подвижностью, они образуют переходные зоны разной протяженности. В итоге состав и строение ореолов рассеяния очень сложны.
Изложенный материал свидетельствует о неравномерном распределении рассеянных элементов в земной коре. Поэтому наряду с определением кларков, т. е. величины средней концентрации элементов в земной коре в целом, необходимо учитывать способность их концентрироваться или рассеиваться в различных объектах – разных типах горных пород или в однотипных породах, но находящихся в разных геохимических провинциях, в рудах и пр. Чтобы количественно оценить неоднородность распределения химических элементов в земной коре, В.И. Вернадский ввел специальный показатель – кларк концентрации (Кк). Его величина характеризует отклонение содержания элемента в данном объекте от кларка:
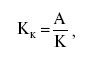
где А – содержание химического элемента в горной породе, руде, минерале и пр., К – кларк этого элемента в земной коре.
Если кларк концентрации больше 1, то это указывает на обогащение элементом, если меньше – означает снижение его содержания по сравнению с данными для земной коры в целом.
Отклонение от нормы (кларка местного геохимического фона), повышенная и пониженная концентрация химических элементов на некоторых участках – не отдельные исключения, а характерная черта геохимии земной коры. Это имеет очень важное значение, так как кора служит основанием, на котором формируются природно-территориальные комплексы. Неодинаковые уровни концентрации рассеянных элементов в разных геохимических провинциях, наличие природных геохимических аномалий с очень высокой концентрацией элементов играли не последнюю роль в формообразовании и эволюции органического мира.
Главные химические элементы образуют минералы, слагающие горные породы. Последние сложено сочетаются в тектонических структурах земной коры. Смена типов горных пород сопровождается изменением концентрации главных элементов. Не менее сильным колебаниям подвержена величина концентрации элементов с низкими кларками. Сочетание всех ранее рассмотренных форм нахождения рассеянных элементов сильно меняется в зависимости от многих факторов. Соответственно меняется суммарное содержание элементов в разных участках земной коры. Поэтому для объективной оценки распределения их концентраций в пространстве необходимы методы математической статистики.
Прежде всего, необходимо выяснить закон распределения содержаний. Как отмечалось выше, большое количество независимых причин вызывает варьирование содержания элемента в разных пробах. Когда распределение величины определяется достаточно большим числом примерно равнодействующих и взаимно независимых причин, то распределение подчиняется так называемому нормальному закону Гаусса. Его графическим выражением является кривая с симметричными ветвями по обе стороны максимальной ординаты. При нормальном распределении наиболее вероятным значением служит среднее арифметическое (х), которое совпадает с наиболее часто встречающимися значениями (модой). Растянутость симметричной кривой по оси абсцисс, т. е. разброс значений в большую и меньшую стороны от моды, характеризуется средним квадратичным отклонением, которое обозначается о.
Нормальное распределение может также проявляться не для численного значения содержания элемента, а для его логарифма. Это называется логарифмически нормальным (логнормальным) законом распределения. В этом случае мода совпадает со средним геометрическим, а разброс значений характеризуется логарифмом о.
В 1940 г. Н.К. Разумовский чисто эмпирически обнаружил, что содержание металлов в рудах соответствует логарифмически нормальному распределению. Л. Х. Аренс в 1954 г., обработав обширный материал, независимо от Разумовского, установил, что распределение рассеянных элементов в магматических породах приближается к логарифмически нормальному закону. Многочисленные факты указывают на то, что распределение элементов с высокими кларками обычно подчиняется нормальному закону, а рассеянных – логнормальному (рис. 4). Этим еще раз подчеркивается принципиальное различие главных и рассеянных элементов.

Рис. 4. Распределение концентраций химических элементов:
а – нормальное распределение Al2O3 в ледниковых глинах Норвегии; б – логарифмически-нормальное распределение никеля в четвертичных отложениях Хибин (1) и Мончетундры (2)
Хотя нормальный и логнормальный – наиболее распространенные законы распределения химических элементов в земной коре, встречаются случаи и более сложных функций. Обычно это связано со взаимным наложением нескольких природных процессов.
Среднее содержание химического элемента представляет собой норму, так называемый геохимический фон для данного типа пород в определенном районе. Отклонения от среднего значения в большую сторону указывают на тенденцию к аккумуляции элемента, а в меньшую – на усиление его рассеяния. Используя статистическую обработку массовых аналитических данных, во-первых, можно обнаружить участки повышенных концентраций и ореолы рассеяния месторождений; во-вторых, статистический анализ дает возможность установить закономерные изменения величины геохимического фона в пространстве и выявить геохимические провинции. В пределах этих провинций горные породы одного типа обладают выдержанными статистическими параметрами, в первую очередь величиной среднего содержания одного, или нескольких рассеянных элементов. Однотипные породы разных геохимических провинций могут различаться величиной среднего содержания некоторых рассеянных элементов в несколько раз. При этом химический состав этих пород, определяемый содержанием главных элементов, остается одинаковым или имеет очень слабые отличия. Например, в гранитах разных провинций, имеющих практически одинаковое количество кремния, алюминия, железа, концентрация олова, свинца, молибдена, урана может различаться в 2–3 раза. Это еще раз указывает на принципиальное различие элементов с высокими и низкими кларками.
Кларк – это интегрированная величина, характеризующая общий уровень концентрации элемента. В реальных объектах встречаются постоянные отклонения от этой величины как в сторону меньших, так и больших значений. Аккумуляции некоторых необходимых для промышленности элементов (например, металлов) могут быть такими, что их экономически выгодно и технически возможно разрабатывать. В этом случае мы имеем дело с месторождениями руд.
Способностью создавать очень высокие концентрации на небольших участках обладают только рассеянные элементы. Если максимальная степень концентрации металлов с высоким кларком (более 1 %) может достигать 10–20, то для металлов с низким кларком эта величина обычно составляет несколько сотен или даже тысяч. Степень концентрации рассеянных металлов в рудах промышленных месторождений может быть охарактеризована следующими показателями:
Марганец, медь, цинк, ванадий, ниобий…… n·100
Свинец, никель, литий, олово, вольфрам,
бериллий, уран, хром……………………………….. n·100—1000
Золото, молибден, кобальт……………………….. n·1000—10000
Ртуть, сурьма……………………………………………. n·10000—100000
В месторождениях сосредоточены громадные количества металлов. По состоянию на 1976 г. общемировые запасы руд (без данных для СССР и социалистических стран) составляли (в млн т): меди – 465; цинка – 214; свинца – 135; никеля – 96; молибдена – 8,4; олова– 6,7; кобальта – 4,0; сурьмы – 1,6; ртути – 0,4. В связи с этим возникает вопрос: не сконцентрирована ли основная масса металлов в месторождениях руд?
Чтобы ответить на этот вопрос, необходимо оценить массу этих металлов, находящихся в земной коре или хотя бы в ее верхней части, в «гранитном» слое.
Приведенные в табл. 3 данные свидетельствуют о том, что только в километровом слое верхней части земной коры континентов содержатся такие количества металлов в рассеянном состоянии, по сравнению с которыми их массы, сконцентрированные в месторождениях руд, составляют тысячные доли процента.
Таблица 3
Соотношение масс рассеянных металлов и их рудных концентраций

Следовательно, основная масса металлов с низкими кларками находится в рассеянном состоянии, а в месторождениях руд сконцентрирована лишь ничтожно малая часть их массы.
Участки высоких (рудных) концентраций связаны с окружающими горными породами постепенными переходами. Рудные тела находятся как бы в чехле постепенно убывающей концентрации металлов. Такие образования получили название ореолов рассеяния. Первичные, так называемые сингенетические рудные ореолы возникают одновременно с рудными телами и в результате одних и тех же процессов. Они имеют разнообразную конфигурацию в зависимости от геологического строения, состава вмещающих пород и условий рудообразования (рис. 5).

Рис. 5. Эндогенные ореолы рассеяния металлов вокруг рудных тел:
1 – рудные тела; 2 – внутренняя часть ореола с повышенной концентрацией металлов; 3 – наружная часть ореола с ослабленной концентрацией; 4 – тектонические нарушения
В рудах наряду с одним или несколькими главными рудообразующими элементами присутствуют сопутствующие элементы, концентрация которых также повышена, хотя и не так сильно, как главных. Элементы-спутники часто образуют изоморфные замещения главных. Например, в цинковых рудах постоянно содержится кадмий, в меньшем количестве – индий, галлий, германий. В медно-никелевых рудах присутствует значительная примесь кобальта, в меньшем количестве – селена и теллура. Все эти сопутствующие элементы также рассеиваются вокруг рудных тел. Обладая неодинаковой геохимической подвижностью, они образуют переходные зоны разной протяженности. В итоге состав и строение ореолов рассеяния очень сложны.
Изложенный материал свидетельствует о неравномерном распределении рассеянных элементов в земной коре. Поэтому наряду с определением кларков, т. е. величины средней концентрации элементов в земной коре в целом, необходимо учитывать способность их концентрироваться или рассеиваться в различных объектах – разных типах горных пород или в однотипных породах, но находящихся в разных геохимических провинциях, в рудах и пр. Чтобы количественно оценить неоднородность распределения химических элементов в земной коре, В.И. Вернадский ввел специальный показатель – кларк концентрации (Кк). Его величина характеризует отклонение содержания элемента в данном объекте от кларка:
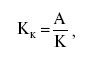
где А – содержание химического элемента в горной породе, руде, минерале и пр., К – кларк этого элемента в земной коре.
Если кларк концентрации больше 1, то это указывает на обогащение элементом, если меньше – означает снижение его содержания по сравнению с данными для земной коры в целом.
Отклонение от нормы (кларка местного геохимического фона), повышенная и пониженная концентрация химических элементов на некоторых участках – не отдельные исключения, а характерная черта геохимии земной коры. Это имеет очень важное значение, так как кора служит основанием, на котором формируются природно-территориальные комплексы. Неодинаковые уровни концентрации рассеянных элементов в разных геохимических провинциях, наличие природных геохимических аномалий с очень высокой концентрацией элементов играли не последнюю роль в формообразовании и эволюции органического мира.
Контрольные вопросы
1. Дайте определение термина «кларк химического элемента».
2. Перечислите главные закономерности содержания химических элементов в земной коре.
3. Расскажите о принципах геохимической классификации химических элементов.
4. Каковы принципиальные различия главных и рассеянных химических элементов?
5. Каким ученым разработано представление о рассеянном состоянии химических элементов?
6. Какой смысл имеет геохимический параметр «кларк концентрации» (Кк). Напишите его формулу.
7. Каковы закономерности варьирования содержания химических элементов в земной коре?
8. Дайте определение понятиям «геохимический фон», «геохимическая провинция», «геохимическая аномалия».
2. Перечислите главные закономерности содержания химических элементов в земной коре.
3. Расскажите о принципах геохимической классификации химических элементов.
4. Каковы принципиальные различия главных и рассеянных химических элементов?
5. Каким ученым разработано представление о рассеянном состоянии химических элементов?
6. Какой смысл имеет геохимический параметр «кларк концентрации» (Кк). Напишите его формулу.
7. Каковы закономерности варьирования содержания химических элементов в земной коре?
8. Дайте определение понятиям «геохимический фон», «геохимическая провинция», «геохимическая аномалия».
Задания для самостоятельной работы
1. Рассчитайте кларки концентрации тяжелых металлов для распространенных типов магматических пород.
2. По имеющимся данным постройте гистограммы распределения содержания двух химических элементов, определите их среднее арифметическое и модальное значения.
3. Изложите историю открытия рассеянного состояния химических элементов.
2. По имеющимся данным постройте гистограммы распределения содержания двух химических элементов, определите их среднее арифметическое и модальное значения.
3. Изложите историю открытия рассеянного состояния химических элементов.
Глава II
СОСТАВ И ГЕОХИМИЧЕСКАЯ ДИНАМИКА ГИДРОСФЕРЫ
Кларки Мирового океана
Основную массу водной оболочки Земли образуют соленые воды Мирового океана. Их объем примерно равен 1370 млн км3, в то время как объем всех вод суши (включая ледники и подземные воды до глубины 5 км) менее 90 млн км3. Так как океанические воды составляют около 93 % всех вод географической оболочки, можно считать, что их химический состав определяет основные черты состава гидросферы в целом.
Химические элементы в гидросфере, так же как и в земной коре, представлены разнообразными формами нахождения, геохимия которых неодинакова. Наиболее характерные для гидросферы формы – простые и сложные ионы, а также молекулы, находящиеся в состоянии сильно разбавленных растворов. Весьма распространены ионы, сорбционно связанные с частицами коллоидных и субколлоидных размеров, находящиеся в морской воде в виде тонкой взвеси. Третью группу форм составляют элементы, входящие в состав мертвого органического вещества. Значительная масса химических элементов связана в живых организмах, населяющих Мировой океан. Элементы могут переходить из одной формы нахождения в другую. Например, ион, находящийся в растворе, может быть сорбирован частицей взвеси и в дальнейшем разделяет судьбу взвешенных частиц и не подчиняется законам растворов.
Обратимся к элементам и соединениям, находящимся в океанической воде в растворенном состоянии. Общее количество растворенных соединений в морской воде называется соленостью (ее обозначают заглавной буквой латинского алфавита S). Соленость в поверхностных слоях океанов и окраинных морей колеблется от 3,2 до 4,0 %, т. е. в 1 кг воды содержится 32–37 г растворимых солей. Во внутриконтинентальных морях соленость меняется более сильно. В среднем соленость вод океана равна 33%о[1]. Нетрудно подсчитать, сколько всего растворенных солей в Мировом океане. Суммарный объем вод океана 1370 млн км3, т. е. 1370-1018 л. Так как в каждом литре содержится в среднем 35 г солей, то во всем объеме океанических вод будет 1370-1018-35 г = 47950-1018 г = 47950-1012 т, или округлено около 50–1015 т.
Еще в середине прошлого века ученые обнаружили замечательную геохимическую особенность океанической воды. Эта особенность заключается в том, что, несмотря на колебания солености, соотношение главных ионов остается постоянным. Солевой состав океана является своего рода геохимической константой.
Как видно из табл. 4, основную массу солей составляют хлориды распространенных щелочных и щелочно-земельных элементов, меньше содержится сульфатов, еще меньше – бикарбонатов (и карбонатов). Кроме главных анионов и катионов, в морской воде присутствуют в растворенном состоянии элементы-примеси. Их концентрация на три математических порядка ниже, чем в горных породах, и измеряется не в миллиграммах/килограмм (1-10-4%), а в микрограммах/литр (1-10-7%). В качестве примесей выступают как главные элементы земной коры (например, алюминий, железо), так и элементы с малыми кларками (рассеянные). Несмотря на незначительное содержание и большие трудности анализа, в результате настойчивой работы ученых многих стран был накоплен обширный аналитический материал по содержанию элементов в воде морей и океанов. Наиболее обоснованные значения были опубликованы Э.Д. Голдбергом (1963), А.П. Виноградовым (1967), Б. Мейсоном (1971), Р. Хорном (1972), А.П. Лисициным (1978), К.Н. Турекианом (1969). В табл. 4 использованы данные преимущественно двух последних авторов.
Химические элементы в гидросфере, так же как и в земной коре, представлены разнообразными формами нахождения, геохимия которых неодинакова. Наиболее характерные для гидросферы формы – простые и сложные ионы, а также молекулы, находящиеся в состоянии сильно разбавленных растворов. Весьма распространены ионы, сорбционно связанные с частицами коллоидных и субколлоидных размеров, находящиеся в морской воде в виде тонкой взвеси. Третью группу форм составляют элементы, входящие в состав мертвого органического вещества. Значительная масса химических элементов связана в живых организмах, населяющих Мировой океан. Элементы могут переходить из одной формы нахождения в другую. Например, ион, находящийся в растворе, может быть сорбирован частицей взвеси и в дальнейшем разделяет судьбу взвешенных частиц и не подчиняется законам растворов.
Обратимся к элементам и соединениям, находящимся в океанической воде в растворенном состоянии. Общее количество растворенных соединений в морской воде называется соленостью (ее обозначают заглавной буквой латинского алфавита S). Соленость в поверхностных слоях океанов и окраинных морей колеблется от 3,2 до 4,0 %, т. е. в 1 кг воды содержится 32–37 г растворимых солей. Во внутриконтинентальных морях соленость меняется более сильно. В среднем соленость вод океана равна 33%о[1]. Нетрудно подсчитать, сколько всего растворенных солей в Мировом океане. Суммарный объем вод океана 1370 млн км3, т. е. 1370-1018 л. Так как в каждом литре содержится в среднем 35 г солей, то во всем объеме океанических вод будет 1370-1018-35 г = 47950-1018 г = 47950-1012 т, или округлено около 50–1015 т.
Еще в середине прошлого века ученые обнаружили замечательную геохимическую особенность океанической воды. Эта особенность заключается в том, что, несмотря на колебания солености, соотношение главных ионов остается постоянным. Солевой состав океана является своего рода геохимической константой.
Как видно из табл. 4, основную массу солей составляют хлориды распространенных щелочных и щелочно-земельных элементов, меньше содержится сульфатов, еще меньше – бикарбонатов (и карбонатов). Кроме главных анионов и катионов, в морской воде присутствуют в растворенном состоянии элементы-примеси. Их концентрация на три математических порядка ниже, чем в горных породах, и измеряется не в миллиграммах/килограмм (1-10-4%), а в микрограммах/литр (1-10-7%). В качестве примесей выступают как главные элементы земной коры (например, алюминий, железо), так и элементы с малыми кларками (рассеянные). Несмотря на незначительное содержание и большие трудности анализа, в результате настойчивой работы ученых многих стран был накоплен обширный аналитический материал по содержанию элементов в воде морей и океанов. Наиболее обоснованные значения были опубликованы Э.Д. Голдбергом (1963), А.П. Виноградовым (1967), Б. Мейсоном (1971), Р. Хорном (1972), А.П. Лисициным (1978), К.Н. Турекианом (1969). В табл. 4 использованы данные преимущественно двух последних авторов.
