Страница:
Усиливают всасывание жиров парасимпатические влияния, гормоны коры надпочечников, щитовидной железы и гипофиза, а также гормоны двенадцатиперстной кишки (секретин и холецистокинин-панкреозимин).
При нарушении ферментативной деятельности поджелудочной железы, кишечника в кале появляются нейтральный жир, измененные мышечные волокна, внеклеточный крахмал. Недостаток желчи приводит к повышению жирных кислот, а при нарушении процессов всасывания в кале увеличиваются мыла.
В тонкой кишке происходит интенсивное всасывание воды, связанное с транспортом сахаров, аминокислот и особенно ионов Na+ и С1. Замедляют всасывание воды отсутствие желчи, торможение центральной нервной системы (например, во время сна), гормоны желудочно-кишечного тракта (гастрин, секретин и холецистокинин-панкреозимин).
Растворимые в воде витамины всасываются путем диффузии (витамин С, рибофлавин). Всасывание жирорастворимых витаминов (A, D, Е, К) тесно связано с всасыванием жиров.
Из подвздошной кишки через илеоцекальное отверстие пищевые массы попадают в толстую кишку.
Толстая кишка является последним отделом пищеварительной системы. В толстой кишке выделяют слепую, ободочную и прямую кишки.
Слепая кишка – представляет собой мешковидное выпячивание и расположена в правой подвздошной ямке. От ее заднемедиальной поверхности отходит червеобразный отросток.
Ободочная кишка – основная часть толстой кишки. В ее состав входят восходящая ободочная кишка, поперечная ободочная кишка, нисходящая ободочная кишка и сигмовидная ободочная кишка, расположенная в левой подвздошной ямке.
Прямая кишка – конечная часть толстой кишки, расположена в полости малого таза и открывается наружу анальным отверстием, через которое непереваренные остатки пищи (каловые массы) во время дефекации выводятся из организма.
В слизистой оболочке толстой кишки имеется много бокаловидных и слизистых желез. Вырабатываемая ими слизь покрывает всю слизистую оболочку, защищая ее от механического повреждения. Секреторная деятельность толстой кишки выражена слабо. Здесь выделяется небольшое количество сока, бедного ферментами. В соке толстой кишки в небольшом количестве содержатся катепсин, пептидазы, липаза, амилаза и нуклеазы.
В толстой кишке происходит накопление кишечного содержимого, заканчиваются процессы переваривания (в основном клетчатки). Всасывание в толстой кишке выражено незначительно. В основном здесь всасывается вода, в небольших количествах могут всасываться глюкоза, аминокислоты и др. Сформировавшиеся каловые массы (детрит – останки бактерий, кишечного эпителия, нерастворимые соли, неперевариваемая клетчатка) выводятся наружу.
Появление в кале перевариваемой клетчатки и внутриклеточного крахмала свидетельствует о нарушении переваривания в тонкой и толстой кишке.
Большое значение в жизнедеятельности организма и функций пищеварительного тракта имеет нормальная микрофлора. В желудке микрофлоры содержится мало, значительно больше ее в тонком отделе кишечника и особенно много в толстой кишке.
Значение микрофлоры кишечника заключается в том, что она участвует в:
• конечном расщеплении непереваренных в тонкой кишке остатков пищи (особенно клетчатки), ферментов и других биологически активных веществ;
• обмене белков, холестерина, желчных и жирных кислот;
• синтезе витамина К и витаминов группы В;
• продукции секреторных IgA;
• подавлении патогенной и гнилостной флоры;
• поддержании в нормальном состоянии перистальтики кишечника.
Анатомо-физиологические особенности пищеварительной системы у детей раннего возраста
Глава 2. Характеристика острых кишечных инфекций у детей шигеллезы (бактериальная дизентерия)
При нарушении ферментативной деятельности поджелудочной железы, кишечника в кале появляются нейтральный жир, измененные мышечные волокна, внеклеточный крахмал. Недостаток желчи приводит к повышению жирных кислот, а при нарушении процессов всасывания в кале увеличиваются мыла.
В тонкой кишке происходит интенсивное всасывание воды, связанное с транспортом сахаров, аминокислот и особенно ионов Na+ и С1. Замедляют всасывание воды отсутствие желчи, торможение центральной нервной системы (например, во время сна), гормоны желудочно-кишечного тракта (гастрин, секретин и холецистокинин-панкреозимин).
Растворимые в воде витамины всасываются путем диффузии (витамин С, рибофлавин). Всасывание жирорастворимых витаминов (A, D, Е, К) тесно связано с всасыванием жиров.
Из подвздошной кишки через илеоцекальное отверстие пищевые массы попадают в толстую кишку.
Толстая кишка является последним отделом пищеварительной системы. В толстой кишке выделяют слепую, ободочную и прямую кишки.
Слепая кишка – представляет собой мешковидное выпячивание и расположена в правой подвздошной ямке. От ее заднемедиальной поверхности отходит червеобразный отросток.
Ободочная кишка – основная часть толстой кишки. В ее состав входят восходящая ободочная кишка, поперечная ободочная кишка, нисходящая ободочная кишка и сигмовидная ободочная кишка, расположенная в левой подвздошной ямке.
Прямая кишка – конечная часть толстой кишки, расположена в полости малого таза и открывается наружу анальным отверстием, через которое непереваренные остатки пищи (каловые массы) во время дефекации выводятся из организма.
В слизистой оболочке толстой кишки имеется много бокаловидных и слизистых желез. Вырабатываемая ими слизь покрывает всю слизистую оболочку, защищая ее от механического повреждения. Секреторная деятельность толстой кишки выражена слабо. Здесь выделяется небольшое количество сока, бедного ферментами. В соке толстой кишки в небольшом количестве содержатся катепсин, пептидазы, липаза, амилаза и нуклеазы.
В толстой кишке происходит накопление кишечного содержимого, заканчиваются процессы переваривания (в основном клетчатки). Всасывание в толстой кишке выражено незначительно. В основном здесь всасывается вода, в небольших количествах могут всасываться глюкоза, аминокислоты и др. Сформировавшиеся каловые массы (детрит – останки бактерий, кишечного эпителия, нерастворимые соли, неперевариваемая клетчатка) выводятся наружу.
Появление в кале перевариваемой клетчатки и внутриклеточного крахмала свидетельствует о нарушении переваривания в тонкой и толстой кишке.
Большое значение в жизнедеятельности организма и функций пищеварительного тракта имеет нормальная микрофлора. В желудке микрофлоры содержится мало, значительно больше ее в тонком отделе кишечника и особенно много в толстой кишке.
Значение микрофлоры кишечника заключается в том, что она участвует в:
• конечном расщеплении непереваренных в тонкой кишке остатков пищи (особенно клетчатки), ферментов и других биологически активных веществ;
• обмене белков, холестерина, желчных и жирных кислот;
• синтезе витамина К и витаминов группы В;
• продукции секреторных IgA;
• подавлении патогенной и гнилостной флоры;
• поддержании в нормальном состоянии перистальтики кишечника.
Анатомо-физиологические особенности пищеварительной системы у детей раннего возраста
Слизистая оболочка полости рта нежная. Слюна имеет низкую бактерицидную способность (мало лизоцима, пропердина, секреторного IgA) и нейтральную или слабокислую реакцию, что может способствовать развитию молочницы слизистой оболочки полости рта.
Ферментативная активность слюны низкая, ее действие направлено на створаживание молока в желудке с образованием мелких хлопьев для облегчения гидролиза казеина.
При грудном вскармливании происходит частичный гидролиз белков, жиров и углеводов за счет ферментов женского молока, активность которых повышается в желудке ребенка.
Слабая выраженность анатомических сужений пищевода (особенно в кардиальном отделе), горизонтальное расположение желудка, преобладание вагусных влияний на моторную функцию пищеварительного тракта (замедлена перистальтика желудка и снижен тонус кардиального сфинктера) предрасполагают у детей грудного возраста к забрасыванию желудочного содержимого в пищевод, частым срыгиваниям и рвоте.
Кислотность желудочного сока обусловлена в основном молочной кислотой и в постнатальном периоде приближается к нейтральной (pH 4–6). Ферментативная активность желудочного сока более низкая и направлена на гидролиз белков и эмульгированных жиров молока. Изменение характера питания стимулирует развитие секреции соляной кислоты и к концу первого года жизни реакция желудочного сока становится более кислой (pH 3–4).
Значительно снижена секреция панкреатического сока и содержание в нем ферментов, принимающих участие в полостном пищеварении. Из-за низкой концентрации в желчи желчных кислот ограничена активность липазы поджелудочной железы, что может приводить к недостаточному перевариванию и адсорбции жиров в тонкой кишке и появлению их в кале (стеаторея).
Низкая секреция кишечного сока и активность гидролитических ферментов обуславливают недостаточность полостного пищеварения, что компенсируется участием в гидролизе относительно большей части тонкой кишки, увеличением удельного веса мембранного и внутриклеточного пищеварения. С возрастанием секреторной деятельности пищеварительных желез пищеварение становится более активным в верхней трети тонкой кишки.
Быстрое развитие пищеварительных желез и их секреторной деятельности в течение первого года жизни обеспечивает адаптацию ЖКТ к быстро изменяющемуся характеру пищи.
Вследствие низкого объема секреции пищеварительных соков, соляной кислоты и слизи снижена барьерная функция ЖКТ, что позволяет патогенной микрофлоре беспрепятственно проникать в кишечник, размножаться и вызывать воспалительные изменения.
Богатая васкуляризация слизистой оболочки тонкой кишки и повышенная ее проницаемость способствуют быстрому всасыванию токсинов и микробов из полости кишечника в кровоток.
Недостаточное развитие эластичной и мышечной ткани стенок кишечника (продольная мускулатура развита лучше циркулярной), несформированность интрамуральной нервной системы предрасполагают к возникновению спазмов, кишечных колик и дискинезий ЖКТ.
Недостаточность фиксирующих мышечно-связочных структур (более длинная и легко растяжимая брыжейка, слабость илеоцекальной заслонки) может приводить к перекрутам и инвагинации кишечника.
Прямая кишка относительно длиннее, слизистая оболочка кишечника значительно тоньше, слабо фиксированы слизистый и подслизистый слои, в связи с чем при тенезмах и упорных запорах возможно выпадение слизистой оболочки прямой кишки через анальное отверстие.
У детей раннего возраста отмечается функциональная незрелость местных специфических и неспецифических защитных систем:
• недостаточное количество пейеровых бляшек, склонность к незавершенности фагоцитоза облегчает размножение и проникновение инфекционных агентов через кишечную стенку с развитием генерализованных (септических) форм кишечных инфекций;
• дифференцировка Th-лимфоцитов направлена преимущественно на образование Th2 (с повышением продукции IL-4, IL-10, IgG и IgE), что, с одной стороны, способствует формированию пищевой аллергии у детей с периода новорожденности, с другой стороны, снижение образования Thl (с понижением продукции IL-6, IL-12, IL-18, IFN-y и IgA) у детей в этом возрасте способствует снижению противовирусной защиты организма в целом и предрасполагает к развитию вирусных кишечных инфекций;
• недостаточен синтез иммуноглобулинов в кишечнике – продукция SIgA начинается с 3-месячного возраста и окончательно формируется лишь к 7–8 годам. Кроме того, защитная функция SIgA усиливается в присутствии лактоферрина, который у детей раннего возраста вырабатывается еще в низких концентрациях. Микрофлора кишечника детей первых месяцев жизни зависит от характера питания, отличается малым разнообразием и недостаточной способностью к саморегуляции. При грудном вскармливании характерен более высокий уровень бифидобактерий, при искусственном, как правило, высеваются аэробные и анаэробные условно-патогенные микробы. После введения прикорма состав флоры становится более разнообразным, меняется состав бифидо-флоры, увеличивается количество лактобактерий и строгих анаэробов. Окончательное формирование биоценоза кишечника происходит к 2-летнему возрасту.
Ферментативная активность слюны низкая, ее действие направлено на створаживание молока в желудке с образованием мелких хлопьев для облегчения гидролиза казеина.
При грудном вскармливании происходит частичный гидролиз белков, жиров и углеводов за счет ферментов женского молока, активность которых повышается в желудке ребенка.
Слабая выраженность анатомических сужений пищевода (особенно в кардиальном отделе), горизонтальное расположение желудка, преобладание вагусных влияний на моторную функцию пищеварительного тракта (замедлена перистальтика желудка и снижен тонус кардиального сфинктера) предрасполагают у детей грудного возраста к забрасыванию желудочного содержимого в пищевод, частым срыгиваниям и рвоте.
Кислотность желудочного сока обусловлена в основном молочной кислотой и в постнатальном периоде приближается к нейтральной (pH 4–6). Ферментативная активность желудочного сока более низкая и направлена на гидролиз белков и эмульгированных жиров молока. Изменение характера питания стимулирует развитие секреции соляной кислоты и к концу первого года жизни реакция желудочного сока становится более кислой (pH 3–4).
Значительно снижена секреция панкреатического сока и содержание в нем ферментов, принимающих участие в полостном пищеварении. Из-за низкой концентрации в желчи желчных кислот ограничена активность липазы поджелудочной железы, что может приводить к недостаточному перевариванию и адсорбции жиров в тонкой кишке и появлению их в кале (стеаторея).
Низкая секреция кишечного сока и активность гидролитических ферментов обуславливают недостаточность полостного пищеварения, что компенсируется участием в гидролизе относительно большей части тонкой кишки, увеличением удельного веса мембранного и внутриклеточного пищеварения. С возрастанием секреторной деятельности пищеварительных желез пищеварение становится более активным в верхней трети тонкой кишки.
Быстрое развитие пищеварительных желез и их секреторной деятельности в течение первого года жизни обеспечивает адаптацию ЖКТ к быстро изменяющемуся характеру пищи.
Вследствие низкого объема секреции пищеварительных соков, соляной кислоты и слизи снижена барьерная функция ЖКТ, что позволяет патогенной микрофлоре беспрепятственно проникать в кишечник, размножаться и вызывать воспалительные изменения.
Богатая васкуляризация слизистой оболочки тонкой кишки и повышенная ее проницаемость способствуют быстрому всасыванию токсинов и микробов из полости кишечника в кровоток.
Недостаточное развитие эластичной и мышечной ткани стенок кишечника (продольная мускулатура развита лучше циркулярной), несформированность интрамуральной нервной системы предрасполагают к возникновению спазмов, кишечных колик и дискинезий ЖКТ.
Недостаточность фиксирующих мышечно-связочных структур (более длинная и легко растяжимая брыжейка, слабость илеоцекальной заслонки) может приводить к перекрутам и инвагинации кишечника.
Прямая кишка относительно длиннее, слизистая оболочка кишечника значительно тоньше, слабо фиксированы слизистый и подслизистый слои, в связи с чем при тенезмах и упорных запорах возможно выпадение слизистой оболочки прямой кишки через анальное отверстие.
У детей раннего возраста отмечается функциональная незрелость местных специфических и неспецифических защитных систем:
• недостаточное количество пейеровых бляшек, склонность к незавершенности фагоцитоза облегчает размножение и проникновение инфекционных агентов через кишечную стенку с развитием генерализованных (септических) форм кишечных инфекций;
• дифференцировка Th-лимфоцитов направлена преимущественно на образование Th2 (с повышением продукции IL-4, IL-10, IgG и IgE), что, с одной стороны, способствует формированию пищевой аллергии у детей с периода новорожденности, с другой стороны, снижение образования Thl (с понижением продукции IL-6, IL-12, IL-18, IFN-y и IgA) у детей в этом возрасте способствует снижению противовирусной защиты организма в целом и предрасполагает к развитию вирусных кишечных инфекций;
• недостаточен синтез иммуноглобулинов в кишечнике – продукция SIgA начинается с 3-месячного возраста и окончательно формируется лишь к 7–8 годам. Кроме того, защитная функция SIgA усиливается в присутствии лактоферрина, который у детей раннего возраста вырабатывается еще в низких концентрациях. Микрофлора кишечника детей первых месяцев жизни зависит от характера питания, отличается малым разнообразием и недостаточной способностью к саморегуляции. При грудном вскармливании характерен более высокий уровень бифидобактерий, при искусственном, как правило, высеваются аэробные и анаэробные условно-патогенные микробы. После введения прикорма состав флоры становится более разнообразным, меняется состав бифидо-флоры, увеличивается количество лактобактерий и строгих анаэробов. Окончательное формирование биоценоза кишечника происходит к 2-летнему возрасту.
Глава 2. Характеристика острых кишечных инфекций у детей шигеллезы (бактериальная дизентерия)
Шигеллезы (Shigellosis) – инфекционные заболевания человека, вызываемые бактериями рода шигелл, с фекально-оральным механизмом передачи, характеризующиеся развитием острого инфекционного токсикоза и преимущественным поражением слизистой оболочки дистального отдела толстой кишки.
Исторические данные. Термин «дизентерия» существует со времен Гиппократа (460–372 гг. до н. э.). До начала XIX в. он объединял заболевания, сопровождающиеся «кровавым» или «натужным» поносом.
В 1875 г. петербургский профессор Ф. А. Леш открыл амебу и доказал ее роль в этиологии колитов. В 1891 г. А. В. Григорьев выделил, изучил и подробно описал микроорганизмы, обнаруженные в испражнениях больных дизентерией. В 1898 г. японский исследователь К. Шига окончательно доказал этиологическую роль выделенного микроба, и в честь первооткрывателей данный возбудитель был назван бактерией Григорьева-Шиги. Позже зарубежные исследователи открыли и описали ряд сходных микроорганизмов данного рода: в 1906 г. – бактерии Флекснера, в 1915 г. – Зонне, в 1916 г. – Штутцера-Шмитца, в 1929 г. – Ньюкасла, в 1936 г. – Бойда, в 1943 г. – Ларджа-Сакса. В настоящее время изучено и описано более 50 сероваров шигелл.
Этиология. Возбудители шигеллезов относятся к семейству Enterobacteriaceae, роду Shigella. Шигеллы – палочки с закругленными концами, размерами 2–3 х 0,5–7 мкм, неподвижны, спор, капсул, жгутиков не имеют, грамотрицательны. Являются факультативными аэробами, хорошо растут на обычных питательных средах, образуя S-и R-колонии. Биохимическая активность выражена слабо: способны ферментировать глюкозу и некоторые другие углеводы с образованием кислоты без газа (не расщепляют адонит, инозит, не гидролизуют мочевину, не разжижают желатин). Часть шигелл (S.flexneri, S. sonnei) способны расщеплять маннит, шигелла Зонне обладает способностью медленно ферментировать лактозу. Наибольшую биохимическую активность имеют шигеллы Зонне, наименьшую – Григорьева-Шиги.
В основу современной классификации шигелл положены два принципа: биохимические свойства и антигенная структура. Согласно современной классификации (табл. 1) род Shigella включает 4 подгруппы (А, В, С, D) и 4 вида: S. dysenteriae (бактерии Григорьева-Шиги, Штутцера-Шмитца и Ларджа-Сакса); S. flexneri с подвидом S. Newcastle, S. boydii, S. sonnei.
Таблица 1
Классификация бактерий рода Shigella

Все виды шигелл, кроме Зонне, имеют несколько сероваров, а S. flexneri – и подсеровары. Шигеллы Зонне разделяют на 7 ферментативных типов и 64 фаготипа.
Шигеллы имеют О– и К-антигены. О-антиген определяет серологическую специфичность, К-антиген является оболочечной структурой.
В состав клеточной стенки шигелл входит эндотоксин (липополисахарид), который высвобождается при гибели микроорганизма. Бактерии вида S. dysenteriae серовара 1 продуцируют высокоактивный цитотоксин, названный токсином Шиги (или шига-токсин). Шига-токсин необратимо ингибирует синтез белков рибосомами клеток кишечного эпителия, а также обладает свойствами энтеротоксина и нейротоксина. Предполагают, что шига-токсин способен разрушать эндотелий капилляров и вызывать ишемию в тканях кишечника, а следствием системной абсорбции этого экзотоксина может стать гемолитико-уремический синдром и тромботическая микроангиопатия. Способностью вырабатывать различные экзотоксины обладают все представители рода Shigella.
Шигеллы обладают инвазивностью (проникновение в эпителиальные клетки слизистой оболочки толстой кишки и размножение в них) и колициногенностью (образование биологически активных веществ), а также продуцируют токсичные вещества и ферменты (гиалуронидазу, фибринолизин, лецитиназу). Они устойчивы к воздействию физических, химических, биологических факторов окружающей среды. В воде, почве, пищевых продуктах, на предметах, посуде, овощах, фруктах остаются жизнеспособными в течение 5-14 сут., в канализационных водах – до 25–30 сут. Под действием ультрафиолетовых лучей шигеллы погибают в течение 10 мин, прямые солнечные лучи, а также 1 % раствор фенола убивают и× через 30 мин, кипячение – мгновенно. Наибольшей устойчивостью обладают S. sonnei, наименьшей – Григорьева-Шиги, промежуточное положение занимают S. flexneri.
Эпидемиология. Шигеллез – типичная антропонозная инфекция. Источником инфекции являются больные острым или хроническим шигеллезом, а также бактериовыделители. Наибольшее эпидемиологическое значение имеют больные с легкими, стертыми и бессимптомными формами заболевания, так как они продолжают посещать общественные места, детские учреждения и при нарушении санитарно-гигиенического режима легко инфицируют окружающие предметы и здоровых детей. Установлено, что в острый период заболевания во внешнюю среду выделяется 107-108 микробных тел (1 г фекалий), тогда как минимальная инфицирующая доза для шигеллеза Григорьева-Шиги составляет 10 микробных тел в 1 г инфицирующего материала, для шигеллеза Флекснера – 102, а для шигеллеза Зонне – 107-108.
Механизм передачи – фекально-оральный. Ведущие пути передачи: пищевой, водный, контактно-бытовой. Основными факторами передачи являются пищевые продукты, инфицированная вода, руки, белье, игрушки, посуда, мухи. Наибольшее значение имеют продукты, не подвергнутые термической обработке: молоко, мясо, салаты, компоты, ягоды. При этом регистрируются эпидемические вспышки с внезапным началом и быстрым увеличением числа заболевших: отмечается связь с одним из предприятий общественного питания и одним продуктом. Для пищевых вспышек характерны минимальный инкубационный период, преобладание манифестных и тяжелых форм болезни, выделение возбудителя одного серовара, фаговара и биовара.
В связи с легкостью загрязнения воды и продолжительным сохранением в ней шигелл водный путь передачи инфекции является довольно частым. Способствуют развитию водных вспышек неблагоприятные погодные условия (дожди, паводки), аварии водопровода и канализации. Вспышки имеют взрывной и локальный характер, связаны с водоисточником. Заболевание характеризуется продолжительным течением.
Контактно-бытовой путь инфицирования наиболее характерен для детей раннего возраста. Факторами передачи являются загрязненные игрушки, посуда, постельное белье, дверные ручки, другие предметы домашнего обихода. При контактно-бытовом пути передачи обычно возникают спорадические случаи, значительно реже – вспышки.
Ведущий путь передачи при шигеллезе Григорьева-Шиги – контактно-бытовой, при шигеллезе Флекснера – водный, при шигеллезе Зонне – пищевой.
Заболеваемость. Шигеллезы имеют повсеместное распространение и занимают значительное место среди диарейных заболеваний в странах Африки, Азии и Латинской Америки. Эволюция этиологической структуры шигеллеза обусловлена сменой ведущих возбудителей: S. dysenteriae, S. flexneri, S. sonnei. В 1920-1930-е гг. в структуре шигеллезов доминировали штаммы Григорьева-Шиги, вызывающие эпидемические вспышки. С начала 1940-х гг. возрос удельный вес шигеллеза Флекснера, стал регистрироваться шигеллез Зонне. С начала 1990-х гг. на фоне резкого изменения социально-экономических, санитарно-гигиенических и экологических условий жизни населения в некоторых регионах России отмечается процесс смены шигеллеза Зонне на шигеллез Флекснера 2а. В эпидемический процесс вовлекаются социально незащищенные слои взрослого населения, лица, ослабленные тяжелой сопутствующей патологией, дети из специализированных учреждений (дома ребенка, школы-интернаты, психоневрологические дома ребенка).
Динамика эпидемиологических показателей при дизентерии в Санкт-Петербурге представлена на диаграммах 5–6.
Возрастная структура. Удельный вес случаев шигеллеза у детей в общей структуре заболеваемости составляет 60–70 %. Наиболее восприимчивы дети в возрасте от 2 до 7 лет.
Сезонность. Заболеваемость шигеллезом регистрируется в течение всего года, однако пик приходится на летне-осенний период. Главную роль в сезонном повышении заболеваемости играют климатические факторы, увеличение потребления овощей, фруктов, купание в водоемах, загрязненных сточными водами, усиление миграции населения.
Иммунитет, вырабатываемый во время заболевания шигеллезом, нестоек и моноспецифичен – антитела вырабатываются только к тому виду и серотипу, который вызвал заболевание, что обусловливает повторные заражения.
Патогенез. Входными воротами является ротовая полость, где начинается воздействие на возбудителей факторов неспецифического иммунитета – лизоцима, макрофагов, нейтрофилов. В желудке под действием соляной кислоты, пищеварительных ферментов шигеллы частично гибнут, при этом высвобождается эндотоксин. Часть микроорганизмов попадает в тонкую кишку и под действием желчи разрушается. Далее возбудители достигают дистальных отделов толстого кишечника, где происходит как их размножение, так и гибель.
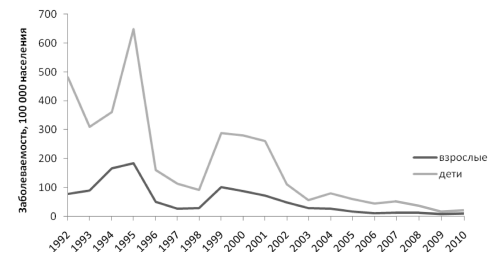
Диаграмма 5. Показатели заболеваемости бактериальной дизентерией среди различны групп населения, Санкт-Петербург, 1992–2010 гг

Диаграмма 6. Показатели заболеваемости бактериальной дизентерией детей различного возраста, Санкт-Петербург, 1992–2010 гг
При разрушении шигелл выделяется целый ряд токсичных продуктов, которые не только вызывают различные морфологические изменения в кишечнике, но и, всасываясь в кровь, приводят к развитию острого инфекционного токсикоза.
Токсины шигелл оказывают повреждающее действие на все органы и системы организма, прежде всего на ЦНС. Поражение нервной системы происходит как в результате непосредственного действия токсина на интерорецепторы сосудов нервной ткани, так и за счет сложных рефлекторных взаимодействий, возникающих в результате раздражения окончаний нервных волокон, расположенных в слизистой оболочке кишки. Изменения ЦНС имеют неспецифический характер: нарушаются взаимоотношения между процессами возбуждения и торможения в коре головного мозга, значительно страдают функции вегетативного отдела нервной системы. В начале болезни кратковременно преобладает тонус симпатической, а затем, уже более длительное время, парасимпатической нервной системы.
В остром периоде шигеллеза в крови повышается концентрация гистамина и ацетилхолина, снижаются ингибиторные свойства крови и содержание ацетил– и холинэстеразы.
Отмечаются изменения в эндокринной системе: усиливается деятельность коры надпочечников, нарушается гипофизарно-надпочечниковая регуляция и активность ренин-ангиотензин-альдостероновой системы.
Дисфункция вегетативной нервной системы, гемодинамические расстройства, а также непосредственное действие токсина на сердечную мышцу приводят к поражению сердечно-сосудистой системы. У больных выявляются снижение сократительной функции миокарда, тонуса сосудов, кратковременное повышение артериального давления, систолический шум на верхушке сердца. При тяжелых формах возможно снижение артериального давления, развитие коллаптоидных состояний.
Эндотоксины шигелл усиливают проницаемость сосудистой стенки, увеличивают ее ломкость, резко снижают количество тромбоцитов, что нередко приводит к развитию ДВС-синдрома. В результате распада тромбоцитов выделяется большое количество серотонина, что обусловливает местный спазм сосудов и усиливает развитие циркуляторных расстройств. Эндотоксины шигелл активно воздействуют на печень, вызывая нарушение всех видов обмена (белкового, углеводного, жирового, витаминного) и снижение ее дезинтоксикационной функции. У большинства больных с острым шигеллезом нарушается экскреторная функция поджелудочной железы как в острый период, так и в период ранней реконвалесценции. Степень вовлечения в патологический процесс почек зависит от тяжести заболевания. При среднетяжелой и, особенно, тяжелой форме шигеллеза, происходит токсическое поражение почек: выявляются изменения в мочевом осадке (белок, эритроциты, цилиндры), увеличивается содержание мочевины и креатинина в сыворотке крови. В тяжелых случаях возможно развитие острой почечной недостаточности и гемолитико-уремического синдрома. В патологический процесс вовлекаются желудок, тонкая кишка, развивается гипермоторная дискинезия толстой кишки, нарушается капиллярная гемодинамика, появляется клеточная сенсибилизация.
Наряду с токсинемией в патогенезе дизентерии играет роль местный воспалительный процесс в кишечнике, преимущественно в его дистальном отделе.
Взаимодействие со слизистой оболочкой кишечника начинается с прикрепления микроорганизмов к клеткам эпителия за счет межбактериальной агрегации и адсорбции, а затем адгезии (прилипание микробов к гликокаликсу и рецепторам мембраны кишечных эпителиоцитов). Адгезия сопровождается разбуханием и отторжением микроворсинок в местах прикрепления возбудителя с развитием воспаления. Проникновение шигелл в энтероциты, активное размножение в них, выделение ряда ферментов и биологически активных веществ обусловливают распространение возбудителя в ткани кишки и усиливают воспалительный процесс.
Одновременно с токсинемией и инвазией шигелл в энтероциты формируются защитные иммунологические реакции организма. В межклеточном пространстве слизистой оболочки кишечника шигеллы подвергаются воздействию макрофагов. В дальнейшем антигены возбудителя взаимодействуют с Т-хелперами, затем информация переносится на В-лимфоциты. В ранние сроки повышается содержание IgM, позднее – IgG и IgA. В собственной пластинке слизистой оболочки толстой кишки в 2–3 раза увеличивается число клеток, продуцирующих IgA и IgM. Происходит активация естественных киллеров и синтеза α– и у-интерферонов. Наряду с этим развивается вторичный иммунодефицит: снижается общее количество циркулирующих Т– и В-лимфоцитов, увеличивается число Т-супрессоров и уменьшается количество Т-хелперов, возрастает количество лимфоцитов, сенсибилизированных к антигенам шигелл и компонентам собственных тканей организма.
При удовлетворительном состоянии системы механизмов защиты и адекватной терапии шигеллез в большинстве случаев заканчивается быстрым выздоровлением. У детей раннего возраста с отягощенным преморбидным фоном, а также при неадекватной терапии возможно затяжное течение, а иногда и переход в хроническую форму.
Патоморфология. При шигеллезах в слизистой оболочке полости рта, желудка, тонкой кишки могут обнаруживаться явления ослизнения эпителия с небольшими периваскулярными инфильтратами. Однако наиболее выраженные изменения выявляются в дистальном отделе толстой кишки (нисходящая ободочная, сигмовидная и прямая кишка). Слизистая оболочка указанных отделов гиперемирована, отечна, нередко наблюдаются мелкие кровоизлияния, обнаруживается мутная слизь (катаральный колит). У некоторых больных на фоне диффузного катара слизистой оболочки отмечаются обширные рыхлые, желтовато-серые, пленчатые наложения фибрина (фибринозный колит). Язвенный колит чаще выявляется при тяжелых формах шигеллеза. Фибринознонекротические массы постепенно истончаются и исчезают. По мере их удаления начинают формироваться изъязвления, которые обычно имеют неправильную форму. Края язв набухшие или плотные, дно желтовато-красноватое. Изъязвления могут наблюдаться и без фибринозного воспаления. В этом случае язвы чаще имеют округлую форму. Ткань кишки вокруг них обычно полнокровнее, чем в соседних участках. При этом отмечаются выраженные расстройства кровообращения и лимфообращения в кишечнике, в частности, отек подслизистой оболочки.
Регенерация эпителия при катаральном воспалении начинается на 2-3-и сутки болезни, однако полное анатомическое восстановление наступает не раньше 2–3 мес. При деструктивных изменениях репарация происходит медленно.
При хронической форме шигеллеза характерно вялое течение воспалительного процесса с деформацией крипт и участками атрофии слизистой оболочки кишки. Для шигеллеза типичны дистрофические изменения в нервных сплетениях с частичной гибелью клеток (в ганглиях солнечного сплетения, шейных симпатических узлах и узловом ганглии блуждающего нерва). Отмечаются также дистрофические изменения нефротелия; полнокровие, отек и дистрофические процессы в печени; выраженные дистрофические изменения миокарда; очаговый отек промежуточной ткани; полнокровие, незначительные некротические очаги в корковом и мозговом слоях надпочечников; дегенеративно-деструктивные явления в ганглиозных клетках и миелиновых волокнах.
Исторические данные. Термин «дизентерия» существует со времен Гиппократа (460–372 гг. до н. э.). До начала XIX в. он объединял заболевания, сопровождающиеся «кровавым» или «натужным» поносом.
В 1875 г. петербургский профессор Ф. А. Леш открыл амебу и доказал ее роль в этиологии колитов. В 1891 г. А. В. Григорьев выделил, изучил и подробно описал микроорганизмы, обнаруженные в испражнениях больных дизентерией. В 1898 г. японский исследователь К. Шига окончательно доказал этиологическую роль выделенного микроба, и в честь первооткрывателей данный возбудитель был назван бактерией Григорьева-Шиги. Позже зарубежные исследователи открыли и описали ряд сходных микроорганизмов данного рода: в 1906 г. – бактерии Флекснера, в 1915 г. – Зонне, в 1916 г. – Штутцера-Шмитца, в 1929 г. – Ньюкасла, в 1936 г. – Бойда, в 1943 г. – Ларджа-Сакса. В настоящее время изучено и описано более 50 сероваров шигелл.
Этиология. Возбудители шигеллезов относятся к семейству Enterobacteriaceae, роду Shigella. Шигеллы – палочки с закругленными концами, размерами 2–3 х 0,5–7 мкм, неподвижны, спор, капсул, жгутиков не имеют, грамотрицательны. Являются факультативными аэробами, хорошо растут на обычных питательных средах, образуя S-и R-колонии. Биохимическая активность выражена слабо: способны ферментировать глюкозу и некоторые другие углеводы с образованием кислоты без газа (не расщепляют адонит, инозит, не гидролизуют мочевину, не разжижают желатин). Часть шигелл (S.flexneri, S. sonnei) способны расщеплять маннит, шигелла Зонне обладает способностью медленно ферментировать лактозу. Наибольшую биохимическую активность имеют шигеллы Зонне, наименьшую – Григорьева-Шиги.
В основу современной классификации шигелл положены два принципа: биохимические свойства и антигенная структура. Согласно современной классификации (табл. 1) род Shigella включает 4 подгруппы (А, В, С, D) и 4 вида: S. dysenteriae (бактерии Григорьева-Шиги, Штутцера-Шмитца и Ларджа-Сакса); S. flexneri с подвидом S. Newcastle, S. boydii, S. sonnei.
Таблица 1
Классификация бактерий рода Shigella

Все виды шигелл, кроме Зонне, имеют несколько сероваров, а S. flexneri – и подсеровары. Шигеллы Зонне разделяют на 7 ферментативных типов и 64 фаготипа.
Шигеллы имеют О– и К-антигены. О-антиген определяет серологическую специфичность, К-антиген является оболочечной структурой.
В состав клеточной стенки шигелл входит эндотоксин (липополисахарид), который высвобождается при гибели микроорганизма. Бактерии вида S. dysenteriae серовара 1 продуцируют высокоактивный цитотоксин, названный токсином Шиги (или шига-токсин). Шига-токсин необратимо ингибирует синтез белков рибосомами клеток кишечного эпителия, а также обладает свойствами энтеротоксина и нейротоксина. Предполагают, что шига-токсин способен разрушать эндотелий капилляров и вызывать ишемию в тканях кишечника, а следствием системной абсорбции этого экзотоксина может стать гемолитико-уремический синдром и тромботическая микроангиопатия. Способностью вырабатывать различные экзотоксины обладают все представители рода Shigella.
Шигеллы обладают инвазивностью (проникновение в эпителиальные клетки слизистой оболочки толстой кишки и размножение в них) и колициногенностью (образование биологически активных веществ), а также продуцируют токсичные вещества и ферменты (гиалуронидазу, фибринолизин, лецитиназу). Они устойчивы к воздействию физических, химических, биологических факторов окружающей среды. В воде, почве, пищевых продуктах, на предметах, посуде, овощах, фруктах остаются жизнеспособными в течение 5-14 сут., в канализационных водах – до 25–30 сут. Под действием ультрафиолетовых лучей шигеллы погибают в течение 10 мин, прямые солнечные лучи, а также 1 % раствор фенола убивают и× через 30 мин, кипячение – мгновенно. Наибольшей устойчивостью обладают S. sonnei, наименьшей – Григорьева-Шиги, промежуточное положение занимают S. flexneri.
Эпидемиология. Шигеллез – типичная антропонозная инфекция. Источником инфекции являются больные острым или хроническим шигеллезом, а также бактериовыделители. Наибольшее эпидемиологическое значение имеют больные с легкими, стертыми и бессимптомными формами заболевания, так как они продолжают посещать общественные места, детские учреждения и при нарушении санитарно-гигиенического режима легко инфицируют окружающие предметы и здоровых детей. Установлено, что в острый период заболевания во внешнюю среду выделяется 107-108 микробных тел (1 г фекалий), тогда как минимальная инфицирующая доза для шигеллеза Григорьева-Шиги составляет 10 микробных тел в 1 г инфицирующего материала, для шигеллеза Флекснера – 102, а для шигеллеза Зонне – 107-108.
Механизм передачи – фекально-оральный. Ведущие пути передачи: пищевой, водный, контактно-бытовой. Основными факторами передачи являются пищевые продукты, инфицированная вода, руки, белье, игрушки, посуда, мухи. Наибольшее значение имеют продукты, не подвергнутые термической обработке: молоко, мясо, салаты, компоты, ягоды. При этом регистрируются эпидемические вспышки с внезапным началом и быстрым увеличением числа заболевших: отмечается связь с одним из предприятий общественного питания и одним продуктом. Для пищевых вспышек характерны минимальный инкубационный период, преобладание манифестных и тяжелых форм болезни, выделение возбудителя одного серовара, фаговара и биовара.
В связи с легкостью загрязнения воды и продолжительным сохранением в ней шигелл водный путь передачи инфекции является довольно частым. Способствуют развитию водных вспышек неблагоприятные погодные условия (дожди, паводки), аварии водопровода и канализации. Вспышки имеют взрывной и локальный характер, связаны с водоисточником. Заболевание характеризуется продолжительным течением.
Контактно-бытовой путь инфицирования наиболее характерен для детей раннего возраста. Факторами передачи являются загрязненные игрушки, посуда, постельное белье, дверные ручки, другие предметы домашнего обихода. При контактно-бытовом пути передачи обычно возникают спорадические случаи, значительно реже – вспышки.
Ведущий путь передачи при шигеллезе Григорьева-Шиги – контактно-бытовой, при шигеллезе Флекснера – водный, при шигеллезе Зонне – пищевой.
Заболеваемость. Шигеллезы имеют повсеместное распространение и занимают значительное место среди диарейных заболеваний в странах Африки, Азии и Латинской Америки. Эволюция этиологической структуры шигеллеза обусловлена сменой ведущих возбудителей: S. dysenteriae, S. flexneri, S. sonnei. В 1920-1930-е гг. в структуре шигеллезов доминировали штаммы Григорьева-Шиги, вызывающие эпидемические вспышки. С начала 1940-х гг. возрос удельный вес шигеллеза Флекснера, стал регистрироваться шигеллез Зонне. С начала 1990-х гг. на фоне резкого изменения социально-экономических, санитарно-гигиенических и экологических условий жизни населения в некоторых регионах России отмечается процесс смены шигеллеза Зонне на шигеллез Флекснера 2а. В эпидемический процесс вовлекаются социально незащищенные слои взрослого населения, лица, ослабленные тяжелой сопутствующей патологией, дети из специализированных учреждений (дома ребенка, школы-интернаты, психоневрологические дома ребенка).
Динамика эпидемиологических показателей при дизентерии в Санкт-Петербурге представлена на диаграммах 5–6.
Возрастная структура. Удельный вес случаев шигеллеза у детей в общей структуре заболеваемости составляет 60–70 %. Наиболее восприимчивы дети в возрасте от 2 до 7 лет.
Сезонность. Заболеваемость шигеллезом регистрируется в течение всего года, однако пик приходится на летне-осенний период. Главную роль в сезонном повышении заболеваемости играют климатические факторы, увеличение потребления овощей, фруктов, купание в водоемах, загрязненных сточными водами, усиление миграции населения.
Иммунитет, вырабатываемый во время заболевания шигеллезом, нестоек и моноспецифичен – антитела вырабатываются только к тому виду и серотипу, который вызвал заболевание, что обусловливает повторные заражения.
Патогенез. Входными воротами является ротовая полость, где начинается воздействие на возбудителей факторов неспецифического иммунитета – лизоцима, макрофагов, нейтрофилов. В желудке под действием соляной кислоты, пищеварительных ферментов шигеллы частично гибнут, при этом высвобождается эндотоксин. Часть микроорганизмов попадает в тонкую кишку и под действием желчи разрушается. Далее возбудители достигают дистальных отделов толстого кишечника, где происходит как их размножение, так и гибель.

Диаграмма 5. Показатели заболеваемости бактериальной дизентерией среди различны групп населения, Санкт-Петербург, 1992–2010 гг

Диаграмма 6. Показатели заболеваемости бактериальной дизентерией детей различного возраста, Санкт-Петербург, 1992–2010 гг
При разрушении шигелл выделяется целый ряд токсичных продуктов, которые не только вызывают различные морфологические изменения в кишечнике, но и, всасываясь в кровь, приводят к развитию острого инфекционного токсикоза.
Токсины шигелл оказывают повреждающее действие на все органы и системы организма, прежде всего на ЦНС. Поражение нервной системы происходит как в результате непосредственного действия токсина на интерорецепторы сосудов нервной ткани, так и за счет сложных рефлекторных взаимодействий, возникающих в результате раздражения окончаний нервных волокон, расположенных в слизистой оболочке кишки. Изменения ЦНС имеют неспецифический характер: нарушаются взаимоотношения между процессами возбуждения и торможения в коре головного мозга, значительно страдают функции вегетативного отдела нервной системы. В начале болезни кратковременно преобладает тонус симпатической, а затем, уже более длительное время, парасимпатической нервной системы.
В остром периоде шигеллеза в крови повышается концентрация гистамина и ацетилхолина, снижаются ингибиторные свойства крови и содержание ацетил– и холинэстеразы.
Отмечаются изменения в эндокринной системе: усиливается деятельность коры надпочечников, нарушается гипофизарно-надпочечниковая регуляция и активность ренин-ангиотензин-альдостероновой системы.
Дисфункция вегетативной нервной системы, гемодинамические расстройства, а также непосредственное действие токсина на сердечную мышцу приводят к поражению сердечно-сосудистой системы. У больных выявляются снижение сократительной функции миокарда, тонуса сосудов, кратковременное повышение артериального давления, систолический шум на верхушке сердца. При тяжелых формах возможно снижение артериального давления, развитие коллаптоидных состояний.
Эндотоксины шигелл усиливают проницаемость сосудистой стенки, увеличивают ее ломкость, резко снижают количество тромбоцитов, что нередко приводит к развитию ДВС-синдрома. В результате распада тромбоцитов выделяется большое количество серотонина, что обусловливает местный спазм сосудов и усиливает развитие циркуляторных расстройств. Эндотоксины шигелл активно воздействуют на печень, вызывая нарушение всех видов обмена (белкового, углеводного, жирового, витаминного) и снижение ее дезинтоксикационной функции. У большинства больных с острым шигеллезом нарушается экскреторная функция поджелудочной железы как в острый период, так и в период ранней реконвалесценции. Степень вовлечения в патологический процесс почек зависит от тяжести заболевания. При среднетяжелой и, особенно, тяжелой форме шигеллеза, происходит токсическое поражение почек: выявляются изменения в мочевом осадке (белок, эритроциты, цилиндры), увеличивается содержание мочевины и креатинина в сыворотке крови. В тяжелых случаях возможно развитие острой почечной недостаточности и гемолитико-уремического синдрома. В патологический процесс вовлекаются желудок, тонкая кишка, развивается гипермоторная дискинезия толстой кишки, нарушается капиллярная гемодинамика, появляется клеточная сенсибилизация.
Наряду с токсинемией в патогенезе дизентерии играет роль местный воспалительный процесс в кишечнике, преимущественно в его дистальном отделе.
Взаимодействие со слизистой оболочкой кишечника начинается с прикрепления микроорганизмов к клеткам эпителия за счет межбактериальной агрегации и адсорбции, а затем адгезии (прилипание микробов к гликокаликсу и рецепторам мембраны кишечных эпителиоцитов). Адгезия сопровождается разбуханием и отторжением микроворсинок в местах прикрепления возбудителя с развитием воспаления. Проникновение шигелл в энтероциты, активное размножение в них, выделение ряда ферментов и биологически активных веществ обусловливают распространение возбудителя в ткани кишки и усиливают воспалительный процесс.
Одновременно с токсинемией и инвазией шигелл в энтероциты формируются защитные иммунологические реакции организма. В межклеточном пространстве слизистой оболочки кишечника шигеллы подвергаются воздействию макрофагов. В дальнейшем антигены возбудителя взаимодействуют с Т-хелперами, затем информация переносится на В-лимфоциты. В ранние сроки повышается содержание IgM, позднее – IgG и IgA. В собственной пластинке слизистой оболочки толстой кишки в 2–3 раза увеличивается число клеток, продуцирующих IgA и IgM. Происходит активация естественных киллеров и синтеза α– и у-интерферонов. Наряду с этим развивается вторичный иммунодефицит: снижается общее количество циркулирующих Т– и В-лимфоцитов, увеличивается число Т-супрессоров и уменьшается количество Т-хелперов, возрастает количество лимфоцитов, сенсибилизированных к антигенам шигелл и компонентам собственных тканей организма.
При удовлетворительном состоянии системы механизмов защиты и адекватной терапии шигеллез в большинстве случаев заканчивается быстрым выздоровлением. У детей раннего возраста с отягощенным преморбидным фоном, а также при неадекватной терапии возможно затяжное течение, а иногда и переход в хроническую форму.
Патоморфология. При шигеллезах в слизистой оболочке полости рта, желудка, тонкой кишки могут обнаруживаться явления ослизнения эпителия с небольшими периваскулярными инфильтратами. Однако наиболее выраженные изменения выявляются в дистальном отделе толстой кишки (нисходящая ободочная, сигмовидная и прямая кишка). Слизистая оболочка указанных отделов гиперемирована, отечна, нередко наблюдаются мелкие кровоизлияния, обнаруживается мутная слизь (катаральный колит). У некоторых больных на фоне диффузного катара слизистой оболочки отмечаются обширные рыхлые, желтовато-серые, пленчатые наложения фибрина (фибринозный колит). Язвенный колит чаще выявляется при тяжелых формах шигеллеза. Фибринознонекротические массы постепенно истончаются и исчезают. По мере их удаления начинают формироваться изъязвления, которые обычно имеют неправильную форму. Края язв набухшие или плотные, дно желтовато-красноватое. Изъязвления могут наблюдаться и без фибринозного воспаления. В этом случае язвы чаще имеют округлую форму. Ткань кишки вокруг них обычно полнокровнее, чем в соседних участках. При этом отмечаются выраженные расстройства кровообращения и лимфообращения в кишечнике, в частности, отек подслизистой оболочки.
Регенерация эпителия при катаральном воспалении начинается на 2-3-и сутки болезни, однако полное анатомическое восстановление наступает не раньше 2–3 мес. При деструктивных изменениях репарация происходит медленно.
При хронической форме шигеллеза характерно вялое течение воспалительного процесса с деформацией крипт и участками атрофии слизистой оболочки кишки. Для шигеллеза типичны дистрофические изменения в нервных сплетениях с частичной гибелью клеток (в ганглиях солнечного сплетения, шейных симпатических узлах и узловом ганглии блуждающего нерва). Отмечаются также дистрофические изменения нефротелия; полнокровие, отек и дистрофические процессы в печени; выраженные дистрофические изменения миокарда; очаговый отек промежуточной ткани; полнокровие, незначительные некротические очаги в корковом и мозговом слоях надпочечников; дегенеративно-деструктивные явления в ганглиозных клетках и миелиновых волокнах.
