Страница:
Уже давно при изучении простейших было обращено внимание на то, что эти организмы далеко не безразлично относятся к окружающей их среде. Высыхает ли капелька воды, в которой они живут, меняется ли температура и освещение- все это отражается так или иначе на поведении простейших. Так, например, некоторые амебы и инфузории избегают яркого света, другие, наоборот, стремятся к более освещенным местам. Если через воду, в которой сидят инфузории пропускать слабый электрический ток, то инфузории устремятся к одному из полюсов тока, избегая другого. Если в воде с инфузориями образуется пузырек воздуха, то инфузории устремятся к нему и облепят его со всех сторон, как бы стараясь высосать заключающийся в нем воздух. Все эти явления заставляют предполагать, что простейшие обладают какими-то приспособлениями, позволяющими разбираться в окружающей среде. После того, что было сказано, в этом для нас нет ничего удивительного, раз мы знаем, что в теле инфузорий есть разнообразные органы, подобные органам высших животных.
Является невольный вопрос: если строение органов простейших можно сравнить с органами многоклеточных высших животных, и если они способны реагировать соответствующим образом на окружающую среду, то нельзя ли найти что-либо общее в функциях этих органов, что позволило бы и с этой стороны сопоставить их с многоклеточными и тем более закрепить за ними право называться совершенными самостоятельными организмами? Такой вопрос, естественно, заинтересовал ученых после того, как они ближе ознакомились со строением простейших. Эта трудная по своему разрешению проблема еще не дала окончательных результатов, но некоторые работы в этом направлении и особенно выводы заслуживают безусловного интереса.
В последнее время разрешением одного из вопросов этой проблемы у нас в СССР занялся профессор В. А. Догель. Интересные результаты его работы были недавно доложены им на 3 Всесоюзном съезде анатомов зоологов и гистологов в Ленинграде.
Первой задачей проф. В. А. Догеля было изучение пищеварительного процесса инфузорий под влиянием различных солей и сравнение пищеварительного процесса у простейших с процессами пищеварения у высших многоклеточных животных. Объектом для своих исследований он выбрал всем хорошо известную инфузорию туфельку, которая легко и во множестве разводится в лабораторных условиях (рис. I). Нормальный ход пищеварения у инфузории туфельки уже давно хорошо изучен. Обычно он представляется в таком виде: плавая в воде, инфузория своим ротовым отверстием с (см, рис.), при помощи околоротовых ресничек, заглатывает кусочки пищи, которые затем проникают в так называемую "глотку" (су). Далее, поступая в тело инфузории, они окружаются так называемой пищеварительной вакуолью (п) и, в виде пузырьков, набитых пищей, начинают путешествовать внутри тела инфузории до тех пор, пока не достигнут выводного отверстия (а), через которое, уже в переваренном виде, выбрасываются наружу. Еще ранее было известно, что такое путешествие вакуолей с пищей, внутри тела инфузории, не представляется беспорядочным. Ниренштейн в 1905 году установил так называемый большой и малый круг пищеварения, подчиняясь которому пища внутри тела инфузории следует по строго установленным путям, перетерпиевая за это время процесс переваривания. Что процесс переваривания действительно имеет место в теле инфузорий, было доказано тем же Ниренштейном. Если к воде, где плавают туфельки, прибавить немного понарошку особой краски конго-рот (kongo-rot), обычно коричневато-красного цвета, то, при заглатывании инфузорией частичек краски, вакуоли в начале процесса имеют сине-фиолетовый цвет и к концу процесса переходят в коричнево-красный, что несомненно доказывает, что здесь мы имеем реакцию, химическое воздействие на частичку краски, вызванные пищеварительным процессом. Аналогичное химическое воздействие на частицы пищи происходит и в кишечнике высших позвоночных животных, где, как известно, пища, попадая в желудок, подвергается действию особого вещества - фермента пепсина, входящего в состав желудочного сока, и приобретет здесь кислую реакцию, а затем переходит в двенадцатиперстную кишку, где, под влиянием другого вещества - трипсина, вырабатываемого поджелудочной железой, нейтрализуется, приобретая щелочную реакцию, и химически перерабатывается окончательно и полностью.
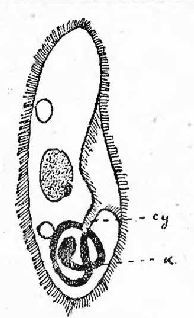 Рис 2. Инфузория Туфелька в растворе хлористого магния, су-глотка, в - тушевая "кишка", (по Догелю).
Рис 2. Инфузория Туфелька в растворе хлористого магния, су-глотка, в - тушевая "кишка", (по Догелю).
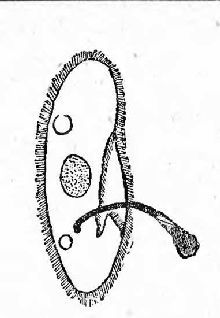 Рис 3. Инфузория Туфелька, при помещении в слабые раствор сернокислого железа претерпевает процесс обратного выведения пищи - процесс, аналогичный рвоте (по Догелю).
Рис 3. Инфузория Туфелька, при помещении в слабые раствор сернокислого железа претерпевает процесс обратного выведения пищи - процесс, аналогичный рвоте (по Догелю).
 Рис. 4. Туфелька в слабом растворе хлористого литии: су-глотка, пищевые вокуоли V-сократительная вокуоль, е- экскременты.
Рис. 4. Туфелька в слабом растворе хлористого литии: су-глотка, пищевые вокуоли V-сократительная вокуоль, е- экскременты.
Чрезвычайно интересные результаты процессов в теле инфузорий дали опыты проф. Догеля при прибавлении к воде, в которой плавают инфузории, некоторых солей. Так, к воде с инфузориями прибавлялись, например, в очень слабом растворе соли хлористого магния MgCl и MgSO
или т. наз. горькая соль; чтобы при этом яснее видеть ход всего процесса в теле инфузории, к воде прибавляется немного мелко растертой туши. Тотчас по прибавлении в воду туши и соли, мы замечаем, что заглатываемая пища (в данном случае тушь) устремляется в глотку инфузории непрерывным потоком и уже через 2-5 минут внутри тела инфузории получается длинная непрерывная изогнутая тушевая лента, которая, все увеличиваясь, вскоре образует несколько спирально извитых петель (рис. 2). Правда по истечении некоторого времени эта лента распадается на мелкие отдельности, и образуются нормальные маленькие вакуоли, но все же в течение нескольких минут (10-15) в теле инфузории образуется как бы сплошной тушевой "кишечный канал", который "до чрезвычайности напоминает кишечник некоторых Metazoa (многоклеточных животных), например улитки или червя Sipunculus (Догель).
Если внимательно проследить за образованием такой тушевой кишки, то можно заметить, что поток туши в теле инфузории следует по так называемому "малому кругу пищеварения", установленному Ниреиштейном. "В результате наших опытов с солями Mg, говорит проф. Догель, обрисовывается с одной стороны строгая определенность пути следования вакуолей, с другой стороны возможность искусственно превратить прерывистый пищевой путь в непрерывный пищеварительный тракт, имитируя таким образом сплошную кишку Meraazoa" (многоклеточных).
Если взять вместо соли магния соли железа, например, раствор сернокислого железа FeSO, то при этом получается несколько иная картина процесса. Вначале при заглатывании туши образуется такая же "тушевая кишка", только менее извитая, чем при магнии. Однако, спустя некоторое время, в солях железа такая кишка уже не распадается в теле инфузории на отдельные вакуоли, а постепенно высовывается из ротового отверстия наружу и вскоре, в виде гибкой, совершенно черной нити, выбрасывается целиком из глотки наружу (рис 3). "Нельзя не признать", говорит Догель, "что описанный процесс всем своим ходом весьма напоминает явление рвоты у многоклеточных организмов", Здесь мы наталкиваемся на случай вредноговоздействия пиши, когда организм инфузории, подобно высшим животным, не принимает несвойственной ему пищи, освобождаясь от нее путем процесса "рвоты".
Говоря об освобождении тела инфузории от пищи, мы, естественно, должны коснуться вопроса т. наз. "дефекации" или опоражнивания пищевых вакуолей инфузорий - процесса, соответствующего испражнению высших животных. Оказывается, что на ходе того процесса у инфузорий также влияет состав окружающей пищи. Введение в тело некоторых солей различным образом отражается па ходе этого процесса.
Нормально процесс дефекации происходит так: пищеварительные вакуоли, пройдя в теле инфузорий большой и малый круги пищеварения, с неперевариваемыми остатками пищи подходят по одному к задней трети тела, где расположено выводное отверстие и через него выталкиваются наружу. Однако, в обычных условиях процесс дефекации пронаблюдать очень трудно во-первых потому, что выбрасываемые наружу фекальные массы - вакуоли с отбросами обычно жидки и прозрачны; во-вторых, процесс дефекации происходит через каждые 8 -12 минут, а на прохождение кругов пищеварения каждая вакуоль затрачивает 50-60 минут, так что срок наблюдения должен быть очень продолжителен. Поэтому, чтобы изучить этот процесс, необходимо, во первых, к культуре с инфузориями прибавить раствора туши, а во-вторых, начать наблюдение не ранее, как через час после кормления тушью.
По наблюдениям профессора Догеля, оказалось, что процесс дефекации можно, по желанию, искусственно или ускорить, или замедлить. Это достигается прибавлением к культуре инфузорий слабых растворов солей металлов I и II группы (например, MgQ2, CaCl2, CaSO4, и соли Na, К, Li, Ва, Со, Ni и т. д.). Соли кальция и марганца задерживают процесс, соли натрия, лития, бария и др. ускоряют.
При наблюдении в слабом растворе хлористого лития процесс дефекации рисуется в таком виде: подошедшие к выводному отверстию пищеварительные вакуоли скопляются здесь по нескольку штук (9-10) в один ряд, и затем все это скопление медленно, но за один прием выдавливается наружу (рис. 4). Этот процесс весьма напоминает скопление фекальных масс в задней кишке высших животных перед испражнением.
Далее, замечено было, что если в нормальных условиях промежуток времени между процессами дефекации определяется в 6-12 минут, то в растворе солей бария или магния (ВаС12, MgQ-) он сокращается до 2 или 1 минуты. Наоборот, в солях кальция (СаО) промежуток времени между дефекациями удлиняется до 30 или 40 минут.
Если мы вспомним, что в медицине, в качестве слабительных средств, (которые не только меняют консистенцию фекальных масс, но и учащают процесс дефекации) употребляются препараты солей магния и бария, а в качестве закрепляющих (задерживающих)- соли кальция, то мы увидим, что и в этом случае наблюдается сходство между процессами в теле одноклеточных и высших животных. "Этот факт интересен тем", говорит проф. Догель "что он обнруживает глубокий физический параллелизм между процессами пищеварения у одноклеточных и многоклеточных организмов.
Все вышеизложенные факты указывают нам на то, что круг изучения простейших организмов здесь как бы замыкается: высказанная сто лет назад Эрнбергом теоретическая мысль о простейших, как совершенных организмах, подтверждается целым рядом современных т чных наблюдений, достигнутых точнейшими методами современного научного исследования. Мысль о единстве строения природы и управляющих ею законов вновь и вновь подтверждается неоднократными наблюдениями, и в то же время выясняется глубокая сложность и разнообразие в строении живых существ, и углубленное изучение жизни, открывая нам новые горизонты, в то же время все больше и больше ставит перед нами сложных и глубоко интересных задач, к разрешению которых неуклонно стремится человеческая мысль и знание.
В. Цветков Инж, П. Д. ДАИКОВ Коллоидная химия и вопросы научной организации быта
Является невольный вопрос: если строение органов простейших можно сравнить с органами многоклеточных высших животных, и если они способны реагировать соответствующим образом на окружающую среду, то нельзя ли найти что-либо общее в функциях этих органов, что позволило бы и с этой стороны сопоставить их с многоклеточными и тем более закрепить за ними право называться совершенными самостоятельными организмами? Такой вопрос, естественно, заинтересовал ученых после того, как они ближе ознакомились со строением простейших. Эта трудная по своему разрешению проблема еще не дала окончательных результатов, но некоторые работы в этом направлении и особенно выводы заслуживают безусловного интереса.
В последнее время разрешением одного из вопросов этой проблемы у нас в СССР занялся профессор В. А. Догель. Интересные результаты его работы были недавно доложены им на 3 Всесоюзном съезде анатомов зоологов и гистологов в Ленинграде.
Первой задачей проф. В. А. Догеля было изучение пищеварительного процесса инфузорий под влиянием различных солей и сравнение пищеварительного процесса у простейших с процессами пищеварения у высших многоклеточных животных. Объектом для своих исследований он выбрал всем хорошо известную инфузорию туфельку, которая легко и во множестве разводится в лабораторных условиях (рис. I). Нормальный ход пищеварения у инфузории туфельки уже давно хорошо изучен. Обычно он представляется в таком виде: плавая в воде, инфузория своим ротовым отверстием с (см, рис.), при помощи околоротовых ресничек, заглатывает кусочки пищи, которые затем проникают в так называемую "глотку" (су). Далее, поступая в тело инфузории, они окружаются так называемой пищеварительной вакуолью (п) и, в виде пузырьков, набитых пищей, начинают путешествовать внутри тела инфузории до тех пор, пока не достигнут выводного отверстия (а), через которое, уже в переваренном виде, выбрасываются наружу. Еще ранее было известно, что такое путешествие вакуолей с пищей, внутри тела инфузории, не представляется беспорядочным. Ниренштейн в 1905 году установил так называемый большой и малый круг пищеварения, подчиняясь которому пища внутри тела инфузории следует по строго установленным путям, перетерпиевая за это время процесс переваривания. Что процесс переваривания действительно имеет место в теле инфузорий, было доказано тем же Ниренштейном. Если к воде, где плавают туфельки, прибавить немного понарошку особой краски конго-рот (kongo-rot), обычно коричневато-красного цвета, то, при заглатывании инфузорией частичек краски, вакуоли в начале процесса имеют сине-фиолетовый цвет и к концу процесса переходят в коричнево-красный, что несомненно доказывает, что здесь мы имеем реакцию, химическое воздействие на частичку краски, вызванные пищеварительным процессом. Аналогичное химическое воздействие на частицы пищи происходит и в кишечнике высших позвоночных животных, где, как известно, пища, попадая в желудок, подвергается действию особого вещества - фермента пепсина, входящего в состав желудочного сока, и приобретет здесь кислую реакцию, а затем переходит в двенадцатиперстную кишку, где, под влиянием другого вещества - трипсина, вырабатываемого поджелудочной железой, нейтрализуется, приобретая щелочную реакцию, и химически перерабатывается окончательно и полностью.



Чрезвычайно интересные результаты процессов в теле инфузорий дали опыты проф. Догеля при прибавлении к воде, в которой плавают инфузории, некоторых солей. Так, к воде с инфузориями прибавлялись, например, в очень слабом растворе соли хлористого магния MgCl и MgSO
или т. наз. горькая соль; чтобы при этом яснее видеть ход всего процесса в теле инфузории, к воде прибавляется немного мелко растертой туши. Тотчас по прибавлении в воду туши и соли, мы замечаем, что заглатываемая пища (в данном случае тушь) устремляется в глотку инфузории непрерывным потоком и уже через 2-5 минут внутри тела инфузории получается длинная непрерывная изогнутая тушевая лента, которая, все увеличиваясь, вскоре образует несколько спирально извитых петель (рис. 2). Правда по истечении некоторого времени эта лента распадается на мелкие отдельности, и образуются нормальные маленькие вакуоли, но все же в течение нескольких минут (10-15) в теле инфузории образуется как бы сплошной тушевой "кишечный канал", который "до чрезвычайности напоминает кишечник некоторых Metazoa (многоклеточных животных), например улитки или червя Sipunculus (Догель).
Если внимательно проследить за образованием такой тушевой кишки, то можно заметить, что поток туши в теле инфузории следует по так называемому "малому кругу пищеварения", установленному Ниреиштейном. "В результате наших опытов с солями Mg, говорит проф. Догель, обрисовывается с одной стороны строгая определенность пути следования вакуолей, с другой стороны возможность искусственно превратить прерывистый пищевой путь в непрерывный пищеварительный тракт, имитируя таким образом сплошную кишку Meraazoa" (многоклеточных).
Если взять вместо соли магния соли железа, например, раствор сернокислого железа FeSO, то при этом получается несколько иная картина процесса. Вначале при заглатывании туши образуется такая же "тушевая кишка", только менее извитая, чем при магнии. Однако, спустя некоторое время, в солях железа такая кишка уже не распадается в теле инфузории на отдельные вакуоли, а постепенно высовывается из ротового отверстия наружу и вскоре, в виде гибкой, совершенно черной нити, выбрасывается целиком из глотки наружу (рис 3). "Нельзя не признать", говорит Догель, "что описанный процесс всем своим ходом весьма напоминает явление рвоты у многоклеточных организмов", Здесь мы наталкиваемся на случай вредноговоздействия пиши, когда организм инфузории, подобно высшим животным, не принимает несвойственной ему пищи, освобождаясь от нее путем процесса "рвоты".
Говоря об освобождении тела инфузории от пищи, мы, естественно, должны коснуться вопроса т. наз. "дефекации" или опоражнивания пищевых вакуолей инфузорий - процесса, соответствующего испражнению высших животных. Оказывается, что на ходе того процесса у инфузорий также влияет состав окружающей пищи. Введение в тело некоторых солей различным образом отражается па ходе этого процесса.
Нормально процесс дефекации происходит так: пищеварительные вакуоли, пройдя в теле инфузорий большой и малый круги пищеварения, с неперевариваемыми остатками пищи подходят по одному к задней трети тела, где расположено выводное отверстие и через него выталкиваются наружу. Однако, в обычных условиях процесс дефекации пронаблюдать очень трудно во-первых потому, что выбрасываемые наружу фекальные массы - вакуоли с отбросами обычно жидки и прозрачны; во-вторых, процесс дефекации происходит через каждые 8 -12 минут, а на прохождение кругов пищеварения каждая вакуоль затрачивает 50-60 минут, так что срок наблюдения должен быть очень продолжителен. Поэтому, чтобы изучить этот процесс, необходимо, во первых, к культуре с инфузориями прибавить раствора туши, а во-вторых, начать наблюдение не ранее, как через час после кормления тушью.
По наблюдениям профессора Догеля, оказалось, что процесс дефекации можно, по желанию, искусственно или ускорить, или замедлить. Это достигается прибавлением к культуре инфузорий слабых растворов солей металлов I и II группы (например, MgQ2, CaCl2, CaSO4, и соли Na, К, Li, Ва, Со, Ni и т. д.). Соли кальция и марганца задерживают процесс, соли натрия, лития, бария и др. ускоряют.
При наблюдении в слабом растворе хлористого лития процесс дефекации рисуется в таком виде: подошедшие к выводному отверстию пищеварительные вакуоли скопляются здесь по нескольку штук (9-10) в один ряд, и затем все это скопление медленно, но за один прием выдавливается наружу (рис. 4). Этот процесс весьма напоминает скопление фекальных масс в задней кишке высших животных перед испражнением.
Далее, замечено было, что если в нормальных условиях промежуток времени между процессами дефекации определяется в 6-12 минут, то в растворе солей бария или магния (ВаС12, MgQ-) он сокращается до 2 или 1 минуты. Наоборот, в солях кальция (СаО) промежуток времени между дефекациями удлиняется до 30 или 40 минут.
Если мы вспомним, что в медицине, в качестве слабительных средств, (которые не только меняют консистенцию фекальных масс, но и учащают процесс дефекации) употребляются препараты солей магния и бария, а в качестве закрепляющих (задерживающих)- соли кальция, то мы увидим, что и в этом случае наблюдается сходство между процессами в теле одноклеточных и высших животных. "Этот факт интересен тем", говорит проф. Догель "что он обнруживает глубокий физический параллелизм между процессами пищеварения у одноклеточных и многоклеточных организмов.
Все вышеизложенные факты указывают нам на то, что круг изучения простейших организмов здесь как бы замыкается: высказанная сто лет назад Эрнбергом теоретическая мысль о простейших, как совершенных организмах, подтверждается целым рядом современных т чных наблюдений, достигнутых точнейшими методами современного научного исследования. Мысль о единстве строения природы и управляющих ею законов вновь и вновь подтверждается неоднократными наблюдениями, и в то же время выясняется глубокая сложность и разнообразие в строении живых существ, и углубленное изучение жизни, открывая нам новые горизонты, в то же время все больше и больше ставит перед нами сложных и глубоко интересных задач, к разрешению которых неуклонно стремится человеческая мысль и знание.
В. Цветков Инж, П. Д. ДАИКОВ Коллоидная химия и вопросы научной организации быта
Коллоидная химия недавно заняла подобающее ей место в ряду наук, изучающих природу и делающих практически-приложимые выводы. Еще лет 15-20 тому назад ее не существовало, и лишь отдельные, не связанные друг с другом факты были рассеяны по хранилищам различных областей знания. Но уже в начале настоящего столетия внимание исследователей обратилось к тем явлениям, систематизация и плодотворнее разъяснение которых и создали науку о коллоидах.
Коллоидная химия по своей области применения в науке и технике настолько обширна, что дать очерк, более или менее исчерпывающий ее, в настоящей статье нет возможности. Здесь мы ограничимся лишь беглым знакомством с основными данными науки о коллоидах, с вопросом определения признаков коллоидов и, наконец, с некоторыми приложениями этой науки в задаче по выбору и приготовлению нищи. Вместе с этим мы остановимся и на некоторых других вопросах, связывающих коллоидную химию с бытом.
Мы очень много узнали о двух мирах, противоположных по своим размерам: мире материальных тел, видимых "простым" глазом, и мире элементов матерки- молекул и атомов. В своих представлениях мы строили физические тела из молекул и атомов, как возводят здания из кирпичей. Но во многих случаях при этом мы делали ошибки, приводившие нас к заблуждениям.
Коллоидная химия нарисовала нам действительную картину. Она показала, что многое в природе и во всем том, что нас окружает, построено из частиц материи, значительно больших чем молекулы и атомы, и обладающих особенными, им только присущими свойствами. Вот их то и можно назвать кирпичами здания природы и, если позволительно углубить эту аналогию, то атомы и молекулы явятся здесь теми песчинками и частицами глины, из которых эти кирпичики сформированы.
Указанные частицы, названные коллоидными (от лат. слова "соllа"-клей), образуют мускульные ткани животных (миозин и коллаген), кожу их, серум крови (фибогрсн и др:), белок и желток яйца (альбумины и вителлин), жиры и белки молока (казеин и лактальбумин); хлебные злаки (растительный белок, крахмал и целлюлоза), шелк (фиброген) древесину (целлюлоза), краски, ткани для одежды, почвы; многие горные породы, минералы, драгоценные камни, жемчуг, перламутр, многие металлические сплавы и еще очень многое, о чем в короткой статье не расскажешь. По и этот краткий перечень достаточно сильно говорит о роли коллоидной химики в мировой науке.
Не нужно думать, что коллоиды - коллоидные частицы есть что-то новое и имеющее место только в лабораториях. Нет, это все наши старые знакомые, с которыми мы повседневно встречаемся. Вставая утром с постели, вы идете умываться и пользуетесь мылом, которое есть не что иное, как коллоидная система из солей жирных кислот; пена, которая получается при намыливании, тоже есть коллоидная система из коллоидных частиц жирных кислот, воды и воздуха, а самый процесс вымывания есть процесс коллоидный (объяснение- которого мы дадим в дальнейшем). После умывания, вы принимаетесь за чай или кофе; и то, и другое суть типичные коллоиды, распределенные в воде; они подчиняются всем правилам, установленным коллоидной химией для подобных частиц материи. Хлеб, 2 масло, сыр, колбаса и почти все питательные продукты, которые вы употребляете за чаем, состоят из тех же коллоидных частиц и поступают так, как и полагается всякой коллоидной системе. Отправляясь на работу; вы одеваетесь - в построенное из коллоидных частиц платье,- а- на работе обрабатываете металлы стальными резцами, состоящими из коллоидальной смеси железа и углерода, или точите изделия из- дерева, созданного из коллоида-целлюлозы, или пишете коллоидальными чернилами ко бумаге, сделанной из коллоидного материала. Можно итти дальше в описании рабочего дня человека и доказать, что он всюду сталкивается с коллоидами.
Из сказанного, однако, не следует заключать, что все в природе построено из коллоидных частиц. Нередко мы можем встретить физические тела-кристаллоиды, организованные непосредственно из молекул и атомов. Но роль их в жизни и быту; конечно, менее значительна, нежели роль коллоидов. VU.)
Как же отличить коллоиды от кристаллоидов? Коллоидохимки имеют для этого очень много методов, но наиболее старый способ - способ фильтрации растворов коллоидов через животные перепонки (пергамент и др.) остался и до сих пор очень надежным. При фильтровании крупные коллоидные частицы не проходят через мелкие поры перепонки, тогда как маленькие
молекулы кристаллоидного вещества легко через них проникают.
Казалось бы, микроскопом можно было бы обнаружить мельчайшие частицы. Но в том то и дело, что величина коллоидных частиц лежит как раз но средине между размерами молекул и атомов (которые для нас всегда останутся невидимыми) и величиною, обнаруживаемою наиболее совершенным микроскопом (0,001 мм). К счастью, коллоидная химия получила в свои руки могучее орудие - ультра-микроскоп, изобретенный немецким ученым Зигмонди. Принцип этого прибора можно понять 'по рис. 1. Стеклянный сосудик с раствором коллоида (напр. водной окиси железа или металлического золота или серебра) помещается на столик хорошего микроскопа и освещается сбоку узким пучком интенсивного света так, что часть раствора находится в фокусе собирательного стекла, поставленного между источником света и сосудиком. При этом в поле микроскопа мы увидим прекрасную картину: блестящие точки беспорядочно двигаются в темной массе раствора. Характер движения этих точек приближается к характеру общеизвестного броуновского движения. Разница здесь по существу - в броуновском движении мы видим самые движущиеся частицы, здесь же нами наблюдаются не коллоидные частицы, а дифракционные кольца, вызванные каждой из них.
Наконец, очень простой способ, воспроизводимый во всякой, даже домашней обстановке, заключается в реализации так называемого эффекта Типдаля. Если взять, напр. слабый раствор желатины (очень характерного коллоида) в воде и в темной комнате пропустить через него узкий пучек света, то лучи, встречая на своем пути сравнительно крупные коллоидные частицы, рассеиваются, почему мы ясно видим резко очерченную часть раствора, в которую проникает свет. Это явление подобно тому, как освещаются пылинки в воздухе в комнате с закрытыми ставнями, через щели которых проникают пучки света. И здесь коллоидное явление, т. к. пылинки (коль скоро они достаточно малы) могут быть названы коллоидными частицами. Одинаковый эффект имеет место и в случае растворов других коллоидов.
Из свойств коллоидов особенно большое значение имеет их чрезвычайная изменчивость. Они постоянно находятся в движении и постоянно изменяются, очень чутко отвечая на каждое внешнее воздействие. Эта изменчивость, вероятно, и сделала их теми необходимыми элементами животного и растительного организма, механизма, как известно очень чувствительного и изменчивого. Состояние коллоида, характеризующееся в довольно равномерном и устойчивом распределении в объеме растворителя (чаще всего воды) называется золем, когда же коллоидные частицы под влиянием какого-либо фактора собираются в более или менее крупные образования и обычно выпадают (коагулируют) в виде осадка или образуют достаточно плотный студень, тогда они носят название геля. Эти превращения коллоидных частиц иногда являются необратимыми, иногда обратимыми; т. е. напр., камен (составная часть молока) или альбумин (составная часть белка яйца) при нагревании свертываются (коагулирует) и выпадают из растворяющей среды и уже никаким способом не могут быть возвращены в прежнее состояние (состояние золя - мелкого раздробления); наоборот, другая составная часть молока - лактольбумнн может каогулировать и снова вернуться в состояние золя. Действием химических (чаще электрохимических) агентов мы можем вызвать в различных коллоидных растворах явление коагуляции и обратное явление - раздробление сгустка до золя. Эти превращения имеют место во многих случаях при самом незначительном воздействии извне, и на них то изучена изумительная чувствительность коллоидов к внешним влияниям. Электролиты, т. е. большинство неорганических солей и различных кислот, в своих растворах заключают электрически заряженные частицы. Поэтому их влияние на состояние коллоидных частиц оказалось таким значительным, т. к. и сами коллоидные частицы нередко бывают отрицательно или положительно заряженными. Последний факт установлен целым рядом исследований. Чаще всего, напр., положительно заряженные частицы электролита, взаимодействуя с отрицательной частицей коллоида, вызывают его коагуляцию (свертывание, осаждение). Наблюдалось и обратное явление, но для него имеется довольно сложное объяснение.
Большой интерес имеет также явление набухания студеей(напр. студня желатины, крахмала); это явление соответствует, вообще говоря, явлению перехода геля в золь,-разница лишь в том. что частицы коллоида не распределяются в объеме растворителя, а поглощают его. Изучению вопроса о набухании посвящено очень много исследовании.
Благодаря своим малым размерам, коллоидные частицы, сохраняя присущее им в микроскопическом виде свойства, развивают в максимальной степени свойство поглощения своими поверхностями различных веществ. Явление поглощения,
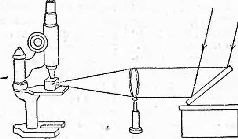 Рис 1. Схема установки ультра-микроскопа для исследования коллоидальных растворов.
Рис 1. Схема установки ультра-микроскопа для исследования коллоидальных растворов.
Называемое адсорбцией, характеризуется тем, что поглощаемое вещество (напр. краска) прилипает к поверхности поглотителя (ткани) и, попятно, чем больше поверхность поглотителя, тем больше эффект поглощения (адсорбции). Поэтому то выводы коллоидной химии стали играть громадную роль в технике крашения: как ткани, так и краски почти без исключения образованы из коллоидных частиц. Из приведенных примеров мы видим, как близки объекты коллоидной химии к домашнему быту. И, выполняя принципы НОБ'а, мы должны сделать и коллоидную химию столь же близкою нам, сколь близки нам ее объекты. В самом деле, начиная с процесса стирки белья и кончая процессом приготовлением сладкого торта, знание коллоидной химии дает возможность многое объяснить и рационально поступить в каждом отдельном случае. Еще ни одна наука так близко не подходила к вопросам быта, как коллоидная химия, и, конечно, прав был известный немецкий ученый проф. В. Оствальд, когда сказал, что …коллоидохимик в каждой умелой стряпухе должен приветствовать своего коллегу по специальности.
Теперь задачи приготовления пищи нашли уже себе место в науке, называемой "броматикой", и недалеко то время, когда поварское искусство превратится в поварскую науку.
Всем известно, что соленую рыбу люди предпочитают есть, запивая водой. Это становится понятным, когда мы посмотрим на дело с точки зрения коллоида. Рыба - почти сплошь образована из коллоидных материалов. Попадая в желудок, они начинают набухать, т. е. как уже было указано, переходить в более раздробленные формы; вода, вводимая в желудок, вымывает из соленых продуктов (рыбы) соли, т. к. соли препятствуют набуханию. Последнее же необходимо для удобоваримости.
При исследовании молока раньше обращали внимание лишь на количество белков, жира и сахара и др., входящих в состав молока. Теперь же громадное значение придают и тому состоянию, в котором находятся эти вещества. Белки, казеин и лактольбумин, находящиеся в молоке, являются в виде коллоидов: казеина, в виде очень нестойкого и после свертывания не возвращающегося к прежнему состоянию, лактальбумина, очень стойкого и обратимого коллоида. При этом лактальбумин играет роль "защитного" вещества по отношению к казеину: он обволакивает частицы казеина и этим самым сообщает ему свои стойкие свойства. Если в молоке мало лактальбумина, то молоко может еще до скисании свернуться. Мы знаем, что, подобно лактальбумину, желатина (и многие другие коллоидные вещества), весьма стойкий коллоид, может служить в качестве "защитного" коллоида; поэтому полезно бывает добавлять в молоко желатину. Но нужно при этом знать, что при сквашивании молоко с добавкой желатины не свернется, т. к. защитное" свойство желатины так велико, что образующиеся при сквашивании кислоты не могут свернуть (коагулировать) казеин молока. Точно также добавление соды в молоко препятствует свертыванию при скисании, хотя процессу (при этом сода нейтрализует кислоты) скисания не мешает. Соду добавляют и при приготовлении вегетарианских соусов, дабы молоко не коагулировало под влиянием плодовых кислот.

 Рис 2. Рис. В
Рис 2. Рис. В
На рисунках 2 и 3 изображен ход лучей в установке для ультрамикроскопического исследования коллоидальных, растворов: а - световой конус сходящихся лучей в кюветке с раствором; б - световой конус расходящихся лучей; с - фокус - место отчетливого наблюдения световых точек дифракционных колец, вызванных коллоидальными частицами.
 Другой вид пищи - мясо тоже состоит из коллоидов - миозина и коллагена. Коллоидная химия сделала уже определенные выводы о том, как различить, в каком состоянии находится мясо и удобно ли оно для употребления. По способности к набуханию (в воде) можно судить о свежести мяса; чем оно старее, тем менее способно к набуханию и тем менее удобоваримо. Телячье мясо более всего набухает в воде, тогда как свинина очень мало. Теория варки и жаренья мяса имеет тоже свои коллоидно-химические основания.
Другой вид пищи - мясо тоже состоит из коллоидов - миозина и коллагена. Коллоидная химия сделала уже определенные выводы о том, как различить, в каком состоянии находится мясо и удобно ли оно для употребления. По способности к набуханию (в воде) можно судить о свежести мяса; чем оно старее, тем менее способно к набуханию и тем менее удобоваримо. Телячье мясо более всего набухает в воде, тогда как свинина очень мало. Теория варки и жаренья мяса имеет тоже свои коллоидно-химические основания.
Обращаясь к такому важному продукту питания, как хлеб, мы и здесь увидим, что это коллоидная система. Мука состоит из водных гелей белка, крахмала и целлюлозы. Там же содержится небольшое количество солей и сахара. Тесто будет той же коллоидной системой - только произошел процесс набухания муки под влиянием воды. Но если мука до этого была нагрета до 60°, то обратимость гелей муки исчезает, и тесто из такой муки получить уже затруднительно, если не невозможно.
При печении теста происходят очень незначительные химические изменения, но коллоидно-химические процессы протекают очень радикально: частицы крахмала переходят в более мелкие коллоидные формы, белок, наоборот, уплотняется (коагулирует). Газы, выделяющиеся при печении, задерживаются тестом и образуют мелко раздробленную систему, что и обусловливает известную своеобразную пористую структуру хлеба. Эта пористость очень важна для удобоваримости хлеба. Коллоидная химия нашла рациональный способ определения степени пекарской пригодности муки при помощи определения вязкости теста из нее. Чем более вязкость, тем выше пекарская способность муки.
Коллоидная химия по своей области применения в науке и технике настолько обширна, что дать очерк, более или менее исчерпывающий ее, в настоящей статье нет возможности. Здесь мы ограничимся лишь беглым знакомством с основными данными науки о коллоидах, с вопросом определения признаков коллоидов и, наконец, с некоторыми приложениями этой науки в задаче по выбору и приготовлению нищи. Вместе с этим мы остановимся и на некоторых других вопросах, связывающих коллоидную химию с бытом.
Мы очень много узнали о двух мирах, противоположных по своим размерам: мире материальных тел, видимых "простым" глазом, и мире элементов матерки- молекул и атомов. В своих представлениях мы строили физические тела из молекул и атомов, как возводят здания из кирпичей. Но во многих случаях при этом мы делали ошибки, приводившие нас к заблуждениям.
Коллоидная химия нарисовала нам действительную картину. Она показала, что многое в природе и во всем том, что нас окружает, построено из частиц материи, значительно больших чем молекулы и атомы, и обладающих особенными, им только присущими свойствами. Вот их то и можно назвать кирпичами здания природы и, если позволительно углубить эту аналогию, то атомы и молекулы явятся здесь теми песчинками и частицами глины, из которых эти кирпичики сформированы.
Указанные частицы, названные коллоидными (от лат. слова "соllа"-клей), образуют мускульные ткани животных (миозин и коллаген), кожу их, серум крови (фибогрсн и др:), белок и желток яйца (альбумины и вителлин), жиры и белки молока (казеин и лактальбумин); хлебные злаки (растительный белок, крахмал и целлюлоза), шелк (фиброген) древесину (целлюлоза), краски, ткани для одежды, почвы; многие горные породы, минералы, драгоценные камни, жемчуг, перламутр, многие металлические сплавы и еще очень многое, о чем в короткой статье не расскажешь. По и этот краткий перечень достаточно сильно говорит о роли коллоидной химики в мировой науке.
Не нужно думать, что коллоиды - коллоидные частицы есть что-то новое и имеющее место только в лабораториях. Нет, это все наши старые знакомые, с которыми мы повседневно встречаемся. Вставая утром с постели, вы идете умываться и пользуетесь мылом, которое есть не что иное, как коллоидная система из солей жирных кислот; пена, которая получается при намыливании, тоже есть коллоидная система из коллоидных частиц жирных кислот, воды и воздуха, а самый процесс вымывания есть процесс коллоидный (объяснение- которого мы дадим в дальнейшем). После умывания, вы принимаетесь за чай или кофе; и то, и другое суть типичные коллоиды, распределенные в воде; они подчиняются всем правилам, установленным коллоидной химией для подобных частиц материи. Хлеб, 2 масло, сыр, колбаса и почти все питательные продукты, которые вы употребляете за чаем, состоят из тех же коллоидных частиц и поступают так, как и полагается всякой коллоидной системе. Отправляясь на работу; вы одеваетесь - в построенное из коллоидных частиц платье,- а- на работе обрабатываете металлы стальными резцами, состоящими из коллоидальной смеси железа и углерода, или точите изделия из- дерева, созданного из коллоида-целлюлозы, или пишете коллоидальными чернилами ко бумаге, сделанной из коллоидного материала. Можно итти дальше в описании рабочего дня человека и доказать, что он всюду сталкивается с коллоидами.
Из сказанного, однако, не следует заключать, что все в природе построено из коллоидных частиц. Нередко мы можем встретить физические тела-кристаллоиды, организованные непосредственно из молекул и атомов. Но роль их в жизни и быту; конечно, менее значительна, нежели роль коллоидов. VU.)
Как же отличить коллоиды от кристаллоидов? Коллоидохимки имеют для этого очень много методов, но наиболее старый способ - способ фильтрации растворов коллоидов через животные перепонки (пергамент и др.) остался и до сих пор очень надежным. При фильтровании крупные коллоидные частицы не проходят через мелкие поры перепонки, тогда как маленькие
молекулы кристаллоидного вещества легко через них проникают.
Казалось бы, микроскопом можно было бы обнаружить мельчайшие частицы. Но в том то и дело, что величина коллоидных частиц лежит как раз но средине между размерами молекул и атомов (которые для нас всегда останутся невидимыми) и величиною, обнаруживаемою наиболее совершенным микроскопом (0,001 мм). К счастью, коллоидная химия получила в свои руки могучее орудие - ультра-микроскоп, изобретенный немецким ученым Зигмонди. Принцип этого прибора можно понять 'по рис. 1. Стеклянный сосудик с раствором коллоида (напр. водной окиси железа или металлического золота или серебра) помещается на столик хорошего микроскопа и освещается сбоку узким пучком интенсивного света так, что часть раствора находится в фокусе собирательного стекла, поставленного между источником света и сосудиком. При этом в поле микроскопа мы увидим прекрасную картину: блестящие точки беспорядочно двигаются в темной массе раствора. Характер движения этих точек приближается к характеру общеизвестного броуновского движения. Разница здесь по существу - в броуновском движении мы видим самые движущиеся частицы, здесь же нами наблюдаются не коллоидные частицы, а дифракционные кольца, вызванные каждой из них.
Наконец, очень простой способ, воспроизводимый во всякой, даже домашней обстановке, заключается в реализации так называемого эффекта Типдаля. Если взять, напр. слабый раствор желатины (очень характерного коллоида) в воде и в темной комнате пропустить через него узкий пучек света, то лучи, встречая на своем пути сравнительно крупные коллоидные частицы, рассеиваются, почему мы ясно видим резко очерченную часть раствора, в которую проникает свет. Это явление подобно тому, как освещаются пылинки в воздухе в комнате с закрытыми ставнями, через щели которых проникают пучки света. И здесь коллоидное явление, т. к. пылинки (коль скоро они достаточно малы) могут быть названы коллоидными частицами. Одинаковый эффект имеет место и в случае растворов других коллоидов.
Из свойств коллоидов особенно большое значение имеет их чрезвычайная изменчивость. Они постоянно находятся в движении и постоянно изменяются, очень чутко отвечая на каждое внешнее воздействие. Эта изменчивость, вероятно, и сделала их теми необходимыми элементами животного и растительного организма, механизма, как известно очень чувствительного и изменчивого. Состояние коллоида, характеризующееся в довольно равномерном и устойчивом распределении в объеме растворителя (чаще всего воды) называется золем, когда же коллоидные частицы под влиянием какого-либо фактора собираются в более или менее крупные образования и обычно выпадают (коагулируют) в виде осадка или образуют достаточно плотный студень, тогда они носят название геля. Эти превращения коллоидных частиц иногда являются необратимыми, иногда обратимыми; т. е. напр., камен (составная часть молока) или альбумин (составная часть белка яйца) при нагревании свертываются (коагулирует) и выпадают из растворяющей среды и уже никаким способом не могут быть возвращены в прежнее состояние (состояние золя - мелкого раздробления); наоборот, другая составная часть молока - лактольбумнн может каогулировать и снова вернуться в состояние золя. Действием химических (чаще электрохимических) агентов мы можем вызвать в различных коллоидных растворах явление коагуляции и обратное явление - раздробление сгустка до золя. Эти превращения имеют место во многих случаях при самом незначительном воздействии извне, и на них то изучена изумительная чувствительность коллоидов к внешним влияниям. Электролиты, т. е. большинство неорганических солей и различных кислот, в своих растворах заключают электрически заряженные частицы. Поэтому их влияние на состояние коллоидных частиц оказалось таким значительным, т. к. и сами коллоидные частицы нередко бывают отрицательно или положительно заряженными. Последний факт установлен целым рядом исследований. Чаще всего, напр., положительно заряженные частицы электролита, взаимодействуя с отрицательной частицей коллоида, вызывают его коагуляцию (свертывание, осаждение). Наблюдалось и обратное явление, но для него имеется довольно сложное объяснение.
Большой интерес имеет также явление набухания студеей(напр. студня желатины, крахмала); это явление соответствует, вообще говоря, явлению перехода геля в золь,-разница лишь в том. что частицы коллоида не распределяются в объеме растворителя, а поглощают его. Изучению вопроса о набухании посвящено очень много исследовании.
Благодаря своим малым размерам, коллоидные частицы, сохраняя присущее им в микроскопическом виде свойства, развивают в максимальной степени свойство поглощения своими поверхностями различных веществ. Явление поглощения,

Называемое адсорбцией, характеризуется тем, что поглощаемое вещество (напр. краска) прилипает к поверхности поглотителя (ткани) и, попятно, чем больше поверхность поглотителя, тем больше эффект поглощения (адсорбции). Поэтому то выводы коллоидной химии стали играть громадную роль в технике крашения: как ткани, так и краски почти без исключения образованы из коллоидных частиц. Из приведенных примеров мы видим, как близки объекты коллоидной химии к домашнему быту. И, выполняя принципы НОБ'а, мы должны сделать и коллоидную химию столь же близкою нам, сколь близки нам ее объекты. В самом деле, начиная с процесса стирки белья и кончая процессом приготовлением сладкого торта, знание коллоидной химии дает возможность многое объяснить и рационально поступить в каждом отдельном случае. Еще ни одна наука так близко не подходила к вопросам быта, как коллоидная химия, и, конечно, прав был известный немецкий ученый проф. В. Оствальд, когда сказал, что …коллоидохимик в каждой умелой стряпухе должен приветствовать своего коллегу по специальности.
Теперь задачи приготовления пищи нашли уже себе место в науке, называемой "броматикой", и недалеко то время, когда поварское искусство превратится в поварскую науку.
Всем известно, что соленую рыбу люди предпочитают есть, запивая водой. Это становится понятным, когда мы посмотрим на дело с точки зрения коллоида. Рыба - почти сплошь образована из коллоидных материалов. Попадая в желудок, они начинают набухать, т. е. как уже было указано, переходить в более раздробленные формы; вода, вводимая в желудок, вымывает из соленых продуктов (рыбы) соли, т. к. соли препятствуют набуханию. Последнее же необходимо для удобоваримости.
При исследовании молока раньше обращали внимание лишь на количество белков, жира и сахара и др., входящих в состав молока. Теперь же громадное значение придают и тому состоянию, в котором находятся эти вещества. Белки, казеин и лактольбумин, находящиеся в молоке, являются в виде коллоидов: казеина, в виде очень нестойкого и после свертывания не возвращающегося к прежнему состоянию, лактальбумина, очень стойкого и обратимого коллоида. При этом лактальбумин играет роль "защитного" вещества по отношению к казеину: он обволакивает частицы казеина и этим самым сообщает ему свои стойкие свойства. Если в молоке мало лактальбумина, то молоко может еще до скисании свернуться. Мы знаем, что, подобно лактальбумину, желатина (и многие другие коллоидные вещества), весьма стойкий коллоид, может служить в качестве "защитного" коллоида; поэтому полезно бывает добавлять в молоко желатину. Но нужно при этом знать, что при сквашивании молоко с добавкой желатины не свернется, т. к. защитное" свойство желатины так велико, что образующиеся при сквашивании кислоты не могут свернуть (коагулировать) казеин молока. Точно также добавление соды в молоко препятствует свертыванию при скисании, хотя процессу (при этом сода нейтрализует кислоты) скисания не мешает. Соду добавляют и при приготовлении вегетарианских соусов, дабы молоко не коагулировало под влиянием плодовых кислот.


На рисунках 2 и 3 изображен ход лучей в установке для ультрамикроскопического исследования коллоидальных, растворов: а - световой конус сходящихся лучей в кюветке с раствором; б - световой конус расходящихся лучей; с - фокус - место отчетливого наблюдения световых точек дифракционных колец, вызванных коллоидальными частицами.

Обращаясь к такому важному продукту питания, как хлеб, мы и здесь увидим, что это коллоидная система. Мука состоит из водных гелей белка, крахмала и целлюлозы. Там же содержится небольшое количество солей и сахара. Тесто будет той же коллоидной системой - только произошел процесс набухания муки под влиянием воды. Но если мука до этого была нагрета до 60°, то обратимость гелей муки исчезает, и тесто из такой муки получить уже затруднительно, если не невозможно.
При печении теста происходят очень незначительные химические изменения, но коллоидно-химические процессы протекают очень радикально: частицы крахмала переходят в более мелкие коллоидные формы, белок, наоборот, уплотняется (коагулирует). Газы, выделяющиеся при печении, задерживаются тестом и образуют мелко раздробленную систему, что и обусловливает известную своеобразную пористую структуру хлеба. Эта пористость очень важна для удобоваримости хлеба. Коллоидная химия нашла рациональный способ определения степени пекарской пригодности муки при помощи определения вязкости теста из нее. Чем более вязкость, тем выше пекарская способность муки.
