Страница:
Преднизолон применяют в среднем по 20 мг/сутки, при необходимости доводя эту дозу до 60 мг/сутки.
Кортикостероидная терапия оказывает хорошее влияние как на отечный, так и на мочевой синдром. Она может способствовать выздоровлению и предупреждать переход острого нефрита в хронический.
При наличии тенденции к повышению артериального давления и нарастанию отеков лечение кортикостероидными гормонами следует сочетать с гипотензивными и диуретическими средствами.
При осложнении острого гломерулонефрита эклампсией применяют кровопускание, вводят сульфат магния (10 мл 25 %-ного раствора) внутривенно, дают снотворные и наркотические средства (хлоралгидрат и др.). Показаны ганглиоблокаторы, например гексоний по 10–20 мг 0,5–1 мл 2%-ного раствора внутримышечно. В предэклампсическом периоде целесообразно назначение резерпина, а также урегита, гипотиазида или лазикса; последний особенно ценен в виде инъекций как обезвоживающее средство при явлениях отека мозга.
Прогноз, трудоспособность. При остром нефрите прогноз различен. Может наблюдаться полное выздоровление. Летальный исход в остром периоде заболевания бывает редко, он чаще связан с кровоизлияниями в мозг на фоне эклампсии, реже – с сердечной недостаточностью, пневмонией или острой уремией. Переход острого нефрита в хроническое заболевание наблюдается приблизительно в 1/3 случаев.
Прогноз острого нефрита в значительной степени зависит от раннего распознавания и правильного лечения заболевания. В связи с применением в последние годы кортикостероидной терапии он значительно улучшился.
В остром периоде больные нетрудоспособны и должны находится в стационаре. При типичном течении через 2–3 месяца может наступить полное выздоровление: больные могут возвратиться к трудовой деятельности даже при наличии умеренного мочевого синдрома или остаточной альбуминурии.
Весьма важно диспансерное наблюдение за лицами, перенесшими острый нефрит, так как клиническое выздоровление нередко может быть кажущимся. Особенно это важно при наличии даже умеренного мочевого синдрома. Во избежание рецидивов особенное внимание следует уделять борьбе с инфекционными очагами в организме. Необходимо в течение года избегать работы, связанной с охлаждением, особенно с действием влажного холода.
Профилактика острого нефрита в основном сводится к предупреждению и раннему энергичному лечению острых инфекционных болезней и устранению очаговой инфекции, особенно в миндалинах, предупреждению резкого охлаждения.
Хронический гломерулонефрит – длительно протекающее иммуновоспалительное двустороннее заболевание почек с клиническими проявлениями классической брайтовой болезни, приводящее к прогрессирующей гибели клубочков, снижению деятельности почек, развитию артериальной гипертонии с последующим развитием почечной недостаточности.
Этиология. Хронический нефрит может быть исходом как острого нефрита, так и первично хроническим, без предшествующей острой атаки. Нередко встречаются хронические гломерулонефриты преимущественно иммунной природы: сывороточный, вакцинный, связанный с приемом пищевых антигенов, ядов, после перенесенной травмы, охлаждения. Ряд медикаментов, помимо обычного поражения почек типа «острой» токсической почки, нередко одновременно с
лихорадкой, поражением кожи, суставов, печени и селезенки. Хронический гломерулонефрит является частым осложнением подострого септического эндокардита. Описаны случаи развития диффузного поражения почек у больных, страдающих туберкулезом, сифилисом.
Диффузные тяжелые поражения почечной паренхимы при системных аутоиммунных заболеваниях, таких как геморрагический васкулит, узелковый периартрит, системная красная волчанка.
Патогенез. При переходе нефрита в хроническую форму в прогрессировании его основная роль принадлежит реактивности макроорганизма, степени аутоиммунных нарушений.
Клиническая картина. Клиническая картина хронического гломерулонефрита полиморфна. Она включает развитие отеков, гипертонию, мочевой синдром (протеинурия, гематурия, цилиндрурия), гипопротеинемию, гиперхолестеринемию. Наиболее часто жалобы больных связаны с почечной гипертонией – нарушение зрения, развитие сердечной недостаточности, приступы кардиальной астмы; с явлениями почечной недостаточности – слабость, сухость кожи, нарушение сна, зуд, плохой аппетит; с поражением почек – боли в области поясницы, дизурические явления, никтурия и т. д. В зависимости от превалирования тех или иных синдромов Е. М. Тареев выделяет следующие формы течения хронического гломерулонефрита: злокачественный (экстракапиллярный), латентный, гипертонический, нефротический и смешанный. Общим для течения указанных форм гломерулонефрита является прогрессирующий характер течения с возможностью сохранения в течение длительного времени нормальной функции почек с последующим развитием хронической почечной недостаточности.
Подострый, злокачественный нефрит приводит к прогрессирующей гибели нефритов, деформации архитектоники почки.
В биопсийном материале определяется пролиферативный гломерулонефрит с фибринозно-эпителиальными полулуниями, который может развиться спустя неделю после начала заболевания. Одновременно отмечается канальцевое и интерстициальное поражение, часто обнаруживается фибриноидный некроз клубочков и артериол.
Клинически злокачественное течение нефрита можно подозревать, если через 4–6 недель остро начавшегося заболевания наблюдается снижение относительной плотности мочи, повышение содержания креатинина и индикана сыворотки крови, стабильно остается на высоких цифрах артериальное давление. Развитие отечного синдрома встречается редко при подостром нефрите. Основным клиническим проявлением являются быстрое и стойкое снижение функции почек, нарастающие изменения глазного дна. Прогноз злокачественного течения гломерулонефрита остается крайне тяжелым.
Латентный хронический диффузный гломерулонефрит. Это довольно частая форма, проявляющаяся обычно лишь слабо выраженным мочевым синдромом без артериальной гипертонии и отеков. Латентная форма хронического гломерулонефрита приобретает драматическую форму в случаях, когда выявляется хроническая почечная недостаточность, казалось бы, среди полного здоровья. Годами эти больные сохраняют полную работоспособность, не считая себя больными. Наиболее часто болезнь выявляется при диспансеризации, когда врач обращает внимание на мочевой синдром (гематурия, протенкурия), снижение относительной плотности, никтурию, незначительное повышение артериального давления. Иногда выявляются повышенная скорость оседания эритроцитов, гипопротеинемия, гиперхолестеринемия. Эта форма хронического гломерулонефрита имеет длительное течение (30–40 лет), особенно в случаях, когда больным удается исключить провоцирующие обострение факторы.
Нефротическая форма (ранее называвшаяся нефрозонефритом, или паренхиматозным нефритом). При нефротической форме характерна большая протеинурия (более 3,5 г/сутки), гипопротеинемия и диспротеинемия с уменьшением содержания альбуминов в плазме, значительным снижением альбумино-глобулинового коэффициента, высокая гиперхолестеринемия 104–260 ммоль/л (400—1 тыс. мг%), выделение с мочой двояко преломляющихся субстанций. Большей частью у больных с этой формой наблюдаются массивные отеки, обусловленные в основном снижением коллоидоосмотического давления белков плазмы, связанным с гипопротеинемией (50–40 г/л (5–4 г %)) и диспротеинемией, вследствие потери белка с мочой. Отечный синдром развивается постепенно. Обычно по утрам появляются отечность под глазами, отеки лодыжек. В дальнейшем отеки становятся постоянными, распространяются на туловище, присоединяется гидроторакс, асцит, гидроперикард. В этой стадии наблюдаются сухость кожи, снижение ее эластичности, гипертрофия мышц. Степень протеинурии коррелирует с нарастанием содержания триглицеридов и свободного холестерина в плазме крови, с образованием крупных липопротеидов – латексценция.
Для нефротической формы хронического гломерулонефрита, в отличие от чистого липоидного нефроза, характерно сочетание нефротического синдрома с признаками воспалительного поражения почек: умеренной гематурией и снижением фильтрационной функции. Повышения артериального давления, как правило, не наблюдается. Клиническая картина заболевания может долго определяться нефротическим синдромом, и только в дальнейшем наступает прогрессирование нефрита с нарушением азотовыделительной функции почек и артериальной гипертонией.
Гипертоническая форма хронического нефрита. В течение длительного времени ведущим и часто единственным симптомом является гипертония.
Под влиянием различных факторов – холода, эмоциональных воздействий – артериальное давление может подвергаться большим колебаниям. При осмотре обращают на себя внимание приподнимающийся верхушечный толчок, расширение относительной тупости сердца влево, акцент II тона над аортой, у части больных выслушивается ритм галопа. При прогрессировании сердечной недостаточности развивается клиника застоя по малому кругу, возможны кровохарканье, приступы сердечной астмы, в редких случаях – отек легких. Как правило, гипертония при хроническом гломерулонефрите, в отличие от подострого, не приобретает злокачественного характера. Она не склонна к быстрому прогрессированию; артериальное давление, кровоизлияния в сетчатку редки; экссудация и отеки сетчатки, так же как и изменения сосочков зрительного нерва, появляются только в финале болезни. Что касается патогенеза артериальной гипертонии при этой форме нефрита, то имеются более или менее определенные данные, указывающие на значение почечно-ишемического, ренин-гипертензивного механизма ее развития. С прогрессированием болезни развивается хроническая почечная недостаточность, и болезнь может приобрести черты злокачественной гипертонии.
Смешанная форма диффузного гломерулонефрита. Для смешанной формы хронического гломерулонефрита характерно наличие большинства основных синдромов и симптомов классического паренхиматозного нефрита: отеки, гематурия, протеинурия, гипертония, однако степень их проявления в большинстве случаев не столь выражена, как это отмечается при других формах. В большинстве случаев клинике обострений хронического гломерулонефрита свойственно преобладание того или иного синдрома. Нередко длительно могут наблюдаться только мочевые симптомы и самочувствие больных не нарушено. В это время только при специальных исследованиях обнаруживаются некоторые нарушения функции почек, в первую очередь снижение фильтрации, а затем и концентрационной способности. Значительно позже появляются признаки хронической почечной недостаточности – хронической азотемической уремии.
Внезапное обострение заболевания, характеризующееся ухудшением общего самочувствия, с выраженным проявлением основных синдромов, снижением удельного веса мочи, повышение экскреции белка – все это может указывать на неблагоприятную эволюцию заболевания. Прогрессирование заболевания в дальнейшем проявляется повышением уровня мочевины, креатинина, индикана в плазме крови, снижением клубочковой фильтрации и возрастанием фильтрационной фракции.
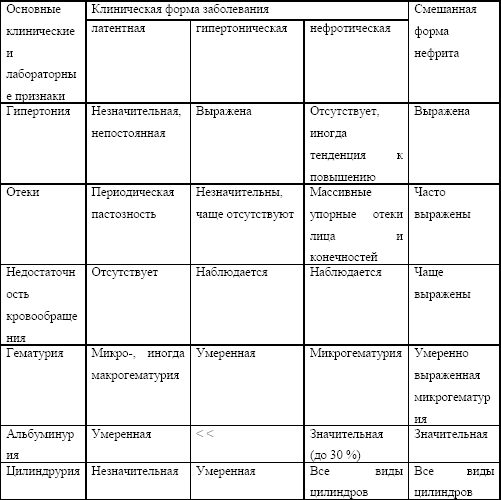
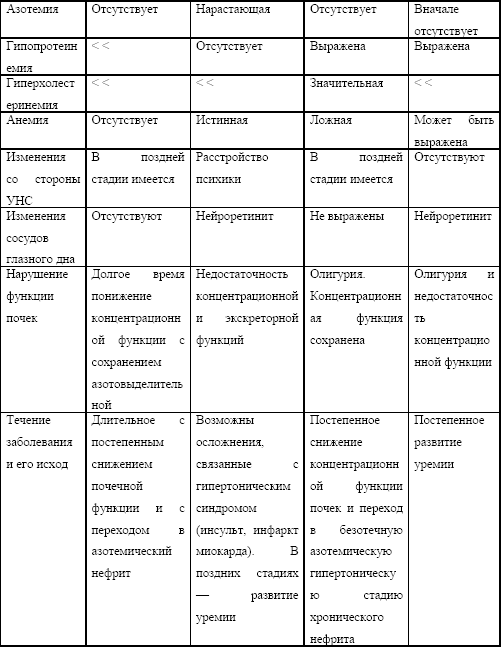
Таблица № 1. Критерии диагностики основных форм хронического нефрита
Прогноз. Исходом хронического гломерулонефрита является сморщивание почек с развитием хронической почечной недостаточности – хронической уремии. Этот исход до последнего времени наблюдался во всех случаях хронического гломерулонефрита, правда в различные сроки от начала заболевания. За последние 10–15 лет прогноз хронического гломерулонефрита в связи с введением в клиническую практику иммунодепрессивной терапии стал значительно лучше. При применении иммунодепрессивной терапии, в частности кортикостероидной, в 70–80 % случаев наблюдается положительный эффект, причем в 14–18 % случаев – полная ремиссия болезни с исчезновением как общих, так и мочевых симптомов.
Профилактика и лечение. Основной профилактикой хронического нефрита является полноценное лечение острого нефрита. В этом отношении огромное значение имеет прежде всего ранняя и точная диагностика острого гломерулонефрита, что дает возможность своевременно госпитализировать и эффективно лечить больного. Имеет значение и устранение очагов инфекции (удаление миндалин, санация полости рта). Длительные диетические ограничения (соли и белков) не предупреждают перехода острого нефрита в хронический.
Больные хроническим нефритом должны избегать охлаждения, особенно воздействия влажного холода. Им рекомендуется сухой и теплый климат. При удовлетворительном общем состоянии и отсутствии осложнений показано санаторно-курортное лечение на курортах Средней Азии (Байроли-Али) или на южном берегу Крыма (Ялта). Постельный режим необходим только в период значительных отеков или сердечной недостаточности, а также в терминальной стадии при симптомах уремии. Режим при хроническом нефрите в фазе ремиссии должен быть щадящим. Противопоказаны тяжелый физический труд, работа в ночную смену, на открытом воздухе в холодное время года, в горячих цехах, душных, плохо проветриваемых помещениях. Больные должны избегать нервного и физического переутомления. В случаях возникновения острого интеркуррентного заболевания рекомендуется соответствующее лечение с применением антимикробных лекарственных средств на фоне постельного режима.
В лечении больных хроническим гломерулонефритом существенное значение имеет диета, которая должна варьироваться в зависимости от формы и стадии заболевания. При нефротической и смешанной формах (при наличии отеков) содержание хлорида натрия в диете должно быть ограничено до 1,5–2,5 г; при условии достаточной выделительной функции почек диета должна содержать достаточное количество белков – до 2–2,5 г на 1 кг массы тела больного, что способствует положительному азотистому балансу и компенсации белковых потерь. При гипертонической форме рекомендуется умеренно ограничивать прием хлорида натрия – до 5 г/сутки при нормальном содержании в рационе белков и углеводов. Латентная форма существенных ограничений в питании больных не требует, питание должно быть полноценным, разнообразным и богатым витаминами. Витамины (С, комплекс В, А) должны входить в рацион и при других формах хронического гломерулонефрита. Следует указать, что длительная безбелковая диета без соли не предупреждает прогрессирования нефрита и плохо отражается на общем состоянии больных.
Большинство клиницистов рекомендует 35–50 г белка в день плюс количество белка, теряемого с мочой за сутки. Количество пищевого белка уменьшают лишь при снижении почечных функций. Диета должна быть богата фруктовыми и овощными соками, содержащими витамины А, группы В, С и Е.
Особенно большое значение имеет кортикостероидная терапия, являющаяся основой патогенетической терапии при этом заболевании. Начинают лечение обычно с 15–20 мг преднизолона, при необходимости увеличивая дозу до 60–80 мг/сутки, затем постепенно ее снижают. При обострении заболевания курсы лечения глюкокортикоидами повторяют.
Иногда применяется прерывистая терапия глюкокортикоидами – 3 дня (подряд) в неделю, которая снижает возможность развития «стероидного кушингоида», стероидных язв, сохраняя лечебный эффект гормонов.
Применение кортикостероидов ведет к уменьшению воспалительного процесса в клубочках почек, что способствует улучшению фильтрации и выражается в уменьшении мочевого синдрома, гематурии и протеинурии, что вторично ведет к улучшению и белкового состава крови. При лечении кортикостероидами нередко могут развиться синдром Кушинга, стероидные язвы, остеопороз.
Противопоказанием к применению кортикостероидов у больных хроническим нефритом является прогрессирующая азотемия. При противопоказаниях к применению кортикостероидов или неэффективности лечения рекомендуются негормональные иммунодепрессанты: азапмоприн (имурана), 6-меркаптопурин. Эти препараты более эффективны, однако они вызывают выраженную лейкопению. Лечение ими лучше переносится при одновременном применении преднизолона в умеренной дозе по 10–30 мг/сутки, что предупреждает токсические влияния негормональных иммунодепрессантов на лейкопоэз.
В последних стадиях – при склерозе клубочков и атрофии с высокой гипертонией – иммунодепрессанты и стероидные гормоны противопоказаны, так как иммунологической активности в клубочках уже нет и продолжение такого лечения только усугубляет гипертонию.
Легким эффектом иммунодепрессантов обладают препараты 4-аминохинолинового ряда – хингамин (делагил, резохин, хлорохин), гидроксихлорохин (плаквенил). Резохин (хлорохин) применяют по 0,25 г 1–3 раза в день в течение 2–8 месяцев. Для лечения воспалительных изменений в почечной паренхиме применяются также нестероидные противовоспалительные препараты, в частности индометацин, который, помимо обезболивающего и жаропонижающего действия, воздействует на медиаторы иммунологического повреждения. Под влиянием индометацина снижается протеинурия. Назначают его внутрь по 25 мг 2–3 раза в день, затем в зависимости от переносимости увеличивают дозу до 100–150 мг/сутки. Лечение проводится длительно, в течение нескольких месяцев. Одновременное применение стероидных гормонов и индометацина позволяет значительно снизить дозу кортикостероидов с постепенной полной отменой.
В последние годы для лечения хронического диффузного гломерулонефрита стали применять антикоагулянты.
В случае упорных отеков при нефротической и смешанной формах рекомендуется одновременно с назначением преднизолона назначать:
– различные салуретики: фуросемид, этакриновую кислоту и т. д.;
– конкурентные блокаторы альдостерона (верошпирон, альдактон).
При упорных отеках на фоне гипопротеинемии можно рекомендовать применение высокомолекулярного углевода – полиглюкина (декстрана) в виде капельного внутривенного введения 500 мл раствора, что приводит к повышению коллоидно-осмотического давления плазмы крови, способствует перемещению жидкости из тканей в кровь и вызывает диурез. При нарушении белкового обмена, особенно при нефротической форме, показано применение анаболических стероидных гормонов, особенно в сочетании с пластическими продуктами (аминокислоты, мононуклеотиды и т. д.). Анаболические стероиды-гормоны можно назначать в виде инъекционной формы – ретаболил 50 мг внутримышечно один раз в 10–15 дней или метандростенагон орально 10–15 мг в течение 2–3 недель. Имеются указания, что в ранней стадии почечной недостаточности анаболические гормоны способствуют улучшению белкового обмена.
При лечении гипертонической формы хронического гломерулонефрита могут быть использованы гипотензивные средства, применяемые при лечении гипертонической болезни: резерпин, комбинация резерпина с бета-адреноблокаторами, миолитики.
Можно использовать и ганглиоблокирующие препараты, в частности гексоний и пентамин. Однако следует избегать резких колебаний артериального давления и ортостатического его падения, которые могут приводить к ухудшению почечного кровотока и фильтрационной функции почек. Поэтому эти гипотензивные препараты желательно комбинировать с резерпином, что уменьшает склонность к резким колебаниям артериального давления и ведет к более медленному и постепенному улучшению функции почек и уменьшению других симптомов, связанных с гипертонией (изменения глазного дна, сердца и т. д.). Показано при гипертонической форме хронического гломерулонефрита и применение препаратов, подавляющих синтез катехоламинов в надпочечниках. Это α-метилдофа (альдамет, допегит), которые назначают по 750—1 тыс. мг/сутки. Эти препараты способствуют постепенному снижению артериального давления, не вызывают резких его колебаний и ортостатического падения и существенных побочных явлений. Бета-адреноблокаторы применяются изолированно или в сочетании с салуретиками и миолитиками. Пропраналол (анаприлин, обзидан, индерал) назначается больным с хорошим состоянием сократительной функции миокарда в дозе не менее 120 мг/сутки. К препаратам, обладающим выраженным миолитическим эффектом, относятся гидрохлорид прозасина, диоксид, нитропрусид натрия. Два последних лекарственных средства наиболее часто применяются при высоком стабильном артериальном давлении. В период ремиссии заболеваний можно рекомендовать санаторно-курортное лечение.
Трудоспособность определяется стадией и формой течения заболевания, наличием осложнений. В стадии хронической почечной недостаточности больные нетрудоспособны и нуждаются в переводе на инвалидность.
Нефротический синдром – симптомокомплекс, характеризующийся выраженной протеинурией, диспротеинемией, гипопротеинемией (в основном за счет гипоальбуминемии), гиперлипидемией (гиперхолестеринемией) и отеками.
Нефротический синдром наблюдается при хроническом гломерулонефрите, амилоидозе, малярии, сепсисе, туберкулезе, коллагенозах, сахарном диабете и некоторых других заболеваниях. В более редких случаях причину возникновения нефротического синдрома установить сразу не удается, однако в большинстве из них детальный анализ анамнестических данных и тщательное обследование больного позволяют выявить хронический гломерулонефрит, в результате которого и возник нефротический синдром. Чаще такие формы нефротического синдрома наблюдаются у детей. Те же случаи, когда причина развития дистрофических явлений в почках остается неясной, обозначаются как липоидный нефроз.
Считается, что причиной нефротического синдрома являются резкие расстройства обмена веществ, в основном жирового и белкового, с последующим нарушением трофики и проницаемости стенки капилляров клубочков. Белковые частицы и липоиды, в большом количестве содержавшиеся в первичной моче этих больных, инфильтрируют стенку канальцев, вызывая грубые дистрофические изменения в эпителиальных клетках. Большое значение в развитии хронического нефротического синдрома отводится также аутоиммунному механизму, что подтверждается, в частности, экспериментами на животных. Так, в экспериментах при введении кроликам малых доз нефротической сыворотки возникал нефрит, при введении больших доз наблюдалась картина, характерная для нефротического синдрома.
Патологическая анатомия. Помимо изменений, свойственных основному заболеванию, выявляются следующие морфологические признаки нефротического синдрома. Почки увеличены в объеме («большие белые почки»), их капсула снимается легко. При гистологическом исследовании выявляются дистрофические изменения эпителия канальцев, особенно извитых. В базальных частях эпителиальных клеток видно отложение липидов. Наблюдается дистрофия клубочков, особенно характерны изменения подоцитов и эндотелиальных клеток, с которыми и связывается нарушение проницаемости в клубочковые мембраны.
Клиническая картина. Основной и нередко единственной жалобой больных являются упорные отеки. Особенно заметны отеки на лице: оно одутловатое, бледное, веки набухшие, глазные щели узкие, утром глаза открываются с трудом. Отекают также ноги, поясница, кожа живота и кистей рук. Отеки подвижны: при давлении на кожу в ней легко остается ямка, которая сравнительно быстро исчезает. Жидкость накапливается также во внутренних органах и серозных полостях. В типичных случаях артериальное давление не изменено или даже снижено.
В период нарастания отеков обычно уменьшен диурез, нередко за сутки выделяется всего 250–400 мл мочи. Она имеет высокую относительную плотность (1,030—1,040) и содержит большое количество белка – до 10–20 г/л и более (описаны случаи с содержанием в моче даже 24 г/л белка), преобладают более мелкодисперсные молекулы альбуминов. Предполагается, что в происхождении протеинурии при нефротическом синдроме имеет значение как повышение фильтрации белка плазмы через стенку капилляров клубочков, так и нарушение реабсорбции белковых молекул поврежденным эпителием канальцев. В осадке мочи определяется большое количество гиалиновых, зернистых и восковидных цилиндров, клеток почечного эпителия. Наличие лейкоцитов и эритроцитов в осадке мочи для нефротического синдрома нехарактерно. Обычно обнаруживаются двоякопреломляющие кристаллы холестерина, которые при заболеваниях почек, протекающих без нефротического синдрома, обычно не встречаются. Длительная и упорная протеинурия приводит к обеднению организма белком и стойкому снижению содержания его в плазме крови (в 1/2 и даже в 2 раза), причем особенно сильно уменьшается содержание альбуминов, так что альбуминглобулиновый коэффициент, в норме равный 1,2–2,0, значительно уменьшается. Несколько увеличивается содержание альфа-2-глобулинов, а также и гамма-глобулинов. Протеинурией и гипопротеинемией (особенно гипоальбуминемией) в значительной мере и объясняется возникновение отеков при нефротическом синдроме. Как установлено, потерю белка с мочой усугубляет так называемой почечный катаболизм белков плазмы (пропиолиз части сывороточного белка при его реабсорбции в канальцах), а также, по-видимому, повышенная потеря через пищеварительный тракт. Постоянным симптомом является резкая гиперлипидемия, увеличивается концентрация в плазме холестерина в 2–3 раза (до 13–15 ммоль/л и выше), фосфолипидов и нейтрального жира. Эти изменения, по-видимому, возникают вторично на фоне нарушения белкового обмена и гипопротеинемии. Таким образом, лабораторное исследование позволяет выявить три характерных признака: протеинурию, гипопротеинемию и нарушение липидного обмена – гипохолестеринемию.
Кровоочистительная функция почек при нефротическом синдроме в типичных случаях существенно не страдает, азотемии длительное время не наблюдается. Основные функциональные пробы почек длительное время остаются нормальными, однако может выявляться снижение канальцевой секреции. Биопсия почек дает очень ценные данные для выяснения природы нефротического синдрома при хронических заболеваниях почек.
Течение. Если основное заболевание не прогрессирует, – длительное, годами. Временами, чаще под влиянием присоединившейся инфекции, наблюдается усиление отеков и мочевого синдрома. Вообще больные с нефротическим синдромом чувствительны к кокковой инфекции. У них нередко наблюдаются повторные пневмонии, рожистые воспаления кожи, от которых раньше, до открытия антибиотиков, такие больные умирали. Отмечено также более легкое возникновение у них сосудистых тромбозов. Прогноз во многом определяется основным заболеванием и присоединением различных инфекций.
Лечение. Терапия основного заболевания. Дополнительно при резкой гипопротеинемии назначают диету, богатую белком (2–2,5 г/кг без учета отеков) с ограничением хлорида натрия, вводятся внутривенно плазма или концентрированный человеческий альбумин. Назначают кортикостероидные препараты (преднизолон) и иммунодепрессивные средства (имуран и др.). При выраженных отеках назначают мочегонные: фурантрил (фуросемид) по 0,04 г внутрь через 1–2 дня в сочетании с верошпироном (внутрь по 0,075—0,15 г/сутки) – до схождения отеков. В период относительной ремиссии рекомендуется санаторное лечение на курортах с сухим климатом типа Байрам-Али в Средней Азии.
Амилоидоз почек служит одним из проявлений общего заболевания – амилоидной болезни, или амилоидоза.
Этиология и патогенез. Различают амилоидоз генетический (наследственный), первичный и вторичный. Вторичный амилоидоз возникает на фоне резких нарушений белкового обмена, чаще всего у больных с хроническими воспалительными заболеваниями: туберкулезом, остеомиелитом, бронхоэктатической болезнью. Реже развитие амилоидоза наблюдается при деформирующем полиартрите, лимфогранулематозе и некоторых других заболеваниях. Считается, что при всех этих заболеваниях в связи с хроническим воздействием инфекции и токсических продуктов, а также с происходящим в организме распадом тканей и лейкоцитов извращается синтез белков в ретикулоэндотелиальной системе. На каком-то этапе в процесс включается аутоиммунный механизм, вырабатываются антитела к собственным видоизмененным белкам, и комплексы антиген-антитело в виде специфической плотной амилоидной субстанции, представляющей собой соединение глобулина с мукополисахаридами, откладываются в различных органах, и прежде всего в стенках мелких сосудов и капилляров под аргирофильной мембраной, под собственной оболочкой желез, в ретикулярной строме различных органов. В результате отложения амилоида нарушается метаболизм в расположенных вблизи клетках; они и другие тканевые элементы сдавливаются, атрофируются. Генетический амилоидоз является результатом наследственных дефектов энзимных систем, выделяющихся синтезом белка. Этиология спорадически встречающегося первичного амилоидоза не установлена.
Патологическая анатомия. Наибольшие изменения при амилоидозе находят в селезенке, почках, печени, надпочечниках, желудочно-кишечном тракте, реже – в лимфатических узлах и других органах. Почки при амилоидозе увеличены, плотные, серого цвета («большая сальная почка»). При гистологическом исследовании под аргирофильной мембраной артерий и капилляров клубочков видны глыбки амилоида. Капиллярные петли запустевают, клубочки замещаются глыбками амилоида или соединительно-тканным рубчиком. Одновременно наблюдаются дистрофические изменения эпителия канальцев. Результатом далеко зашедшего процесса является амилоидно-сморщенная почка.
Кортикостероидная терапия оказывает хорошее влияние как на отечный, так и на мочевой синдром. Она может способствовать выздоровлению и предупреждать переход острого нефрита в хронический.
При наличии тенденции к повышению артериального давления и нарастанию отеков лечение кортикостероидными гормонами следует сочетать с гипотензивными и диуретическими средствами.
При осложнении острого гломерулонефрита эклампсией применяют кровопускание, вводят сульфат магния (10 мл 25 %-ного раствора) внутривенно, дают снотворные и наркотические средства (хлоралгидрат и др.). Показаны ганглиоблокаторы, например гексоний по 10–20 мг 0,5–1 мл 2%-ного раствора внутримышечно. В предэклампсическом периоде целесообразно назначение резерпина, а также урегита, гипотиазида или лазикса; последний особенно ценен в виде инъекций как обезвоживающее средство при явлениях отека мозга.
Прогноз, трудоспособность. При остром нефрите прогноз различен. Может наблюдаться полное выздоровление. Летальный исход в остром периоде заболевания бывает редко, он чаще связан с кровоизлияниями в мозг на фоне эклампсии, реже – с сердечной недостаточностью, пневмонией или острой уремией. Переход острого нефрита в хроническое заболевание наблюдается приблизительно в 1/3 случаев.
Прогноз острого нефрита в значительной степени зависит от раннего распознавания и правильного лечения заболевания. В связи с применением в последние годы кортикостероидной терапии он значительно улучшился.
В остром периоде больные нетрудоспособны и должны находится в стационаре. При типичном течении через 2–3 месяца может наступить полное выздоровление: больные могут возвратиться к трудовой деятельности даже при наличии умеренного мочевого синдрома или остаточной альбуминурии.
Весьма важно диспансерное наблюдение за лицами, перенесшими острый нефрит, так как клиническое выздоровление нередко может быть кажущимся. Особенно это важно при наличии даже умеренного мочевого синдрома. Во избежание рецидивов особенное внимание следует уделять борьбе с инфекционными очагами в организме. Необходимо в течение года избегать работы, связанной с охлаждением, особенно с действием влажного холода.
Профилактика острого нефрита в основном сводится к предупреждению и раннему энергичному лечению острых инфекционных болезней и устранению очаговой инфекции, особенно в миндалинах, предупреждению резкого охлаждения.
Хронический гломерулонефрит – длительно протекающее иммуновоспалительное двустороннее заболевание почек с клиническими проявлениями классической брайтовой болезни, приводящее к прогрессирующей гибели клубочков, снижению деятельности почек, развитию артериальной гипертонии с последующим развитием почечной недостаточности.
Этиология. Хронический нефрит может быть исходом как острого нефрита, так и первично хроническим, без предшествующей острой атаки. Нередко встречаются хронические гломерулонефриты преимущественно иммунной природы: сывороточный, вакцинный, связанный с приемом пищевых антигенов, ядов, после перенесенной травмы, охлаждения. Ряд медикаментов, помимо обычного поражения почек типа «острой» токсической почки, нередко одновременно с
лихорадкой, поражением кожи, суставов, печени и селезенки. Хронический гломерулонефрит является частым осложнением подострого септического эндокардита. Описаны случаи развития диффузного поражения почек у больных, страдающих туберкулезом, сифилисом.
Диффузные тяжелые поражения почечной паренхимы при системных аутоиммунных заболеваниях, таких как геморрагический васкулит, узелковый периартрит, системная красная волчанка.
Патогенез. При переходе нефрита в хроническую форму в прогрессировании его основная роль принадлежит реактивности макроорганизма, степени аутоиммунных нарушений.
Клиническая картина. Клиническая картина хронического гломерулонефрита полиморфна. Она включает развитие отеков, гипертонию, мочевой синдром (протеинурия, гематурия, цилиндрурия), гипопротеинемию, гиперхолестеринемию. Наиболее часто жалобы больных связаны с почечной гипертонией – нарушение зрения, развитие сердечной недостаточности, приступы кардиальной астмы; с явлениями почечной недостаточности – слабость, сухость кожи, нарушение сна, зуд, плохой аппетит; с поражением почек – боли в области поясницы, дизурические явления, никтурия и т. д. В зависимости от превалирования тех или иных синдромов Е. М. Тареев выделяет следующие формы течения хронического гломерулонефрита: злокачественный (экстракапиллярный), латентный, гипертонический, нефротический и смешанный. Общим для течения указанных форм гломерулонефрита является прогрессирующий характер течения с возможностью сохранения в течение длительного времени нормальной функции почек с последующим развитием хронической почечной недостаточности.
Подострый, злокачественный нефрит приводит к прогрессирующей гибели нефритов, деформации архитектоники почки.
В биопсийном материале определяется пролиферативный гломерулонефрит с фибринозно-эпителиальными полулуниями, который может развиться спустя неделю после начала заболевания. Одновременно отмечается канальцевое и интерстициальное поражение, часто обнаруживается фибриноидный некроз клубочков и артериол.
Клинически злокачественное течение нефрита можно подозревать, если через 4–6 недель остро начавшегося заболевания наблюдается снижение относительной плотности мочи, повышение содержания креатинина и индикана сыворотки крови, стабильно остается на высоких цифрах артериальное давление. Развитие отечного синдрома встречается редко при подостром нефрите. Основным клиническим проявлением являются быстрое и стойкое снижение функции почек, нарастающие изменения глазного дна. Прогноз злокачественного течения гломерулонефрита остается крайне тяжелым.
Латентный хронический диффузный гломерулонефрит. Это довольно частая форма, проявляющаяся обычно лишь слабо выраженным мочевым синдромом без артериальной гипертонии и отеков. Латентная форма хронического гломерулонефрита приобретает драматическую форму в случаях, когда выявляется хроническая почечная недостаточность, казалось бы, среди полного здоровья. Годами эти больные сохраняют полную работоспособность, не считая себя больными. Наиболее часто болезнь выявляется при диспансеризации, когда врач обращает внимание на мочевой синдром (гематурия, протенкурия), снижение относительной плотности, никтурию, незначительное повышение артериального давления. Иногда выявляются повышенная скорость оседания эритроцитов, гипопротеинемия, гиперхолестеринемия. Эта форма хронического гломерулонефрита имеет длительное течение (30–40 лет), особенно в случаях, когда больным удается исключить провоцирующие обострение факторы.
Нефротическая форма (ранее называвшаяся нефрозонефритом, или паренхиматозным нефритом). При нефротической форме характерна большая протеинурия (более 3,5 г/сутки), гипопротеинемия и диспротеинемия с уменьшением содержания альбуминов в плазме, значительным снижением альбумино-глобулинового коэффициента, высокая гиперхолестеринемия 104–260 ммоль/л (400—1 тыс. мг%), выделение с мочой двояко преломляющихся субстанций. Большей частью у больных с этой формой наблюдаются массивные отеки, обусловленные в основном снижением коллоидоосмотического давления белков плазмы, связанным с гипопротеинемией (50–40 г/л (5–4 г %)) и диспротеинемией, вследствие потери белка с мочой. Отечный синдром развивается постепенно. Обычно по утрам появляются отечность под глазами, отеки лодыжек. В дальнейшем отеки становятся постоянными, распространяются на туловище, присоединяется гидроторакс, асцит, гидроперикард. В этой стадии наблюдаются сухость кожи, снижение ее эластичности, гипертрофия мышц. Степень протеинурии коррелирует с нарастанием содержания триглицеридов и свободного холестерина в плазме крови, с образованием крупных липопротеидов – латексценция.
Для нефротической формы хронического гломерулонефрита, в отличие от чистого липоидного нефроза, характерно сочетание нефротического синдрома с признаками воспалительного поражения почек: умеренной гематурией и снижением фильтрационной функции. Повышения артериального давления, как правило, не наблюдается. Клиническая картина заболевания может долго определяться нефротическим синдромом, и только в дальнейшем наступает прогрессирование нефрита с нарушением азотовыделительной функции почек и артериальной гипертонией.
Гипертоническая форма хронического нефрита. В течение длительного времени ведущим и часто единственным симптомом является гипертония.
Под влиянием различных факторов – холода, эмоциональных воздействий – артериальное давление может подвергаться большим колебаниям. При осмотре обращают на себя внимание приподнимающийся верхушечный толчок, расширение относительной тупости сердца влево, акцент II тона над аортой, у части больных выслушивается ритм галопа. При прогрессировании сердечной недостаточности развивается клиника застоя по малому кругу, возможны кровохарканье, приступы сердечной астмы, в редких случаях – отек легких. Как правило, гипертония при хроническом гломерулонефрите, в отличие от подострого, не приобретает злокачественного характера. Она не склонна к быстрому прогрессированию; артериальное давление, кровоизлияния в сетчатку редки; экссудация и отеки сетчатки, так же как и изменения сосочков зрительного нерва, появляются только в финале болезни. Что касается патогенеза артериальной гипертонии при этой форме нефрита, то имеются более или менее определенные данные, указывающие на значение почечно-ишемического, ренин-гипертензивного механизма ее развития. С прогрессированием болезни развивается хроническая почечная недостаточность, и болезнь может приобрести черты злокачественной гипертонии.
Смешанная форма диффузного гломерулонефрита. Для смешанной формы хронического гломерулонефрита характерно наличие большинства основных синдромов и симптомов классического паренхиматозного нефрита: отеки, гематурия, протеинурия, гипертония, однако степень их проявления в большинстве случаев не столь выражена, как это отмечается при других формах. В большинстве случаев клинике обострений хронического гломерулонефрита свойственно преобладание того или иного синдрома. Нередко длительно могут наблюдаться только мочевые симптомы и самочувствие больных не нарушено. В это время только при специальных исследованиях обнаруживаются некоторые нарушения функции почек, в первую очередь снижение фильтрации, а затем и концентрационной способности. Значительно позже появляются признаки хронической почечной недостаточности – хронической азотемической уремии.
Внезапное обострение заболевания, характеризующееся ухудшением общего самочувствия, с выраженным проявлением основных синдромов, снижением удельного веса мочи, повышение экскреции белка – все это может указывать на неблагоприятную эволюцию заболевания. Прогрессирование заболевания в дальнейшем проявляется повышением уровня мочевины, креатинина, индикана в плазме крови, снижением клубочковой фильтрации и возрастанием фильтрационной фракции.
Таблица № 1. Критерии диагностики основных форм хронического нефрита


Прогноз. Исходом хронического гломерулонефрита является сморщивание почек с развитием хронической почечной недостаточности – хронической уремии. Этот исход до последнего времени наблюдался во всех случаях хронического гломерулонефрита, правда в различные сроки от начала заболевания. За последние 10–15 лет прогноз хронического гломерулонефрита в связи с введением в клиническую практику иммунодепрессивной терапии стал значительно лучше. При применении иммунодепрессивной терапии, в частности кортикостероидной, в 70–80 % случаев наблюдается положительный эффект, причем в 14–18 % случаев – полная ремиссия болезни с исчезновением как общих, так и мочевых симптомов.
Профилактика и лечение. Основной профилактикой хронического нефрита является полноценное лечение острого нефрита. В этом отношении огромное значение имеет прежде всего ранняя и точная диагностика острого гломерулонефрита, что дает возможность своевременно госпитализировать и эффективно лечить больного. Имеет значение и устранение очагов инфекции (удаление миндалин, санация полости рта). Длительные диетические ограничения (соли и белков) не предупреждают перехода острого нефрита в хронический.
Больные хроническим нефритом должны избегать охлаждения, особенно воздействия влажного холода. Им рекомендуется сухой и теплый климат. При удовлетворительном общем состоянии и отсутствии осложнений показано санаторно-курортное лечение на курортах Средней Азии (Байроли-Али) или на южном берегу Крыма (Ялта). Постельный режим необходим только в период значительных отеков или сердечной недостаточности, а также в терминальной стадии при симптомах уремии. Режим при хроническом нефрите в фазе ремиссии должен быть щадящим. Противопоказаны тяжелый физический труд, работа в ночную смену, на открытом воздухе в холодное время года, в горячих цехах, душных, плохо проветриваемых помещениях. Больные должны избегать нервного и физического переутомления. В случаях возникновения острого интеркуррентного заболевания рекомендуется соответствующее лечение с применением антимикробных лекарственных средств на фоне постельного режима.
В лечении больных хроническим гломерулонефритом существенное значение имеет диета, которая должна варьироваться в зависимости от формы и стадии заболевания. При нефротической и смешанной формах (при наличии отеков) содержание хлорида натрия в диете должно быть ограничено до 1,5–2,5 г; при условии достаточной выделительной функции почек диета должна содержать достаточное количество белков – до 2–2,5 г на 1 кг массы тела больного, что способствует положительному азотистому балансу и компенсации белковых потерь. При гипертонической форме рекомендуется умеренно ограничивать прием хлорида натрия – до 5 г/сутки при нормальном содержании в рационе белков и углеводов. Латентная форма существенных ограничений в питании больных не требует, питание должно быть полноценным, разнообразным и богатым витаминами. Витамины (С, комплекс В, А) должны входить в рацион и при других формах хронического гломерулонефрита. Следует указать, что длительная безбелковая диета без соли не предупреждает прогрессирования нефрита и плохо отражается на общем состоянии больных.
Большинство клиницистов рекомендует 35–50 г белка в день плюс количество белка, теряемого с мочой за сутки. Количество пищевого белка уменьшают лишь при снижении почечных функций. Диета должна быть богата фруктовыми и овощными соками, содержащими витамины А, группы В, С и Е.
Особенно большое значение имеет кортикостероидная терапия, являющаяся основой патогенетической терапии при этом заболевании. Начинают лечение обычно с 15–20 мг преднизолона, при необходимости увеличивая дозу до 60–80 мг/сутки, затем постепенно ее снижают. При обострении заболевания курсы лечения глюкокортикоидами повторяют.
Иногда применяется прерывистая терапия глюкокортикоидами – 3 дня (подряд) в неделю, которая снижает возможность развития «стероидного кушингоида», стероидных язв, сохраняя лечебный эффект гормонов.
Применение кортикостероидов ведет к уменьшению воспалительного процесса в клубочках почек, что способствует улучшению фильтрации и выражается в уменьшении мочевого синдрома, гематурии и протеинурии, что вторично ведет к улучшению и белкового состава крови. При лечении кортикостероидами нередко могут развиться синдром Кушинга, стероидные язвы, остеопороз.
Противопоказанием к применению кортикостероидов у больных хроническим нефритом является прогрессирующая азотемия. При противопоказаниях к применению кортикостероидов или неэффективности лечения рекомендуются негормональные иммунодепрессанты: азапмоприн (имурана), 6-меркаптопурин. Эти препараты более эффективны, однако они вызывают выраженную лейкопению. Лечение ими лучше переносится при одновременном применении преднизолона в умеренной дозе по 10–30 мг/сутки, что предупреждает токсические влияния негормональных иммунодепрессантов на лейкопоэз.
В последних стадиях – при склерозе клубочков и атрофии с высокой гипертонией – иммунодепрессанты и стероидные гормоны противопоказаны, так как иммунологической активности в клубочках уже нет и продолжение такого лечения только усугубляет гипертонию.
Легким эффектом иммунодепрессантов обладают препараты 4-аминохинолинового ряда – хингамин (делагил, резохин, хлорохин), гидроксихлорохин (плаквенил). Резохин (хлорохин) применяют по 0,25 г 1–3 раза в день в течение 2–8 месяцев. Для лечения воспалительных изменений в почечной паренхиме применяются также нестероидные противовоспалительные препараты, в частности индометацин, который, помимо обезболивающего и жаропонижающего действия, воздействует на медиаторы иммунологического повреждения. Под влиянием индометацина снижается протеинурия. Назначают его внутрь по 25 мг 2–3 раза в день, затем в зависимости от переносимости увеличивают дозу до 100–150 мг/сутки. Лечение проводится длительно, в течение нескольких месяцев. Одновременное применение стероидных гормонов и индометацина позволяет значительно снизить дозу кортикостероидов с постепенной полной отменой.
В последние годы для лечения хронического диффузного гломерулонефрита стали применять антикоагулянты.
В случае упорных отеков при нефротической и смешанной формах рекомендуется одновременно с назначением преднизолона назначать:
– различные салуретики: фуросемид, этакриновую кислоту и т. д.;
– конкурентные блокаторы альдостерона (верошпирон, альдактон).
При упорных отеках на фоне гипопротеинемии можно рекомендовать применение высокомолекулярного углевода – полиглюкина (декстрана) в виде капельного внутривенного введения 500 мл раствора, что приводит к повышению коллоидно-осмотического давления плазмы крови, способствует перемещению жидкости из тканей в кровь и вызывает диурез. При нарушении белкового обмена, особенно при нефротической форме, показано применение анаболических стероидных гормонов, особенно в сочетании с пластическими продуктами (аминокислоты, мононуклеотиды и т. д.). Анаболические стероиды-гормоны можно назначать в виде инъекционной формы – ретаболил 50 мг внутримышечно один раз в 10–15 дней или метандростенагон орально 10–15 мг в течение 2–3 недель. Имеются указания, что в ранней стадии почечной недостаточности анаболические гормоны способствуют улучшению белкового обмена.
При лечении гипертонической формы хронического гломерулонефрита могут быть использованы гипотензивные средства, применяемые при лечении гипертонической болезни: резерпин, комбинация резерпина с бета-адреноблокаторами, миолитики.
Можно использовать и ганглиоблокирующие препараты, в частности гексоний и пентамин. Однако следует избегать резких колебаний артериального давления и ортостатического его падения, которые могут приводить к ухудшению почечного кровотока и фильтрационной функции почек. Поэтому эти гипотензивные препараты желательно комбинировать с резерпином, что уменьшает склонность к резким колебаниям артериального давления и ведет к более медленному и постепенному улучшению функции почек и уменьшению других симптомов, связанных с гипертонией (изменения глазного дна, сердца и т. д.). Показано при гипертонической форме хронического гломерулонефрита и применение препаратов, подавляющих синтез катехоламинов в надпочечниках. Это α-метилдофа (альдамет, допегит), которые назначают по 750—1 тыс. мг/сутки. Эти препараты способствуют постепенному снижению артериального давления, не вызывают резких его колебаний и ортостатического падения и существенных побочных явлений. Бета-адреноблокаторы применяются изолированно или в сочетании с салуретиками и миолитиками. Пропраналол (анаприлин, обзидан, индерал) назначается больным с хорошим состоянием сократительной функции миокарда в дозе не менее 120 мг/сутки. К препаратам, обладающим выраженным миолитическим эффектом, относятся гидрохлорид прозасина, диоксид, нитропрусид натрия. Два последних лекарственных средства наиболее часто применяются при высоком стабильном артериальном давлении. В период ремиссии заболеваний можно рекомендовать санаторно-курортное лечение.
Трудоспособность определяется стадией и формой течения заболевания, наличием осложнений. В стадии хронической почечной недостаточности больные нетрудоспособны и нуждаются в переводе на инвалидность.
Нефротический синдром – симптомокомплекс, характеризующийся выраженной протеинурией, диспротеинемией, гипопротеинемией (в основном за счет гипоальбуминемии), гиперлипидемией (гиперхолестеринемией) и отеками.
Нефротический синдром наблюдается при хроническом гломерулонефрите, амилоидозе, малярии, сепсисе, туберкулезе, коллагенозах, сахарном диабете и некоторых других заболеваниях. В более редких случаях причину возникновения нефротического синдрома установить сразу не удается, однако в большинстве из них детальный анализ анамнестических данных и тщательное обследование больного позволяют выявить хронический гломерулонефрит, в результате которого и возник нефротический синдром. Чаще такие формы нефротического синдрома наблюдаются у детей. Те же случаи, когда причина развития дистрофических явлений в почках остается неясной, обозначаются как липоидный нефроз.
Считается, что причиной нефротического синдрома являются резкие расстройства обмена веществ, в основном жирового и белкового, с последующим нарушением трофики и проницаемости стенки капилляров клубочков. Белковые частицы и липоиды, в большом количестве содержавшиеся в первичной моче этих больных, инфильтрируют стенку канальцев, вызывая грубые дистрофические изменения в эпителиальных клетках. Большое значение в развитии хронического нефротического синдрома отводится также аутоиммунному механизму, что подтверждается, в частности, экспериментами на животных. Так, в экспериментах при введении кроликам малых доз нефротической сыворотки возникал нефрит, при введении больших доз наблюдалась картина, характерная для нефротического синдрома.
Патологическая анатомия. Помимо изменений, свойственных основному заболеванию, выявляются следующие морфологические признаки нефротического синдрома. Почки увеличены в объеме («большие белые почки»), их капсула снимается легко. При гистологическом исследовании выявляются дистрофические изменения эпителия канальцев, особенно извитых. В базальных частях эпителиальных клеток видно отложение липидов. Наблюдается дистрофия клубочков, особенно характерны изменения подоцитов и эндотелиальных клеток, с которыми и связывается нарушение проницаемости в клубочковые мембраны.
Клиническая картина. Основной и нередко единственной жалобой больных являются упорные отеки. Особенно заметны отеки на лице: оно одутловатое, бледное, веки набухшие, глазные щели узкие, утром глаза открываются с трудом. Отекают также ноги, поясница, кожа живота и кистей рук. Отеки подвижны: при давлении на кожу в ней легко остается ямка, которая сравнительно быстро исчезает. Жидкость накапливается также во внутренних органах и серозных полостях. В типичных случаях артериальное давление не изменено или даже снижено.
В период нарастания отеков обычно уменьшен диурез, нередко за сутки выделяется всего 250–400 мл мочи. Она имеет высокую относительную плотность (1,030—1,040) и содержит большое количество белка – до 10–20 г/л и более (описаны случаи с содержанием в моче даже 24 г/л белка), преобладают более мелкодисперсные молекулы альбуминов. Предполагается, что в происхождении протеинурии при нефротическом синдроме имеет значение как повышение фильтрации белка плазмы через стенку капилляров клубочков, так и нарушение реабсорбции белковых молекул поврежденным эпителием канальцев. В осадке мочи определяется большое количество гиалиновых, зернистых и восковидных цилиндров, клеток почечного эпителия. Наличие лейкоцитов и эритроцитов в осадке мочи для нефротического синдрома нехарактерно. Обычно обнаруживаются двоякопреломляющие кристаллы холестерина, которые при заболеваниях почек, протекающих без нефротического синдрома, обычно не встречаются. Длительная и упорная протеинурия приводит к обеднению организма белком и стойкому снижению содержания его в плазме крови (в 1/2 и даже в 2 раза), причем особенно сильно уменьшается содержание альбуминов, так что альбуминглобулиновый коэффициент, в норме равный 1,2–2,0, значительно уменьшается. Несколько увеличивается содержание альфа-2-глобулинов, а также и гамма-глобулинов. Протеинурией и гипопротеинемией (особенно гипоальбуминемией) в значительной мере и объясняется возникновение отеков при нефротическом синдроме. Как установлено, потерю белка с мочой усугубляет так называемой почечный катаболизм белков плазмы (пропиолиз части сывороточного белка при его реабсорбции в канальцах), а также, по-видимому, повышенная потеря через пищеварительный тракт. Постоянным симптомом является резкая гиперлипидемия, увеличивается концентрация в плазме холестерина в 2–3 раза (до 13–15 ммоль/л и выше), фосфолипидов и нейтрального жира. Эти изменения, по-видимому, возникают вторично на фоне нарушения белкового обмена и гипопротеинемии. Таким образом, лабораторное исследование позволяет выявить три характерных признака: протеинурию, гипопротеинемию и нарушение липидного обмена – гипохолестеринемию.
Кровоочистительная функция почек при нефротическом синдроме в типичных случаях существенно не страдает, азотемии длительное время не наблюдается. Основные функциональные пробы почек длительное время остаются нормальными, однако может выявляться снижение канальцевой секреции. Биопсия почек дает очень ценные данные для выяснения природы нефротического синдрома при хронических заболеваниях почек.
Течение. Если основное заболевание не прогрессирует, – длительное, годами. Временами, чаще под влиянием присоединившейся инфекции, наблюдается усиление отеков и мочевого синдрома. Вообще больные с нефротическим синдромом чувствительны к кокковой инфекции. У них нередко наблюдаются повторные пневмонии, рожистые воспаления кожи, от которых раньше, до открытия антибиотиков, такие больные умирали. Отмечено также более легкое возникновение у них сосудистых тромбозов. Прогноз во многом определяется основным заболеванием и присоединением различных инфекций.
Лечение. Терапия основного заболевания. Дополнительно при резкой гипопротеинемии назначают диету, богатую белком (2–2,5 г/кг без учета отеков) с ограничением хлорида натрия, вводятся внутривенно плазма или концентрированный человеческий альбумин. Назначают кортикостероидные препараты (преднизолон) и иммунодепрессивные средства (имуран и др.). При выраженных отеках назначают мочегонные: фурантрил (фуросемид) по 0,04 г внутрь через 1–2 дня в сочетании с верошпироном (внутрь по 0,075—0,15 г/сутки) – до схождения отеков. В период относительной ремиссии рекомендуется санаторное лечение на курортах с сухим климатом типа Байрам-Али в Средней Азии.
Амилоидоз почек служит одним из проявлений общего заболевания – амилоидной болезни, или амилоидоза.
Этиология и патогенез. Различают амилоидоз генетический (наследственный), первичный и вторичный. Вторичный амилоидоз возникает на фоне резких нарушений белкового обмена, чаще всего у больных с хроническими воспалительными заболеваниями: туберкулезом, остеомиелитом, бронхоэктатической болезнью. Реже развитие амилоидоза наблюдается при деформирующем полиартрите, лимфогранулематозе и некоторых других заболеваниях. Считается, что при всех этих заболеваниях в связи с хроническим воздействием инфекции и токсических продуктов, а также с происходящим в организме распадом тканей и лейкоцитов извращается синтез белков в ретикулоэндотелиальной системе. На каком-то этапе в процесс включается аутоиммунный механизм, вырабатываются антитела к собственным видоизмененным белкам, и комплексы антиген-антитело в виде специфической плотной амилоидной субстанции, представляющей собой соединение глобулина с мукополисахаридами, откладываются в различных органах, и прежде всего в стенках мелких сосудов и капилляров под аргирофильной мембраной, под собственной оболочкой желез, в ретикулярной строме различных органов. В результате отложения амилоида нарушается метаболизм в расположенных вблизи клетках; они и другие тканевые элементы сдавливаются, атрофируются. Генетический амилоидоз является результатом наследственных дефектов энзимных систем, выделяющихся синтезом белка. Этиология спорадически встречающегося первичного амилоидоза не установлена.
Патологическая анатомия. Наибольшие изменения при амилоидозе находят в селезенке, почках, печени, надпочечниках, желудочно-кишечном тракте, реже – в лимфатических узлах и других органах. Почки при амилоидозе увеличены, плотные, серого цвета («большая сальная почка»). При гистологическом исследовании под аргирофильной мембраной артерий и капилляров клубочков видны глыбки амилоида. Капиллярные петли запустевают, клубочки замещаются глыбками амилоида или соединительно-тканным рубчиком. Одновременно наблюдаются дистрофические изменения эпителия канальцев. Результатом далеко зашедшего процесса является амилоидно-сморщенная почка.
Конец бесплатного ознакомительного фрагмента
