Страница:
Главный и добавочный протоки изнутри выстланы цилиндрическим эпителием с бокаловидными клетками. Наружный слой главного протока состоит из фиброзной ткани с эластическими и гладкомышечными волокнами. Протоки первого и второго порядка выстланы низким цилиндрическим эпителием, междольковые протоки имеют кубический эпителий, вставочные отделы – плоский эпителий.
Структурной единицей поджелудочной железы принято считать ацинус – группу клеток, секретирующих панкреатические ферменты. Ацинусы в виде грозди винограда образуют экзокринную часть поджелудочной железы. В свою очередь 5–8 ацинозных клеток своими верхушками (апиксами) обращены в центральную полость ацинуса. В эту полость входят мельчайшие протоки. Размер ацинуса составляет около 20 мкм.
Кроме того, по всей поджелудочной железе рассеяны так называемые островки полигональных клеток (Лангерганса), состоящие из трех видов клеток: альфа (20 %), бета (75 %) и дельта. Альфа-клетки выделяют глюкагон, бета-клетки выделяют инсулин, дельта-клетки – соматостатин.
Экзокринная функция поджелудочной железы выражается в выделении в двенадцатиперстную кишку панкреатического сока. Панкреатический сок содержит ферменты, слизистые вещества, электролиты (натрий, калий, кальций, фосфор, хлор), микроэлементы (цинк, медь, марганец), гидрокарбонат. Общее количество сока может составить 1000–4000 мл/сутки. В двенадцатиперстную кишку выделяется приблизительно половина этого количества (Spiro, 1977 г.).
Экзокринная панкреатическая секреция подразделяется на межпищеварительную и пищеварительную. Межпищеварительная экзокринная секреция осуществляется циклически. Каждый цикл длится около 90 мин и координирован с моторикой желудочно-кишечного тракта, секрецией желудком кислоты, сокращением желчного пузыря. I фаза характеризуется отсутствием моторики двенадцатиперстной кишки и секреторной активности поджелудочной железы, желудка и поступления желчи. Во II фазе секреция и моторная активность нарастают, достигая максимума непосредственно перед III фазой, которая представляет собой 5—10-минутный период сократительной активности, следующей вниз по пищеварительному тракту. IV фаза представляет собой кратковременную нерегулярную активность, переходящую в состояние покоя.
Прием пищи преобразует межпищеварительную периодическую панкреатическую секрецию в постоянную секрецию, которая на 75 % превышает максимальный уровень секреции в конце II фазы (E. P. DiMAGNO, 1989 г.).
Ферменты панкреатического сока, участвующие в переваривании пищи, выделяются ацинозными клетками. Эти клетки синтезируют ферменты из аминокислот, глюкозы, липидов и других элементов, поступающих к ним с кровью и лимфой. Синтез белка в ацинозных клетках происходит постоянно, даже в покое ферменты ритмично выделяются в систему протоков. Поджелудочная железа содержит около 3 г ферментных белков.
Панкреатические ферменты подразделяются на амилолитические, протеолитические, липолитические и нуклеолитические.
Альфа-амилаза расщепляет крахмал и гликоген до дисахаридов, которые далее трансформируются с помощью инвертазы, мальтазы и лактазы до соответствующих моносахаридов.
К панкреатическим ферментам, участвующим в липолизе, относят липазу (гидролиз триглицеридов), фосфорилазу А (гидролиз фосфолипидов) и карбоксилэстеразу (гидролиз эфиров жирных кислот).
Протеолитические ферменты синтезируются ацинозными клетками в виде проферментов, которые активируются в кишечнике. Так, трипсиноген под воздействием энтерокиназы активируется до состояния трипсина. Аналогичные превращения происходят и с другими эндопептидазами – химотрипсиногенами, проэластазами и экзопепетидазами – карбоксипептидазами, аминопептидазами и другими белками (например, калликреиногеном).
К нуклеолитическим ферментам панкреатического сока относятся фосфодиэстеразы – рибонуклеаза (гидролиз рибонуклеиновой кислоты) и дезоксирибонуклеаза.
Кроме того, в панкреатическом соке обнаруживаются и другие белки, не играющие роли в пищеварении: секреторный и иммуноглобулин А, карциноэмбриональный антиген, лактоферрин и др.
Секреция кислых мукополисахаридов эпителием протоков в физиологических условиях защищает эпителий от влияния ферментов.
Секреция электролитов, воды и гидрокарбоната осуществляется преимущественно в дистальных отделах протоков. Источником синтеза гидрокарбонатов является углекислый газ крови и воды с помощью карбоангидразы в клетках эпителия вставочных отделов и других мелких протоков поджелудочной железы. Гидрокарбонаты диффундируют через эпителий из-за разницы потенциалов между протоками и кровью, а в обратном направлении диффундируют хлориды. Максимальная концентрация гидрокарбоната в дуоденальном содержимом составляет 100–150 ммоль/л.
«Натриевый насос» обеспечивает диффузию ионов натрия из эпителия протоков в состав панкреатического сока, а ионов водорода в кровь. Натрий составляет 95 % всех катионов панкреатического сока. Концентрация калия в панкреатическом соке приблизительно такая же, как и в плазме крови.
Секреция воды происходит пассивно по разнице осмотического давления в крови – чем больше осмотическое давление в протоках, тем больше в них поступает воды из крови.
Регуляция экзокринной функции поджелудочной железы осуществляется взаимодействием нервных и гормональных механизмов.
Парасимпатическая часть вегетативной системы стимулирует секрецию поджелудочной железы. Холинергические волокна в составе блуждающих нервов подходят к поджелудочной железе непосредственно и через чревный узел, а также в виде ветвей от двенадцатиперстной кишки, обеспечивая таким образом структурно-энтеропанкреатический рефлекс секреции. Адренергические нервы ингибруют секрецию, снижая ток крови в сосудах железы (норадренолин тормозит панкреатическую секрецию, сужая сосуды) и напрямую влияя на ацинозные клетки. (VaysseN., Chayvialle J. F., Pradayrol L. Et al., 1981 г.)). Кроме того, существует пептидергические влияния на структуры поджелудочной железы, приводящие к стимуляции и ингибированию секреции. В пептидергическую систему входят нервные волокна и ганглионарные клетки, которыми вырабатываются биологически активные пептиды – вазоактивный интестинальный полипепетид (ВИП), холецистокинин, панкреатический полипептид (ПП) и др.
Активное участие в регуляции панкреатической секреции принимают гормоны (гастроинтестинальные). Одни из них стимулируют, другие (избирательно или совместно) тормозят секрецию белка и бикарбоната (табл. № 1).
Таблица № 1. Гоморальная регуляция экзокринной панкреатической секреции (Г. Р. Гринберг, 1989 г.).
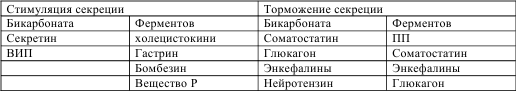
Рефлексы и гормоны определенным образом влияют на секреторную функцию поджелудочной железы в каждой фазе процесса – центральной, желудочной и кишечной. В центральной фазе, как и в фазе желудочной, поджелудочной железой выделяется панкреатический сок, богатый ферментами и содержащий относительно мало воды, гидрокарбоната и электролитов. Объясняется данный факт влиянием на ацинозные клетки парасимпатической активацией и гастрина.
В кишечной фазе поступление хлористоводородной кислоты и продуктов переваривания пищи в двенадцатиперстную кишку ведет к выбросу гастроинтестинальных гормонов (эндогенных полипепетидов), обладающих широким спектром биологической активности. В частности, происходит выделение холецистокинина и секретина. Секретин и холецистокинин действуют, потенцируя друг друга. Под их влиянием происходит изменение содержания панкреатического сока в сторону усиления присутствия в нем бикарбоната, воды и электролитов.
Желчь, попадая в двенадцатиперстную кишку, стимулирует панкреатическую секрецию. Секретин и холецистокинин являются в свою очередь стимуляторами выделения желчи. Физиологическим торможением процесса секреции поджелудочной железы является прекращение опорожнения желудка. Тормозные импульсы возникают в подвздошной и толстой кишке, когда прекращается всасывание воды и электролитов (Harper, Scratcherd, 1979 г.).
Эндогенная функция поджелудочной железы определяется функционированием клеток островков Лангерганса: альфа-клетками, бета-клетками и дельта-клетками.
Глюкагон активирует гликогенолиз в сердечной мышце и печени, стимулирует глюконеогенез, а также триглицеридлипазную активность в жировой ткани, что приводит к мобилизации жирных кислот. Глюкагон также увеличивает поступление аминокислот в печень.
Инсулин усиливает транспорт глюкозы через мембрану мышечных клеток. Инсулин стимулирует биосинтез белка, углеводов и жиров. Инсулин увеличивает скорость синтеза РНК в мышцах. Со стимуляцией гликогенеза и липогенеза происходит понижение уровня глюкозы в сыворотке крови. Абсолютный или относительный недостаток инсулина является причиной сахарного диабета.
Соматостатин тормозит секрецию глюкагона и инсулина. (Waldhause et al., 1977 г.). Его секреция стимулируется глюкозой, аргинином, лейцином, кальцием, холецистокинином и глюкагоном, тормозится адреналином. Недостаточное выделение соматостатина приводит к усиленному всасыванию пищи и гипергликемии, а затем и гипергликемии (Orci, Unger, 1975 г.).
Болезни желудка и двенадцатиперстной кишки
Язвенная болезнь желудка
Структурной единицей поджелудочной железы принято считать ацинус – группу клеток, секретирующих панкреатические ферменты. Ацинусы в виде грозди винограда образуют экзокринную часть поджелудочной железы. В свою очередь 5–8 ацинозных клеток своими верхушками (апиксами) обращены в центральную полость ацинуса. В эту полость входят мельчайшие протоки. Размер ацинуса составляет около 20 мкм.
Кроме того, по всей поджелудочной железе рассеяны так называемые островки полигональных клеток (Лангерганса), состоящие из трех видов клеток: альфа (20 %), бета (75 %) и дельта. Альфа-клетки выделяют глюкагон, бета-клетки выделяют инсулин, дельта-клетки – соматостатин.
Экзокринная функция поджелудочной железы выражается в выделении в двенадцатиперстную кишку панкреатического сока. Панкреатический сок содержит ферменты, слизистые вещества, электролиты (натрий, калий, кальций, фосфор, хлор), микроэлементы (цинк, медь, марганец), гидрокарбонат. Общее количество сока может составить 1000–4000 мл/сутки. В двенадцатиперстную кишку выделяется приблизительно половина этого количества (Spiro, 1977 г.).
Экзокринная панкреатическая секреция подразделяется на межпищеварительную и пищеварительную. Межпищеварительная экзокринная секреция осуществляется циклически. Каждый цикл длится около 90 мин и координирован с моторикой желудочно-кишечного тракта, секрецией желудком кислоты, сокращением желчного пузыря. I фаза характеризуется отсутствием моторики двенадцатиперстной кишки и секреторной активности поджелудочной железы, желудка и поступления желчи. Во II фазе секреция и моторная активность нарастают, достигая максимума непосредственно перед III фазой, которая представляет собой 5—10-минутный период сократительной активности, следующей вниз по пищеварительному тракту. IV фаза представляет собой кратковременную нерегулярную активность, переходящую в состояние покоя.
Прием пищи преобразует межпищеварительную периодическую панкреатическую секрецию в постоянную секрецию, которая на 75 % превышает максимальный уровень секреции в конце II фазы (E. P. DiMAGNO, 1989 г.).
Ферменты панкреатического сока, участвующие в переваривании пищи, выделяются ацинозными клетками. Эти клетки синтезируют ферменты из аминокислот, глюкозы, липидов и других элементов, поступающих к ним с кровью и лимфой. Синтез белка в ацинозных клетках происходит постоянно, даже в покое ферменты ритмично выделяются в систему протоков. Поджелудочная железа содержит около 3 г ферментных белков.
Панкреатические ферменты подразделяются на амилолитические, протеолитические, липолитические и нуклеолитические.
Альфа-амилаза расщепляет крахмал и гликоген до дисахаридов, которые далее трансформируются с помощью инвертазы, мальтазы и лактазы до соответствующих моносахаридов.
К панкреатическим ферментам, участвующим в липолизе, относят липазу (гидролиз триглицеридов), фосфорилазу А (гидролиз фосфолипидов) и карбоксилэстеразу (гидролиз эфиров жирных кислот).
Протеолитические ферменты синтезируются ацинозными клетками в виде проферментов, которые активируются в кишечнике. Так, трипсиноген под воздействием энтерокиназы активируется до состояния трипсина. Аналогичные превращения происходят и с другими эндопептидазами – химотрипсиногенами, проэластазами и экзопепетидазами – карбоксипептидазами, аминопептидазами и другими белками (например, калликреиногеном).
К нуклеолитическим ферментам панкреатического сока относятся фосфодиэстеразы – рибонуклеаза (гидролиз рибонуклеиновой кислоты) и дезоксирибонуклеаза.
Кроме того, в панкреатическом соке обнаруживаются и другие белки, не играющие роли в пищеварении: секреторный и иммуноглобулин А, карциноэмбриональный антиген, лактоферрин и др.
Секреция кислых мукополисахаридов эпителием протоков в физиологических условиях защищает эпителий от влияния ферментов.
Секреция электролитов, воды и гидрокарбоната осуществляется преимущественно в дистальных отделах протоков. Источником синтеза гидрокарбонатов является углекислый газ крови и воды с помощью карбоангидразы в клетках эпителия вставочных отделов и других мелких протоков поджелудочной железы. Гидрокарбонаты диффундируют через эпителий из-за разницы потенциалов между протоками и кровью, а в обратном направлении диффундируют хлориды. Максимальная концентрация гидрокарбоната в дуоденальном содержимом составляет 100–150 ммоль/л.
«Натриевый насос» обеспечивает диффузию ионов натрия из эпителия протоков в состав панкреатического сока, а ионов водорода в кровь. Натрий составляет 95 % всех катионов панкреатического сока. Концентрация калия в панкреатическом соке приблизительно такая же, как и в плазме крови.
Секреция воды происходит пассивно по разнице осмотического давления в крови – чем больше осмотическое давление в протоках, тем больше в них поступает воды из крови.
Регуляция экзокринной функции поджелудочной железы осуществляется взаимодействием нервных и гормональных механизмов.
Парасимпатическая часть вегетативной системы стимулирует секрецию поджелудочной железы. Холинергические волокна в составе блуждающих нервов подходят к поджелудочной железе непосредственно и через чревный узел, а также в виде ветвей от двенадцатиперстной кишки, обеспечивая таким образом структурно-энтеропанкреатический рефлекс секреции. Адренергические нервы ингибруют секрецию, снижая ток крови в сосудах железы (норадренолин тормозит панкреатическую секрецию, сужая сосуды) и напрямую влияя на ацинозные клетки. (VaysseN., Chayvialle J. F., Pradayrol L. Et al., 1981 г.)). Кроме того, существует пептидергические влияния на структуры поджелудочной железы, приводящие к стимуляции и ингибированию секреции. В пептидергическую систему входят нервные волокна и ганглионарные клетки, которыми вырабатываются биологически активные пептиды – вазоактивный интестинальный полипепетид (ВИП), холецистокинин, панкреатический полипептид (ПП) и др.
Активное участие в регуляции панкреатической секреции принимают гормоны (гастроинтестинальные). Одни из них стимулируют, другие (избирательно или совместно) тормозят секрецию белка и бикарбоната (табл. № 1).
Таблица № 1. Гоморальная регуляция экзокринной панкреатической секреции (Г. Р. Гринберг, 1989 г.).

Рефлексы и гормоны определенным образом влияют на секреторную функцию поджелудочной железы в каждой фазе процесса – центральной, желудочной и кишечной. В центральной фазе, как и в фазе желудочной, поджелудочной железой выделяется панкреатический сок, богатый ферментами и содержащий относительно мало воды, гидрокарбоната и электролитов. Объясняется данный факт влиянием на ацинозные клетки парасимпатической активацией и гастрина.
В кишечной фазе поступление хлористоводородной кислоты и продуктов переваривания пищи в двенадцатиперстную кишку ведет к выбросу гастроинтестинальных гормонов (эндогенных полипепетидов), обладающих широким спектром биологической активности. В частности, происходит выделение холецистокинина и секретина. Секретин и холецистокинин действуют, потенцируя друг друга. Под их влиянием происходит изменение содержания панкреатического сока в сторону усиления присутствия в нем бикарбоната, воды и электролитов.
Желчь, попадая в двенадцатиперстную кишку, стимулирует панкреатическую секрецию. Секретин и холецистокинин являются в свою очередь стимуляторами выделения желчи. Физиологическим торможением процесса секреции поджелудочной железы является прекращение опорожнения желудка. Тормозные импульсы возникают в подвздошной и толстой кишке, когда прекращается всасывание воды и электролитов (Harper, Scratcherd, 1979 г.).
Эндогенная функция поджелудочной железы определяется функционированием клеток островков Лангерганса: альфа-клетками, бета-клетками и дельта-клетками.
Глюкагон активирует гликогенолиз в сердечной мышце и печени, стимулирует глюконеогенез, а также триглицеридлипазную активность в жировой ткани, что приводит к мобилизации жирных кислот. Глюкагон также увеличивает поступление аминокислот в печень.
Инсулин усиливает транспорт глюкозы через мембрану мышечных клеток. Инсулин стимулирует биосинтез белка, углеводов и жиров. Инсулин увеличивает скорость синтеза РНК в мышцах. Со стимуляцией гликогенеза и липогенеза происходит понижение уровня глюкозы в сыворотке крови. Абсолютный или относительный недостаток инсулина является причиной сахарного диабета.
Соматостатин тормозит секрецию глюкагона и инсулина. (Waldhause et al., 1977 г.). Его секреция стимулируется глюкозой, аргинином, лейцином, кальцием, холецистокинином и глюкагоном, тормозится адреналином. Недостаточное выделение соматостатина приводит к усиленному всасыванию пищи и гипергликемии, а затем и гипергликемии (Orci, Unger, 1975 г.).
Болезни желудка и двенадцатиперстной кишки
Язвенная болезнь желудка
Язвенная болезнь желудка – хроническое, циклически протекающее заболевание с разнообразной клинической картиной и характеризующееся возникновением в период обострения изъязвления слизистой оболочки желудка.
Несмотря на отсутствие точных статистических данных, в последние десятилетия наблюдается несомненный рост числа заболеваний язвенной болезнью среди населения.
По статистическим данным язвенная болезнь встречается в 8—10 % случаев среди мужского населения, на 1000 населения приходится 8,2 больного язвенной болезнью мужчины и 2 женщины.
Рост заболеваемости язвенной болезнью связывают с урбанизацией, нерегулярным питанием, загрязнением внешней среды и развитием тканевой гипоксии. Вторая мировая война оказала несомненное влияние на увеличение числа случаев язвенной болезни.
Заболевание встречается в любом возрасте но чаще в 30–40 лет. В последние десятилетия установлено, что язвенная болезнь нередко встречается в юношеском и детском возрасте. Убедительных данных о взаимосвязи между профессией и язвенной болезнью не имеется.
Helicobacter pylory (HP) – грамотрицательная микроаэрофильная бактерия изогнутой или спиралевидной формы с множеством жгутиков. Она обнаруживается в глубине желудочных ямок и на поверхности эпителиальных клеток, в основном под защитным слоем слизи, выстилающим слизистую оболочку желудка. Несмотря на столь необычное окружение, конкуренции Hp со стороны других микроорганизмов нет. Среди естественных резервуаров Нр-инфекции можно отметить следующие: на первом месте стоит человек, однако инфекцию можно обнаружить также и у домашних животных. Среди путей передачи можно выделить всего два: фекально-оральный и, орально-оральный, причем последний встречается в меньшей степени.
В большинстве случаев, как показывает практика, родители или близкоконтактирующие люди инфицируют ребенка хеликобактерной инфекцией еще в раннем детском возрасте, а вследствие того, что адекватное лечение отсутствует по причине низкой диагностики, данный микроорганизм у большинства людей по достижении зрелого возраста уже персистирует в организме довольно продолжительное время, вызывая сенсибилизацию организма. По этой причине у 10 детей из 100 уже в дошкольном возрасте можно выявить специальными методами наличие Нр-инфекции, а по достижении взрослого возраста, как показывает статистика, Нр обнаруживается практически у всех обследованных. Имеется связь между степенью инфицированности Нр населения и уровнем социально-экономического развития страны, причем отмечена такая особенность, что чем ниже уровень социально-экономического развития страны, тем большим становится риск инфицирования в детском возрасте.
На основании проведенных многочисленных исследований были выявлены группы риска населения, у которых риск заразиться Нр-инфекцией намного выше, чем у среднестатистического человека. Данную группу риска возглавили те профессии, которым в силу профессиональных особенностей приходится близко контактировать с инфицированными животными (доярки, работники скотобоен, рубщики мяса, рабочие мясоперерабатывающей продукции). Также риск заразиться Нр высок у медицинского персонала и врачей-гастроэнтерологов.
Следует подчеркнуть, что первая стадия наблюдается главным образом в молодом, нередко в юношеском и старшем детском возрасте.
Вторая стадия — быстрой регенерации (или раннего заживления). Характеризуется появлением органических изменений вначале в форме структурной перестройки слизистой оболочки с развитием гастродуоденита. Продолжительность около двух недель. Агрессивные факторы вновь приходят в равновесие с защитными. Эта стадия характеризуется повреждением сосудов, наличием большого количества некротических масс, выраженным отеком слизистой оболочки с лимфо– и капилляростазом. В зону повреждения привлекаются макрофаги, лимфоциты, плазматические клетки, а также факторы роста (эпидермальный, трансформирующие и др.) Происходит образование различных антител, очищение язвы от продуктов распада, идут интенсивные процессы коллагенообразования и регенерации эпителия, требующие значительных энергозатрат. Через 12 ч от начала формирования язвы определяется интенсивный синтез ДНК.
Третья стадия — медленная регенерация (или позднее заживление)
Продолжается 3–4 недели. Продолжают действовать факторы роста, иммунные механизмы, которые берут на себя основную роль защиты, более интенсивно функционируют ферментно-гормональные факторы. Все эти составляющие приводят к завершению эпителизации язвы, реконструкции микроциркуляции, дифференциации клеток и их созреванию.
Четвертая стадия сопровождается развитием осложнений либо восстановлением функциональной активности слизистой оболочки. Продолжительность этой стадии может завершиться полным восстановлением функциональной активности клеток (выздоровление или продолжительная ремиссия) или не завершиться. В последнем случае ремиссия будет короткой, заболевание часто или непрерывно рецидивирует. В эту стадию в основном действуют гормонально-ферментные факторы.
1) впервые выявленная;
2) рецидивирующая.
2. Локализация язв:
1) В желудке:
а) кардиальные и субкардиальные;
б) медиогастральные (тело, малая и большая кривизна);
в) антральные;
г) пилорического канала;
2) в двенадцатиперстной кишке (бульбарные, постбульбарные);
3. Фаза процесса:
1) обострение (язвенный дефект, признаки воспаления в желудке или двенадцатиперстной кишке)
2) затухающее обострение (язвенный рубец, остаются признаки воспаления);
3) ремиссия (язвенный рубец, исчезновение проявлений воспаления).
4. Течение болезни:
1) тяжелое (обострение 3 раза в год и чаще);
2) среднетяжелое (обострение 2 раза в год);
3) легкое (обострение 1 раз в 1–2 года и реже);
4) латентное (отсутствие клинических признаков, язва выявляется случайно при рентгенографии или гастроскопии).
5. Секреторная функция:
1) повышенная;
2) нормальная;
3) сниженная;
4) ахлоргидрия.
6. Осложнения:
1) кровотечение;
2) пенетрация;
3) перфорация;
4) рубцовая деформация;
5) стеноз пилорического отдела:
а) компенсированный;
6) субкомпенсированный;
в) декомпенсированный;
б) малигнизация (язвы желудка).
Проявления язвенной болезни весьма разнообразны. Имеют значение влияние внешней среды, пол и возраст больного, локализация язвенного дефекта, его величина. Так называемые типичные признаки язвенной болезни наблюдаются только у 25 % больных. Возможны различные варианты болевого синдрома: появление или усиление болей после еды у пациентов с дуоденальной язвой, отсутствие зависимости между приемом пищи и болевыми ощущениями, постоянные, приступообразные или эпизодические боли. К атипичным проявлениям язвенной болезни относятся также случаи безболевого течения, преобладание в клинической картине диспепсических симптомов, кишечных расстройств (запоров), снижение веса тела или астено-невротического синдрома.
Ведущим симптомом в клинической картине язвенной болезни является боль. Ее отличительными особенностями следует считать периодичность (чередование периодов обострений и ремиссий), ритмичность (связь болей с приемом пищи), сезонность (обострение болей весной и осенью, а у ряда больных – зимой и летом), нарастающий характер болей по мере развития заболевания, изменение и исчезновение болей после приема пищи, антацидов, применения тепла, антихолинергических средств, после рвоты.
По времени появления болей после приема пищи они делятся на ранние, возникающие вскоре после еды, поздние и ночные. Ранние боли свойственны язвам, расположенным в верхнем отделе желудка. Для язв антрального отдела желудка и язв двенадцатиперстной кишки характерны поздние и ночные боли, которые могут быть и «голодными», так как уменьшаются или прекращаются после еды.
Боли при язвенной болезни достигают максимальной силы на высоте пищеварения, и только «голодные» боли исчезают после приема пищи. При наличии перигастрита или перидуоденита боли усиливаются при физическом напряжении. Уменьшение или прекращение болей после случайно возникшей рвоты приводит к тому, что больные при появлении болей вызывают рвоту искусственным путем. Не менее типично для язвенной болезни молниеносное прекращение болей после приема щелочей.
Локализация болей при язвенной болезни различна и не всегда определяется местонахождением язвы. При расположении язвы на малой кривизне желудка боли чаще возникают в подложечной области, при локализации язвы в двенадцатиперстной кишке – в подложечной области справа от средней линии, а при язвах кардиального отдела желудка – за мечевидным отростком. Иррадиация болей различна: при язвах верхнего отдела желудка они иррадиируют в левую половину грудной клетки, левую лопатку и нередко приводят к неправильному диагнозу ишемической болезни сердца. Наблюдается иррадиация болей в пояснично-крестцовую область, симулирующая пояснично-крестцовый радикулит. Интенсивность болей при неосложненной язвенной болезни нерезкая и обычно не требует назначения наркотиков. Применение тепла, антиспастических и антихолинергических медикаментозных средств является достаточным для их уменьшения и прекращения.
Язвенная болезнь не всегда проявляется болями, а иногда только изжогой, чувством переполнения в подложечной области; боли же присоединяются только впоследствии.
Установлено, что обычные раздражители, при действии которых на кожных покровах возникает ощущение боли, воздействуя на стенку желудка и кишечника, не вызывают болей. Адекватными раздражителями для указанных органов являются усиленная мышечная активность, особенно спазм, повышение внутриполостного давления, воздействие на измененную слизистую оболочку желудка или двенадцатиперстной кишки активного желудочного сока. Нередко боли при язвенной болезни связаны со спазмом привратника, ишемией, вызванной спазмом сосудистой стенки, а также раздражением брюшины в связи с воспалительным процессом, возникшим при обострении болезни.
Рвота при язвенной болезни возникает без предшествующей тошноты, на высоте болей в разгар пищеварения, при различной локализации язвенного процесса частота ее варьирует. Выделение активного желудочного сока натощак нередко сопровождается рвотой. Частая утренняя рвота остатками пищи, съеденной накануне, свидетельствует о нарушении эвакуаторной функции желудка. Третьим кардинальным признаком язвенной болезни раньше считали кровотечение. Это положение в настоящее время опровергнуто. Явное кровотечение, проявляющееся кровавой рвотой или черным стулом, считается осложнением язвенной болезни. Скрытые кровотечения, как правило, сопровождают периоды обострения болезни, отличаются периодичностью и в период ремиссии не наблюдаются. Из диспепсических явлений при язвенной болезни чаще возникает изжога (у 60–80 % всех больных язвенной болезнью). С диагностической точки зрения важно, что отмечается она не только в периоды обострений, но может им предшествовать в течение ряда лет и имеет те же типичные черты, что и боли (периодичность, сезонность). Изжога связана с нарушением моторной функции пищевода и желудка. При раздувании пищевода, желудка, двенадцатиперстной кишки с помощью резинового баллона можно вызвать чувство жжения разной степени вплоть до ощущения жгучей судороги.
Аппетит при язвенной болезни не только сохранен, но иногда даже резко усилен. Так как боли обычно связаны с приемом пищи, то иногда у больных появляется страх перед едой. У некоторых лиц, страдающих язвенной болезнью, периодически наблюдается усиленное слюноотделение, которому предшествует тошнота. Нередко возникает ощущение давления и тяжести в подложечной области. Этим явлениям свойственны те же закономерности, что и болям.
Запоры нередко отмечаются в период обострения. Они обусловлены характером питания больных, постельным режимом и главным образом нервно-мышечной дистонией толстой кишки вагусного происхождения. Общее питание больных язвенной болезни болезнью не нарушено. Похудание может наблюдаться в период обострения болезни, когда больной ограничивает прием пищи из-за страха перед возникновением болей. При поверхностной пальпации живота можно обнаружить напряжение правой прямой мышцы, которое по мере затихания патологического процесса уменьшается. Симптом Менделя при обострении обычно положительный.
Определяемый натощак шум плеска может быть вызван гиперсекрецией желудочного сока либо является симптомом спазма или органического стеноза привратника желудка. Существовавшее раньше мнение, что при круглой язве кислотность желудочного сока всегда повышена, опровергнуто накопившимися фактическими данными. Гиперхлоргидрия обнаруживается примерно у 50 % лиц, страдающих язвенной болезнью. Не существует полного параллелизма между степенью кислотности желудочного содержимого и локализацией язвы. Ахлоргидрия или ахилия при язвенной болезни почти не встречаются, особенно при локализации язвы в двенадцатиперстной кишке. Несколько чаще понижение кислотности желудочного сока наблюдается при язвах желудка. Переход язвы в рак может сопровождаться прогрессирующим снижением кислотообразующей и секреторной функции желудка вплоть до полного прекращения.
Большое значение в диагностике язвенной болезни имеет определение базальной секреции. Выраженная постоянная базальная гиперсекреция, когда натощак удается получить до 500 мл чистого желудочного сока, в подавляющем большинстве случаев обусловлена локализацией язвы в пилорическом отделе желудка или двенадцатиперстной кишке. Секреторный аппарат желудка при язвенной болезни может быть в состоянии парабиоза, поэтому максимальная степень секреции и кислотности не всегда выявляется сильным раздражителем.
Несмотря на отсутствие точных статистических данных, в последние десятилетия наблюдается несомненный рост числа заболеваний язвенной болезнью среди населения.
По статистическим данным язвенная болезнь встречается в 8—10 % случаев среди мужского населения, на 1000 населения приходится 8,2 больного язвенной болезнью мужчины и 2 женщины.
Рост заболеваемости язвенной болезнью связывают с урбанизацией, нерегулярным питанием, загрязнением внешней среды и развитием тканевой гипоксии. Вторая мировая война оказала несомненное влияние на увеличение числа случаев язвенной болезни.
Заболевание встречается в любом возрасте но чаще в 30–40 лет. В последние десятилетия установлено, что язвенная болезнь нередко встречается в юношеском и детском возрасте. Убедительных данных о взаимосвязи между профессией и язвенной болезнью не имеется.
Этиология
К факторам риска, способствующим язвообразованию, можно отнести конституционально-наследственные особенности (0 группа крови, HLA-B5 антиген, снижение активности a1-антитрипсина), инфицирование Helicobacter pylori, стрессовые ситуации, курение, употребление алкоголя, а также некоторых лекарственных препаратов (нестероидных противовоспалительных препаратов, глюкокортикоидов, химикатов) и другие факторы.Helicobacter pylory (HP) – грамотрицательная микроаэрофильная бактерия изогнутой или спиралевидной формы с множеством жгутиков. Она обнаруживается в глубине желудочных ямок и на поверхности эпителиальных клеток, в основном под защитным слоем слизи, выстилающим слизистую оболочку желудка. Несмотря на столь необычное окружение, конкуренции Hp со стороны других микроорганизмов нет. Среди естественных резервуаров Нр-инфекции можно отметить следующие: на первом месте стоит человек, однако инфекцию можно обнаружить также и у домашних животных. Среди путей передачи можно выделить всего два: фекально-оральный и, орально-оральный, причем последний встречается в меньшей степени.
В большинстве случаев, как показывает практика, родители или близкоконтактирующие люди инфицируют ребенка хеликобактерной инфекцией еще в раннем детском возрасте, а вследствие того, что адекватное лечение отсутствует по причине низкой диагностики, данный микроорганизм у большинства людей по достижении зрелого возраста уже персистирует в организме довольно продолжительное время, вызывая сенсибилизацию организма. По этой причине у 10 детей из 100 уже в дошкольном возрасте можно выявить специальными методами наличие Нр-инфекции, а по достижении взрослого возраста, как показывает статистика, Нр обнаруживается практически у всех обследованных. Имеется связь между степенью инфицированности Нр населения и уровнем социально-экономического развития страны, причем отмечена такая особенность, что чем ниже уровень социально-экономического развития страны, тем большим становится риск инфицирования в детском возрасте.
На основании проведенных многочисленных исследований были выявлены группы риска населения, у которых риск заразиться Нр-инфекцией намного выше, чем у среднестатистического человека. Данную группу риска возглавили те профессии, которым в силу профессиональных особенностей приходится близко контактировать с инфицированными животными (доярки, работники скотобоен, рубщики мяса, рабочие мясоперерабатывающей продукции). Также риск заразиться Нр высок у медицинского персонала и врачей-гастроэнтерологов.
Патогенез
Патогенез заболевания является многогранным и складывается из нескольких взаимосвязанных факторов, в основе которых лежит нарушение динамического равновесия между защитными механизмами слизистой оболочки стенки желудка (выработка защитной слизи, слущивание и регенерация эпителия, выработка компонентов защитных буферных систем, продукция простагландинов и других медиаторов) с одной стороны, а с другой стороны – чрезмерным патогенным действием агрессивных факторов, таких как соляная кислота, острая и горячая пища, токсины. Под действием агрессивных факторов происходит срыв и возникает дефицит защитных систем как желудка, так и всего организма в целом, что ведет к выраженным расстройствам нервной и гуморальной регуляции желудка, к нарушению адекватного кровоснабжения, и вследствие этого по прошествии определенного времени как итог происходит изъязвление слизистой оболочки желудка.Стадии язвы
Первая стадия – прелюдия язвы, характеризуется выраженными нарушениями деятельности вегетативной нервной системы и функциональными расстройствами желудка и двенадцатиперстной кишки. Продолжительность начальной стадии составляет 48–72 ч. В эту стадию происходит порыв защитного барьера на ограниченном участке слизистой оболочки желудка или двенадцатиперстной кишки и наблюдается максимальное воздействие агрессивных факторов, обусловливающих распространение язвенного дефекта в глубину и ширину.Следует подчеркнуть, что первая стадия наблюдается главным образом в молодом, нередко в юношеском и старшем детском возрасте.
Вторая стадия — быстрой регенерации (или раннего заживления). Характеризуется появлением органических изменений вначале в форме структурной перестройки слизистой оболочки с развитием гастродуоденита. Продолжительность около двух недель. Агрессивные факторы вновь приходят в равновесие с защитными. Эта стадия характеризуется повреждением сосудов, наличием большого количества некротических масс, выраженным отеком слизистой оболочки с лимфо– и капилляростазом. В зону повреждения привлекаются макрофаги, лимфоциты, плазматические клетки, а также факторы роста (эпидермальный, трансформирующие и др.) Происходит образование различных антител, очищение язвы от продуктов распада, идут интенсивные процессы коллагенообразования и регенерации эпителия, требующие значительных энергозатрат. Через 12 ч от начала формирования язвы определяется интенсивный синтез ДНК.
Третья стадия — медленная регенерация (или позднее заживление)
Продолжается 3–4 недели. Продолжают действовать факторы роста, иммунные механизмы, которые берут на себя основную роль защиты, более интенсивно функционируют ферментно-гормональные факторы. Все эти составляющие приводят к завершению эпителизации язвы, реконструкции микроциркуляции, дифференциации клеток и их созреванию.
Четвертая стадия сопровождается развитием осложнений либо восстановлением функциональной активности слизистой оболочки. Продолжительность этой стадии может завершиться полным восстановлением функциональной активности клеток (выздоровление или продолжительная ремиссия) или не завершиться. В последнем случае ремиссия будет короткой, заболевание часто или непрерывно рецидивирует. В эту стадию в основном действуют гормонально-ферментные факторы.
Классификация
1. Форма заболевания:1) впервые выявленная;
2) рецидивирующая.
2. Локализация язв:
1) В желудке:
а) кардиальные и субкардиальные;
б) медиогастральные (тело, малая и большая кривизна);
в) антральные;
г) пилорического канала;
2) в двенадцатиперстной кишке (бульбарные, постбульбарные);
3. Фаза процесса:
1) обострение (язвенный дефект, признаки воспаления в желудке или двенадцатиперстной кишке)
2) затухающее обострение (язвенный рубец, остаются признаки воспаления);
3) ремиссия (язвенный рубец, исчезновение проявлений воспаления).
4. Течение болезни:
1) тяжелое (обострение 3 раза в год и чаще);
2) среднетяжелое (обострение 2 раза в год);
3) легкое (обострение 1 раз в 1–2 года и реже);
4) латентное (отсутствие клинических признаков, язва выявляется случайно при рентгенографии или гастроскопии).
5. Секреторная функция:
1) повышенная;
2) нормальная;
3) сниженная;
4) ахлоргидрия.
6. Осложнения:
1) кровотечение;
2) пенетрация;
3) перфорация;
4) рубцовая деформация;
5) стеноз пилорического отдела:
а) компенсированный;
6) субкомпенсированный;
в) декомпенсированный;
б) малигнизация (язвы желудка).
Клиническая картина
Язвенная болезнь встречается у 5 % взрослого населения, у мужчин в 3–7 раз чаще, чем у женщин. Преобладают больные в возрасте 35–64 лет. Отмечена наследственная предрасположенность: пептическая язва наблюдается в 2–5 раз чаще у родственников больных. Отношение язв двенадцатиперстной кишки и язвы желудка 4: 1.Проявления язвенной болезни весьма разнообразны. Имеют значение влияние внешней среды, пол и возраст больного, локализация язвенного дефекта, его величина. Так называемые типичные признаки язвенной болезни наблюдаются только у 25 % больных. Возможны различные варианты болевого синдрома: появление или усиление болей после еды у пациентов с дуоденальной язвой, отсутствие зависимости между приемом пищи и болевыми ощущениями, постоянные, приступообразные или эпизодические боли. К атипичным проявлениям язвенной болезни относятся также случаи безболевого течения, преобладание в клинической картине диспепсических симптомов, кишечных расстройств (запоров), снижение веса тела или астено-невротического синдрома.
Ведущим симптомом в клинической картине язвенной болезни является боль. Ее отличительными особенностями следует считать периодичность (чередование периодов обострений и ремиссий), ритмичность (связь болей с приемом пищи), сезонность (обострение болей весной и осенью, а у ряда больных – зимой и летом), нарастающий характер болей по мере развития заболевания, изменение и исчезновение болей после приема пищи, антацидов, применения тепла, антихолинергических средств, после рвоты.
По времени появления болей после приема пищи они делятся на ранние, возникающие вскоре после еды, поздние и ночные. Ранние боли свойственны язвам, расположенным в верхнем отделе желудка. Для язв антрального отдела желудка и язв двенадцатиперстной кишки характерны поздние и ночные боли, которые могут быть и «голодными», так как уменьшаются или прекращаются после еды.
Боли при язвенной болезни достигают максимальной силы на высоте пищеварения, и только «голодные» боли исчезают после приема пищи. При наличии перигастрита или перидуоденита боли усиливаются при физическом напряжении. Уменьшение или прекращение болей после случайно возникшей рвоты приводит к тому, что больные при появлении болей вызывают рвоту искусственным путем. Не менее типично для язвенной болезни молниеносное прекращение болей после приема щелочей.
Локализация болей при язвенной болезни различна и не всегда определяется местонахождением язвы. При расположении язвы на малой кривизне желудка боли чаще возникают в подложечной области, при локализации язвы в двенадцатиперстной кишке – в подложечной области справа от средней линии, а при язвах кардиального отдела желудка – за мечевидным отростком. Иррадиация болей различна: при язвах верхнего отдела желудка они иррадиируют в левую половину грудной клетки, левую лопатку и нередко приводят к неправильному диагнозу ишемической болезни сердца. Наблюдается иррадиация болей в пояснично-крестцовую область, симулирующая пояснично-крестцовый радикулит. Интенсивность болей при неосложненной язвенной болезни нерезкая и обычно не требует назначения наркотиков. Применение тепла, антиспастических и антихолинергических медикаментозных средств является достаточным для их уменьшения и прекращения.
Язвенная болезнь не всегда проявляется болями, а иногда только изжогой, чувством переполнения в подложечной области; боли же присоединяются только впоследствии.
Установлено, что обычные раздражители, при действии которых на кожных покровах возникает ощущение боли, воздействуя на стенку желудка и кишечника, не вызывают болей. Адекватными раздражителями для указанных органов являются усиленная мышечная активность, особенно спазм, повышение внутриполостного давления, воздействие на измененную слизистую оболочку желудка или двенадцатиперстной кишки активного желудочного сока. Нередко боли при язвенной болезни связаны со спазмом привратника, ишемией, вызванной спазмом сосудистой стенки, а также раздражением брюшины в связи с воспалительным процессом, возникшим при обострении болезни.
Рвота при язвенной болезни возникает без предшествующей тошноты, на высоте болей в разгар пищеварения, при различной локализации язвенного процесса частота ее варьирует. Выделение активного желудочного сока натощак нередко сопровождается рвотой. Частая утренняя рвота остатками пищи, съеденной накануне, свидетельствует о нарушении эвакуаторной функции желудка. Третьим кардинальным признаком язвенной болезни раньше считали кровотечение. Это положение в настоящее время опровергнуто. Явное кровотечение, проявляющееся кровавой рвотой или черным стулом, считается осложнением язвенной болезни. Скрытые кровотечения, как правило, сопровождают периоды обострения болезни, отличаются периодичностью и в период ремиссии не наблюдаются. Из диспепсических явлений при язвенной болезни чаще возникает изжога (у 60–80 % всех больных язвенной болезнью). С диагностической точки зрения важно, что отмечается она не только в периоды обострений, но может им предшествовать в течение ряда лет и имеет те же типичные черты, что и боли (периодичность, сезонность). Изжога связана с нарушением моторной функции пищевода и желудка. При раздувании пищевода, желудка, двенадцатиперстной кишки с помощью резинового баллона можно вызвать чувство жжения разной степени вплоть до ощущения жгучей судороги.
Аппетит при язвенной болезни не только сохранен, но иногда даже резко усилен. Так как боли обычно связаны с приемом пищи, то иногда у больных появляется страх перед едой. У некоторых лиц, страдающих язвенной болезнью, периодически наблюдается усиленное слюноотделение, которому предшествует тошнота. Нередко возникает ощущение давления и тяжести в подложечной области. Этим явлениям свойственны те же закономерности, что и болям.
Запоры нередко отмечаются в период обострения. Они обусловлены характером питания больных, постельным режимом и главным образом нервно-мышечной дистонией толстой кишки вагусного происхождения. Общее питание больных язвенной болезни болезнью не нарушено. Похудание может наблюдаться в период обострения болезни, когда больной ограничивает прием пищи из-за страха перед возникновением болей. При поверхностной пальпации живота можно обнаружить напряжение правой прямой мышцы, которое по мере затихания патологического процесса уменьшается. Симптом Менделя при обострении обычно положительный.
Определяемый натощак шум плеска может быть вызван гиперсекрецией желудочного сока либо является симптомом спазма или органического стеноза привратника желудка. Существовавшее раньше мнение, что при круглой язве кислотность желудочного сока всегда повышена, опровергнуто накопившимися фактическими данными. Гиперхлоргидрия обнаруживается примерно у 50 % лиц, страдающих язвенной болезнью. Не существует полного параллелизма между степенью кислотности желудочного содержимого и локализацией язвы. Ахлоргидрия или ахилия при язвенной болезни почти не встречаются, особенно при локализации язвы в двенадцатиперстной кишке. Несколько чаще понижение кислотности желудочного сока наблюдается при язвах желудка. Переход язвы в рак может сопровождаться прогрессирующим снижением кислотообразующей и секреторной функции желудка вплоть до полного прекращения.
Большое значение в диагностике язвенной болезни имеет определение базальной секреции. Выраженная постоянная базальная гиперсекреция, когда натощак удается получить до 500 мл чистого желудочного сока, в подавляющем большинстве случаев обусловлена локализацией язвы в пилорическом отделе желудка или двенадцатиперстной кишке. Секреторный аппарат желудка при язвенной болезни может быть в состоянии парабиоза, поэтому максимальная степень секреции и кислотности не всегда выявляется сильным раздражителем.
