Страница:
Мозговой слой надпочечников:
высший орган симпатического отдела периферической нервной системы, не имеет тропного гормона гипофиза.
→ Транспорт гормонов в периферической крови
Гипофизотропных гормонов гипоталамуса в периферической крови крайне малое количество.
Тропные гормоны гипофиза (ТТГ, АКТГ, ГнРГ, пролактин) циркулируют в крови в свободном состоянии. Гормон роста циркулирует в крови в связи с белком, который идентичен его рецептору. Гормоны передней гипоталамической области, накапливающиеся в задней доле гипофиза, – антидиуретический гормон, вазопрессин и окситоцин – циркулируют в крови в связанном с нейрофизином виде.
Тиреоидные гормоны тироксин (Т4) и трийодтиронин (Т3) циркулируют в крови в связанном с белком виде (тироксинсвязывающим глобулином) и лишь очень небольшое количество – в свободном виде, и только свободные Т3 и Т4 биологически активны.
Кортизол циркулирует в крови в связи с кортизолсвязывающим глобулином (транскортином) и лишь крайне малое количество находится в свободном, биологически активном состоянии.
Половые гормоны циркулируют в крови в связи с половым гормоносвязывающим глобулином, и лишь крайне малое количество их находится в свободном, биологически активном виде. Прогестерон циркулирует в крови в связи с транскортином.
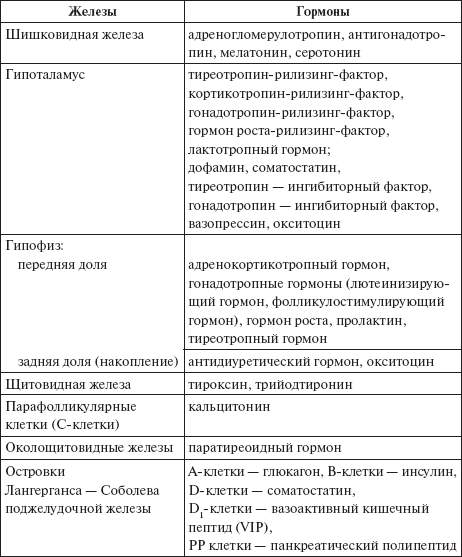
Таблица 1
Эндокринные железы и их гормоны

→ Метаболизм гормонов
Метаболизм тиреоидных гормонов
Тиреоидные гормоны Т4 (тироксин) и Т3 (трийодтиронин) циркулируют в сыворотке крови в связи с белком: в основном с тироксинсвязывающим глобулином и в незначительном количестве с альбумином. Содержание Т4 в свободном виде в сыворотке крови составляет 0,04%, а Т3 – 0,4% их общего количества. Деградация тиреоидных гормонов происходит в периферических тканях под влиянием энзима 1,5´-дейодиназы через ряд метаболитов, конечный из которых – трийодтироацетовая кислота – выводится с желчью.
Метаболизм катехоламинов
Действие катехоламинов краткое, и диссоциация их после связи со своим рецептором происходит очень быстро. Только около 2 – 3% норадреналина и адреналина экскретируется с мочой. В основном адреналин и норадреналин метаболизируются в печени и экскрементируются с мочой в виде метаболитов.
Метаболиты адреналина: метанефрин и норметанефрин.
Метаболиты норадреналина: ваналилмандальная кислота и гомованильная кислота.
Метаболизм пептидных гормонов
Большинство пептидных гормонов циркулирует в сыворотке крови в свободном виде, исключение составляет гормон роста, циркулирующий в связи с белком, идентичным его рецептору. Окситоцин и вазопрессин циркулируют в связи с нейрофизином. Деградация пептидных гормонов происходит на поверхности клетки после связи с рецептором. Затем продукты деградации пептидных гормонов поступают в клетку, где под влиянием энзимов, содержащих лизосомы, подвергаются деаминированию.
Метаболиты стероидных гормонов – метаболиты кортизола и надпочечниковых андрогенов.
В печени кортизол и надпочечниковые андрогены путем конъюгации с глюкуроновыми и сульфатными группами превращаются в водорастворимые соединения: кортизол – в 17-гидроксикортикостероиды, андрогены – в 17-кетостероиды, которые экскретируются с мочой. В небольшом количестве с мочой экскретируется свободный кортизол (от 5 до 50 мкг/сут). Исследование свободного кортизола имеет важное диагностическое значение в дифференциации диагнозов: ожирение и синдром Кушинга. При ожирении обычно увеличивается экскреция 17-гидроксикортикостероидов, но количество свободного кортизола в суточной моче остается в пределах нормы. При синдроме Кушинга количество свободного кортизола в суточной моче в разной степени превышает норму.
Тестостерон и эстрогены преимущественно циркулируют в сыворотке крови в связи с половыми гормонами, связывающими глобулин, и лишь небольшое количество их – с альбумином. Около 2% тестостерона циркулирует в сыворотке крови в свободном виде. Бóльшая часть тестостерона, циркулирующего в крови, в печени превращается в андростендиол и этиохаланолон, которые конъюгируются с кислотами – глюкуроновой или сульфатной и экскретируются с мочой в виде 17β-кетостероидов.
Эстрадиол (главным образом яичникового происхождения) быстро превращается в печени в эстрон под влиянием 17β-гидроксистероид дегидрогеназы (тип 1). Эстрон в основном конъюгируется в эстрон-сульфат, а конечный продукт эстрона – неактивный эстриол – конъюгируется в 3-сульфат-16-глюкуронид и экскретируется с мочой.
Прогестерон циркулирует в сыворотке крови в связи с транскортином (кортикостероидсвязывающий глобулин). В печени прогестерон быстро превращается в прегнандиол, конъюгируется с глюкуроновой кислотой и в виде прегнандиола глюкуроната экскретируется с мочой.
Взаимосвязь нервной и эндокринной систем
Глава 3
2.1. ГИПОТАЛАМУС
МОРФОФУНКЦИОНАЛЬНАЯ ХАРАКТЕРИСТИКА
ВОЗРАСТНАЯ МОРФОЛОГИЯ И ГИСТОФИЗИОЛОГИЯ
высший орган симпатического отдела периферической нервной системы, не имеет тропного гормона гипофиза.
→ Транспорт гормонов в периферической крови
Гипофизотропных гормонов гипоталамуса в периферической крови крайне малое количество.
Тропные гормоны гипофиза (ТТГ, АКТГ, ГнРГ, пролактин) циркулируют в крови в свободном состоянии. Гормон роста циркулирует в крови в связи с белком, который идентичен его рецептору. Гормоны передней гипоталамической области, накапливающиеся в задней доле гипофиза, – антидиуретический гормон, вазопрессин и окситоцин – циркулируют в крови в связанном с нейрофизином виде.
Тиреоидные гормоны тироксин (Т4) и трийодтиронин (Т3) циркулируют в крови в связанном с белком виде (тироксинсвязывающим глобулином) и лишь очень небольшое количество – в свободном виде, и только свободные Т3 и Т4 биологически активны.
Кортизол циркулирует в крови в связи с кортизолсвязывающим глобулином (транскортином) и лишь крайне малое количество находится в свободном, биологически активном состоянии.
Половые гормоны циркулируют в крови в связи с половым гормоносвязывающим глобулином, и лишь крайне малое количество их находится в свободном, биологически активном виде. Прогестерон циркулирует в крови в связи с транскортином.
Таблица 1
Эндокринные железы и их гормоны


→ Метаболизм гормонов
Метаболизм тиреоидных гормонов
Тиреоидные гормоны Т4 (тироксин) и Т3 (трийодтиронин) циркулируют в сыворотке крови в связи с белком: в основном с тироксинсвязывающим глобулином и в незначительном количестве с альбумином. Содержание Т4 в свободном виде в сыворотке крови составляет 0,04%, а Т3 – 0,4% их общего количества. Деградация тиреоидных гормонов происходит в периферических тканях под влиянием энзима 1,5´-дейодиназы через ряд метаболитов, конечный из которых – трийодтироацетовая кислота – выводится с желчью.
Метаболизм катехоламинов
Действие катехоламинов краткое, и диссоциация их после связи со своим рецептором происходит очень быстро. Только около 2 – 3% норадреналина и адреналина экскретируется с мочой. В основном адреналин и норадреналин метаболизируются в печени и экскрементируются с мочой в виде метаболитов.
Метаболиты адреналина: метанефрин и норметанефрин.
Метаболиты норадреналина: ваналилмандальная кислота и гомованильная кислота.
Метаболизм пептидных гормонов
Большинство пептидных гормонов циркулирует в сыворотке крови в свободном виде, исключение составляет гормон роста, циркулирующий в связи с белком, идентичным его рецептору. Окситоцин и вазопрессин циркулируют в связи с нейрофизином. Деградация пептидных гормонов происходит на поверхности клетки после связи с рецептором. Затем продукты деградации пептидных гормонов поступают в клетку, где под влиянием энзимов, содержащих лизосомы, подвергаются деаминированию.
Метаболиты стероидных гормонов – метаболиты кортизола и надпочечниковых андрогенов.
В печени кортизол и надпочечниковые андрогены путем конъюгации с глюкуроновыми и сульфатными группами превращаются в водорастворимые соединения: кортизол – в 17-гидроксикортикостероиды, андрогены – в 17-кетостероиды, которые экскретируются с мочой. В небольшом количестве с мочой экскретируется свободный кортизол (от 5 до 50 мкг/сут). Исследование свободного кортизола имеет важное диагностическое значение в дифференциации диагнозов: ожирение и синдром Кушинга. При ожирении обычно увеличивается экскреция 17-гидроксикортикостероидов, но количество свободного кортизола в суточной моче остается в пределах нормы. При синдроме Кушинга количество свободного кортизола в суточной моче в разной степени превышает норму.
Тестостерон и эстрогены преимущественно циркулируют в сыворотке крови в связи с половыми гормонами, связывающими глобулин, и лишь небольшое количество их – с альбумином. Около 2% тестостерона циркулирует в сыворотке крови в свободном виде. Бóльшая часть тестостерона, циркулирующего в крови, в печени превращается в андростендиол и этиохаланолон, которые конъюгируются с кислотами – глюкуроновой или сульфатной и экскретируются с мочой в виде 17β-кетостероидов.
Эстрадиол (главным образом яичникового происхождения) быстро превращается в печени в эстрон под влиянием 17β-гидроксистероид дегидрогеназы (тип 1). Эстрон в основном конъюгируется в эстрон-сульфат, а конечный продукт эстрона – неактивный эстриол – конъюгируется в 3-сульфат-16-глюкуронид и экскретируется с мочой.
Прогестерон циркулирует в сыворотке крови в связи с транскортином (кортикостероидсвязывающий глобулин). В печени прогестерон быстро превращается в прегнандиол, конъюгируется с глюкуроновой кислотой и в виде прегнандиола глюкуроната экскретируется с мочой.
Взаимосвязь нервной и эндокринной систем
В организме человека имеются две сложные системы управления функциями: нервная и эндокринная, тесно связанные между собой и осуществляющие единую нейрогуморальную регуляцию: центральная нервная система, в том числе кора большого мозга, регулирует функции желез внутренней секреции путем непосредственной регуляции органов и тканей;
эндокринная система осуществляет регулирующее влияние с помощью переносимых кровью, лимфой, тканевой жидкостью гормонов.
Общее для нервных и эндокринных клеток – выработка гуморальных регулирующих факторов. Эндокринные клетки синтезируют гормоны и выделяют их в кровь, а нейроны синтезируют нейротрансмиттеры (большинство из которых является нейроаминами): норадреналин, дофамин, серотонин и др., выделяющиеся в синаптические щели. В гипоталамусе расположены секреторные нейроны, совмещающие свойства нервных и эндокринных клеток; они способны образовывать и нейрамины, и олигопептидные гормоны.
Гипоталамус является центром регуляции эндокринных функций, он координирует нервные и гормональные механизмы регуляции функций внутренних органов, объединяет нервные и эндокринные регуляторные механизмы в общую нейроэндокринную систему. Гипоталамус образует с гипофизом единый функциональный комплекс, в котором гипоталамус играет регулирующую роль, а гипофиз – эффекторную.
Деятельность эндокринных желез тесно связана с деятельностью нервной системы, внутренних органов, органов чувств, половой сферы и др. При поражении эндокринных желез возникают изменения и в соответствующих органах и системах организма, что дает основание рассматривать любое эндокринное заболевание как болезнь всего организма.
эндокринная система осуществляет регулирующее влияние с помощью переносимых кровью, лимфой, тканевой жидкостью гормонов.
Общее для нервных и эндокринных клеток – выработка гуморальных регулирующих факторов. Эндокринные клетки синтезируют гормоны и выделяют их в кровь, а нейроны синтезируют нейротрансмиттеры (большинство из которых является нейроаминами): норадреналин, дофамин, серотонин и др., выделяющиеся в синаптические щели. В гипоталамусе расположены секреторные нейроны, совмещающие свойства нервных и эндокринных клеток; они способны образовывать и нейрамины, и олигопептидные гормоны.
Гипоталамус является центром регуляции эндокринных функций, он координирует нервные и гормональные механизмы регуляции функций внутренних органов, объединяет нервные и эндокринные регуляторные механизмы в общую нейроэндокринную систему. Гипоталамус образует с гипофизом единый функциональный комплекс, в котором гипоталамус играет регулирующую роль, а гипофиз – эффекторную.
Деятельность эндокринных желез тесно связана с деятельностью нервной системы, внутренних органов, органов чувств, половой сферы и др. При поражении эндокринных желез возникают изменения и в соответствующих органах и системах организма, что дает основание рассматривать любое эндокринное заболевание как болезнь всего организма.
Глава 3
ГИПОТАЛАМО-ГИПОФИЗАРНАЯ СИСТЕМА
По генетическим признакам железы внутренней секреции подразделяют на две группы: чисто эндокринные и смешанные железы, в которых секреция гормонов является лишь частью разнообразных функций органа.
К первой группе – чисто эндокринные железы – относятся шишковидная железа, нейросекреторные ядра гипоталамической области головного мозга, гипофиз, щитовидная железа, околощитовидные железы, надпочечники.
Вторую группу – смешанные железы – составляют тимус, поджелудочная железа, семенники, яичники. В последние годы описаны гормонпродуцирующие клетки в стенке желудочно-кишечного тракта, дыхательных путях, сердце (правое предсердие), мочевой и половой системах и в других органах, которые также относятся к эндокринной системе, поскольку оказывают местное (локальное) воздействие. Ко второй группе принадлежат также хромаффинные органы, или параганглии, – скопления клеточных элементов, выполняющих эндокринную функцию в разных участках тела: межсонный параганглий, надсердечные параганглии, поясничные параганглии и др.
Как уже отмечалось выше (рис. 2), на основе структурно-функциональных особенностей желез внутренней секреции выделяют:
центральное звено эндокринной системы (эпиталамус + шишковидная железа и гипоталамус + гипофиз);
периферическое звено, представленное железами, зависимыми от передней доли гипофиза (щитовидная железа, кора надпочечников, гонады) и независимыми от него (паращитовидные железы, мозговая часть надпочечников и гормонпродуцирующие клетки внутренних органов).
Морфологически эндокринные железы созревают еще в период утробной жизни и во второй половине периода начинают функционировать. У новорожденных и детей грудного возраста функция большинства эндокринных желез высокоактивна, как при стрессе. Это связано с тем, что гормоны многих желез участвуют в развитии приспособительных реакций к сверхсильным нагрузкам при изменении условий существования. В процессе роста и развития ребенка значение желез внутренней секреции неодинаково: каждая на определенном этапе особенно сильно влияет на организм. В позднем онтогенезе гомеостаз организма поддерживается благодаря функции гипоталамуса, так как при старении изменяется чувствительность эндокринных желез к тропным гормонам гипофиза. Возрастные изменения в нейроэндокринной системе являются фоном, на котором развивается патологический процесс, этот фон придает особенности болезням, присущим лицам пожилого и старческого возраста.
К первой группе – чисто эндокринные железы – относятся шишковидная железа, нейросекреторные ядра гипоталамической области головного мозга, гипофиз, щитовидная железа, околощитовидные железы, надпочечники.
Вторую группу – смешанные железы – составляют тимус, поджелудочная железа, семенники, яичники. В последние годы описаны гормонпродуцирующие клетки в стенке желудочно-кишечного тракта, дыхательных путях, сердце (правое предсердие), мочевой и половой системах и в других органах, которые также относятся к эндокринной системе, поскольку оказывают местное (локальное) воздействие. Ко второй группе принадлежат также хромаффинные органы, или параганглии, – скопления клеточных элементов, выполняющих эндокринную функцию в разных участках тела: межсонный параганглий, надсердечные параганглии, поясничные параганглии и др.
Как уже отмечалось выше (рис. 2), на основе структурно-функциональных особенностей желез внутренней секреции выделяют:
центральное звено эндокринной системы (эпиталамус + шишковидная железа и гипоталамус + гипофиз);
периферическое звено, представленное железами, зависимыми от передней доли гипофиза (щитовидная железа, кора надпочечников, гонады) и независимыми от него (паращитовидные железы, мозговая часть надпочечников и гормонпродуцирующие клетки внутренних органов).
Морфологически эндокринные железы созревают еще в период утробной жизни и во второй половине периода начинают функционировать. У новорожденных и детей грудного возраста функция большинства эндокринных желез высокоактивна, как при стрессе. Это связано с тем, что гормоны многих желез участвуют в развитии приспособительных реакций к сверхсильным нагрузкам при изменении условий существования. В процессе роста и развития ребенка значение желез внутренней секреции неодинаково: каждая на определенном этапе особенно сильно влияет на организм. В позднем онтогенезе гомеостаз организма поддерживается благодаря функции гипоталамуса, так как при старении изменяется чувствительность эндокринных желез к тропным гормонам гипофиза. Возрастные изменения в нейроэндокринной системе являются фоном, на котором развивается патологический процесс, этот фон придает особенности болезням, присущим лицам пожилого и старческого возраста.
2.1. ГИПОТАЛАМУС
МОРФОФУНКЦИОНАЛЬНАЯ ХАРАКТЕРИСТИКА
Гипоталамус (hypothalamus, рис. 3) занимает базальную область промежуточного мозга, окружая нижнюю часть III желудочка головного мозга. Гипоталамус контролирует все висцеральные функции организма и объединяет эндокринные механизмы регуляций с нервными будучи мозговым центром симпатического и парасимпатического отделов вегетативной нервной системы. В сером веществе гипоталамуса выделяют свыше 30 пар ядер, которые группируются в передней, дорсальной, промежуточной, латеральной и задней гипоталамических областях, а также в гипоталамических зонах. Часть ядер представляет собой скопление нейросекреторных клеток, другие образованы сочетанием нейросекреторных клеток и обычных нейронов.
В передней гипоталамической области расположены: переднее ядро гипоталамуса (n. anterior hypothalami); вентральное перивентрикулярное ядро (n. periventricularis ventralis); передние интерстициальные ядра (nn. intersticiales hypothalami anteriores); латеральное и медиальное предоптические ядра (nn. preopticus lateralis et medialis); срединное предоптическое ядро (n. preopticus medianus); паравентрикулярное ядро гипоталамуса (n. paraventricularis hypothalami); перивентрикулярное предоптическое ядро (n. preopticus perivetricularis); надперекрестное ядро (n. suprachiasmaticus); супраоптическое ядро (n. supraopticus) .
Наиболее важными для функции эндокринной системы являются парные – супраоптическое и паравентрикулярное – ядра, образованные крупными нейросекреторными клетками. Аксоны этих клеток проходят через гипофизарную ножку в заднюю долю гипофиза, где и заканчиваются на кровеносных капиллярах утолщенными терминалями (тельца Херринга). В ядрах передней гипоталамической области вырабатываются нейрогормоны вазопрессин, или антидиуретический гормон (супраоптическое ядро), и окситоцин (паравентрикулярное ядро), которые накапливаются в задней доле гипофиза.
Дорсальная гипоталамическая область включает: дорсомедиальное ядро (n. dorsomedialis); внутриножковое ядро (n. endopeduncularis); ядро чечевицеобразной петли (n. ansae lenticularis).
В состав промежуточной гипоталамической области входят: дорсальное ядро гипоталамуса (n. dorsalis hypothalami); дорсомедиальное ядро (n. dorsomedialis); дугообразное ядро, или ядро воронки (n. arcuatus seu n. infundibularis); перивентрикулярное ядро (n. periventricularis); заднее перивентрикулярное ядро (n. periventricularis posterior); позадиперекрестная область (area retrochiasmatica); латеральные серобугорные ядра (nn. tuberales laterales); вентромедиальное ядро гипоталамуса (n. ventromedialis hypothalami).
Латеральная гипоталамическая область объединяет: предоптическую область; латеральные серобугорные ядра; перифорникальное ядро; серобугорно-сосцевидное ядро.
В ядрах дорсальной, промежуточной и латеральной гипоталамических областей, образованных мелкими нейросекреторными клетками, вырабатываются аденогипофизотропные гормоны, которые либо стимулируют (рилизинг-факторы, или либерины), либо угнетают (ингибирущие факторы, или статины) соответствующие гормонообразовательные функции аденогипофиза.
Задняя гипоталамическая область включает: дорсальное предсосцевидное ядро (n. premammilaris dorsalis); латеральное и медиальное сосцевидные ядра (nn. mammillares laterales et mediales); надсосцевидное ядро (n. supramammillaris); вентральное предсосцевидное ядро (n. premammillares ventralis); заднее ядро гипоталамуса (n. posterior hypothalami).
В состав гипоталамуса также входят: сосудистый орган терминальной пластинки; медиальная, латеральная и перивентрикулярная гипоталамические зоны. Функции ядер задней гипоталамической зоны мало изучены.
→ Гипофизотропные нейрогормоны, или факторы гипоталамуса
В гипоталамусе синтезируются тиреотропин-рилизинг-фактор, кортикотропин-рилизинг-фактор, гонадотропин-рилизинг-фактор, соматотропин-рилизинг-фактор, пролактинстимулирующий фактор, соматостатин, дофамин.
Тиреотропин-рилизинг-фактор (ТРФ)
ТРФ стимулирует синтез и секрецию тиреотропного гормона (ТТГ); по строению – трипептид. Синтезируется в нейронах медиальных отделов паравентрикулярных ядер гипоталамуса, а затем по аксонам этих нейронов поступает в срединное возвышение гипоталамуса, из которого по воротной вене гипофиза достигает своих клеток-мишеней – тиреотропов – и стимулирует в них синтез и секрецию ТТГ.
ТРФ секретируется пульсаторно, через каждые 30 – 40 минут.
Кортикотропин-рилизинг-φaκmop (КРФ)
КРФ стимулирует синтез и секрецию адренокортикотропного гормона (АКТГ). Синтезируется КРФ в нейронах преоптических ядер гипоталамуса и по их аксонам поступает в срединное возвышение гипоталамуса, из которого по воротной вене перемещается в гипофиз к клеткам-мишеням – кортикотропам. КРФ размещается на своих рецепторах на поверхности кортикотропов и стимулирует в них синтез и секрецию АКТГ.
Гонадотропин-рилизинг-фактор (ГнРФ)
ГнРФ стимулирует синтез и секрецию гонадотропных гормонов; по строению – декапептид. Синтезируется ГнРФ в нейронах преоптических ядер гипоталамуса, по аксонам которых перемещается в срединное возвышение гипоталамуса и затем по воротной вене в гипофиз к клеткам-мишеням – гонадотропам. ГнРФ занимает свои рецепторы на поверхности гонадотропов и стимулирует в них синтез и секрецию гонадотропных гормонов: фолликулостимулирующего гормона (ФСГ) и лютеинизирующего гормона (ЛГ).
ГнРФ секретируется пульсаторно, через каждые 40 – 60 минут. Подобно ГнРФ пульсаторно секретируются ФСГ и ЛГ.
Соматотропин-рилизинг-фактор (СТРФ)
СТРФ стимулирует синтез и секрецию гормона роста. Синтезируется СТРФ в нейронах дугообразных ядер гипоталамуса и по их аксонам поступает в срединное возвышение гипоталамуса, из которого по воротной вене поступает в гипофиз к клеткам-мишеням – соматотропам. СТРФ занимает рецепторы на поверхности соматотропов и стимулирует синтез и секрецию гормона роста.
Пролактинстимулирующий фактор (ПрСФ)
(пролактинвысвобождающий фактор)
ПрСФ стимулирует синтез и секрецию пролактина; по строению аналогичен тиреотропин-рилизинг-фактору, и допускается, что это один и тот же гормон. Однако ПрСФ и ТРФ не идентично действуют на тиреотропы и лактотропы:
ПрСФ стимулирует только лактотропы и синтез в них пролактина;
ТРФ, стимулируя тиреотропы и секрецию тиреотропного гормона, не действует стимулирующе на секрецию лактотропами пролактина, хотя в некоторых случаях стимулирует секрецию пролактина лактотропами, не увеличивая секрецию ТТГ тиреотропами. При патологических состояниях (первичный гипотиреоз) ТРФ стимулирует секрецию обоих гормонов.
Кроме ПрСФ и ТРФ, секрецию пролактина в гипофизе усиливает также гипоталамический пептид – вазоактивный кишечный пептид, который синтезируется и в гипоталамусе, и в островках поджелудочной железы, и в кишечнике.
На секрецию пролактина действует стимулирующе также серотонин – нейротрансмиттер в гипоталамусе. Это подтверждается тем, что лечение антагонистами серотонина снижает секрецию пролактина. ПрСГ по аксонам нейронов, в которых он синтезировался, поступает в срединное возвышение гипоталамуса и затем по воротной вене – к лактотропам гипофиза. ПрСГ (в определенных случаях ТРФ) занимает места на своих рецепторах на лактотропах и стимулирует синтез и секрецию пролактина.
Соматостатин
Соматостатин тормозит секрецию гормона роста и тиреотропного гормона; является тетрадекапептидом. Синтезируется в нейронах паравентрикулярных ядер гипоталамуса, затем по их аксонам перемещается в срединное возвыше гипоталамуса, далее по воротной вене поступает в гипофиз к клеткам-мишеням – соматотропам и тиреотропам, занимает места на рецепторах этих клеток и тормозит секрецию гормона роста и ТТГ. Соматостатин, кроме гипоталамуса, синтезируется в В-клетках островков поджелудочной железы и в желудочно-кишечном тракте.
Дофамин
Дофамин – пролактинингибирующий гормон.
Поступая из срединного возвышения гипоталамуса в воротную вену гипофиза, дофамин достигает лактотропов, занимает свои рецепторы на их поверхности и тормозит секрецию пролактина. Установлено, что секрецию пролактина также тормозит нейротрансмиттер – аминобутировая кислота.
Некоторые гипофизотропные гормоны, а именно соматостатин и вазоактивный кишечный пептид, помимо гипоталамуса синтезируются в островках Лангерганса – Соболева поджелудочной железы и в желудочно-кишечном тракте. Соматостатин также синтезируется в парафолликулярных С-клетках щитовидной железы.
Регуляцию секреции ядер гипоталамуса со стороны ЦНС осуществляют лимбическая система (миндалевидные ядра и гиппокамп), ретикулярная формация среднего мозга и шишковидная железа. В осуществлении этих влияний большое значение принадлежит нейроаминам – катехоламинам (дофамин и норадреналин), серотонину и ацетилхолину. Кроме того, на нейросекреторные функции гипоталамуса существенно влияют некоторые гормоны (эндорфины и энкефалины), вырабатываемые нейронами головного мозга.
В передней гипоталамической области расположены: переднее ядро гипоталамуса (n. anterior hypothalami); вентральное перивентрикулярное ядро (n. periventricularis ventralis); передние интерстициальные ядра (nn. intersticiales hypothalami anteriores); латеральное и медиальное предоптические ядра (nn. preopticus lateralis et medialis); срединное предоптическое ядро (n. preopticus medianus); паравентрикулярное ядро гипоталамуса (n. paraventricularis hypothalami); перивентрикулярное предоптическое ядро (n. preopticus perivetricularis); надперекрестное ядро (n. suprachiasmaticus); супраоптическое ядро (n. supraopticus) .
Наиболее важными для функции эндокринной системы являются парные – супраоптическое и паравентрикулярное – ядра, образованные крупными нейросекреторными клетками. Аксоны этих клеток проходят через гипофизарную ножку в заднюю долю гипофиза, где и заканчиваются на кровеносных капиллярах утолщенными терминалями (тельца Херринга). В ядрах передней гипоталамической области вырабатываются нейрогормоны вазопрессин, или антидиуретический гормон (супраоптическое ядро), и окситоцин (паравентрикулярное ядро), которые накапливаются в задней доле гипофиза.
Дорсальная гипоталамическая область включает: дорсомедиальное ядро (n. dorsomedialis); внутриножковое ядро (n. endopeduncularis); ядро чечевицеобразной петли (n. ansae lenticularis).
В состав промежуточной гипоталамической области входят: дорсальное ядро гипоталамуса (n. dorsalis hypothalami); дорсомедиальное ядро (n. dorsomedialis); дугообразное ядро, или ядро воронки (n. arcuatus seu n. infundibularis); перивентрикулярное ядро (n. periventricularis); заднее перивентрикулярное ядро (n. periventricularis posterior); позадиперекрестная область (area retrochiasmatica); латеральные серобугорные ядра (nn. tuberales laterales); вентромедиальное ядро гипоталамуса (n. ventromedialis hypothalami).
Латеральная гипоталамическая область объединяет: предоптическую область; латеральные серобугорные ядра; перифорникальное ядро; серобугорно-сосцевидное ядро.
В ядрах дорсальной, промежуточной и латеральной гипоталамических областей, образованных мелкими нейросекреторными клетками, вырабатываются аденогипофизотропные гормоны, которые либо стимулируют (рилизинг-факторы, или либерины), либо угнетают (ингибирущие факторы, или статины) соответствующие гормонообразовательные функции аденогипофиза.
Задняя гипоталамическая область включает: дорсальное предсосцевидное ядро (n. premammilaris dorsalis); латеральное и медиальное сосцевидные ядра (nn. mammillares laterales et mediales); надсосцевидное ядро (n. supramammillaris); вентральное предсосцевидное ядро (n. premammillares ventralis); заднее ядро гипоталамуса (n. posterior hypothalami).
В состав гипоталамуса также входят: сосудистый орган терминальной пластинки; медиальная, латеральная и перивентрикулярная гипоталамические зоны. Функции ядер задней гипоталамической зоны мало изучены.
→ Гипофизотропные нейрогормоны, или факторы гипоталамуса
В гипоталамусе синтезируются тиреотропин-рилизинг-фактор, кортикотропин-рилизинг-фактор, гонадотропин-рилизинг-фактор, соматотропин-рилизинг-фактор, пролактинстимулирующий фактор, соматостатин, дофамин.
Тиреотропин-рилизинг-фактор (ТРФ)
ТРФ стимулирует синтез и секрецию тиреотропного гормона (ТТГ); по строению – трипептид. Синтезируется в нейронах медиальных отделов паравентрикулярных ядер гипоталамуса, а затем по аксонам этих нейронов поступает в срединное возвышение гипоталамуса, из которого по воротной вене гипофиза достигает своих клеток-мишеней – тиреотропов – и стимулирует в них синтез и секрецию ТТГ.
ТРФ секретируется пульсаторно, через каждые 30 – 40 минут.
Кортикотропин-рилизинг-φaκmop (КРФ)
КРФ стимулирует синтез и секрецию адренокортикотропного гормона (АКТГ). Синтезируется КРФ в нейронах преоптических ядер гипоталамуса и по их аксонам поступает в срединное возвышение гипоталамуса, из которого по воротной вене перемещается в гипофиз к клеткам-мишеням – кортикотропам. КРФ размещается на своих рецепторах на поверхности кортикотропов и стимулирует в них синтез и секрецию АКТГ.
Гонадотропин-рилизинг-фактор (ГнРФ)
ГнРФ стимулирует синтез и секрецию гонадотропных гормонов; по строению – декапептид. Синтезируется ГнРФ в нейронах преоптических ядер гипоталамуса, по аксонам которых перемещается в срединное возвышение гипоталамуса и затем по воротной вене в гипофиз к клеткам-мишеням – гонадотропам. ГнРФ занимает свои рецепторы на поверхности гонадотропов и стимулирует в них синтез и секрецию гонадотропных гормонов: фолликулостимулирующего гормона (ФСГ) и лютеинизирующего гормона (ЛГ).
ГнРФ секретируется пульсаторно, через каждые 40 – 60 минут. Подобно ГнРФ пульсаторно секретируются ФСГ и ЛГ.
Соматотропин-рилизинг-фактор (СТРФ)
СТРФ стимулирует синтез и секрецию гормона роста. Синтезируется СТРФ в нейронах дугообразных ядер гипоталамуса и по их аксонам поступает в срединное возвышение гипоталамуса, из которого по воротной вене поступает в гипофиз к клеткам-мишеням – соматотропам. СТРФ занимает рецепторы на поверхности соматотропов и стимулирует синтез и секрецию гормона роста.
Пролактинстимулирующий фактор (ПрСФ)
(пролактинвысвобождающий фактор)
ПрСФ стимулирует синтез и секрецию пролактина; по строению аналогичен тиреотропин-рилизинг-фактору, и допускается, что это один и тот же гормон. Однако ПрСФ и ТРФ не идентично действуют на тиреотропы и лактотропы:
ПрСФ стимулирует только лактотропы и синтез в них пролактина;
ТРФ, стимулируя тиреотропы и секрецию тиреотропного гормона, не действует стимулирующе на секрецию лактотропами пролактина, хотя в некоторых случаях стимулирует секрецию пролактина лактотропами, не увеличивая секрецию ТТГ тиреотропами. При патологических состояниях (первичный гипотиреоз) ТРФ стимулирует секрецию обоих гормонов.
Кроме ПрСФ и ТРФ, секрецию пролактина в гипофизе усиливает также гипоталамический пептид – вазоактивный кишечный пептид, который синтезируется и в гипоталамусе, и в островках поджелудочной железы, и в кишечнике.
На секрецию пролактина действует стимулирующе также серотонин – нейротрансмиттер в гипоталамусе. Это подтверждается тем, что лечение антагонистами серотонина снижает секрецию пролактина. ПрСГ по аксонам нейронов, в которых он синтезировался, поступает в срединное возвышение гипоталамуса и затем по воротной вене – к лактотропам гипофиза. ПрСГ (в определенных случаях ТРФ) занимает места на своих рецепторах на лактотропах и стимулирует синтез и секрецию пролактина.
Соматостатин
Соматостатин тормозит секрецию гормона роста и тиреотропного гормона; является тетрадекапептидом. Синтезируется в нейронах паравентрикулярных ядер гипоталамуса, затем по их аксонам перемещается в срединное возвыше гипоталамуса, далее по воротной вене поступает в гипофиз к клеткам-мишеням – соматотропам и тиреотропам, занимает места на рецепторах этих клеток и тормозит секрецию гормона роста и ТТГ. Соматостатин, кроме гипоталамуса, синтезируется в В-клетках островков поджелудочной железы и в желудочно-кишечном тракте.
Дофамин
Дофамин – пролактинингибирующий гормон.
Поступая из срединного возвышения гипоталамуса в воротную вену гипофиза, дофамин достигает лактотропов, занимает свои рецепторы на их поверхности и тормозит секрецию пролактина. Установлено, что секрецию пролактина также тормозит нейротрансмиттер – аминобутировая кислота.
Некоторые гипофизотропные гормоны, а именно соматостатин и вазоактивный кишечный пептид, помимо гипоталамуса синтезируются в островках Лангерганса – Соболева поджелудочной железы и в желудочно-кишечном тракте. Соматостатин также синтезируется в парафолликулярных С-клетках щитовидной железы.
Регуляцию секреции ядер гипоталамуса со стороны ЦНС осуществляют лимбическая система (миндалевидные ядра и гиппокамп), ретикулярная формация среднего мозга и шишковидная железа. В осуществлении этих влияний большое значение принадлежит нейроаминам – катехоламинам (дофамин и норадреналин), серотонину и ацетилхолину. Кроме того, на нейросекреторные функции гипоталамуса существенно влияют некоторые гормоны (эндорфины и энкефалины), вырабатываемые нейронами головного мозга.
ВОЗРАСТНАЯ МОРФОЛОГИЯ И ГИСТОФИЗИОЛОГИЯ
Гипоталамус развивается из базальной части промежуточного пузыря зачатка головного мозга. В эмбриогенезе время закладки и темп развития определенных групп ядер гипоталамуса различны: супраоптические и паравентрикулярные ядра, например, появляются в самые ранние сроки – у эмбриона 2-месячного возраста (на 8-й неделе), а на 3-м месяце происходит закладка мелкоклеточных ядер.
Сроки клеточной дифференцировки гипоталамических ядер различны: у 2 – 3-месячных эмбрионов гипоталамус представлен однородными округлыми клетками размером 3 – 5 мкм; у 4-месячного плода можно обнаружить первые нейросекреторные клетки супраоптического и паравентрикулярного ядер. На 6-м месяце развития плода отдельные нейросекреторные клетки паравентрикулярного и супраоптического ядер достигают 8 – 10 мкм, отмечается рост аксонов; в этот же период начинает формироваться гипоталамо-гипофизарный тракт, состоящий из небольшого числа тонких аксонов. Усиленное формирование структуры гипоталамуса к 6-му месяцу коррелирует с организацией всех жизненно важных систем организма плода. Именно к этому возрасту плода в гипоталамусе заканчиваются в основном топографические изменения ядер.
Во второй половине беременности происходит интенсивная дифференцировка клеточных элементов, что совпадает с подготовкой сложных и специфических реакций плода человека к процессу становления регуляции гипоталамусом вегетативных функций.
Влияние гипоталамуса на развивающийся гипофиз отмечается со второй половины внутриутробного развития, когда начинают устанавливаться типичные гипоталамо-гипофизарные связи.
В ходе эмбрионального развития увеличивается объем и всего гипоталамуса, и его отдельных ядер. Наибольший рост гипоталамуса отмечается в 8 – 9-й месяцы эмбриогенеза.
У новорожденного дифференцировка клеточных элементов разных ядер гипоталамуса еще не завершена, развитие и созревание ядер гипоталамуса заканчивается в разные периоды постнатального онтогенеза.
Архитектоническое формирование гипоталамуса у человека заканчивается к 2 – 4 годам жизни, далее происходят изменения, связанные как с развитием нервно-волокнистых систем, так и с более тонкими внутриклеточными структурными процессами. Так, дифференцировка мамиллярных ядер и тела Льюиса заканчивается к трем годам; паравентрикулярные и надоптические ядра, которые являются гипофизарно-нейросекреторными, созревают к 7 годам.
В 13 – 14 лет в клетках секреторных ядер гипоталамуса появляются вакуоли и просветления, а сама цитоплазма делается мутной, зернистой, богатой коллоидом, что связано с процессом полового созревания, когда отмечается усиленная инкреторная деятельность ядерных образований переднего гипоталамуса. В этот же период происходит интенсивное развитие связей гипофиза с передним отделом гипоталамуса. Клеточные элементы серого бугра – филогенетически нового образования гипоталамуса – созревают к шестилетнему возрасту ребенка. Центральная серая субстанция гипоталамуса заканчивает развитие в период полового созревания – к 13 – 17 годам.
В процессе роста и развития организма в ядрах гипоталамуса происходит ряд изменений:
уменьшается количество клеток на единицу площади, увеличиваются отдельные клетки и проводящие пути;
повышается количество пигмента в клетках гипоталамуса – раньше всего пигмент появляется в мамиллярных телах, позже всего в клетках центрального серого вещества;
более быстрыми темпами, чем кора мозга, формируется гипоталамическая область, при этом обращает на себя внимание то, что сроки развития гипоталамуса близки к срокам и темпам формирования ретикулярной формации мозгового ствола;
меняются объемные и топографические соотношения между ядерными и проводниковыми структурами.
Гипоталамус структурно и функционально стареет неравномерно: в одних его ядрах (в супраоптическом, паравентрикулярном и аркуатном) происходят выраженные структурные нарушения, гибель нейронов, а в других ядрах (переднем интерстициальном, надперекрестном и др.) сдвиги не очень выражены. В заднем гипоталамусе снижается плотность расположения нейронов, что выражено в наибольшей степени в латеральном мамиллярном, префорникатном и заднегипоталамическом ядрах. Как и в других структурах ЦНС, в нейроцитах ядер гипоталамуса откладывается липофусцин («пигмент старения»). Происходит это неравномерно, и обнаруживается закономерное нарастание дистрофических процессов: вначале тела нейроцитов набухают, дендриты укорачиваются, появляются перетяжки на дендритах, уменьшается число дендритических шипиков; в последующем поверхность нейронов и дендритов деформируется, контур нейронов становится неправильным, появляются сморщенные дендриты. Вместе с тем при анализе возрастных изменений ядер заднего и среднего гипоталамуса необходимо учитывать следующее:
локальные особенности нейронов этой области;
многообразие типов нейронов;
возможность проявления в структуре нейронов псевдодегенеративных черт (к ним относят вакуолизацию цитоплазмы, наличие зоны перинуклеарного псевдохроматолиза, расположение базофильного вещества по периферии клеточного тела, гиперхроматоз клеточных тел при сохранении размеров ядер, пролиферацию сателлитов).
В дальнейшем в телах нейроцитов нарастает тигролиз, они сморщиваются и деформируются. Атрофируется дендритическое дерево. Аксоны претерпевают дегенеративные изменения. Отмечается нейронофагия погибших клеток. Электронно-микроскопически в митохондриях нейроцитов обнаруживается набухание части митохондрий, редукция крист, просветление матрикса. В канальцах эндоплазматического ретикулума появляются расширения и вакуоли.
С возрастом существенно изменяются количество и расположение глиальных элементов, их взаимоотношения с нервными клетками:
у молодых количество глиальных элементов в ядрах гипоталамуса небольшое, явления сателлитоза редки;
у старых наблюдаются пролиферация макроглиальных элементов и значительное нарастание явлений сателлитоза.
В эпендимальной выстилке III желудочка, к которому примыкают структуры медиобазального гипоталамуса, у старых людей также можно обнаружить: 1) признаки дегенерации и атрофии клеток; 2) уменьшение числа эпендимоцитов на единицу площади; 3) накопление в эпендимоцитах липофусцина и гликогена. В связи с этим в старости могут происходить сдвиги в барьерных функциях эпендимы, что приводит к изменению функциональных взаимоотношений в системе нервная ткань – цереброспинальная жидкость, к нарастанию проницаемости барьера для ряда физиологически активных веществ.
Физиологическая активность нейросекреторного процесса в ядрах гипоталамуса в старости или снижается, или не меняется. Отмечается ослабление реакции нейросекреторной системы на рефлекторные (кожно-болевое раздражение) или афферентные нервные раздражения (стимуляция ядер миндалевидного комплекса). Усиливается реакция на гуморальные раздражители: введение адреналина, что, по-видимому, связано с ростом чувствительности нейросекреторных элементов к действию катехоламинов.
Сроки клеточной дифференцировки гипоталамических ядер различны: у 2 – 3-месячных эмбрионов гипоталамус представлен однородными округлыми клетками размером 3 – 5 мкм; у 4-месячного плода можно обнаружить первые нейросекреторные клетки супраоптического и паравентрикулярного ядер. На 6-м месяце развития плода отдельные нейросекреторные клетки паравентрикулярного и супраоптического ядер достигают 8 – 10 мкм, отмечается рост аксонов; в этот же период начинает формироваться гипоталамо-гипофизарный тракт, состоящий из небольшого числа тонких аксонов. Усиленное формирование структуры гипоталамуса к 6-му месяцу коррелирует с организацией всех жизненно важных систем организма плода. Именно к этому возрасту плода в гипоталамусе заканчиваются в основном топографические изменения ядер.
Во второй половине беременности происходит интенсивная дифференцировка клеточных элементов, что совпадает с подготовкой сложных и специфических реакций плода человека к процессу становления регуляции гипоталамусом вегетативных функций.
Влияние гипоталамуса на развивающийся гипофиз отмечается со второй половины внутриутробного развития, когда начинают устанавливаться типичные гипоталамо-гипофизарные связи.
В ходе эмбрионального развития увеличивается объем и всего гипоталамуса, и его отдельных ядер. Наибольший рост гипоталамуса отмечается в 8 – 9-й месяцы эмбриогенеза.
У новорожденного дифференцировка клеточных элементов разных ядер гипоталамуса еще не завершена, развитие и созревание ядер гипоталамуса заканчивается в разные периоды постнатального онтогенеза.
Архитектоническое формирование гипоталамуса у человека заканчивается к 2 – 4 годам жизни, далее происходят изменения, связанные как с развитием нервно-волокнистых систем, так и с более тонкими внутриклеточными структурными процессами. Так, дифференцировка мамиллярных ядер и тела Льюиса заканчивается к трем годам; паравентрикулярные и надоптические ядра, которые являются гипофизарно-нейросекреторными, созревают к 7 годам.
В 13 – 14 лет в клетках секреторных ядер гипоталамуса появляются вакуоли и просветления, а сама цитоплазма делается мутной, зернистой, богатой коллоидом, что связано с процессом полового созревания, когда отмечается усиленная инкреторная деятельность ядерных образований переднего гипоталамуса. В этот же период происходит интенсивное развитие связей гипофиза с передним отделом гипоталамуса. Клеточные элементы серого бугра – филогенетически нового образования гипоталамуса – созревают к шестилетнему возрасту ребенка. Центральная серая субстанция гипоталамуса заканчивает развитие в период полового созревания – к 13 – 17 годам.
В процессе роста и развития организма в ядрах гипоталамуса происходит ряд изменений:
уменьшается количество клеток на единицу площади, увеличиваются отдельные клетки и проводящие пути;
повышается количество пигмента в клетках гипоталамуса – раньше всего пигмент появляется в мамиллярных телах, позже всего в клетках центрального серого вещества;
более быстрыми темпами, чем кора мозга, формируется гипоталамическая область, при этом обращает на себя внимание то, что сроки развития гипоталамуса близки к срокам и темпам формирования ретикулярной формации мозгового ствола;
меняются объемные и топографические соотношения между ядерными и проводниковыми структурами.
Гипоталамус структурно и функционально стареет неравномерно: в одних его ядрах (в супраоптическом, паравентрикулярном и аркуатном) происходят выраженные структурные нарушения, гибель нейронов, а в других ядрах (переднем интерстициальном, надперекрестном и др.) сдвиги не очень выражены. В заднем гипоталамусе снижается плотность расположения нейронов, что выражено в наибольшей степени в латеральном мамиллярном, префорникатном и заднегипоталамическом ядрах. Как и в других структурах ЦНС, в нейроцитах ядер гипоталамуса откладывается липофусцин («пигмент старения»). Происходит это неравномерно, и обнаруживается закономерное нарастание дистрофических процессов: вначале тела нейроцитов набухают, дендриты укорачиваются, появляются перетяжки на дендритах, уменьшается число дендритических шипиков; в последующем поверхность нейронов и дендритов деформируется, контур нейронов становится неправильным, появляются сморщенные дендриты. Вместе с тем при анализе возрастных изменений ядер заднего и среднего гипоталамуса необходимо учитывать следующее:
локальные особенности нейронов этой области;
многообразие типов нейронов;
возможность проявления в структуре нейронов псевдодегенеративных черт (к ним относят вакуолизацию цитоплазмы, наличие зоны перинуклеарного псевдохроматолиза, расположение базофильного вещества по периферии клеточного тела, гиперхроматоз клеточных тел при сохранении размеров ядер, пролиферацию сателлитов).
В дальнейшем в телах нейроцитов нарастает тигролиз, они сморщиваются и деформируются. Атрофируется дендритическое дерево. Аксоны претерпевают дегенеративные изменения. Отмечается нейронофагия погибших клеток. Электронно-микроскопически в митохондриях нейроцитов обнаруживается набухание части митохондрий, редукция крист, просветление матрикса. В канальцах эндоплазматического ретикулума появляются расширения и вакуоли.
С возрастом существенно изменяются количество и расположение глиальных элементов, их взаимоотношения с нервными клетками:
у молодых количество глиальных элементов в ядрах гипоталамуса небольшое, явления сателлитоза редки;
у старых наблюдаются пролиферация макроглиальных элементов и значительное нарастание явлений сателлитоза.
В эпендимальной выстилке III желудочка, к которому примыкают структуры медиобазального гипоталамуса, у старых людей также можно обнаружить: 1) признаки дегенерации и атрофии клеток; 2) уменьшение числа эпендимоцитов на единицу площади; 3) накопление в эпендимоцитах липофусцина и гликогена. В связи с этим в старости могут происходить сдвиги в барьерных функциях эпендимы, что приводит к изменению функциональных взаимоотношений в системе нервная ткань – цереброспинальная жидкость, к нарастанию проницаемости барьера для ряда физиологически активных веществ.
Физиологическая активность нейросекреторного процесса в ядрах гипоталамуса в старости или снижается, или не меняется. Отмечается ослабление реакции нейросекреторной системы на рефлекторные (кожно-болевое раздражение) или афферентные нервные раздражения (стимуляция ядер миндалевидного комплекса). Усиливается реакция на гуморальные раздражители: введение адреналина, что, по-видимому, связано с ростом чувствительности нейросекреторных элементов к действию катехоламинов.
