Страница:
Средний корпускулярный объем (СКО)
В связи с переходом на автоматический анализ состава периферической крови цветовой показатель может быть с неменьшим успехом заменен на другой показатель – средний корпускулярный объем (СКО), измеряемый в фемтолитрах, или мкм3 (fl, фл). Его измеряют прямым способом с помощью автоматизированного счетчика. Нормальное значение СКО представляет 80—90 фл (нормоцитоз). Снижение СКО менее 80—95 фл – микроцитоз. Повышение СКО выше 95 фл – макроцитоз.
Снижение концентрации гемоглобина в крови часто происходит при одновременном уменьшении количества эритроцитов и изменением их качественного состава. Любая анемия приводит к снижению дыхательной функции крови и развитию кислородного голодания тканей, что чаще всего выражается такими симптомами, как бледность кожных покровов, повышенная утомляемость, слабость, головные боли, головокружение, сердцебиение, одышка и другими.
При рутинном исследовании мазка периферической крови морфолог указывает на отклонение размера эритроцитов в меньшую сторону (микроцитоз) или в большую сторону (макроцитоз), но такая оценка, если она производится без специальных приспособлений – микрометров, не может быть свободна от субъективизма. Достоинством автоматического анализа крови является стандартизация показателя – СКО.
Замена цветового показателя на показатель СКО не нарушает привычной классификации анемий, построенной на основании цветового показателя.
Снижение концентрации гемоглобина в крови часто происходит при одновременном уменьшении количества эритроцитов и изменением их качественного состава. Любая анемия приводит к снижению дыхательной функции крови и развитию кислородного голодания тканей, что чаще всего выражается такими симптомами, как бледность кожных покровов, повышенная утомляемость, слабость, головные боли, головокружение, сердцебиение, одышка и другими.
При рутинном исследовании мазка периферической крови морфолог указывает на отклонение размера эритроцитов в меньшую сторону (микроцитоз) или в большую сторону (макроцитоз), но такая оценка, если она производится без специальных приспособлений – микрометров, не может быть свободна от субъективизма. Достоинством автоматического анализа крови является стандартизация показателя – СКО.
Замена цветового показателя на показатель СКО не нарушает привычной классификации анемий, построенной на основании цветового показателя.
Классификация и проявление анемий
По своим проявлениям анемии делятся на:
1) Гипохромные (микроцитарные):
# железодефицитная анемия;
# талассемии.
2) Нормохромные (микроцитарные):
# гемолитические анемии (когда скорость разрушения эритроцитов превышает скорость их продукции);
# постгеморрагическая (как результат потери крови вследствие кровотечения или кровоизлияния);
# неопластические заболевания костного мозга;
# апластические анемии;
# внекостномозговые опухоли;
# анемии вследствии снижения выработки эритропоэтина.
3) Гиперхромные (макроцитарные):
# витамин B12-дефицитная анемия;
# фолиеводефицитная анемия;
# миелодиспластический синдром;
# лекарственные анемии.
4) Анемии при хронических воспалениях:
# при инфекциях:
+ туберкулез;
+ бактериальный эндокардит;
+ бронхоэктатическая болезнь;
+ абсцесс легкого;
+ бруцеллез;
+ пиелонефрит;
+ остеомиелит;
+ микозы;
# при коллагенозах:
+ системная красная волчанка;
+ ревматоидный артрит;
+ узелковый полиартериит;
+ болезнь Хортона.
Нередко анемия протекает без выраженных проявлений и часто остается незамеченной, во многих случаях становясь случайной лабораторной находкой у лиц, не предъявляющих специфических жалоб.
Как правило, страдающие анемией отмечают проявления, обусловленные развитием анемической гипоксии. При легких формах это может быть слабость, быстрая утомляемость, общее недомогание, а также снижение концентрации внимания. Люди с более выраженной анемией могут жаловаться на одышку при незначительной или умеренной нагрузке, сердцебиения, головную боль, шум в ушах, могут также встречаться нарушения сна, аппетита, полового влечения. При очень сильной анемии возможно развитие сердечной недостаточности.
Часто встречаемым диагностически важным симптомом умеренной или выраженной анемии является бледность (кожных покровов, видимых слизистых и ногтевых лож). Также ценное значение имеют такие симптомы, как усиление сердечного толчка и появление функционального систолического шума.
Проявления острых и тяжелых анемий всегда более выражены, чем хронических и средней тяжести.
Кроме общих симптомов, непосредственно связанных с гипоксией, у анемий могут быть и другие проявления – в зависимости от их этиологии и патогенеза. Например, развитие нарушений чувствительности при B12-дефицитной анемии, желтуха – при гемолитической анемии и пр.
В клинической практике используют различные расчетные величины, отражающие физико-химические свойства эритроцитов, позволяющие количественно характеризовать важные показатели состояния эритроцитов. Их вычисляют, исходя из величины гематокрита, концентрации гемоглобина, количества эритроцитов.
1) Гипохромные (микроцитарные):
# железодефицитная анемия;
# талассемии.
2) Нормохромные (микроцитарные):
# гемолитические анемии (когда скорость разрушения эритроцитов превышает скорость их продукции);
# постгеморрагическая (как результат потери крови вследствие кровотечения или кровоизлияния);
# неопластические заболевания костного мозга;
# апластические анемии;
# внекостномозговые опухоли;
# анемии вследствии снижения выработки эритропоэтина.
3) Гиперхромные (макроцитарные):
# витамин B12-дефицитная анемия;
# фолиеводефицитная анемия;
# миелодиспластический синдром;
# лекарственные анемии.
4) Анемии при хронических воспалениях:
# при инфекциях:
+ туберкулез;
+ бактериальный эндокардит;
+ бронхоэктатическая болезнь;
+ абсцесс легкого;
+ бруцеллез;
+ пиелонефрит;
+ остеомиелит;
+ микозы;
# при коллагенозах:
+ системная красная волчанка;
+ ревматоидный артрит;
+ узелковый полиартериит;
+ болезнь Хортона.
Нередко анемия протекает без выраженных проявлений и часто остается незамеченной, во многих случаях становясь случайной лабораторной находкой у лиц, не предъявляющих специфических жалоб.
Как правило, страдающие анемией отмечают проявления, обусловленные развитием анемической гипоксии. При легких формах это может быть слабость, быстрая утомляемость, общее недомогание, а также снижение концентрации внимания. Люди с более выраженной анемией могут жаловаться на одышку при незначительной или умеренной нагрузке, сердцебиения, головную боль, шум в ушах, могут также встречаться нарушения сна, аппетита, полового влечения. При очень сильной анемии возможно развитие сердечной недостаточности.
Часто встречаемым диагностически важным симптомом умеренной или выраженной анемии является бледность (кожных покровов, видимых слизистых и ногтевых лож). Также ценное значение имеют такие симптомы, как усиление сердечного толчка и появление функционального систолического шума.
Проявления острых и тяжелых анемий всегда более выражены, чем хронических и средней тяжести.
Кроме общих симптомов, непосредственно связанных с гипоксией, у анемий могут быть и другие проявления – в зависимости от их этиологии и патогенеза. Например, развитие нарушений чувствительности при B12-дефицитной анемии, желтуха – при гемолитической анемии и пр.
В клинической практике используют различные расчетные величины, отражающие физико-химические свойства эритроцитов, позволяющие количественно характеризовать важные показатели состояния эритроцитов. Их вычисляют, исходя из величины гематокрита, концентрации гемоглобина, количества эритроцитов.
Средний объем эритроцита (MCV – Mean Corpuscular Volume)
MCV – средний корпускулярный объем – средняя величина объема эритроцитов, измеряемая в фемтолитрах или мкм3 (fl, фл). Его вычисляют путем деления гематокритной величины (суммы клеточных объемов) на общее количество эритроцитов в крови. На основании значений MCV дифференцируют анемии (микроцитарные, нормоцитарные и макроцитарные) для выбора терапии. Это более точный параметр, чем визуальная оценка размера эритроцитов, однако он не является достоверным при большом количестве эритроцитов с измененной формой.
Изменения MCV могут дать полезную информацию о нарушениях водно-электролитного баланса. Повышенное значение MCV свидетельствует о гипотоническом характере нарушений водно-электролитного баланса, тогда как понижение – о гипертоническом характере.
Значения MCV в норме: 75—95 фл.
Заболевания и состояния, сопровождающиеся изменением MCV:
Значения MCV < 80 fl:
1) Микроцитарные анемии:
# железодефицитные анемии;
# талассемии;
# сидеробластные анемии.
2) Анемии, которые могут сопровождаться микроцитозом:
# гемоглобинопатии;
# нарушения синтеза порфиринов
# отравление свинцом
Значения MCV > 80 fl и < 100 fl:
1) Нормоцитарные анемии:
# апластические;
# гемолитические;
# гемоглобинопатии;
# анемии после кровотечений.
2) Анемии, которые могут сопровождаться нормоцитозом:
# регенераторная фаза железодефицитной анемии.
Значения MCV > 100 fl:
1) Макроцитарные и мегалобластные анемии:
# дефицит витамина В12, фолиевой кислоты.
2) Анемии, которые могут сопровождаться макроцитозом:
# миелодиспластические синдромы;
# гемолитические анемии;
# болезни печени.
Изменения MCV могут дать полезную информацию о нарушениях водно-электролитного баланса. Повышенное значение MCV свидетельствует о гипотоническом характере нарушений водно-электролитного баланса, тогда как понижение – о гипертоническом характере.
Значения MCV в норме: 75—95 фл.
Заболевания и состояния, сопровождающиеся изменением MCV:
Значения MCV < 80 fl:
1) Микроцитарные анемии:
# железодефицитные анемии;
# талассемии;
# сидеробластные анемии.
2) Анемии, которые могут сопровождаться микроцитозом:
# гемоглобинопатии;
# нарушения синтеза порфиринов
# отравление свинцом
Значения MCV > 80 fl и < 100 fl:
1) Нормоцитарные анемии:
# апластические;
# гемолитические;
# гемоглобинопатии;
# анемии после кровотечений.
2) Анемии, которые могут сопровождаться нормоцитозом:
# регенераторная фаза железодефицитной анемии.
Значения MCV > 100 fl:
1) Макроцитарные и мегалобластные анемии:
# дефицит витамина В12, фолиевой кислоты.
2) Анемии, которые могут сопровождаться макроцитозом:
# миелодиспластические синдромы;
# гемолитические анемии;
# болезни печени.
Среднее содержание гемоглобина в эритроците (MCH – Mean Corpuscular Hemoglobin)
Этот показатель отражает абсолютное содержание гемоглобина в одном эритроците, выражаемый в пикограммах (пг). Его определяют путем деления концентрации гемоглобина на число эритроцитов в одинаковом объеме крови. Это истинный показатель дефицита железа в организме или неусвоения железа эритробластами и нарушения синтеза гема (сидеробластные анемии). МСН самостоятельного значения не имеет и всегда соотносится с MCV и МСНС. На основании этих показателей различают нормо-, гипо– и гиперхромные анемии.
Снижение среднего содержания гемоглобина в эритроците (гипохромия) наблюдается вследствие уменьшения объема эритроцитов (микроциты) или понижения содержания гемоглобина в нормальном по объему эритроците.
Нормохромия (нормальное содержание гемоглобина в эритроците) обычно имеет место у здоровых людей, но может отмечаться и при некоторых анемиях (острых постгеморрагических, гемолитических и апластических).
Содержание гемоглобина в эритроците в норме: 27—31 пг.
Cнижение МСН (гипохромия):
# гипохромные и микроцитарные анемии (железодефицитная, анемия при хронических болезнях);
# талассемия;
# некоторые гемоглобинопатии;
# свинцовое отравление;
# нарушение синтеза порфиринов.
Повышение МСН (гиперхромия):
# расстройства обмена витамина В12 или его дефицита (мегалобластные анемии);
# многие хронические гемолитические анемии;
# гипопластическая анемия после острой кровопотери;
# гипотиреоз;
# заболевания печени;
# метастазы злокачественных новообразований;
# прием цитостатиков, контрацептивов, противосудорожных препаратов.
Снижение среднего содержания гемоглобина в эритроците (гипохромия) наблюдается вследствие уменьшения объема эритроцитов (микроциты) или понижения содержания гемоглобина в нормальном по объему эритроците.
Нормохромия (нормальное содержание гемоглобина в эритроците) обычно имеет место у здоровых людей, но может отмечаться и при некоторых анемиях (острых постгеморрагических, гемолитических и апластических).
Содержание гемоглобина в эритроците в норме: 27—31 пг.
Cнижение МСН (гипохромия):
# гипохромные и микроцитарные анемии (железодефицитная, анемия при хронических болезнях);
# талассемия;
# некоторые гемоглобинопатии;
# свинцовое отравление;
# нарушение синтеза порфиринов.
Повышение МСН (гиперхромия):
# расстройства обмена витамина В12 или его дефицита (мегалобластные анемии);
# многие хронические гемолитические анемии;
# гипопластическая анемия после острой кровопотери;
# гипотиреоз;
# заболевания печени;
# метастазы злокачественных новообразований;
# прием цитостатиков, контрацептивов, противосудорожных препаратов.
Средняя концентрация гемоглобина в эритроците (MCHC – Mean Corpuscular Hemoglobin Concentration)
МСНС – отражает степень насыщения эритроцита гемоглобином; характеризует отношение количества гемоглобина к объему клетки (не зависит от объема клетки, в отличие от МСН), выражается в г/л.
МСНС используют для дифференциальной диагностики анемий. Снижение показателя отражает абсолютную гипохромию.
Средняя концентрация гемоглобина в эритроците в норме: 300—380 г/л.
Снижение МСНС:
# гипохромные железодефицитные и сидеробластические анемии
# талассемия;
# гипоосмолярные нарушения водно-электролитного обмена;
# заболевания, сопровождающиеся нарушением синтеза гемоглобина (гемоглобинопатии);
# мегалобластные анемии (когда увеличение объема эритроцитов значительнее насыщения эритроцитов гемоглобином).
Повышение МСНС:
# гиперхромные анемии (сфероцитоз, овалоцитоз);
# гиперосмолярные нарушения водно-электролитного обмена.
МСНС используют для дифференциальной диагностики анемий. Снижение показателя отражает абсолютную гипохромию.
Средняя концентрация гемоглобина в эритроците в норме: 300—380 г/л.
Снижение МСНС:
# гипохромные железодефицитные и сидеробластические анемии
# талассемия;
# гипоосмолярные нарушения водно-электролитного обмена;
# заболевания, сопровождающиеся нарушением синтеза гемоглобина (гемоглобинопатии);
# мегалобластные анемии (когда увеличение объема эритроцитов значительнее насыщения эритроцитов гемоглобином).
Повышение МСНС:
# гиперхромные анемии (сфероцитоз, овалоцитоз);
# гиперосмолярные нарушения водно-электролитного обмена.
Трансферрин
Трансферрин (сидерофилин) – белок в плазме крови, основной переносчик железа. Насыщение трансферрина происходит благодаря его синтезу в печени и зависит от содержания железа в организме. С помощью анализа трансферрина можно оценить функциональное состояние печени. Норма трансферрина в сыворотке крови – 2,0–4,0 г/л. Содержание трансферрина у женщин на 10% выше, уровень трансферрина увеличивается при беременности и снижается у пожилых людей.
Повышенный трансферрин – симптом дефицита железа (предшествует развитию железодефицитной анемии в течение нескольких дней или месяцев). Повышение трансферрина происходит вследствие приема эстрогенов и оральных контрацептивов.
Пониженный трансферрин в сыворотке крови – повод для врача поставить следующий диагноз:
# хронический воспалительный процесс;
# гемохроматоз;
# цирроз печени;
# ожог;
# злокачественная опухоль;
# избыток железа.
Повышение трансферрина в крови происходит также в результате приема андрогенов и глюкокортикоидов.
Повышенный трансферрин – симптом дефицита железа (предшествует развитию железодефицитной анемии в течение нескольких дней или месяцев). Повышение трансферрина происходит вследствие приема эстрогенов и оральных контрацептивов.
Пониженный трансферрин в сыворотке крови – повод для врача поставить следующий диагноз:
# хронический воспалительный процесс;
# гемохроматоз;
# цирроз печени;
# ожог;
# злокачественная опухоль;
# избыток железа.
Повышение трансферрина в крови происходит также в результате приема андрогенов и глюкокортикоидов.
Железосвязывающая способность сыворотки крови
Железосвязываюшая способность сыворотки крови (ЖСС) – показатель, характеризующий способность сыворотки крови к связыванию железа. Железо в организме человека находится в комплексе с белком – трансферрином. ЖСС показывает концентрацию трансферрина в сыворотке крови. Железосвязывающая способность сыворотки крови изменяется при нарушении обмена, распада и транспорта железа в организме. Для диагностики анемии используют определение латентной железосвязывающей способности сыворотки крови (ЛЖСС) – это ЖСС без сывороточного железа. Норма латентной ЖСС – 20—62 мкмоль/л.
Повышение уровня ЛЖСС происходит при дефиците железа, железодефицитной анемии, остром гепатите, на поздних сроках беременности.
Понижение ЛЖСС происходит при уменьшении количества белков в плазме (при нефрозе, голодании, опухолях), при хронических инфекциях, циррозе, гемахроматозе, талассемии.
Повышение уровня ЛЖСС происходит при дефиците железа, железодефицитной анемии, остром гепатите, на поздних сроках беременности.
Понижение ЛЖСС происходит при уменьшении количества белков в плазме (при нефрозе, голодании, опухолях), при хронических инфекциях, циррозе, гемахроматозе, талассемии.
Ферритин
Ферритин – основной показатель запасов железа в организме, играет важную роль в поддержании железа в биологически полезной форме. В состав ферритина входят фосфаты железа. Ферритин содержится во всех клетках и жидкостях организма. Анализ крови на ферритин используется для диагностики железодефицитной анемии и диагностики анемии, сопровождающей инфекционные, ревматические и опухолевые заболевания.
Норма ферритина в крови для взрослых мужчин – 30–310 мкг/л. Для женщин норма анализа крови на ферритин – 22–180 мкг/л.
Избыток ферритина в крови может быть следствием следующих заболеваний:
# избыток железа при гемохроматозе;
# алкогольный гепатит и другие заболевания печени;
# лейкоз;
# острые и хронические инфекционно-воспалительные заболевания (остеомиелит, инфекции легких, ожоги, ревматоидный артрит);
# рак молочной железы.
Повышение уровня ферритина происходит при приеме оральных контрацептивов и голодании. Низкий ферритин – следствие дефицита железа (железодефицитной анемии).
Лечение низкого ферритина всегда назначается только врачом: необходимо точно выяснить, какие нарушения привели к снижению ферритина в анализе крови.
Норма ферритина в крови для взрослых мужчин – 30–310 мкг/л. Для женщин норма анализа крови на ферритин – 22–180 мкг/л.
Избыток ферритина в крови может быть следствием следующих заболеваний:
# избыток железа при гемохроматозе;
# алкогольный гепатит и другие заболевания печени;
# лейкоз;
# острые и хронические инфекционно-воспалительные заболевания (остеомиелит, инфекции легких, ожоги, ревматоидный артрит);
# рак молочной железы.
Повышение уровня ферритина происходит при приеме оральных контрацептивов и голодании. Низкий ферритин – следствие дефицита железа (железодефицитной анемии).
Лечение низкого ферритина всегда назначается только врачом: необходимо точно выяснить, какие нарушения привели к снижению ферритина в анализе крови.
Глава 5. Серологическое исследование крови
Серология (от лат. serum – сыворотка и…логия), буквально учение о свойствах сыворотки крови; обычно под «серологией» понимают раздел иммунологии, изучающий взаимодействие антител сыворотки с антигенами. В основе метода серологической диагностики лежит определение специфических антител, образовавшихся в процессе иммунного ответа на проникновение возбудителя заболевания (антигена).
Серологические реакции применяют в научных и диагностических целях в инфекционной и неинфекционной иммунологии: их используют, например, при переливании крови, для определения групп крови, установления видовой и индивидуальной специфичности белков. Серологические исследования применяют также в эпидемиологии и эпизоотологии для выявления источника инфекции, путей ее передачи, иммунитета у людей и животных, эффективности вакцинации и т. п. Реакция между антигенами и антителами лежит в основе серопрофилактики и серотерапии. Среди основных задач серологии – разработка методов получения высокоспецифических диагностических и лечебных сывороток, оценка их активности и выяснение механизма действия.
Серологические реакции применяют в научных и диагностических целях в инфекционной и неинфекционной иммунологии: их используют, например, при переливании крови, для определения групп крови, установления видовой и индивидуальной специфичности белков. Серологические исследования применяют также в эпидемиологии и эпизоотологии для выявления источника инфекции, путей ее передачи, иммунитета у людей и животных, эффективности вакцинации и т. п. Реакция между антигенами и антителами лежит в основе серопрофилактики и серотерапии. Среди основных задач серологии – разработка методов получения высокоспецифических диагностических и лечебных сывороток, оценка их активности и выяснение механизма действия.
Группы крови
К сожалению, в жизни довольно часто складываются ситуации, чреватые обильной потерей крови (например, дорожные аварии или тяжелые операции), и единственный способ не потерять пациента состоит в том, чтобы возместить часть потерянного объема; без достаточного количества крови ткани не способны получить необходимые вещества, особенно кислород, необходимый для выживания (мозг, в частности, в отсутствие кислорода умирает очень быстро). Казалось бы, чего уж проще – взять немного крови от одного человека и передать ее другому; этот процесс называется переливанием (трансфузией) крови.
Естественно, такая мысль не могла не зародиться у медиков, которым приходилось сталкиваться с печальными последствиями обильной кровопотери, и первое успешное переливание крови было предпринято еще в 1667 г. во Франции неким Жан-Батистом Дени и его коллегой Эфферезом. Для переливания эти отважные люди использовали кровь ягненка. В результате им удалось спасти жизнь 16-летнему юноше. Однако сторонников этого метода ждало еще великое множество разочарований, потому что далеко не все попытки давали желаемый результат. Скорее даже наоборот: слишком часто пациенты погибали по непонятным для медиков причинам, обескураживая даже самых увлеченных энтузиастов. Таким образом наука подошла вплотную к объяснению несовместимости человеческой крови.
Но только эксперименты, проведенные в 1900—1907 гг. австрийцем К. Ландштейнером, окончательно определили систему групп крови у человека, тем самым положив конец осложнениям, являвшимся следствием несовместимости крови.
Прежде чем говорить о группах крови и резус-факторе, имеет смысл немного поговорить о генетике. Ген – это участок хромосомной ДНК, который кодирует специфический белок. Аллелями называют различные формы одного и того же гена, расположенные в одинаковых участках (локусах) гомологичных хромосом. Различные аллели определяют варианты развития одного и того же признака. Так как гены находятся на хромосомах, а хромосомы существуют парами, наши гены обычно присутствуют в виде пары аллелей.
Аллели могут быть доминантными или рецессивными, поэтому комбинация аллелей в паре определяет характерный признак. Доминантная аллель, обозначаемая заглавной буквой, определяет признак (например, цвет глаз) независимо от того, присутствует ли она в одной или двух копиях: WW или Ww. Рецессивная аллель, обозначаемая строчной буквой, определяет признак (например, голубые глаза) только в том случае, если присутствует в двух копиях: ww. Возможны следующие комбинации аллелей: WW, Ww и ww. Физическое проявление признака (например, тип роста волос) определяется набором генов: комбинации WW и Ww дают проявиться доминантным признакам (карие глаза), в то время как ww – рецессивным (голубые глаза).
Теперь о системах антигенов эритроцитов. Группы крови определяются антигенами (в этом случае – гликопротеинами, расположенными на мембране эритроцитов. Хотя в настоящее время известно 25 систем антигенов, важнейшими для человека все же остаются группы крови по системе АВ0 и резус-фактор (Rh). Наличие этих антигенов генетически обусловлено двумя генами: геном АВ0 и Rh-геном. Давайте начнем с Rh-фактора, получившего свое необычное название от обезьян резус, у которых и был впервые обнаружен.
Если унаследована аллель, определяющая образование этого гликопротеина (обозначенная Rh+), то он появится на мембране клетки. Существует и другая аллель (обозначенная Rh-), наличие которой означает отсутствие антигена. Единственный способ получить клетку без Rh-фактора состоит в том, чтобы обе гомологичные хромосомы содержали аллели Rh-. Следовательно, отрицательный резус-фактор – рецессивный признак. Вы будете Rh-положительным, если унаследовали по крайней мере одну Rh+ аллель (то есть «в сумме» ++ или +–).
Ген АВ0, который получил свое странное название от этих трех аллелей, определяет другой тип крови: A, B, ну и конечно 0. Этот ген иллюстрирует другую интересную вещь, которая иногда встречается в наследовании: некоторые гены – кодоминантны. Кодоминантными генами называются такие, у которых две аллели, например А и В, обе являются доминантными, и наличие в генотипе их обеих (АВ) определяет вариант, в котором проявляются оба признака, кодируемые этими генами (то есть гликопротеины А и B).
Подобно Rh-аллели, 0 (I) аллель может воспроизвести группу крови 0 только в том случае, если обе унаследованных аллели – 0 (00), то есть 0-аллель – рецессивная.
Таблица 3
Групповая принадлежность людей по системе АВ0
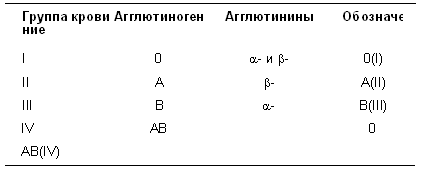
Групповая совместимость крови основывается на факте, что несовместимые образцы крови агглютинируют, или склеиваются при смешивании. Это происходит из-за присутствия антител, атакующих чужеродные поверхностные антигены (А, В или Rh+, но не 0 или Rh-) по этой причине поверхностные антигены иногда называют агглютиногенами, а антитела, находящиеся в плазме, называют агглютининами. Три антитела называют, и законно, анти-А (или – антитела), анти-B (или – антитела), и анти-Rh. – и – антитела всегда находят у людей с определенными группами крови (в таблице представлены варианты групп крови), даже без предшествующего присутствия чужеродного антигена, но анти-Rh вырабатывается иммунной системой только после встречи с антигеном.
Беглый взгляд на таблицу групп крови выявляет некоторые интересные особенности. Любая несовместимая группа крови должна иметь антиген, который является чуждым получателю. AB+ кровь содержит все три антигена (A, B, и Rh+), и ни одного антитела; также нет такого типа крови, который является несовместимым с AB+, универсальным реципиентом крови.
Большинству вообще из нас доводилось слышать, что группа 0(I) – универсальный донор, подразумевая под этим, что такую кровь можно без опасений переливать любому человеку. Это верно лишь отчасти. Вы не забыли, что есть кровь 0(I)+ и 0(I)-? Сверьтесь с таблицей. 0(I)+ имеет Rh-антиген, который будет чуждым любому пациенту с Rh– (А(II)-, В(III)-, АВ(IV)– и 0(I)-). И только группа 0(I)– вообще не имеет чужеродных антигенов, что и делает именно ее универсальным донором.
Таблица 4
Типы крови по содержащимся в них антителам и антигенам с учетом Rh-фактора

При переливании группа крови сперва определяется лечащим врачом и повторно врачом-лаборантом. Такая система двойного контроля позволяет избежать ошибок. Определение резус-принадлежности производится врачом-лаборантом. Данные о группе крови и резус-принадлежности выносятся на первую страницу истории болезни. Непосредственно перед переливанием делают пробу на индивидуальную совместимость крови донора и реципиента.
Даже если больному переливают кровь той же группы, во избежание осложнений врач делает биологическую пробу: вводит по 25 мл крови донора трехкратно, с перерывами по 3 мин. Если при этом у больного не отмечается отрицательная реакция (тревожность, неприятные ощущения), врач переливает намеченное им количество крови полностью.
После открытия резус-фактора, сделанного К. Ландштейнером и А. Винером в 1940 г., ученые смогли объяснить те случаи осложнений, которые отмечались даже при переливании правильно подобранных групп крови. После первого переливания Rh-отрицательному больному Rh-положительной крови у последнего вырабатывались антитела, которые склеивали и разрушали донорские эритроциты при повторной трансфузии. Позже было установлено, что резус-фактор, дающий положительную реакцию, содержится в крови примерно у 85% людей, остальные 15% являются резус-отрицательными.
Резус-фактор влияет не только на совместимость крови у донора и реципиента. Различиями в резус-принадлежности матери и плода объясняется тяжелое заболевание новорожденных – гемолитическая желтуха, развивающаяся в тех случаях, когда резус-отрицательная мать вынашивает резус-положительного ребенка.
Через плаценту в кровь матери проникают Rh+ эритроциты ребенка, и ее иммунная система реагирует на них как на чужеродные антитела, вырабатывая все больше и больше соответствующих антигенов. Эти антигены опять-таки через плаценту попадают в кровеносную систему плода и разрушают его эритроциты. Развивается ситуация, называемые резус-конфликт. В результате ребенок либо погибает еще в утробе, либо рождается тяжело больным.
Первый ребенок от резус-положительного отца и резус-отрицательной матери, как правило, рождается здоровым, но вторая и последующие беременности, равно как и аборт, многократно увеличивают вероятность развития резус-конфликта.
Вот почему в женских консультациях обязательно определяют резус-фактор для всех беременных. И беременная женщина с резус-отрицательной кровью остается под особым наблюдением: у нее постоянно проверяют титр антител, то есть содержание в крови антител к резус-положительным эритроцитам плода. Если титр возрастает, врач немедленно должен предпринять меры, тормозящие выработку антител.
Естественно, такая мысль не могла не зародиться у медиков, которым приходилось сталкиваться с печальными последствиями обильной кровопотери, и первое успешное переливание крови было предпринято еще в 1667 г. во Франции неким Жан-Батистом Дени и его коллегой Эфферезом. Для переливания эти отважные люди использовали кровь ягненка. В результате им удалось спасти жизнь 16-летнему юноше. Однако сторонников этого метода ждало еще великое множество разочарований, потому что далеко не все попытки давали желаемый результат. Скорее даже наоборот: слишком часто пациенты погибали по непонятным для медиков причинам, обескураживая даже самых увлеченных энтузиастов. Таким образом наука подошла вплотную к объяснению несовместимости человеческой крови.
Но только эксперименты, проведенные в 1900—1907 гг. австрийцем К. Ландштейнером, окончательно определили систему групп крови у человека, тем самым положив конец осложнениям, являвшимся следствием несовместимости крови.
Прежде чем говорить о группах крови и резус-факторе, имеет смысл немного поговорить о генетике. Ген – это участок хромосомной ДНК, который кодирует специфический белок. Аллелями называют различные формы одного и того же гена, расположенные в одинаковых участках (локусах) гомологичных хромосом. Различные аллели определяют варианты развития одного и того же признака. Так как гены находятся на хромосомах, а хромосомы существуют парами, наши гены обычно присутствуют в виде пары аллелей.
Аллели могут быть доминантными или рецессивными, поэтому комбинация аллелей в паре определяет характерный признак. Доминантная аллель, обозначаемая заглавной буквой, определяет признак (например, цвет глаз) независимо от того, присутствует ли она в одной или двух копиях: WW или Ww. Рецессивная аллель, обозначаемая строчной буквой, определяет признак (например, голубые глаза) только в том случае, если присутствует в двух копиях: ww. Возможны следующие комбинации аллелей: WW, Ww и ww. Физическое проявление признака (например, тип роста волос) определяется набором генов: комбинации WW и Ww дают проявиться доминантным признакам (карие глаза), в то время как ww – рецессивным (голубые глаза).
Теперь о системах антигенов эритроцитов. Группы крови определяются антигенами (в этом случае – гликопротеинами, расположенными на мембране эритроцитов. Хотя в настоящее время известно 25 систем антигенов, важнейшими для человека все же остаются группы крови по системе АВ0 и резус-фактор (Rh). Наличие этих антигенов генетически обусловлено двумя генами: геном АВ0 и Rh-геном. Давайте начнем с Rh-фактора, получившего свое необычное название от обезьян резус, у которых и был впервые обнаружен.
Если унаследована аллель, определяющая образование этого гликопротеина (обозначенная Rh+), то он появится на мембране клетки. Существует и другая аллель (обозначенная Rh-), наличие которой означает отсутствие антигена. Единственный способ получить клетку без Rh-фактора состоит в том, чтобы обе гомологичные хромосомы содержали аллели Rh-. Следовательно, отрицательный резус-фактор – рецессивный признак. Вы будете Rh-положительным, если унаследовали по крайней мере одну Rh+ аллель (то есть «в сумме» ++ или +–).
Ген АВ0, который получил свое странное название от этих трех аллелей, определяет другой тип крови: A, B, ну и конечно 0. Этот ген иллюстрирует другую интересную вещь, которая иногда встречается в наследовании: некоторые гены – кодоминантны. Кодоминантными генами называются такие, у которых две аллели, например А и В, обе являются доминантными, и наличие в генотипе их обеих (АВ) определяет вариант, в котором проявляются оба признака, кодируемые этими генами (то есть гликопротеины А и B).
Подобно Rh-аллели, 0 (I) аллель может воспроизвести группу крови 0 только в том случае, если обе унаследованных аллели – 0 (00), то есть 0-аллель – рецессивная.
Таблица 3
Групповая принадлежность людей по системе АВ0

Групповая совместимость крови основывается на факте, что несовместимые образцы крови агглютинируют, или склеиваются при смешивании. Это происходит из-за присутствия антител, атакующих чужеродные поверхностные антигены (А, В или Rh+, но не 0 или Rh-) по этой причине поверхностные антигены иногда называют агглютиногенами, а антитела, находящиеся в плазме, называют агглютининами. Три антитела называют, и законно, анти-А (или – антитела), анти-B (или – антитела), и анти-Rh. – и – антитела всегда находят у людей с определенными группами крови (в таблице представлены варианты групп крови), даже без предшествующего присутствия чужеродного антигена, но анти-Rh вырабатывается иммунной системой только после встречи с антигеном.
Беглый взгляд на таблицу групп крови выявляет некоторые интересные особенности. Любая несовместимая группа крови должна иметь антиген, который является чуждым получателю. AB+ кровь содержит все три антигена (A, B, и Rh+), и ни одного антитела; также нет такого типа крови, который является несовместимым с AB+, универсальным реципиентом крови.
Большинству вообще из нас доводилось слышать, что группа 0(I) – универсальный донор, подразумевая под этим, что такую кровь можно без опасений переливать любому человеку. Это верно лишь отчасти. Вы не забыли, что есть кровь 0(I)+ и 0(I)-? Сверьтесь с таблицей. 0(I)+ имеет Rh-антиген, который будет чуждым любому пациенту с Rh– (А(II)-, В(III)-, АВ(IV)– и 0(I)-). И только группа 0(I)– вообще не имеет чужеродных антигенов, что и делает именно ее универсальным донором.
Таблица 4
Типы крови по содержащимся в них антителам и антигенам с учетом Rh-фактора

При переливании группа крови сперва определяется лечащим врачом и повторно врачом-лаборантом. Такая система двойного контроля позволяет избежать ошибок. Определение резус-принадлежности производится врачом-лаборантом. Данные о группе крови и резус-принадлежности выносятся на первую страницу истории болезни. Непосредственно перед переливанием делают пробу на индивидуальную совместимость крови донора и реципиента.
Даже если больному переливают кровь той же группы, во избежание осложнений врач делает биологическую пробу: вводит по 25 мл крови донора трехкратно, с перерывами по 3 мин. Если при этом у больного не отмечается отрицательная реакция (тревожность, неприятные ощущения), врач переливает намеченное им количество крови полностью.
После открытия резус-фактора, сделанного К. Ландштейнером и А. Винером в 1940 г., ученые смогли объяснить те случаи осложнений, которые отмечались даже при переливании правильно подобранных групп крови. После первого переливания Rh-отрицательному больному Rh-положительной крови у последнего вырабатывались антитела, которые склеивали и разрушали донорские эритроциты при повторной трансфузии. Позже было установлено, что резус-фактор, дающий положительную реакцию, содержится в крови примерно у 85% людей, остальные 15% являются резус-отрицательными.
Резус-фактор влияет не только на совместимость крови у донора и реципиента. Различиями в резус-принадлежности матери и плода объясняется тяжелое заболевание новорожденных – гемолитическая желтуха, развивающаяся в тех случаях, когда резус-отрицательная мать вынашивает резус-положительного ребенка.
Через плаценту в кровь матери проникают Rh+ эритроциты ребенка, и ее иммунная система реагирует на них как на чужеродные антитела, вырабатывая все больше и больше соответствующих антигенов. Эти антигены опять-таки через плаценту попадают в кровеносную систему плода и разрушают его эритроциты. Развивается ситуация, называемые резус-конфликт. В результате ребенок либо погибает еще в утробе, либо рождается тяжело больным.
Первый ребенок от резус-положительного отца и резус-отрицательной матери, как правило, рождается здоровым, но вторая и последующие беременности, равно как и аборт, многократно увеличивают вероятность развития резус-конфликта.
Вот почему в женских консультациях обязательно определяют резус-фактор для всех беременных. И беременная женщина с резус-отрицательной кровью остается под особым наблюдением: у нее постоянно проверяют титр антител, то есть содержание в крови антител к резус-положительным эритроцитам плода. Если титр возрастает, врач немедленно должен предпринять меры, тормозящие выработку антител.
Иммуноферментный анализ сыворотки крови (ИФА)
Различают антитела трех классов: иммуноглобулины M, A, G (JgМ, JgА, JgG). Они накапливаются в сыворотке крови и секретах организма через разные промежутки времени от начала инфицирования.
При первичном инфицировании первыми появляются иммуноглобулины класса М, которые выявляются методом ИФА с 5 дня от начала заболевания по 5–6 неделю, затем они в течение нескольких недель или месяцев исчезают из кровотока. Также иммуноглобулины класса М могут вырабатываться при активации хронической инфекции.
Иммуноглобулины класса G выявляются через 3–4 недели от начала первичного инфицирования или от момента обострения хронического заболевания и циркулируют в крови длительно, сохраняясь в течение нескольких месяцев или лет. Увеличение титров JgG в двух последовательно взятых пробах через 2 недели свидетельствует о текущей инфекции или реинфекции. Иммуноглобулинами класса G обеспечивается также постинфекционный или поствакцинальный иммунитет.
Иммуноглобулины класса А выявляются через 2–4 недели от момента инфицирования или обострения хронического заболевания. 20% от их общего количества циркулирует в сыворотке крови, 80% входит в состав секрета слизистых оболочек (их можно определить в семенной или вагинальной жидкостях). Через 2 недели – 2 месяца после изгнания и уничтожения инфекционного агента иммуноглобулины класса А исчезают из кровотока, что является критерием излеченности. Если JgA не исчезают после проведенного лечения, то это указывает на хроническую или персистирующую инфекцию.
У новорожденных и детей до 6–9 месяцев JgG в крови имеют материнское происхождение, так как еще не могут синтезироваться в организме ребенка. В то же время JgМ синтезируются в организме плода с 14-й недели развития, а материнские JgM не проникают через плаценту, поэтому определение специфических JgM в крови новорожденных свидетельствует о внутриутробном инфицировании.
Таблица 5
Интерпретация результатов анализов при исследовании иммуноглобулинов

(–) – отрицательный результат
(+) – положительный результат
При первичном инфицировании первыми появляются иммуноглобулины класса М, которые выявляются методом ИФА с 5 дня от начала заболевания по 5–6 неделю, затем они в течение нескольких недель или месяцев исчезают из кровотока. Также иммуноглобулины класса М могут вырабатываться при активации хронической инфекции.
Иммуноглобулины класса G выявляются через 3–4 недели от начала первичного инфицирования или от момента обострения хронического заболевания и циркулируют в крови длительно, сохраняясь в течение нескольких месяцев или лет. Увеличение титров JgG в двух последовательно взятых пробах через 2 недели свидетельствует о текущей инфекции или реинфекции. Иммуноглобулинами класса G обеспечивается также постинфекционный или поствакцинальный иммунитет.
Иммуноглобулины класса А выявляются через 2–4 недели от момента инфицирования или обострения хронического заболевания. 20% от их общего количества циркулирует в сыворотке крови, 80% входит в состав секрета слизистых оболочек (их можно определить в семенной или вагинальной жидкостях). Через 2 недели – 2 месяца после изгнания и уничтожения инфекционного агента иммуноглобулины класса А исчезают из кровотока, что является критерием излеченности. Если JgA не исчезают после проведенного лечения, то это указывает на хроническую или персистирующую инфекцию.
У новорожденных и детей до 6–9 месяцев JgG в крови имеют материнское происхождение, так как еще не могут синтезироваться в организме ребенка. В то же время JgМ синтезируются в организме плода с 14-й недели развития, а материнские JgM не проникают через плаценту, поэтому определение специфических JgM в крови новорожденных свидетельствует о внутриутробном инфицировании.
Таблица 5
Интерпретация результатов анализов при исследовании иммуноглобулинов

(–) – отрицательный результат
(+) – положительный результат
Глава 6. Биохимическое исследование крови
Современные технологии, компьютеризация и автоматизация многих процессов разительным образом изменили характер работы клинико-диагностических лабораторий, и особенно явно это отражается на биохимических исследованиях.
Автоанализаторы значительно ускорили и упростили выполнение практически всех видов биохимических и других видов исследований, а их подключение к компьютерам позволяет быстро обобщать серии исследований для одного пациента, хранить в памяти все полученные результаты и подготовить обоснованный ответ клиницисту.
В России начат серийный выпуск специальных наборов реагентов для автоанализаторов. Все выпускаемые в настоящее время наборы, а также стандартные, контрольные, калибровочные образцы стандартизированы и зарегистрированы в Минздравсоцразвития РФ.
Все выпускаемые наборы подвергаются тщательной проверке в ведущих лабораториях и медицинских центрах и только после этого регистрируются. Такая стандартизация позволяет сделать сопоставимыми результаты исследований, полученные в самых разных медицинских учреждениях.
Автоанализаторы значительно ускорили и упростили выполнение практически всех видов биохимических и других видов исследований, а их подключение к компьютерам позволяет быстро обобщать серии исследований для одного пациента, хранить в памяти все полученные результаты и подготовить обоснованный ответ клиницисту.
В России начат серийный выпуск специальных наборов реагентов для автоанализаторов. Все выпускаемые в настоящее время наборы, а также стандартные, контрольные, калибровочные образцы стандартизированы и зарегистрированы в Минздравсоцразвития РФ.
Все выпускаемые наборы подвергаются тщательной проверке в ведущих лабораториях и медицинских центрах и только после этого регистрируются. Такая стандартизация позволяет сделать сопоставимыми результаты исследований, полученные в самых разных медицинских учреждениях.
Показатели белкового обмена
Как уже говорилось выше, кровь состоит из жидкой компоненты и клеток, или форменных элементов. Кровь, набранная в сухую пробирку, через несколько минут разделится на сгусток темно-красного цвета и светло-желтую жидкость над сгустком. Это и будет сыворотка крови. В отличие от сыворотки плазма крови содержит белок фибриноген. Он переходит в сгусток крови во время коагуляции, а значит, чтобы получить плазму крови, нужно добавить в цельную кровь консервирующее вещество, препятствующее коагуляции, и только потом подвергнуть ее центрифугированию.
Кровь состоит на 45% из взвешенных в ней форменных элементов и на 55% из плазмы.
Пожалуй, для полноты картины здесь следует напомнить читателям и о межклеточной жидкости, окружающей клетки нашего тела. Конечно, кровь несет главную нагрузку в вопросе транспортировки веществ к и от тканей тела; но фактически клетки тканей получает вещества из кровеносных сосудов через жидкость, их окружающую. Эту жидкость и называют межклеточной жидкостью.
Растворенные в этой жидкости вещества, так же как часть молекул воды, входят в клетки, и таким же образом выходят в межклеточную жидкость из клеток. Кроме того, концентрация различных веществ в межклеточной жидкости может меняться (например, кислород входит в клетки, а углекислый газ выходит). Таким же самым образом концентрация веществ, растворенных в крови, отличается в капиллярных артериях и венах. За исключением кислорода и небольшого количества углекислого газа, все другие вещества, нуждающиеся в транспорте, передаются через плазму. Плазма в большей степени, чем клетки крови, связывает две циркуляторные системы нашего тела, сердечно-сосудистую и лимфатическую. И все вещества перемещаются по организму следующим путем: из плазмы – в межклеточную жидкость – в лимфу – и назад, в плазму. Важно понять, что эти жидкости: кровь, межклеточная жидкость и лимфа – являются по существу одним и тем же, несмотря на любые различия в концентрации; главное различие между ними – местоположение (точно так же, единственное различие между магмой и лавой – местоположение: магма находится под землей, а лава выходит на поверхность). Лимфатические капилляры – открытые сосуды, в стенках которых с известной периодичностью встречаются отверстия, являющиеся местами вхождения межклеточной жидкости. Лимфатическая жидкость в конечном счете соединяется с плазмой через грудной проток в подключичной вене.
В плазме содержится 92% воды, 7% белков и 1% других веществ (углеводов, жиров и минеральных солей). Тот факт, что вода является таким превосходным растворителем, позволяет крови переносить много растворенных веществ. Большинство этих веществ – плазменные белки. Это высокомолекулярные соединения, способные вести себя и как кислоты, и как основания благодаря тому, что их молекулы содержат и карбоксильные (кислотные группы СООН), и аминогруппы (основные группы NH2). Благодаря этим уникальным свойствам плазменные белки способны активно взаимодействовать с самым широким спектром различных веществ, поступающих в кровь.
Кровь состоит на 45% из взвешенных в ней форменных элементов и на 55% из плазмы.
Пожалуй, для полноты картины здесь следует напомнить читателям и о межклеточной жидкости, окружающей клетки нашего тела. Конечно, кровь несет главную нагрузку в вопросе транспортировки веществ к и от тканей тела; но фактически клетки тканей получает вещества из кровеносных сосудов через жидкость, их окружающую. Эту жидкость и называют межклеточной жидкостью.
Растворенные в этой жидкости вещества, так же как часть молекул воды, входят в клетки, и таким же образом выходят в межклеточную жидкость из клеток. Кроме того, концентрация различных веществ в межклеточной жидкости может меняться (например, кислород входит в клетки, а углекислый газ выходит). Таким же самым образом концентрация веществ, растворенных в крови, отличается в капиллярных артериях и венах. За исключением кислорода и небольшого количества углекислого газа, все другие вещества, нуждающиеся в транспорте, передаются через плазму. Плазма в большей степени, чем клетки крови, связывает две циркуляторные системы нашего тела, сердечно-сосудистую и лимфатическую. И все вещества перемещаются по организму следующим путем: из плазмы – в межклеточную жидкость – в лимфу – и назад, в плазму. Важно понять, что эти жидкости: кровь, межклеточная жидкость и лимфа – являются по существу одним и тем же, несмотря на любые различия в концентрации; главное различие между ними – местоположение (точно так же, единственное различие между магмой и лавой – местоположение: магма находится под землей, а лава выходит на поверхность). Лимфатические капилляры – открытые сосуды, в стенках которых с известной периодичностью встречаются отверстия, являющиеся местами вхождения межклеточной жидкости. Лимфатическая жидкость в конечном счете соединяется с плазмой через грудной проток в подключичной вене.
В плазме содержится 92% воды, 7% белков и 1% других веществ (углеводов, жиров и минеральных солей). Тот факт, что вода является таким превосходным растворителем, позволяет крови переносить много растворенных веществ. Большинство этих веществ – плазменные белки. Это высокомолекулярные соединения, способные вести себя и как кислоты, и как основания благодаря тому, что их молекулы содержат и карбоксильные (кислотные группы СООН), и аминогруппы (основные группы NH2). Благодаря этим уникальным свойствам плазменные белки способны активно взаимодействовать с самым широким спектром различных веществ, поступающих в кровь.
Конец бесплатного ознакомительного фрагмента
