Страница:
Чрезвычайно важным защитным механизмом является собственно иммунная система тонкой кишки, которая играет большую роль во взаимодействиях организма хозяина с кишечными бактериями, вирусами, паразитами, лекарственными препаратами, химикалиями, а также при контакте с разными антигенными веществами. К их числу относятся экзогенные пищевые антигены, белки и пептиды пищи, аутогены десквамированных кишечных клеток, антигены микроорганизмов и вирусов, токсины и т. д. В дополнение к нормальной защитной роли кишечная иммунная система может быть значимой в патогенезе некоторых кишечных заболеваний.
Иммунокомпетентная лимфатическая ткань тонкой кишки составляет около 25 % всей ее слизистой оболочки. В анатомическом и функциональном отношениях эта ткань тонкой кишки делится на три отдела:
1) пейеровы бляшки – скопления лимфатических фолликулов, в которых собираются антигены и вырабатываются антитела к ним;
2) лимфоциты и плазматические клетки, вырабатывающие секреторные IgA;
3) внутриэпителиальные лимфоциты, в основном Т-лимфоциты.
Пейеровы бляшки (около 200–300 у взрослого человека) состоят из организованных скоплений лимфатических фолликул, в которых находятся предшественники популяции лимфоцитов. Эти лимфоциты заселяют другие области кишечной слизистой оболочки и принимают участие в ее локальной иммунной деятельности. В этом отношении пейеровы бляшки могут быть рассмотрены как область, инициирующая иммунную деятельность тонкой кишки. Пейеровы бляшки содержат В– и Т-клетки, а в эпителии над бляшками локализовано небольшое количество М-клеток, или мембранных клеток. Предполагается, что эти клетки участвуют в создании благоприятных условий для доступа люминальных антигенов к субэпителиальным лимфоцитам.
Интерэпителиальные клетки тонкой кишки расположены между кишечными клетками в базальной части эпителия, ближе к базальной мембране. Их отношение к другим кишечным клеткам составляет примерно 1: 6. Около 25 % интерэпителиальных лимфоцитов имеют маркеры Т-клеток.
В слизистой оболочке тонкой кишки человека находится более 400 ООО плазматических клеток на 1 мм2, а также около 1 млн лимфоцитов в расчете на 1 см2. В норме в тощей кишке содержится от 6 до 40 лимфоцитов в расчете на 100 эпителиальных клеток. Это означает, что в тонкой кишке кроме эпителиального слоя, разделяющего энтеральную и внутреннюю среды организма, существует еще мощный лейкоцитарный слой.
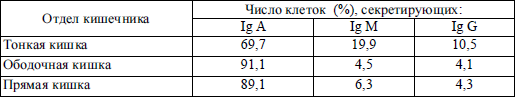
Как отмечено выше, иммунная система кишечника встречает огромное количество экзогенных пищевых антигенов. Клетки тонкой и толстой кишок продуцируют ряд иммуноглобулинов (Ig A, Ig Е, Ig G, Ig М), но преимущественно Ig А (табл. 2.2). Иммуноглобулины А и Е, секретируемые в полость кишки, по-видимому, адсорбируются на структурах кишечной слизистой оболочки, создавая в области гликокаликса дополнительный защитный слой.
Таблица 2.2
Количество клеток тонкой и толстой кишок, продуцирующих иммуноглобулины
 Функции специфического защитного барьера выполняет также слизь, которая покрывает большую часть эпителиальной поверхности тонкой кишки. Это – сложная смесь различных макромолекул, в том числе гликопротеидов, воды, электролитов, микроорганизмов, десквамированных кишечных клеток и т. д. Муцин – компонент слизи, придающий ей гелеобразность, способствует механической защите апикальной поверхности кишечных клеток.
Функции специфического защитного барьера выполняет также слизь, которая покрывает большую часть эпителиальной поверхности тонкой кишки. Это – сложная смесь различных макромолекул, в том числе гликопротеидов, воды, электролитов, микроорганизмов, десквамированных кишечных клеток и т. д. Муцин – компонент слизи, придающий ей гелеобразность, способствует механической защите апикальной поверхности кишечных клеток.
Существует еще один важный барьер, предупреждающий поступление токсических веществ и антигенов из энтеральной во внутреннюю среду организма. Этот барьер можно назвать трансформационным, или энзиматическим, так как он обусловлен ферментными системами тонкой кишки, осуществляющими последовательную деполимеризацию (трансформацию) пищевых поли– и олигомеров до мономеров, способных к утилизации. Энзиматический барьер состоит из ряда отдельных пространственно разделенных барьеров, но в целом образует единую взаимосвязанную систему.
Патофизиология
Толстая кишка
Патофизиология
Иммунокомпетентная лимфатическая ткань тонкой кишки составляет около 25 % всей ее слизистой оболочки. В анатомическом и функциональном отношениях эта ткань тонкой кишки делится на три отдела:
1) пейеровы бляшки – скопления лимфатических фолликулов, в которых собираются антигены и вырабатываются антитела к ним;
2) лимфоциты и плазматические клетки, вырабатывающие секреторные IgA;
3) внутриэпителиальные лимфоциты, в основном Т-лимфоциты.
Пейеровы бляшки (около 200–300 у взрослого человека) состоят из организованных скоплений лимфатических фолликул, в которых находятся предшественники популяции лимфоцитов. Эти лимфоциты заселяют другие области кишечной слизистой оболочки и принимают участие в ее локальной иммунной деятельности. В этом отношении пейеровы бляшки могут быть рассмотрены как область, инициирующая иммунную деятельность тонкой кишки. Пейеровы бляшки содержат В– и Т-клетки, а в эпителии над бляшками локализовано небольшое количество М-клеток, или мембранных клеток. Предполагается, что эти клетки участвуют в создании благоприятных условий для доступа люминальных антигенов к субэпителиальным лимфоцитам.
Интерэпителиальные клетки тонкой кишки расположены между кишечными клетками в базальной части эпителия, ближе к базальной мембране. Их отношение к другим кишечным клеткам составляет примерно 1: 6. Около 25 % интерэпителиальных лимфоцитов имеют маркеры Т-клеток.
В слизистой оболочке тонкой кишки человека находится более 400 ООО плазматических клеток на 1 мм2, а также около 1 млн лимфоцитов в расчете на 1 см2. В норме в тощей кишке содержится от 6 до 40 лимфоцитов в расчете на 100 эпителиальных клеток. Это означает, что в тонкой кишке кроме эпителиального слоя, разделяющего энтеральную и внутреннюю среды организма, существует еще мощный лейкоцитарный слой.
Как отмечено выше, иммунная система кишечника встречает огромное количество экзогенных пищевых антигенов. Клетки тонкой и толстой кишок продуцируют ряд иммуноглобулинов (Ig A, Ig Е, Ig G, Ig М), но преимущественно Ig А (табл. 2.2). Иммуноглобулины А и Е, секретируемые в полость кишки, по-видимому, адсорбируются на структурах кишечной слизистой оболочки, создавая в области гликокаликса дополнительный защитный слой.
Таблица 2.2
Количество клеток тонкой и толстой кишок, продуцирующих иммуноглобулины

Существует еще один важный барьер, предупреждающий поступление токсических веществ и антигенов из энтеральной во внутреннюю среду организма. Этот барьер можно назвать трансформационным, или энзиматическим, так как он обусловлен ферментными системами тонкой кишки, осуществляющими последовательную деполимеризацию (трансформацию) пищевых поли– и олигомеров до мономеров, способных к утилизации. Энзиматический барьер состоит из ряда отдельных пространственно разделенных барьеров, но в целом образует единую взаимосвязанную систему.
Патофизиология
Во врачебной практике довольно часто встречаются нарушения функций тонкой кишки. Они не всегда сопровождаются отчетливой клинической симптоматикой и иногда маскируются внекишечными расстройствами.
По аналогии с принятыми терминами («сердечная недостаточность», «почечная недостаточность», «печеночная недостаточность» и др.), по мнению многих авторов, целесообразно нарушения функций тонкой кишки, ее недостаточность, обозначать термином «энтеральная недостаточность» («недостаточность тонкой кишки»). Под энтеральной недостаточностью принято понимать клинический синдром, обусловленный нарушениями функций тонкой кишки со всеми их интестинальными и экстраинтестинальными проявлениями. Энтеральная недостаточность возникает при патологии самой тонкой кишки, а также при различных заболеваниях других органов и систем. При врожденных первичных формах недостаточности тонкой кишки чаще всего наследуется изолированный селективный пищеварительный или транспортный дефект. При приобретенных формах преобладают множественные дефекты пищеварения и всасывания.
Поступающие в двенадцатиперстную кишку большие порции желудочного содержимого хуже пропитываются дуоденальным соком и медленнее нейтрализуются. Дуоденальное пищеварение страдает и потому, что в отсутствие свободной соляной кислоты или при ее дефиците значительно угнетается синтез секретина и холецистокинина, регулирующих секреторную деятельность поджелудочной железы. Уменьшение образования панкреатического сока в свою очередь приводит к расстройствам кишечного пищеварения. Это служит причиной того, что химус в не подготовленном для всасывания виде поступает в нижележащие отделы тонкой кишки и раздражает рецепторы кишечной стенки. Возникает усиление перистальтики и секреции воды в просвет кишечной трубки, развивается диарея и энтеральная недостаточность как проявление тяжелых расстройств пищеварения.
В условиях гипохлоргидрии и тем более ахилии резко ухудшается всасывательная функция кишечника. Возникают нарушения белкового обмена, приводящие к дистрофическим процессам во многих внутренних органах, особенно в сердце, почках, печени, мышечной ткани. Могут развиться расстройства иммунной системы. Гастрогенная энтеральная недостаточность рано приводит к гиповитаминозам, дефициту в организме минеральных солей, нарушениям гомеостаза и свертывающей системы крови.
В формировании энтеральной недостаточности определенное значение имеют нарушения секреторной функции кишечника. Механическое раздражение слизистой оболочки тонкой кишки резко увеличивает выделение жидкой части сока. В тонкую кишку усиленно секретируются не только вода и низкомолекулярные вещества, но и белки, гликопротеиды, липиды. Описываемые явления, как правило, развиваются при резко угнетенном кислотообразовании в желудке и неполноценном в связи с этим интрагастральным пищеварением: непереваренные компоненты пищевого комка вызывают резкое раздражение рецепторов слизистой оболочки тонкой кишки, инициируя усиление секреции. Аналогичные процессы имеют место у больных, перенесших резекцию желудка, включая пилорический сфинктер. Выпадение резервуарной функции желудка, угнетение желудочной секреции, некоторые другие послеоперационные расстройства способствуют развитию так называемого синдрома «сброса» (демпинг-синдром). Одним из проявлений этого послеоперационного расстройства является усиление секреторной активности тонкой кишки, ее гипермоторика, проявляющиеся поносом тонкокишечного типа. Угнетение продукции кишечного сока, развивающееся при ряде патологических состояний (дистрофия, воспаление, атрофия слизистой оболочки тонкой кишки, ишемическая болезнь органов пищеварения, белково-энергетическая недостаточность организма и др.), уменьшение в нем ферментов составляют патофизиологическую основу нарушений секреторной функции кишечника. При снижении эффективности кишечного пищеварения гидролиз жиров и белков в полости тонкой кишки изменяется мало, так как компенсаторно увеличивается секреция липазы и протеаз с панкреатическим соком.
Наибольшее значение дефекты пищеварительных и транспортных процессов имеют у людей с врожденной или приобретенной ферментопатией вследствие недостатка определенных ферментов. Так, в результате дефицита лактазы в клетках кишечной слизистой оболочки нарушается мембранный гидролиз и усвоение молочного сахара (молочная интолерантность, лактазная недостаточность). Недостаточная продукция клетками слизистой оболочки тонкой кишки сахаразы, α-амилазы, мальтазы и изомальтазы приводит к развитию непереносимости больными соответственно сахарозы и крахмала. Во всех случаях кишечного ферментативного дефицита при неполном гидролизе пищевых субстратов образуются токсические метаболиты, провоцирующие развитие тяжелой клинической симптоматики, не только характеризующей усиление проявлений энтеральной недостаточности, но и экстраинтестинальные расстройства.
При различных заболеваниях желудочно-кишечного тракта наблюдаются нарушения полостного и мембранного пищеварения, а также всасывания. Нарушения могут иметь инфекционную и неинфекционную этиологию, быть приобретенными или наследственными. Дефекты мембранного пищеварения и всасывания возникают при нарушениях распределения ферментативных и транспортных активностей вдоль тонкой кишки после, например, оперативных вмешательств, в частности после резекции тонкой кишки. Патология мембранного пищеварения может быть обусловлена атрофией ворсинок и микроворсинок, нарушением структуры и ультраструктуры кишечных клеток, изменением спектра ферментного слоя и сорбционных свойств структур кишечной слизистой оболочки, расстройств моторики кишечника, при которых нарушается перенос пищевых веществ из полости кишки на ее поверхность, при дисбактериозах ит. д.
Нарушения мембранного пищеварения встречаются при довольно широком круге заболеваний, а также после интенсивной терапии антибиотиками, различных оперативных вмешательств на желудочно-кишечном тракте. При многих вирусных заболеваниях (полиомиелит, свинка, аденовирусный грипп, гепатит, корь) возникают тяжелые расстройства пищеварения и всасывания с явлениями диареи и стеатореи. При этих заболеваниях имеет место выраженная атрофия ворсинок, нарушения ультраструктуры щеточной каймы, недостаточность ферментного слоя кишечной слизистой оболочки, что приводит к нарушениям мембранного пищеварения.
Нередко нарушения ультраструктуры щеточной каймы сочетаются с резким уменьшением ферментативной активности энтероцитов. Известны многочисленные случаи, при которых ультраструктура щеточной каймы остается практически нормальной, но тем не менее обнаруживается недостаточность одного или нескольких пищеварительных кишечных ферментов. Многие пищевые интолерантности обусловлены этими специфическими нарушениями ферментного слоя кишечных клеток. В настоящее время парциальные ферментные недостаточности тонкой кишки широко известны.
Дисахаридазные недостаточности (в том числе сахаразная) могут быть первичными, то есть обусловленными соответствующими генетическими дефектами, и вторичными, развивающимися на фоне различных болезней (спру, энтериты, после оперативных вмешательств, при инфекционной диарее и т. д.). Изолированная сахаразная недостаточность встречается редко и в большинстве случаев комбинируется с изменениями активности других дисахаридов, чаще всего изомальтазы. Особенно широко распространена лактазная недостаточность, в результате которой не усваивается молочный сахар (лактоза) и возникает интолерантность к молоку. Лактазная недостаточность определяется генетически рецессивным путем. Предполагается, что степень репрессии лактазного гена связана с историей данной этнической группы.
Ферментные недостаточности кишечной слизистой оболочки могут быть связаны как с нарушением синтеза ферментов в кишечных клетках, так и с нарушением их встраивания в апикальную мембрану, где они выполняют свои пищеварительные функции. Кроме того, они могут быть обусловлены и ускорением деградации соответствующих кишечных ферментов. Таким образом, для правильной интерпретации ряда заболеваний необходимо учитывать нарушения мембранного пищеварения. Дефекты этого механизма приводят к изменениям поступления необходимых пищевых веществ в организм с далеко идущими последствиями.
Причиной нарушений ассимиляции белков могут быть изменения желудочной фазы их гидролиза, однако дефекты кишечной фазы за счет недостаточности панкреатических и кишечных мембранных ферментов более серьезны. К редким генетическим нарушениям относятся энтеропептидазная и трипсиновая недостаточности. Уменьшение пептидазных активностей в тонкой кишке наблюдается при ряде заболеваний, например неизлечимой форме целиакии, болезни Крона, язве двенадцатиперстной кишки, при радио– и химиотерапии (например 5-фторурацилом) и т. д. Следует упомянуть и аминопептидурию, которая связана с уменьшением активности дипептидаз, расщепляющих пролиновые пептиды внутри кишечных клеток.
Многие нарушения функций кишечника при различных формах патологии могут зависеть от состояния гликокаликса и содержащихся в нем пищеварительных ферментов. Нарушения процессов адсорбции панкреатических ферментов на структурах слизистой оболочки тонкой кишки могут быть причиной малнутриции (недостаточности питания), а атрофия гликокаликса может способствовать повреждающему действию токсических агентов на мембрану энтероцитов.
Нарушения процессов всасывания проявляются в их замедлении или патологическом усилении. Замедление всасывания слизистой оболочкой кишечника может быть обусловлено следующими причинами:
1) недостаточным расщеплением пищевых масс в полостях желудка и тонкой кишки (нарушения полостного пищеварения);
2) нарушениями мембранного пищеварения;
3) застойной гиперемией кишечной стенки (парез сосудов, шок);
4) ишемией кишечной стенки (атеросклероз сосудов брыжейки, рубцовая послеоперационная окклюзия сосудов стенки кишки и др.);
5) воспалением тканевых структур стенки тонкой кишки (энтериты);
6) резекцией большей части тонкой кишки (синдром короткой тонкой кишки);
7) непроходимостью в верхних отделах кишечника, когда пищевые массы не поступают в его дистальные отделы.
Патологическое усиление всасывания связано с повышением проницаемости кишечной стенки, что нередко можно наблюдать у больных с расстройством терморегуляции (тепловые поражения организма), инфекционно-токсическими процессами при ряде заболеваний, пищевой аллергии и др. Под воздействием некоторых факторов повышается порог проницаемости слизистой оболочки тонкой кишки для крупномолекулярных соединений, в том числе продуктов неполного расщепления пищевых веществ, белков и пептидов, аллергенов, метаболитов. Появление в крови, во внутренней среде организма чужеродных веществ способствует развитию общих явлений интоксикации, сенсибилизации организма, возникновению аллергических реакций.
При ряде заболеваний, сопровождающихся воспалительными явлениями в тканях тонкой кишки, при пищевых аллергиях, некоторых психических заболеваниях всасывание интактных белков и пептидов может быть существенным фактором в их патогенезе. Некоторые заболевания желудочно-кишечного тракта сопровождаются увеличением проницаемости кишечного барьера для белков и пептидов, а также снижением уровня пептидазных активностей слизистой оболочки тонкой кишки. К ним относятся болезнь Крона, целиакия, белково-энергетическая недостаточность, инвазия паразитическими формами, вирусные и бактериальные гастроэнтериты, хирургические травмы кишечника.
Нельзя не упомянуть такие заболевания, при которых нарушено всасывание нейтральных аминокислот в тонкой кишке, а также цистинурию. При цистинурии наблюдаются комбинированные нарушения транспорта диаминомонокарбоновых кислот и цистина в тонкой кишке. Кроме этих заболеваний существуют такие как изолированная мальабсорбция метионина, триптофана и ряда других аминокислот.
Развитие энтеральной недостаточности и хроническое ее течение способствуют (за счет нарушения процессов мембранного пищеварения и всасывания) возникновению расстройств белкового, энергетического, витаминного, электролитного и других видов обмена веществ с соответствующей клинической симптоматикой. Отмеченные механизмы развития недостаточности пищеварения в конечном итоге реализуются в полиорганную, мультисиндромную картину заболевания.
В формировании патогенетических механизмов энтеральной патологии ускорение перистальтики является одним из типичных расстройств, сопровождающих большинство органических заболеваний. Наиболее частые причины ускорения перистальтики – воспалительные изменения в слизистой оболочке ЖКТ. При этом химус продвигается по кишечнику быстрее и развивается понос. Диарея возникает также при действии на стенку кишечника необычных раздражителей: непереваренной пищи (например, при ахилии), продуктов брожения и гниения, токсических веществ. К ускорению перистальтики ведет повышение возбудимости центра блуждающего нерва, так как он активизирует моторику кишечника. Поносы, способствующие освобождению организма от неусвояемых или токсических веществ, являются защитными. Но при длительной диарее происходят глубокие расстройства пищеварения, связанные с нарушением секреции кишечного сока, переваривания и всасывания пищевых веществ в кишечнике. Замедление перистальтики тонкой кишки относится к редким патофизиологическим механизмам формирования заболеваний. При этом тормозится продвижение пищевой кашицы по кишечнику и развиваются запоры. Этот клинический синдром, как правило, является следствием патологии толстой кишки.
По аналогии с принятыми терминами («сердечная недостаточность», «почечная недостаточность», «печеночная недостаточность» и др.), по мнению многих авторов, целесообразно нарушения функций тонкой кишки, ее недостаточность, обозначать термином «энтеральная недостаточность» («недостаточность тонкой кишки»). Под энтеральной недостаточностью принято понимать клинический синдром, обусловленный нарушениями функций тонкой кишки со всеми их интестинальными и экстраинтестинальными проявлениями. Энтеральная недостаточность возникает при патологии самой тонкой кишки, а также при различных заболеваниях других органов и систем. При врожденных первичных формах недостаточности тонкой кишки чаще всего наследуется изолированный селективный пищеварительный или транспортный дефект. При приобретенных формах преобладают множественные дефекты пищеварения и всасывания.
Поступающие в двенадцатиперстную кишку большие порции желудочного содержимого хуже пропитываются дуоденальным соком и медленнее нейтрализуются. Дуоденальное пищеварение страдает и потому, что в отсутствие свободной соляной кислоты или при ее дефиците значительно угнетается синтез секретина и холецистокинина, регулирующих секреторную деятельность поджелудочной железы. Уменьшение образования панкреатического сока в свою очередь приводит к расстройствам кишечного пищеварения. Это служит причиной того, что химус в не подготовленном для всасывания виде поступает в нижележащие отделы тонкой кишки и раздражает рецепторы кишечной стенки. Возникает усиление перистальтики и секреции воды в просвет кишечной трубки, развивается диарея и энтеральная недостаточность как проявление тяжелых расстройств пищеварения.
В условиях гипохлоргидрии и тем более ахилии резко ухудшается всасывательная функция кишечника. Возникают нарушения белкового обмена, приводящие к дистрофическим процессам во многих внутренних органах, особенно в сердце, почках, печени, мышечной ткани. Могут развиться расстройства иммунной системы. Гастрогенная энтеральная недостаточность рано приводит к гиповитаминозам, дефициту в организме минеральных солей, нарушениям гомеостаза и свертывающей системы крови.
В формировании энтеральной недостаточности определенное значение имеют нарушения секреторной функции кишечника. Механическое раздражение слизистой оболочки тонкой кишки резко увеличивает выделение жидкой части сока. В тонкую кишку усиленно секретируются не только вода и низкомолекулярные вещества, но и белки, гликопротеиды, липиды. Описываемые явления, как правило, развиваются при резко угнетенном кислотообразовании в желудке и неполноценном в связи с этим интрагастральным пищеварением: непереваренные компоненты пищевого комка вызывают резкое раздражение рецепторов слизистой оболочки тонкой кишки, инициируя усиление секреции. Аналогичные процессы имеют место у больных, перенесших резекцию желудка, включая пилорический сфинктер. Выпадение резервуарной функции желудка, угнетение желудочной секреции, некоторые другие послеоперационные расстройства способствуют развитию так называемого синдрома «сброса» (демпинг-синдром). Одним из проявлений этого послеоперационного расстройства является усиление секреторной активности тонкой кишки, ее гипермоторика, проявляющиеся поносом тонкокишечного типа. Угнетение продукции кишечного сока, развивающееся при ряде патологических состояний (дистрофия, воспаление, атрофия слизистой оболочки тонкой кишки, ишемическая болезнь органов пищеварения, белково-энергетическая недостаточность организма и др.), уменьшение в нем ферментов составляют патофизиологическую основу нарушений секреторной функции кишечника. При снижении эффективности кишечного пищеварения гидролиз жиров и белков в полости тонкой кишки изменяется мало, так как компенсаторно увеличивается секреция липазы и протеаз с панкреатическим соком.
Наибольшее значение дефекты пищеварительных и транспортных процессов имеют у людей с врожденной или приобретенной ферментопатией вследствие недостатка определенных ферментов. Так, в результате дефицита лактазы в клетках кишечной слизистой оболочки нарушается мембранный гидролиз и усвоение молочного сахара (молочная интолерантность, лактазная недостаточность). Недостаточная продукция клетками слизистой оболочки тонкой кишки сахаразы, α-амилазы, мальтазы и изомальтазы приводит к развитию непереносимости больными соответственно сахарозы и крахмала. Во всех случаях кишечного ферментативного дефицита при неполном гидролизе пищевых субстратов образуются токсические метаболиты, провоцирующие развитие тяжелой клинической симптоматики, не только характеризующей усиление проявлений энтеральной недостаточности, но и экстраинтестинальные расстройства.
При различных заболеваниях желудочно-кишечного тракта наблюдаются нарушения полостного и мембранного пищеварения, а также всасывания. Нарушения могут иметь инфекционную и неинфекционную этиологию, быть приобретенными или наследственными. Дефекты мембранного пищеварения и всасывания возникают при нарушениях распределения ферментативных и транспортных активностей вдоль тонкой кишки после, например, оперативных вмешательств, в частности после резекции тонкой кишки. Патология мембранного пищеварения может быть обусловлена атрофией ворсинок и микроворсинок, нарушением структуры и ультраструктуры кишечных клеток, изменением спектра ферментного слоя и сорбционных свойств структур кишечной слизистой оболочки, расстройств моторики кишечника, при которых нарушается перенос пищевых веществ из полости кишки на ее поверхность, при дисбактериозах ит. д.
Нарушения мембранного пищеварения встречаются при довольно широком круге заболеваний, а также после интенсивной терапии антибиотиками, различных оперативных вмешательств на желудочно-кишечном тракте. При многих вирусных заболеваниях (полиомиелит, свинка, аденовирусный грипп, гепатит, корь) возникают тяжелые расстройства пищеварения и всасывания с явлениями диареи и стеатореи. При этих заболеваниях имеет место выраженная атрофия ворсинок, нарушения ультраструктуры щеточной каймы, недостаточность ферментного слоя кишечной слизистой оболочки, что приводит к нарушениям мембранного пищеварения.
Нередко нарушения ультраструктуры щеточной каймы сочетаются с резким уменьшением ферментативной активности энтероцитов. Известны многочисленные случаи, при которых ультраструктура щеточной каймы остается практически нормальной, но тем не менее обнаруживается недостаточность одного или нескольких пищеварительных кишечных ферментов. Многие пищевые интолерантности обусловлены этими специфическими нарушениями ферментного слоя кишечных клеток. В настоящее время парциальные ферментные недостаточности тонкой кишки широко известны.
Дисахаридазные недостаточности (в том числе сахаразная) могут быть первичными, то есть обусловленными соответствующими генетическими дефектами, и вторичными, развивающимися на фоне различных болезней (спру, энтериты, после оперативных вмешательств, при инфекционной диарее и т. д.). Изолированная сахаразная недостаточность встречается редко и в большинстве случаев комбинируется с изменениями активности других дисахаридов, чаще всего изомальтазы. Особенно широко распространена лактазная недостаточность, в результате которой не усваивается молочный сахар (лактоза) и возникает интолерантность к молоку. Лактазная недостаточность определяется генетически рецессивным путем. Предполагается, что степень репрессии лактазного гена связана с историей данной этнической группы.
Ферментные недостаточности кишечной слизистой оболочки могут быть связаны как с нарушением синтеза ферментов в кишечных клетках, так и с нарушением их встраивания в апикальную мембрану, где они выполняют свои пищеварительные функции. Кроме того, они могут быть обусловлены и ускорением деградации соответствующих кишечных ферментов. Таким образом, для правильной интерпретации ряда заболеваний необходимо учитывать нарушения мембранного пищеварения. Дефекты этого механизма приводят к изменениям поступления необходимых пищевых веществ в организм с далеко идущими последствиями.
Причиной нарушений ассимиляции белков могут быть изменения желудочной фазы их гидролиза, однако дефекты кишечной фазы за счет недостаточности панкреатических и кишечных мембранных ферментов более серьезны. К редким генетическим нарушениям относятся энтеропептидазная и трипсиновая недостаточности. Уменьшение пептидазных активностей в тонкой кишке наблюдается при ряде заболеваний, например неизлечимой форме целиакии, болезни Крона, язве двенадцатиперстной кишки, при радио– и химиотерапии (например 5-фторурацилом) и т. д. Следует упомянуть и аминопептидурию, которая связана с уменьшением активности дипептидаз, расщепляющих пролиновые пептиды внутри кишечных клеток.
Многие нарушения функций кишечника при различных формах патологии могут зависеть от состояния гликокаликса и содержащихся в нем пищеварительных ферментов. Нарушения процессов адсорбции панкреатических ферментов на структурах слизистой оболочки тонкой кишки могут быть причиной малнутриции (недостаточности питания), а атрофия гликокаликса может способствовать повреждающему действию токсических агентов на мембрану энтероцитов.
Нарушения процессов всасывания проявляются в их замедлении или патологическом усилении. Замедление всасывания слизистой оболочкой кишечника может быть обусловлено следующими причинами:
1) недостаточным расщеплением пищевых масс в полостях желудка и тонкой кишки (нарушения полостного пищеварения);
2) нарушениями мембранного пищеварения;
3) застойной гиперемией кишечной стенки (парез сосудов, шок);
4) ишемией кишечной стенки (атеросклероз сосудов брыжейки, рубцовая послеоперационная окклюзия сосудов стенки кишки и др.);
5) воспалением тканевых структур стенки тонкой кишки (энтериты);
6) резекцией большей части тонкой кишки (синдром короткой тонкой кишки);
7) непроходимостью в верхних отделах кишечника, когда пищевые массы не поступают в его дистальные отделы.
Патологическое усиление всасывания связано с повышением проницаемости кишечной стенки, что нередко можно наблюдать у больных с расстройством терморегуляции (тепловые поражения организма), инфекционно-токсическими процессами при ряде заболеваний, пищевой аллергии и др. Под воздействием некоторых факторов повышается порог проницаемости слизистой оболочки тонкой кишки для крупномолекулярных соединений, в том числе продуктов неполного расщепления пищевых веществ, белков и пептидов, аллергенов, метаболитов. Появление в крови, во внутренней среде организма чужеродных веществ способствует развитию общих явлений интоксикации, сенсибилизации организма, возникновению аллергических реакций.
При ряде заболеваний, сопровождающихся воспалительными явлениями в тканях тонкой кишки, при пищевых аллергиях, некоторых психических заболеваниях всасывание интактных белков и пептидов может быть существенным фактором в их патогенезе. Некоторые заболевания желудочно-кишечного тракта сопровождаются увеличением проницаемости кишечного барьера для белков и пептидов, а также снижением уровня пептидазных активностей слизистой оболочки тонкой кишки. К ним относятся болезнь Крона, целиакия, белково-энергетическая недостаточность, инвазия паразитическими формами, вирусные и бактериальные гастроэнтериты, хирургические травмы кишечника.
Нельзя не упомянуть такие заболевания, при которых нарушено всасывание нейтральных аминокислот в тонкой кишке, а также цистинурию. При цистинурии наблюдаются комбинированные нарушения транспорта диаминомонокарбоновых кислот и цистина в тонкой кишке. Кроме этих заболеваний существуют такие как изолированная мальабсорбция метионина, триптофана и ряда других аминокислот.
Развитие энтеральной недостаточности и хроническое ее течение способствуют (за счет нарушения процессов мембранного пищеварения и всасывания) возникновению расстройств белкового, энергетического, витаминного, электролитного и других видов обмена веществ с соответствующей клинической симптоматикой. Отмеченные механизмы развития недостаточности пищеварения в конечном итоге реализуются в полиорганную, мультисиндромную картину заболевания.
В формировании патогенетических механизмов энтеральной патологии ускорение перистальтики является одним из типичных расстройств, сопровождающих большинство органических заболеваний. Наиболее частые причины ускорения перистальтики – воспалительные изменения в слизистой оболочке ЖКТ. При этом химус продвигается по кишечнику быстрее и развивается понос. Диарея возникает также при действии на стенку кишечника необычных раздражителей: непереваренной пищи (например, при ахилии), продуктов брожения и гниения, токсических веществ. К ускорению перистальтики ведет повышение возбудимости центра блуждающего нерва, так как он активизирует моторику кишечника. Поносы, способствующие освобождению организма от неусвояемых или токсических веществ, являются защитными. Но при длительной диарее происходят глубокие расстройства пищеварения, связанные с нарушением секреции кишечного сока, переваривания и всасывания пищевых веществ в кишечнике. Замедление перистальтики тонкой кишки относится к редким патофизиологическим механизмам формирования заболеваний. При этом тормозится продвижение пищевой кашицы по кишечнику и развиваются запоры. Этот клинический синдром, как правило, является следствием патологии толстой кишки.
Толстая кишка
Процесс пищеварения завершается в толстой кишке, однако активность механизмов переваривания компонентов пищи в этом органе низка. Здесь химус перемешивается под действием непропульсивной перистальтики, концентрируется в результате реабсорбции воды и подвергается дальнейшему (остаточному) расщеплению под действием локализованных там кишечных ферментов и бактерий. Невысокий уровень ферментативной активности в дистальном отделе желудочно-кишечного тракта выработался в процессе эволюции и связан с тем, что поступающий в толстую кишку химус беден непереваренными пищевыми веществами. Однако активность некоторых ферментов толстой кишки компенсаторно увеличивается при нарушении функций вышележащих органов пищеварительного канала (резекции частей желудка или тонкой кишки, илеостомии и т. д.).
Несмотря на отмеченные физиологические особенности толстой кишки в процессе пищеварения, этот отдел желудочно-кишечного тракта выполняет целый ряд весьма важных функций:
1) всасывательную – всасывание воды и электролитов из химуса и формирование каловых масс; всасывание соединений, образующихся в результате активности микрофлоры кишки: витаминов (К и группы В), продуктов гидролиза клетчатки;
2) механическую – проталкивание содержимого кишки (каловых масс) в дистальном направлении и удаление их из организма;
3) эндокринную – благодаря наличию клеток диффузной эндокринной системы в эпителии кишки, которые вырабатывают гормоны, обладающие локальным и системным действием;
4) иммунную – обеспечивается диффузной лимфоидной тканью в стенке кишки, а также специальными структурами – одиночными лимфатическими узелками и их скоплениями в червеобразном отростке.
В слизистой оболочке толстой кишки, особенно в области аппендикса, наблюдаются скопления лимфатической ткани и плазматических клеток, что очень важно, так как здесь присутствует большая популяция бактерий. Иммунокомпетентные клетки секретируют преимущественно IgA.
В толстой кишке преобладают процессы реабсорбции. Здесь всасываются глюкоза, некоторые витамины и аминокислоты, продуцируемые микробами кишечной полости, до 95 % воды и электролиты. Ободочная кишка всасывает жидкость со скоростью до 2,7 мл/мин (против 5–7 мл/мин в тонкой кишке), то есть на единицу поверхности слизистой оболочки ободочной кишки ее всасывательная активность в 5-10 раз больше, чем в тонкой кишке. Скорее всего это можно объяснить уменьшением площади поверхности толстой кишки по сравнению с тонкой за счет значительного уменьшения числа ворсинок и микроворсинок щеточной каймы кишечных клеток. У здорового человека в толстой кишке может всасываться до 5,5 л воды и до 800-1000 ммоль натрия и хлора в сутки, прежде чем исчерпаются ее возможности и разовьется диарея. Эти физиологические особенности толстой кишки последние годы все шире используют клиницисты для проведения питания, фармакотерапии, восстановления водно-электролитных расстройств путем капельного введения соответствующих лечебных средств в толстую кишку. Кроме воды и электролитов, в толстую кишку поступают органические соединения, к которым относятся растительные волокна и другие растительные компоненты. Это полисахариды, целлюлоза, гемицеллюлоза, пектины и лигнины, то есть углеводы, которые не расщепляются α-амилазой человека. Около 40–50 % грубоволокнистых веществ могут расщепляться кишечными бактериями и всасываться в толстой кишке.
Толстая кишка – область размножения микроорганизмов. Бактериальная флора желудочно-кишечного тракта является необходимым условием нормального существования организма. Количество микроорганизмов в желудке минимально, в тонкой кишке их значительно больше (особенно в дистальном ее отделе). Исключительно велико количество микроорганизмов в толстой кишке – до десятков миллиардов в 1 г содержимого. Ферменты микроорганизмов толстой кишки вызывают деградацию углеводов и распад белков, в результате чего образуются органические кислоты, газы (углекислый газ, метан, сероводород) и токсические вещества (фенол, скатол, индол, крезол). Часть этих веществ обезвреживается в печени. Вследствие микробного брожения расщепляется клетчатка. Преобладающими микробами кишечника взрослого человека являются облигатно анаэробные палочки (около 90 %), на долю факультативно анаэробных микробов (кишечная палочка, молочные бактерии, стрептококки) и спороносных анаэробов приходится около 10 % (табл. 2.3,2.4).
Нормальная микрофлора толстой кишки подавляет патогенные микроорганизмы и предупреждает инфицирование макроорганизма. Нарушение микрофлоры при заболеваниях или в результате введения антибактериальных препаратов нередко влечет за собой бурное размножение в кишечнике дрожжей, стафилококков, протея и других микроорганизмов.
Моторная деятельность толстой кишки обеспечивает накопление кишечного содержимого, всасывание из него воды и ряда электролитов, формирование каловых масс и удаление их из кишечника. Моторика этого отдела кишечника характеризуется частыми слабыми сокращениями, принимающими участие в перемешивании содержимого; редкими (2 раза в 1 мин) и сильными, хорошо координированными, способствующими продвижению содержимого по ходу кишки; тоническими, незначительно уменьшающими просвет кишки и повышающими в ней гидростатическое давление.
Таблица 2.3
Распределение микроорганизмов в желудочно-кишечном тракте человека

Таблица 2.4
Нормальный микробный состав испражнений человека (в расчете на 1 г)

Регуляция моторной деятельности толстой кишки определяется изменениями потенциала гладкомышечных клеток, то есть медленными волнами, связанными с их потенциалами действия, а также модулирующими влияниями центральной и вегетативной нервной системы, гормонов желудочно-кишечного тракта и нейропептидов. Симпатические волокна вегетативной нервной системы тормозят моторику толстой кишки, раздражение парасимпатических волокон стимулирует ее моторную активность. Большое значение в стимуляции моторики толстой кишки имеют механические и химические раздражения. Пищевые волокна как механический раздражитель повышают ее двигательную активность и ускоряют продвижение содержимого.
Раздражение механорецепторов прямой кишки тормозит моторику толстой кишки. Позыв же на дефекацию, то есть опорожнение толстой кишки, возникает при повышении давления в прямой кишке до 40–50 см вод. ст. в результате раздражения рецепторов прямой кишки накопившимися в ней каловыми массами.
Несмотря на отмеченные физиологические особенности толстой кишки в процессе пищеварения, этот отдел желудочно-кишечного тракта выполняет целый ряд весьма важных функций:
1) всасывательную – всасывание воды и электролитов из химуса и формирование каловых масс; всасывание соединений, образующихся в результате активности микрофлоры кишки: витаминов (К и группы В), продуктов гидролиза клетчатки;
2) механическую – проталкивание содержимого кишки (каловых масс) в дистальном направлении и удаление их из организма;
3) эндокринную – благодаря наличию клеток диффузной эндокринной системы в эпителии кишки, которые вырабатывают гормоны, обладающие локальным и системным действием;
4) иммунную – обеспечивается диффузной лимфоидной тканью в стенке кишки, а также специальными структурами – одиночными лимфатическими узелками и их скоплениями в червеобразном отростке.
В слизистой оболочке толстой кишки, особенно в области аппендикса, наблюдаются скопления лимфатической ткани и плазматических клеток, что очень важно, так как здесь присутствует большая популяция бактерий. Иммунокомпетентные клетки секретируют преимущественно IgA.
В толстой кишке преобладают процессы реабсорбции. Здесь всасываются глюкоза, некоторые витамины и аминокислоты, продуцируемые микробами кишечной полости, до 95 % воды и электролиты. Ободочная кишка всасывает жидкость со скоростью до 2,7 мл/мин (против 5–7 мл/мин в тонкой кишке), то есть на единицу поверхности слизистой оболочки ободочной кишки ее всасывательная активность в 5-10 раз больше, чем в тонкой кишке. Скорее всего это можно объяснить уменьшением площади поверхности толстой кишки по сравнению с тонкой за счет значительного уменьшения числа ворсинок и микроворсинок щеточной каймы кишечных клеток. У здорового человека в толстой кишке может всасываться до 5,5 л воды и до 800-1000 ммоль натрия и хлора в сутки, прежде чем исчерпаются ее возможности и разовьется диарея. Эти физиологические особенности толстой кишки последние годы все шире используют клиницисты для проведения питания, фармакотерапии, восстановления водно-электролитных расстройств путем капельного введения соответствующих лечебных средств в толстую кишку. Кроме воды и электролитов, в толстую кишку поступают органические соединения, к которым относятся растительные волокна и другие растительные компоненты. Это полисахариды, целлюлоза, гемицеллюлоза, пектины и лигнины, то есть углеводы, которые не расщепляются α-амилазой человека. Около 40–50 % грубоволокнистых веществ могут расщепляться кишечными бактериями и всасываться в толстой кишке.
Толстая кишка – область размножения микроорганизмов. Бактериальная флора желудочно-кишечного тракта является необходимым условием нормального существования организма. Количество микроорганизмов в желудке минимально, в тонкой кишке их значительно больше (особенно в дистальном ее отделе). Исключительно велико количество микроорганизмов в толстой кишке – до десятков миллиардов в 1 г содержимого. Ферменты микроорганизмов толстой кишки вызывают деградацию углеводов и распад белков, в результате чего образуются органические кислоты, газы (углекислый газ, метан, сероводород) и токсические вещества (фенол, скатол, индол, крезол). Часть этих веществ обезвреживается в печени. Вследствие микробного брожения расщепляется клетчатка. Преобладающими микробами кишечника взрослого человека являются облигатно анаэробные палочки (около 90 %), на долю факультативно анаэробных микробов (кишечная палочка, молочные бактерии, стрептококки) и спороносных анаэробов приходится около 10 % (табл. 2.3,2.4).
Нормальная микрофлора толстой кишки подавляет патогенные микроорганизмы и предупреждает инфицирование макроорганизма. Нарушение микрофлоры при заболеваниях или в результате введения антибактериальных препаратов нередко влечет за собой бурное размножение в кишечнике дрожжей, стафилококков, протея и других микроорганизмов.
Моторная деятельность толстой кишки обеспечивает накопление кишечного содержимого, всасывание из него воды и ряда электролитов, формирование каловых масс и удаление их из кишечника. Моторика этого отдела кишечника характеризуется частыми слабыми сокращениями, принимающими участие в перемешивании содержимого; редкими (2 раза в 1 мин) и сильными, хорошо координированными, способствующими продвижению содержимого по ходу кишки; тоническими, незначительно уменьшающими просвет кишки и повышающими в ней гидростатическое давление.
Таблица 2.3
Распределение микроорганизмов в желудочно-кишечном тракте человека

Таблица 2.4
Нормальный микробный состав испражнений человека (в расчете на 1 г)

Регуляция моторной деятельности толстой кишки определяется изменениями потенциала гладкомышечных клеток, то есть медленными волнами, связанными с их потенциалами действия, а также модулирующими влияниями центральной и вегетативной нервной системы, гормонов желудочно-кишечного тракта и нейропептидов. Симпатические волокна вегетативной нервной системы тормозят моторику толстой кишки, раздражение парасимпатических волокон стимулирует ее моторную активность. Большое значение в стимуляции моторики толстой кишки имеют механические и химические раздражения. Пищевые волокна как механический раздражитель повышают ее двигательную активность и ускоряют продвижение содержимого.
Раздражение механорецепторов прямой кишки тормозит моторику толстой кишки. Позыв же на дефекацию, то есть опорожнение толстой кишки, возникает при повышении давления в прямой кишке до 40–50 см вод. ст. в результате раздражения рецепторов прямой кишки накопившимися в ней каловыми массами.
Патофизиология
Нарушение функций тонкой и толстой кишок может приводить к диарее, в патогенезе которой играют роль повышение осмотического давления в полости кишечника, нарушение всасывания и пассажа кишечного содержимого, кишечные гиперсекреция и гиперэкссудация. Для большинства форм толстокишечной диареи характерно значительное увеличение концентрации электролитов в фекалиях, которая достигает содержания их в плазме крови. В этих случаях суточный объем фекалий может достигать 1 л и более, при этом содержание натрия и хлоридов повышается, а калия снижается до уровня его в плазме. При нарушении всасывания (точнее – усвоения лактозы в патогенезе диареи) преобладает осмотический компонент. Тогда потери воды превышают потери солей.
