Страница:
Пререпликативный комплекс формируется на основе post-RC, этот процесс начинается во всех ориджинах одновременно на границе фаз М и G1 и завершается в конце G1 в ориджинах, активирующихся первыми при переходе в S-фазу. В ориджинах, активирующихся позже в S-фазе, образование рге-RC завершается в соответствующий для каждого из них период S-фазы. В G1-фазе во время сборки рге-RС ОRС способен взаимодействовать с циклинзависимыми киназами (Сdks, cyclin-dependent kinases). Это взаимодействие является одним из механизмов, позволяющих клетке формировать рге-RC после митоза. Первыми к post-RC на границе фаз М/G1 присоединяются белок Сdс6 (cell division cycle protein) и семейство шести белков Мст 2–7 (minichromosome maintenance proteins). Белки Мст 2–7 являются наиболее известными среди семейства «поддерживающих мини-хромосомы» белков, впервые идентифицированных у S.сerevisiae при исследовании мутантов, не способных к поддержанию стабильности мини-хромосом.
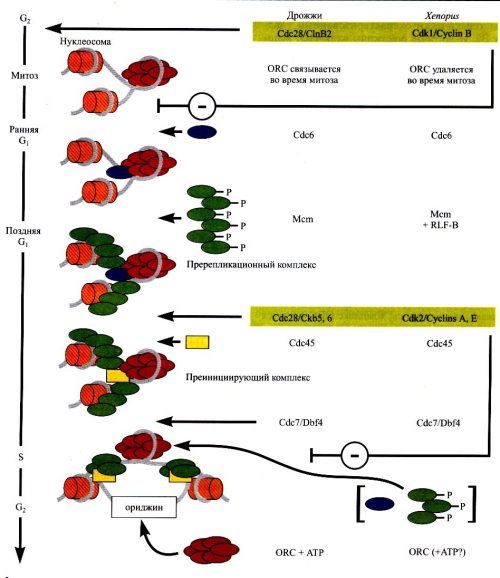
Рис. 7. Схема инициации репликации у эукариот
Белки Сdс6 и Мст 2–7 описаны у многих представителей эукариот, включая млекопитающих. Недавно было показано, что в клетках S.ротbе и высших эукариот в ранней стадии формирования рге-RС участвует еще один белок – Cdt1 (cell division termination). Белки Мст 2–7 образуют гексамерный комплекс МСМ – ключевой компонент рге-RС. МСМ генерирует контрольный сигнал на нереплицированном хроматине для ингибирования преждевременного митоза в G1-фазе. Также он необходим для продвижения клетки по циклу в S-фазу. Присоединение МСМ к ориджину репликации регулируется фосфорилированием-дефосфорилированием отдельных субъединиц этого комплекса. Например, частичное дефосфорилирование Мст4-субъелиницы, гиперфосфорилированной в фазе М, способствует образованию рге-RС, а полное дефосфорилирование Мст3-субъединицы инактивирует комплекс и препятствует его связыванию с хроматином. В то же время, присоединение МСМ к ориджину зависит от белков Сdс6 и Сdt1, которые совместно «насаживают» МСМ на хроматин. В отсутствие Сdс6 клетки S.cerevisiae теряют способность инициировать репликацию ДНК и подвергаются «урезанному» митозу и нереплицированные хромосомы сегрегируют случайным образом к полюсам веретена.
Способность Сdс6 предотвращать «урезанный» митоз до завершения репликации ДНК обеспечивается его взаимодействием с Cdks. Активность Сdс6 в фазе G1 регулируется также его взаимодействием с АТР, так как мутации в консервативных последовательностях АТР-связываюшего мотива Сdс6 приводили к потере способности хроматина присоединять МСМ в клетках S.cerevisiae и к подавлению репликации ДНК в клетках человека. У S.cerevisiae в присоединении МСМ к рге-RС принимает участие еще один белок – Mcm10, который ассоциирован с хроматином и взаимодействует с компонентами Мст2-7. Столь сложный кнтроль связывания МСМ с ориджином свидетельствует о том, что в клетке существует многоступенчатая система регуляторных механизмов, необходимая для недопущения повторного митоза при нереплицированном хроматине. Связывание МСМ с ориджинами репликации необходимо для обеспечения стабильности генома, именно оно переводит хроматин |в состояние, за которым закрепилось название «разрешающего» репликацию (replication-liscensing). У кеенопуса для связывания МCM требуется наличие дополнительного фактора, носящего такое же название, RLF-B (герlication licensing factor B). Белки МCM обнаруживают аффинность к гистонам, а не к ДНК, в результате чего в конце G1-фазы весь пререпликативный комплекс прочно привязывается к хроматину непосредственно в участке ориджина репликации или рядом с ним.
В G1-фазе к частично сформированному рге-RC присоединяется киназа Сdc7 со своей регуляторной субъединицей Dbf4 (DNA binding factor 4), а в поздней G1-фазе или на границе фаз G1/S – белок Сdс45 и связывающий однонитевую ДНК репликативный белок А (RРA, replication protein A). Взаимодействие между Сdс45 и Dbf4/Cdc7 в поздней G1-фазе требуется для последующего «включения» репликации в ориджинах после сборки рге-RС.
Киназа Dbf4/Cdc7 связывается с ori за некоторое время до того, как начинает выполнять свои функции. Присоединившись к рге-RС, киназа Dbf4/Cdc7 «ждет», когда активируются Сdk, и только после этого фосфорилирует свои субстраты. Роль «раннего» связывания этой киназы с ori пока остается неясной.
Связывание Сdс45 с хроматином зависит от белков Сdс6 и Мст2 и от активности киназы Dbf4/Cdc7 и циклинзависимых киназ S-фазы (Cdk-S-фазы – Сdс28/Сkb5,6 у дрожжей и Сdk2/Сусlins А,Е у высших эукариот). Белок Сdc45 может быть фосфорилирован киназой Dbf4/Cdc7, но это происходит только после активации Cdk-S-фазы. Активность Cdk-S в свою очередь регулируется ингибитором Sic1, который в конце фазы G1 подвергается убиквитинзависимому протеолизу. Присоединение белка Сdс45 к рге-RС происходит в поздней G1-фазе клеточного цикла только на ориджинах тех репликонов, которые начинают синтез ДНК первыми при переходе к S-фазе. Cdk-S и Dbf4/Cdc7-зависимое связывание Cdc45 с остальными ориджинами осуществляется в определенное для каждого из них время на протяжении всей S-фазы. Вероятный механизм присоединения Сdс45 к рге-RС таков: Dbf4/Cdc7, связавшаяся со всеми ориджинами репликации в фазе G1, после воздействия Cdk-S фосфорилирует Мст2 в каждом ориджине в тот период фазы S, который определяется индивидуально для каждого ориджина. В результате фосфорилирования Мст2 конформация комплекса МСМ меняется таким образом, что он приобретает способность связывать Сdс45. В то же самое время к рге-RС присоединяется белок RРА. Подобно Сdс45 RРА связывается с ориджином Cdk-S зависимым образом при участии Мст2. Присоединение белков Сdс45 и RРА завершает сборку рге-RС. Сразу после завершения сборки рге-RС происходит частичная его диссоциация, сопровождающаяся началом формирования RС (replication complex). Белок Сdc6 первым диссоциирует из рге-RС при переходе из фазы G1 в S или даже ранее, подвергаясь фосфорилированию под действием Сdks, за которым следуют убиквитинирование и деградация. Этот путь инактивации Сdс6 показан как для низших эукариот, так и для некоторых представителей высших эукариот. В клетках человека уровень Сdc6 остается постоянным на протяжении всего клеточного цикла. Но при переходе в S-фазу Сdс6 транспортируется из ядра в цитоплазму. По всей видимости, и этот процесс регулируется Сdks. Удаление Сdc6р из ядра (путем гидролиза или транспортировки в цитоплазму) является одним из механизмов, предотвращающих множественные акты репликации в течение одного клеточного цикла.
Белок Сdt1 также инактивируется после завершения формирования рге-RС. При этом в клетках низших эукариот Cdt1. периодически экспрессируется, накапливаясь в ядрах в фазе G1, а в фазе G2 его уровень падает. У высших эукариот активность Сdt1 контролируется белком-ингибитором геминином, который отсутствует в клетках в фазе G1, накапливается на протяжении фаз S, G2 и частично – фазы М и исчезает в М-фазе на границе метафазы и анафазы.
В отличие от Сdс6 и Сdt1 белки Мст2-7, RРА и Сdс45, диссоциировав из рге-RС, остаются связанными с хроматином в S-фазе во время синтеза ДНК. Быстрое освобождение МСМ из рте-RС в клетках дрожжей обеспечивается взаимодействием между Мcm10 и Мст7. Разъединению МСМ и Мст10 способствует белок Сdс45.
Субъединицы Мст4,6,7 комплекса МСМ обладают геликазной активностью, проявляющейся только при стимуляции под действием Cdk-S и киназы Dbf4/Cdc7. Белки Мст2-7 существенны не только для инициации, но и для элонгационной фазы репликации, для прогрессии репликативных вилок. МСМ входит в состав RС и принимает участие в раскручивании двунитевой ДНК в репликативных вилках. В клетках человека связывание МСМ с ориджином при формировании RС осуществляется с участием белка Мcm10, который накапливается и образует комплекс с хроматином в S-фазе, в отличие от Мcm10 S.сегevisiae. При переходе клеток из фазы G2 в М Мcm10 гиперфосфорилируется и диссоциирует из хроматина, а на границе фаз М/G1 он подвергается протеолизу по протеосомному механизму. Таким образом, фосфорилирование и протеолиз Мcm10 в клетках человека осуществляют отрицательную регуляцию активности МСМ после завершения репликации ДНК. Кроме того, отрицательная регуляция активности МСМ может быть результатом непосредственного фосфорилирования отдельных компонентов самого этого комплекса. Так, например, фосфорилирование Cdk специфических сайтов Мcm4 в фазе М приводит к потере геликазной активности Мст4,6,7, а высокая концентрация комплекса Cdk-циклин Е в ядрах эмбрионов Хепорus препятствует связыванию Мст3 с ДНК и таким образом предотвращает реассоциацию МСМ с хроматином после завершения репликации. Комплекс МСМ участвует не только в ранних этапах инициации репликации при переходе клеток в фазу G1, но и в завершении этого процесса в фазе S. Причем на завершающем этапе инициации репликации МСМ выполняет две функции: раскручивает ДНК в ориджине и служит остовом, к которому присоединяются остальные компоненты при формировании RС. Поэтому множественные механизмы регуляции активности МСМ вполне объяснимы. Если в фазе G1 эти механизмы направлены на осуществление продвижения клеток к фазе S без повторного митоза, то в фазах S и G2 они предотвращают повторную репликацию уже реплицированного хроматина.
RРА является белком, связывающим однонитевую ДНК и наличие его в RС при инициации репликации необходимо для стабилизирования расплетенного участка ДНК. RРА образован тремя субъединицами с молекулярными массами 70, 34 и 11 кДа, причем активностью, связывающей однонитевую ДНК, обладает субъединица 70 кДа, а субъединица 34 кДа является регуляторной. Последняя фосфорилируется Сdk, что, по-видимому, необходимо для активации репликации ДНК. Подробное описание этого комплекса будет дано далее.
Белок Сdс45 также участвует в формировании RС. Он необходим для присоединения ДНК-полимеразы α к ориджинам репликации. Показано, что белок Сdс45 человека связывается с белком Мст7 человека и субъединицей р70 ДНК-полимеразы α in vitro. Сdс45 присоединяет ДНК-полимеразу α к RС посредством связывания с Мст7. В клетках дрожжей S.cerevisiae Сdс45 присоединяет ДНК-полимеразу α к хроматину с участием Мст2.
Одним из компонентов комплекса, запускающего репликацию ДНК, является ДНК-полимераза α. Из всех многочисленных ДНК-полимераз эукариот именно она содержит праймазную активность, способную синтезировать короткую РНК «затравку» – праймер из рибонуклеозидтрифосфатов. РНК-праймер генерирует сигнал, который является одним из пусковых механизмов репликации. ДНК-полимераза α обнаружена у всех исследованных эукариот и хорошо изучена. Подробное описание этого фермента будет дано в следующем разделе. Показано, что один из путей регуляции инициации репликации связан с фосфорилированием двух больших субъединиц ДНК-полимеразы α под действием Сdk. При этом циклин Е и Сdk стимулируют инициацию репликации при переходе клетки в S-фазу, а циклин А и Сdk ингибируют ее в фазе G2.
Очевидно, что активация упоминавшихся выше «ранне– и позднеактивных» ориджинов S.cerevisiae зависит от киназы Dbf4/Сdс7р. Вероятно, в каждом ориджине происходит локальная регуляция его активности дополнительными протеинкиназами, например Rad53. Киназа Rad53 блокирует запуск "позднеактивных" ориджинов в ранней S-фазе. Когда это блокирование устраняется, киназа Dbf4/Сdс7р активирует МСМ, что приводит сразу к нескольким последствиям: стимуляции геликазной активности МСМ и связыванию белка RРА и ДНК-полимеразы α с ориджинами репликации. Присоединение ДНК-полимеразы α к RС, раскручивание ДНК в ориджине и синтез РНК-праймера завершают процесс инициации репликации ДНК эукариот. Следует отметить, что роль ДНК-полимеразы α ограничивается только запуском репликации ДНК. Эта ДНК-полимераза не способна к процессивному, то еть протяженному, синтезу ДНК и не обладает корректирующей активностью. Поэтому в дальнейшем в процессе репликации она добавляет к РНК-праймеру приблизительно 20 нуклеотидов и замещается ДНК-полимеразами δ или ε.
Роst-RС, с образования которого начинается вся цепь событий процесса инициации репликации ДНК, в S-фазе клеточного цикла претерпевает изменения. Эти изменения касаются сродства ОRС к ДНК. Так, например, белок Orc1 Хепориs образует прочный комплекс с хроматином в ранней интерфазе до тех пор, пока не завершится сборка рге-RС. Затем в S-фазе сродство Огс1 к ДНК уменьшается. У млекопитающих Огс1 диссоциирует из хроматина в S-фазе, превращается в моно– или диубиквитинированную форму, затем деубиквитинируется и вновь связывается с ДНК при переходе из М– в G-1-фазу. Белок Огс2, напротив,
остается связанным с хроматином на протяжении всего клеточного цикла и не является субстратом для убиквитинирования. В клетках человека в S-фазе из хроматина диссоциирует комплекс белков, содержащий Огс1 и Огс2, который реассоциирует в конце митоза. В клетках дрожжей S.ротbе ОRС подвергается посттрансляционным изменениям в клеточном цикле: в фазе S начинается фосфорилирование одной из его субъединиц, Огс2, которое достигает максимума в фазах G2 и М. Таким образом, в клетках эукариот один из механизмов, предотвращающих повторную репликацию уже реплицированного хроматина, связан с инактивацией роst-RС либо путем диссоциации из него Огс1 (у высших эукариот), либо путем фосфорилирования Огс2 (у низших эукариот).
Таблица 2
Комплексы инициации транскрипции у эукариот

Для облегчения понимания последовательности связывания различных белков в зоне инициации репликации см. таблицу 2.
В последние несколько лет значительные успехи достигнуты в понимании механизмов регуляции практически каждой стадии инициации репликации. Они осуществляются на уровне функционирования всех компонентов, образующих пост-, пре– и репликативный комплексы. Эти компоненты подвергаются воздействию не одного, а ряда различных факторов. Примером этому служит регуляция комплекса МСМ, активность которого напрямую зависит от белков Сdc6, Мст10, Сdt1, циклин-зависимых киназ, киназы Dbf4/Сdс7, фосфатаз. До сих пор мало понятны закономерности процесса инициации репликации ДНК в эмбриогенезе и те факторы, которые влияют на эти процессы.
Глава 4. Механизм образования и необходимость РНК-праймера
4.1. Синтез праймера для полимеразной реакции
4.2. Понятие об РНК-ДНК дуплексе
4.3. Ключевые ферменты, участвующие в синтезе ДНК
4.3.1. ДНК-полимеразы
4.3.1.1. ДНК-полимеразы прокариот

Рис. 7. Схема инициации репликации у эукариот
Белки Сdс6 и Мст 2–7 описаны у многих представителей эукариот, включая млекопитающих. Недавно было показано, что в клетках S.ротbе и высших эукариот в ранней стадии формирования рге-RС участвует еще один белок – Cdt1 (cell division termination). Белки Мст 2–7 образуют гексамерный комплекс МСМ – ключевой компонент рге-RС. МСМ генерирует контрольный сигнал на нереплицированном хроматине для ингибирования преждевременного митоза в G1-фазе. Также он необходим для продвижения клетки по циклу в S-фазу. Присоединение МСМ к ориджину репликации регулируется фосфорилированием-дефосфорилированием отдельных субъединиц этого комплекса. Например, частичное дефосфорилирование Мст4-субъелиницы, гиперфосфорилированной в фазе М, способствует образованию рге-RС, а полное дефосфорилирование Мст3-субъединицы инактивирует комплекс и препятствует его связыванию с хроматином. В то же время, присоединение МСМ к ориджину зависит от белков Сdс6 и Сdt1, которые совместно «насаживают» МСМ на хроматин. В отсутствие Сdс6 клетки S.cerevisiae теряют способность инициировать репликацию ДНК и подвергаются «урезанному» митозу и нереплицированные хромосомы сегрегируют случайным образом к полюсам веретена.
Способность Сdс6 предотвращать «урезанный» митоз до завершения репликации ДНК обеспечивается его взаимодействием с Cdks. Активность Сdс6 в фазе G1 регулируется также его взаимодействием с АТР, так как мутации в консервативных последовательностях АТР-связываюшего мотива Сdс6 приводили к потере способности хроматина присоединять МСМ в клетках S.cerevisiae и к подавлению репликации ДНК в клетках человека. У S.cerevisiae в присоединении МСМ к рге-RС принимает участие еще один белок – Mcm10, который ассоциирован с хроматином и взаимодействует с компонентами Мст2-7. Столь сложный кнтроль связывания МСМ с ориджином свидетельствует о том, что в клетке существует многоступенчатая система регуляторных механизмов, необходимая для недопущения повторного митоза при нереплицированном хроматине. Связывание МСМ с ориджинами репликации необходимо для обеспечения стабильности генома, именно оно переводит хроматин |в состояние, за которым закрепилось название «разрешающего» репликацию (replication-liscensing). У кеенопуса для связывания МCM требуется наличие дополнительного фактора, носящего такое же название, RLF-B (герlication licensing factor B). Белки МCM обнаруживают аффинность к гистонам, а не к ДНК, в результате чего в конце G1-фазы весь пререпликативный комплекс прочно привязывается к хроматину непосредственно в участке ориджина репликации или рядом с ним.
В G1-фазе к частично сформированному рге-RC присоединяется киназа Сdc7 со своей регуляторной субъединицей Dbf4 (DNA binding factor 4), а в поздней G1-фазе или на границе фаз G1/S – белок Сdс45 и связывающий однонитевую ДНК репликативный белок А (RРA, replication protein A). Взаимодействие между Сdс45 и Dbf4/Cdc7 в поздней G1-фазе требуется для последующего «включения» репликации в ориджинах после сборки рге-RС.
Киназа Dbf4/Cdc7 связывается с ori за некоторое время до того, как начинает выполнять свои функции. Присоединившись к рге-RС, киназа Dbf4/Cdc7 «ждет», когда активируются Сdk, и только после этого фосфорилирует свои субстраты. Роль «раннего» связывания этой киназы с ori пока остается неясной.
Связывание Сdс45 с хроматином зависит от белков Сdс6 и Мст2 и от активности киназы Dbf4/Cdc7 и циклинзависимых киназ S-фазы (Cdk-S-фазы – Сdс28/Сkb5,6 у дрожжей и Сdk2/Сусlins А,Е у высших эукариот). Белок Сdc45 может быть фосфорилирован киназой Dbf4/Cdc7, но это происходит только после активации Cdk-S-фазы. Активность Cdk-S в свою очередь регулируется ингибитором Sic1, который в конце фазы G1 подвергается убиквитинзависимому протеолизу. Присоединение белка Сdс45 к рге-RС происходит в поздней G1-фазе клеточного цикла только на ориджинах тех репликонов, которые начинают синтез ДНК первыми при переходе к S-фазе. Cdk-S и Dbf4/Cdc7-зависимое связывание Cdc45 с остальными ориджинами осуществляется в определенное для каждого из них время на протяжении всей S-фазы. Вероятный механизм присоединения Сdс45 к рге-RС таков: Dbf4/Cdc7, связавшаяся со всеми ориджинами репликации в фазе G1, после воздействия Cdk-S фосфорилирует Мст2 в каждом ориджине в тот период фазы S, который определяется индивидуально для каждого ориджина. В результате фосфорилирования Мст2 конформация комплекса МСМ меняется таким образом, что он приобретает способность связывать Сdс45. В то же самое время к рге-RС присоединяется белок RРА. Подобно Сdс45 RРА связывается с ориджином Cdk-S зависимым образом при участии Мст2. Присоединение белков Сdс45 и RРА завершает сборку рге-RС. Сразу после завершения сборки рге-RС происходит частичная его диссоциация, сопровождающаяся началом формирования RС (replication complex). Белок Сdc6 первым диссоциирует из рге-RС при переходе из фазы G1 в S или даже ранее, подвергаясь фосфорилированию под действием Сdks, за которым следуют убиквитинирование и деградация. Этот путь инактивации Сdс6 показан как для низших эукариот, так и для некоторых представителей высших эукариот. В клетках человека уровень Сdc6 остается постоянным на протяжении всего клеточного цикла. Но при переходе в S-фазу Сdс6 транспортируется из ядра в цитоплазму. По всей видимости, и этот процесс регулируется Сdks. Удаление Сdc6р из ядра (путем гидролиза или транспортировки в цитоплазму) является одним из механизмов, предотвращающих множественные акты репликации в течение одного клеточного цикла.
Белок Сdt1 также инактивируется после завершения формирования рге-RС. При этом в клетках низших эукариот Cdt1. периодически экспрессируется, накапливаясь в ядрах в фазе G1, а в фазе G2 его уровень падает. У высших эукариот активность Сdt1 контролируется белком-ингибитором геминином, который отсутствует в клетках в фазе G1, накапливается на протяжении фаз S, G2 и частично – фазы М и исчезает в М-фазе на границе метафазы и анафазы.
В отличие от Сdс6 и Сdt1 белки Мст2-7, RРА и Сdс45, диссоциировав из рге-RС, остаются связанными с хроматином в S-фазе во время синтеза ДНК. Быстрое освобождение МСМ из рте-RС в клетках дрожжей обеспечивается взаимодействием между Мcm10 и Мст7. Разъединению МСМ и Мст10 способствует белок Сdс45.
Субъединицы Мст4,6,7 комплекса МСМ обладают геликазной активностью, проявляющейся только при стимуляции под действием Cdk-S и киназы Dbf4/Cdc7. Белки Мст2-7 существенны не только для инициации, но и для элонгационной фазы репликации, для прогрессии репликативных вилок. МСМ входит в состав RС и принимает участие в раскручивании двунитевой ДНК в репликативных вилках. В клетках человека связывание МСМ с ориджином при формировании RС осуществляется с участием белка Мcm10, который накапливается и образует комплекс с хроматином в S-фазе, в отличие от Мcm10 S.сегevisiae. При переходе клеток из фазы G2 в М Мcm10 гиперфосфорилируется и диссоциирует из хроматина, а на границе фаз М/G1 он подвергается протеолизу по протеосомному механизму. Таким образом, фосфорилирование и протеолиз Мcm10 в клетках человека осуществляют отрицательную регуляцию активности МСМ после завершения репликации ДНК. Кроме того, отрицательная регуляция активности МСМ может быть результатом непосредственного фосфорилирования отдельных компонентов самого этого комплекса. Так, например, фосфорилирование Cdk специфических сайтов Мcm4 в фазе М приводит к потере геликазной активности Мст4,6,7, а высокая концентрация комплекса Cdk-циклин Е в ядрах эмбрионов Хепорus препятствует связыванию Мст3 с ДНК и таким образом предотвращает реассоциацию МСМ с хроматином после завершения репликации. Комплекс МСМ участвует не только в ранних этапах инициации репликации при переходе клеток в фазу G1, но и в завершении этого процесса в фазе S. Причем на завершающем этапе инициации репликации МСМ выполняет две функции: раскручивает ДНК в ориджине и служит остовом, к которому присоединяются остальные компоненты при формировании RС. Поэтому множественные механизмы регуляции активности МСМ вполне объяснимы. Если в фазе G1 эти механизмы направлены на осуществление продвижения клеток к фазе S без повторного митоза, то в фазах S и G2 они предотвращают повторную репликацию уже реплицированного хроматина.
RРА является белком, связывающим однонитевую ДНК и наличие его в RС при инициации репликации необходимо для стабилизирования расплетенного участка ДНК. RРА образован тремя субъединицами с молекулярными массами 70, 34 и 11 кДа, причем активностью, связывающей однонитевую ДНК, обладает субъединица 70 кДа, а субъединица 34 кДа является регуляторной. Последняя фосфорилируется Сdk, что, по-видимому, необходимо для активации репликации ДНК. Подробное описание этого комплекса будет дано далее.
Белок Сdс45 также участвует в формировании RС. Он необходим для присоединения ДНК-полимеразы α к ориджинам репликации. Показано, что белок Сdс45 человека связывается с белком Мст7 человека и субъединицей р70 ДНК-полимеразы α in vitro. Сdс45 присоединяет ДНК-полимеразу α к RС посредством связывания с Мст7. В клетках дрожжей S.cerevisiae Сdс45 присоединяет ДНК-полимеразу α к хроматину с участием Мст2.
Одним из компонентов комплекса, запускающего репликацию ДНК, является ДНК-полимераза α. Из всех многочисленных ДНК-полимераз эукариот именно она содержит праймазную активность, способную синтезировать короткую РНК «затравку» – праймер из рибонуклеозидтрифосфатов. РНК-праймер генерирует сигнал, который является одним из пусковых механизмов репликации. ДНК-полимераза α обнаружена у всех исследованных эукариот и хорошо изучена. Подробное описание этого фермента будет дано в следующем разделе. Показано, что один из путей регуляции инициации репликации связан с фосфорилированием двух больших субъединиц ДНК-полимеразы α под действием Сdk. При этом циклин Е и Сdk стимулируют инициацию репликации при переходе клетки в S-фазу, а циклин А и Сdk ингибируют ее в фазе G2.
Очевидно, что активация упоминавшихся выше «ранне– и позднеактивных» ориджинов S.cerevisiae зависит от киназы Dbf4/Сdс7р. Вероятно, в каждом ориджине происходит локальная регуляция его активности дополнительными протеинкиназами, например Rad53. Киназа Rad53 блокирует запуск "позднеактивных" ориджинов в ранней S-фазе. Когда это блокирование устраняется, киназа Dbf4/Сdс7р активирует МСМ, что приводит сразу к нескольким последствиям: стимуляции геликазной активности МСМ и связыванию белка RРА и ДНК-полимеразы α с ориджинами репликации. Присоединение ДНК-полимеразы α к RС, раскручивание ДНК в ориджине и синтез РНК-праймера завершают процесс инициации репликации ДНК эукариот. Следует отметить, что роль ДНК-полимеразы α ограничивается только запуском репликации ДНК. Эта ДНК-полимераза не способна к процессивному, то еть протяженному, синтезу ДНК и не обладает корректирующей активностью. Поэтому в дальнейшем в процессе репликации она добавляет к РНК-праймеру приблизительно 20 нуклеотидов и замещается ДНК-полимеразами δ или ε.
Роst-RС, с образования которого начинается вся цепь событий процесса инициации репликации ДНК, в S-фазе клеточного цикла претерпевает изменения. Эти изменения касаются сродства ОRС к ДНК. Так, например, белок Orc1 Хепориs образует прочный комплекс с хроматином в ранней интерфазе до тех пор, пока не завершится сборка рге-RС. Затем в S-фазе сродство Огс1 к ДНК уменьшается. У млекопитающих Огс1 диссоциирует из хроматина в S-фазе, превращается в моно– или диубиквитинированную форму, затем деубиквитинируется и вновь связывается с ДНК при переходе из М– в G-1-фазу. Белок Огс2, напротив,
остается связанным с хроматином на протяжении всего клеточного цикла и не является субстратом для убиквитинирования. В клетках человека в S-фазе из хроматина диссоциирует комплекс белков, содержащий Огс1 и Огс2, который реассоциирует в конце митоза. В клетках дрожжей S.ротbе ОRС подвергается посттрансляционным изменениям в клеточном цикле: в фазе S начинается фосфорилирование одной из его субъединиц, Огс2, которое достигает максимума в фазах G2 и М. Таким образом, в клетках эукариот один из механизмов, предотвращающих повторную репликацию уже реплицированного хроматина, связан с инактивацией роst-RС либо путем диссоциации из него Огс1 (у высших эукариот), либо путем фосфорилирования Огс2 (у низших эукариот).
Таблица 2
Комплексы инициации транскрипции у эукариот


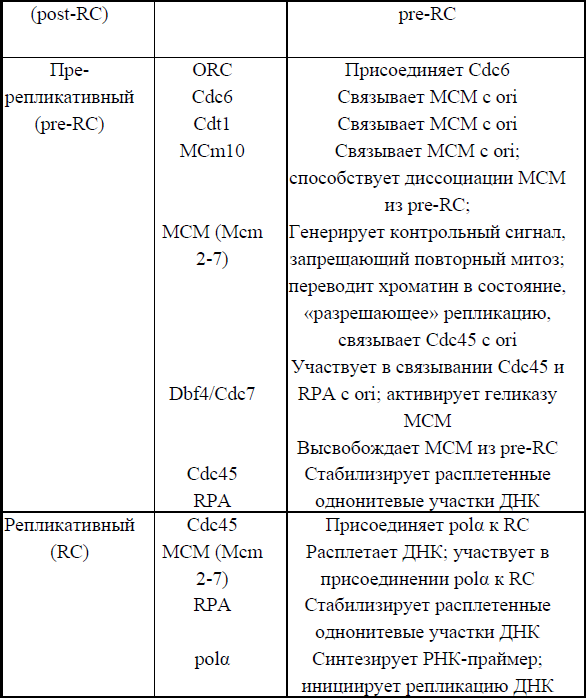
Для облегчения понимания последовательности связывания различных белков в зоне инициации репликации см. таблицу 2.
В последние несколько лет значительные успехи достигнуты в понимании механизмов регуляции практически каждой стадии инициации репликации. Они осуществляются на уровне функционирования всех компонентов, образующих пост-, пре– и репликативный комплексы. Эти компоненты подвергаются воздействию не одного, а ряда различных факторов. Примером этому служит регуляция комплекса МСМ, активность которого напрямую зависит от белков Сdc6, Мст10, Сdt1, циклин-зависимых киназ, киназы Dbf4/Сdс7, фосфатаз. До сих пор мало понятны закономерности процесса инициации репликации ДНК в эмбриогенезе и те факторы, которые влияют на эти процессы.
Глава 4. Механизм образования и необходимость РНК-праймера
4.1. Синтез праймера для полимеразной реакции
ДНК-полимеразы не могут начинать синтез ДНК непосредственно на матрице, а способны только добавлять новые дезоксирибонуклеотидные звенья к 3'-концу уже имеющейся полинуклеотидной цепи. Такую заранее образованную цепь, к которой добавляются нуклеотиды, называют праймером (или затравкой), она состоит из РНК. Короткую РНК-затравку синтезирует из рибонуклеозидтрифосфатов фермент, называемый ДНК-праймазой. Праймазная активность может принадлежать либо отдельному ферменту, либо одной из субъединиц ДНК-полимеразы. Праймаза связывается с геликазой и ДНК, формируя структуру, называемую праймосомой, и синтезирует РНК-праймер. РНК-праймеры удлиняются действием ДНК-полимеразы III у прокарит и ДНК-полимеразой α у эукариот. Схематически этот процесс на отстающей нити показан на рис. 8. У E.coli праймеры синтезирует специальный отдельный фермент – праймаза.
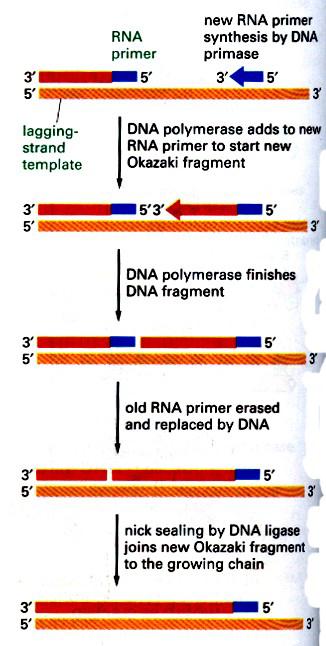
Рис. 8. РНК-праймеры на отстающей нити

Рис. 8. РНК-праймеры на отстающей нити
4.2. Понятие об РНК-ДНК дуплексе
ДНК обычно присутствует в клетке в В-форме. Кроме этого, описаны еще две возможные формы состояния ДНК – А и Z. Эти формы представлены на рис. 9. Взаимодействие оснований в В-форме представлено на рис. 10.
У А-формы плоскости оснований составляют угол в 20 градусов с перпендикуляром к оси спирали (у В-формы – 0), расстояние между парами оснований уменьшается до 0.29 нм (у В-формы – 0.34 нм), число пар на виток увеличивается до 11–12 (у В-формы – 10).
Пары оснований в А-форме очень сильно отодвинуты от оси спирали к периферии молекулы – почти на половину радиуса; сдвиг достигает 4–5 Å, а в В-форме ДНК он близок к нулю.
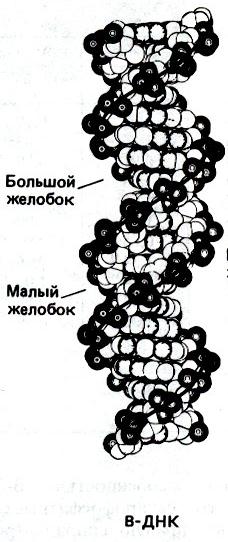

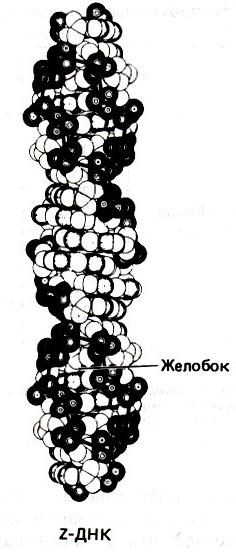
Рис. 9. Возможные формы ДНК
При образовании праймера (подробнее сам процесс его синтеза будет представлен при описании ДНК-полимеразы α эукариот) образуется ДНК-РНК дуплекс, который существует в А-форме. Таким
образом, в А-форме дуплекса обеспечивается оптимальный баланс между гидрофобными и комплементарными взаимодействиями оснований матрицы и праймера.
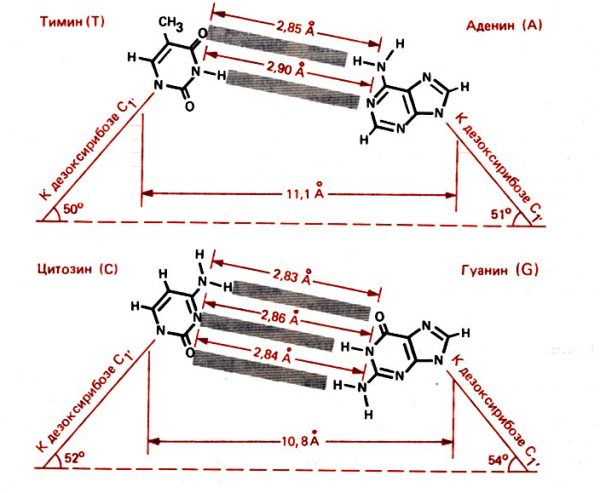
Рис. 10. Взаимное расположение нуклеотидов в ДНК в В-форме
У А-формы плоскости оснований составляют угол в 20 градусов с перпендикуляром к оси спирали (у В-формы – 0), расстояние между парами оснований уменьшается до 0.29 нм (у В-формы – 0.34 нм), число пар на виток увеличивается до 11–12 (у В-формы – 10).
Пары оснований в А-форме очень сильно отодвинуты от оси спирали к периферии молекулы – почти на половину радиуса; сдвиг достигает 4–5 Å, а в В-форме ДНК он близок к нулю.



Рис. 9. Возможные формы ДНК
При образовании праймера (подробнее сам процесс его синтеза будет представлен при описании ДНК-полимеразы α эукариот) образуется ДНК-РНК дуплекс, который существует в А-форме. Таким
образом, в А-форме дуплекса обеспечивается оптимальный баланс между гидрофобными и комплементарными взаимодействиями оснований матрицы и праймера.

Рис. 10. Взаимное расположение нуклеотидов в ДНК в В-форме
4.3. Ключевые ферменты, участвующие в синтезе ДНК
Многие известные теперь детали процесса репликации ДНК удалось установить благодаря исследованию поведения и активности ферментов, обеспечивающих работу аппарата репликации. Наиболее полно изучен механизм репликации бактериальной ДНК, особенно ДНК Е. соli и бактериофагов, которые в ней размножаются. Довольно хорошо известны и ферменты репликации дрожжей, Drosophila, млекопитающих.
4.3.1. ДНК-полимеразы
ДНК-подимсразы присутствуют во всех прокариотических и эукариотических клетках. Более того, многие вирусы бактерий и животных индуцируют образование вирус-специфических ДНК-полимераз или белков, способствующих эффективному участию ДНК-полимераз клеток-хозяев в репликации вирусной ДНК.
Многие прокариотические и эукариотические ДНК-полимеразы выделены в чистом виде, а их физические и ферментативные свойства детально охарактеризованы. И хотя эти свойства не совсем идентичны, механизм катализа для всех указанных ферментов в общих чертах одинаков.
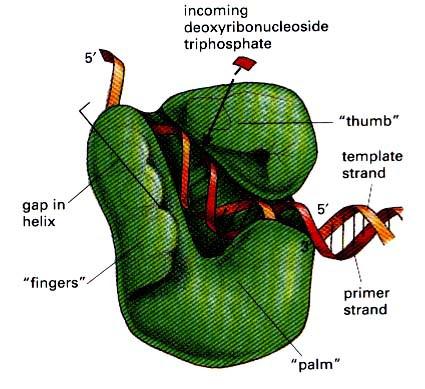
Рис. 11. Общий принцип строения ДНК-полимераз.
В первичной структуре ДНК-полимераз эукариот присутствуют консервативные мотивы, гомологичные соответствующим мотивам прокариотических ферментов. Это подтверждает, что все ДНК-синтезирующие ферменты имеют общий план строения. Общий принцип строения ДНК-полимераз показан на рис. 11. По форме ДНК-полимсразы можно уподобить полураскрытой кисти правой руки, в которой ладонь, большой палец и остальные пальцы представляют три основных пространственных домена и формируют полость, удерживающую ДНК-матрицу и затравку в ходе синтеза. Консервативные мотивы А, В и С образуют активный центр в домене «ладони», «пальцы» удерживают однонитевую матрицу, а «большой палец» прижимает праймер – матричный двунитевой участок.
Применительно к различным типам ДНК-полимераз эукариот эта модель может быть модифицирована. ДНК-полимеразы работают совместно с различными белковыми комплексами, удерживающими их в вилке репликации. Чаще всего их называют «зажим» и «загрузчик зажима» («sliding clamp», «clamp loader»).
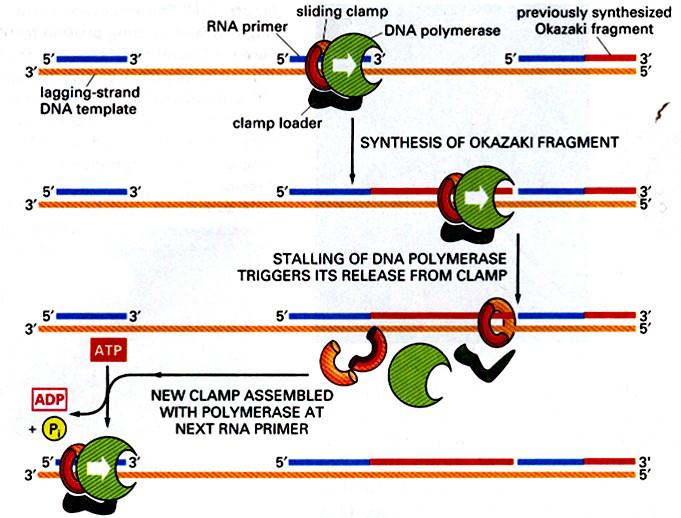
Рис. 12. Загрузка ДНК-полимеразы
После объединения ДНК-полимеразы с зажимом, «загрузчик зажима» отходит от места реакции, но держится поближе к отстающей нити, чтобы провести загрузку на новом месте объединения праймер-матрица, как только ДНК-полимераза диссоциирует при завершении синтеза предыдущего фрагмента Оказаки. Этот процесс схематически изображен на рис. 12. Подробно об этих комплексах у эукариот и их роли в репликации будет рассказано далее.
Многие прокариотические и эукариотические ДНК-полимеразы выделены в чистом виде, а их физические и ферментативные свойства детально охарактеризованы. И хотя эти свойства не совсем идентичны, механизм катализа для всех указанных ферментов в общих чертах одинаков.

Рис. 11. Общий принцип строения ДНК-полимераз.
В первичной структуре ДНК-полимераз эукариот присутствуют консервативные мотивы, гомологичные соответствующим мотивам прокариотических ферментов. Это подтверждает, что все ДНК-синтезирующие ферменты имеют общий план строения. Общий принцип строения ДНК-полимераз показан на рис. 11. По форме ДНК-полимсразы можно уподобить полураскрытой кисти правой руки, в которой ладонь, большой палец и остальные пальцы представляют три основных пространственных домена и формируют полость, удерживающую ДНК-матрицу и затравку в ходе синтеза. Консервативные мотивы А, В и С образуют активный центр в домене «ладони», «пальцы» удерживают однонитевую матрицу, а «большой палец» прижимает праймер – матричный двунитевой участок.
Применительно к различным типам ДНК-полимераз эукариот эта модель может быть модифицирована. ДНК-полимеразы работают совместно с различными белковыми комплексами, удерживающими их в вилке репликации. Чаще всего их называют «зажим» и «загрузчик зажима» («sliding clamp», «clamp loader»).

Рис. 12. Загрузка ДНК-полимеразы
После объединения ДНК-полимеразы с зажимом, «загрузчик зажима» отходит от места реакции, но держится поближе к отстающей нити, чтобы провести загрузку на новом месте объединения праймер-матрица, как только ДНК-полимераза диссоциирует при завершении синтеза предыдущего фрагмента Оказаки. Этот процесс схематически изображен на рис. 12. Подробно об этих комплексах у эукариот и их роли в репликации будет рассказано далее.
4.3.1.1. ДНК-полимеразы прокариот
Полимеразы прокариот обозначаются римскими цифрами (в отличие от полимераз эукариот, которые обозначаются греческими буквами). Наиболее полно изучена ДНК-полимераза I (Ро11) Е. соli. Она представляет собой одиночный полипептид с мультифуикциональными активностями. В качестве ДНК-полимеразы Ро11 катализирует перенос 5'-дезоксинуклеотидильных единиц дезоксинуклеозид-5'-трифосфатов к З'-ОН-группе в цепи ДНК или РНК, после чего происходит спаривание перенесенного основания с соответствующим основанием комплементарной цепи ДНК. Таким образом, для полимеризации ферменту необходимы праймер в качестве акцептора дезоксинуклеотида и матрица, определяющая присоединение нужного нуклеотида. Помимо полимеризации нуклеотидов, Ро11 катализирует две другие реакции, биологическая роль которых очень важна. В одной из них происходит гидролиз фосфодиэфирных связей в одной цепи ДНК или на неспаренном конце дуплексной ДНК, причем за один акт удаляется один нуклеотид, начиная с 3'-конца цепи (3'-5'-экзонуклеаза). Вторая реакция также состоит в отщеплении нуклеотидов, но гидролиз начинается с 5'-конца двунитевой ДНК в направлении к 3'-концу (5'-3'-экзонуклеаза). Эти различные активности присущи разным сайтам полипептидиой цепи РоlI, Если in vitro обработать РоlI трипсином, то полипептидная цепь расщепится на большой и малый фрагменты. Большой, С-концевой фрагмент («фрагмент Кленова») сохраняет ДНК-полимеразную и 3' -5'-экзонуклеазную активности; малый N-концевой фрагмент обладает только 5'-3'-экзонуклеазной активностью.
РоlI и присущие ей экзонуклеазные активности играют очень большую роль в репликации и репарации хромосомной ДНК Е. соli. 3’-5'-экзонуклеазная активность обеспечивает контроль за присоединением каждого нуклеотида и удаление ошибочных нуклеотидов вновь синтезированной цепи. Если эта активность подавлена в результате каких-то мутаций в гене, кодирующем РоlI, то при репликации генома часто происходят мутации – замены оснований.
Способность ДНК-полимеразы удлинять 3'-конец нити, спаренной с матричной нитью, позволяет ей заполнять пробелы между сегментами отстающей нити. РоlI удлиняет фрагменты Оказаки с 3'-концов и удаляет рибонуклеотиды праймера, с которых начинаются 5'-концы соседних фрагментов, что является необходимой предпосылкой для формирования непрерывной отстающей цепи. Поскольку РоlI способна удлинять 3'-конец одной из цепей в месте разрыва в двунитевой ДНК и удалять нуклеотиды с 5'-конца того же разрыва (процесс, называемый ник-трансляцией), этот фермент играет ключевую роль в репарации поврежденной ДНК. Ник-трансляция широко используется in vitro для синтеза радиоактивно меченой ДНК.
У Е. соli имеются и две другие ДНК-полимеразы, но они присутствуют в клетке в меньших количествах. РоlII присоединяет нуклеотиды значительно менее эффективно, чем Ро11, и не обладает 5'-З'-экзонуклеазной активностью. Следовательно, РоlII может заполнять пробелы между фрагментами ДНК, спаренными с матричной цепью, но не способна отщеплять РНК-нуклеотиды от фрагментов Оказаки или осуществлять ник-трансляцию. Роль РоlII в репликации и сохранении хромосомной ДНК Е. соli до настоящего момента неясна. Вероятно, она может участвовать в восстановлении синтеза ДНК после повреждения и остановки вилки репликации. Такой процесс принято называть ресинтезом.
PolIII-холофермент – это ключевой фермент, ответственный за репликацию хромосомной ДНК Е. соli. В каждой клетке содержится только 10–20 копий PolIII – холофермента, но именно он является основным компонентом мультиферментного полимеразного комплекса, инициирующего формирование репликативных вилок в точках начала репликации, участвующего в элонгации лидирующей цепи в вилке и удлиняющего РНК-праймеры с образованием фрагментов Оказаки. Так как PolIII – холофермент не обладает 5'-3'-экзонуклеазной активностью, для репликации отстающей цепи необходимо участие РоlI, чтобы произошло удлинение продукта, образовавшегося при участии PolIII, и удаление РНК-праймеров на 5'-конце фрагментов Оказаки.
Методом направленного мутационного анализа обнаружены изменения в полипептидной цепи основного (кор) фермента PolIII, и изучены аминокислотные замены, которые позволяют приписать определенные виды ферментативной активности конкретным субъединицам ферментного комплекса. Так, α-субъединица обладает полимеразной активностью, а ε-субъединица – 3' 5'-экзонуклеазной. Однако комплекс α– и ε-субъединиц обладает значительно более высокой полимеразной и экзонуклеазной активностями, чем каждая из соответствующих субъединиц в отдельности. Функция третьей, θ-субъединицы пока неясна.
Помимо субъединиц, составляющих PolIII – кор, PolIII-холофермент содержит еще семь субъединиц: τ,γ,β,δ,δ’,χ, и ψ. Перечисленные полипепгиды также существуют во множестве копий, так что в результате мол. масса полимеразного комплекса составляет примерно 103 кДа. Роль β-субъединицы заключается в том, чтобы свести к минимуму вероятность отделения фермента от матрицы до завершения процесса копирования, то есть работает как «зажим». Субъединица τ является фактором димеризации репликативных холоферментов. Точная же функция других субъединиц неизвестна. Вполне возможно, что PolIII-холофермент существует в двух формах, каждая из которых содержит определенный набор вспомогательных субъединиц, придающих ферменту определенные свойства. В одной форме фермент катализирует синтез непрерывной ведущей цепи, а в другой – прерывистой отстающей.
PolIII-холофермент катализирует же реакции синтеза, что и PolI, но работает примерно в 60 раз быстрее. Более того, PolIII-холофермент обладает повышенным сродством к матрице и обеспечивает более высокую эффективность копирования. PolIII-холофермент может связываться и с другими белками, увеличивая эффективность процесса копирования благодаря координации некоторых важных ферментативных этапов репликации. На этом более высоком уровне организации в комплексы могут включаться белки, расплетающие спираль ДНК в точках начала репликации и в репликативных вилках (геликазы), инициирующие образование праймерных РНК (праймазы), обеспечивающие последовательное наращивание цепей ДНК, терминирующие процесс репликации и разделяющие дочерние спирали ДНК.
РоlI и присущие ей экзонуклеазные активности играют очень большую роль в репликации и репарации хромосомной ДНК Е. соli. 3’-5'-экзонуклеазная активность обеспечивает контроль за присоединением каждого нуклеотида и удаление ошибочных нуклеотидов вновь синтезированной цепи. Если эта активность подавлена в результате каких-то мутаций в гене, кодирующем РоlI, то при репликации генома часто происходят мутации – замены оснований.
Способность ДНК-полимеразы удлинять 3'-конец нити, спаренной с матричной нитью, позволяет ей заполнять пробелы между сегментами отстающей нити. РоlI удлиняет фрагменты Оказаки с 3'-концов и удаляет рибонуклеотиды праймера, с которых начинаются 5'-концы соседних фрагментов, что является необходимой предпосылкой для формирования непрерывной отстающей цепи. Поскольку РоlI способна удлинять 3'-конец одной из цепей в месте разрыва в двунитевой ДНК и удалять нуклеотиды с 5'-конца того же разрыва (процесс, называемый ник-трансляцией), этот фермент играет ключевую роль в репарации поврежденной ДНК. Ник-трансляция широко используется in vitro для синтеза радиоактивно меченой ДНК.
У Е. соli имеются и две другие ДНК-полимеразы, но они присутствуют в клетке в меньших количествах. РоlII присоединяет нуклеотиды значительно менее эффективно, чем Ро11, и не обладает 5'-З'-экзонуклеазной активностью. Следовательно, РоlII может заполнять пробелы между фрагментами ДНК, спаренными с матричной цепью, но не способна отщеплять РНК-нуклеотиды от фрагментов Оказаки или осуществлять ник-трансляцию. Роль РоlII в репликации и сохранении хромосомной ДНК Е. соli до настоящего момента неясна. Вероятно, она может участвовать в восстановлении синтеза ДНК после повреждения и остановки вилки репликации. Такой процесс принято называть ресинтезом.
PolIII-холофермент – это ключевой фермент, ответственный за репликацию хромосомной ДНК Е. соli. В каждой клетке содержится только 10–20 копий PolIII – холофермента, но именно он является основным компонентом мультиферментного полимеразного комплекса, инициирующего формирование репликативных вилок в точках начала репликации, участвующего в элонгации лидирующей цепи в вилке и удлиняющего РНК-праймеры с образованием фрагментов Оказаки. Так как PolIII – холофермент не обладает 5'-3'-экзонуклеазной активностью, для репликации отстающей цепи необходимо участие РоlI, чтобы произошло удлинение продукта, образовавшегося при участии PolIII, и удаление РНК-праймеров на 5'-конце фрагментов Оказаки.
Методом направленного мутационного анализа обнаружены изменения в полипептидной цепи основного (кор) фермента PolIII, и изучены аминокислотные замены, которые позволяют приписать определенные виды ферментативной активности конкретным субъединицам ферментного комплекса. Так, α-субъединица обладает полимеразной активностью, а ε-субъединица – 3' 5'-экзонуклеазной. Однако комплекс α– и ε-субъединиц обладает значительно более высокой полимеразной и экзонуклеазной активностями, чем каждая из соответствующих субъединиц в отдельности. Функция третьей, θ-субъединицы пока неясна.
Помимо субъединиц, составляющих PolIII – кор, PolIII-холофермент содержит еще семь субъединиц: τ,γ,β,δ,δ’,χ, и ψ. Перечисленные полипепгиды также существуют во множестве копий, так что в результате мол. масса полимеразного комплекса составляет примерно 103 кДа. Роль β-субъединицы заключается в том, чтобы свести к минимуму вероятность отделения фермента от матрицы до завершения процесса копирования, то есть работает как «зажим». Субъединица τ является фактором димеризации репликативных холоферментов. Точная же функция других субъединиц неизвестна. Вполне возможно, что PolIII-холофермент существует в двух формах, каждая из которых содержит определенный набор вспомогательных субъединиц, придающих ферменту определенные свойства. В одной форме фермент катализирует синтез непрерывной ведущей цепи, а в другой – прерывистой отстающей.
PolIII-холофермент катализирует же реакции синтеза, что и PolI, но работает примерно в 60 раз быстрее. Более того, PolIII-холофермент обладает повышенным сродством к матрице и обеспечивает более высокую эффективность копирования. PolIII-холофермент может связываться и с другими белками, увеличивая эффективность процесса копирования благодаря координации некоторых важных ферментативных этапов репликации. На этом более высоком уровне организации в комплексы могут включаться белки, расплетающие спираль ДНК в точках начала репликации и в репликативных вилках (геликазы), инициирующие образование праймерных РНК (праймазы), обеспечивающие последовательное наращивание цепей ДНК, терминирующие процесс репликации и разделяющие дочерние спирали ДНК.
