Страница:
ДНК-полимеразы, синтезируемые другими бактериями и многими бактериофагами, различаются по своим физической структуре и свойствам. Тем не менее, катализируемые ими реакции практически идентичны реакциям, изученным у Е. соli. У всех ДНК-полимераз есть корректирующая 3'-5'-экзонуклеаза, однако 5'-3'-экзонуклеаза у большинства ферментов отсутствует. Например, ДНК-полимераза фага Т4 может осуществлять 3'-5'-экзонуклеазную реакцию и корректировать ошибки репликации, но не способна катализировать 5'– З'-экзонуклеазную реакцию и поэтому не может обеспечить ник-трансляцию. При репликации ДНК фага Т4 5'-3'-экзонуклеазную реакцию удаления РНК-праймеров перед объединением фрагментов Оказаки катализирует другой кодируемый фагом белок. В процессе прерывистого синтеза отстающих нитей и репарации повреждений ДНК фага Т4 этот фермент работает согласованно с фаговой ДНК-полимеразой. Некоторые вирусы животных (например, герпесвирус, вирус коровьей оспы и вирус гепатита) индуцируют синтез особых полимераз для репликации своих геномов.
Другие вирусы образуют белки, которые стимулируют системы репликации клеточной ДНК или участвуют в репликации вирусной ДНК. Например, паповавирусы синтезируют белки, необходимые для инициации репликации. Аденовирусы человека кодируют белки, «запускающие» инициацию синтеза обеих цепей линейной вирусной ДНК. Они продуцируют также особые ДНК-связывающие белки, облегчающие репликацию.
4.3.1.2. ДНК-полимеразы эукариот
4.3.1.3. ДНК-полимераза α – праймаза
4.3.1.4. Реакция праймирования
Другие вирусы образуют белки, которые стимулируют системы репликации клеточной ДНК или участвуют в репликации вирусной ДНК. Например, паповавирусы синтезируют белки, необходимые для инициации репликации. Аденовирусы человека кодируют белки, «запускающие» инициацию синтеза обеих цепей линейной вирусной ДНК. Они продуцируют также особые ДНК-связывающие белки, облегчающие репликацию.
4.3.1.2. ДНК-полимеразы эукариот
В эукариотических клетках идентифицировано множество ДНК-полимераз, но их физические и функциональные свойства изучены менее детально, чем у соответствующих ферментов прокариот.
Таблица 3
ДНК-полимеразы эукариот
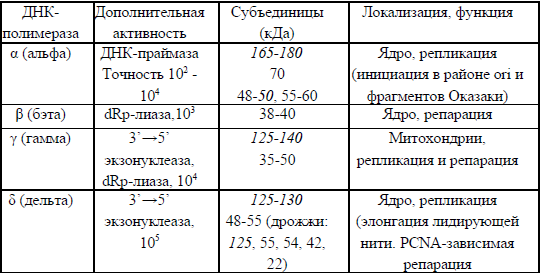

Точная пространственная структура, определенная с помощью рентгеноструктурного анализа, известна лишь для одной ДНК-полимеразы эукариот – полимеразы β-типа, которая заметно отличается по строению от других эукариотических ДНК-полимераз. Сводные данные об основных полимеразах эукариот приведены в таблице 3.
Таблица 3
ДНК-полимеразы эукариот


Точная пространственная структура, определенная с помощью рентгеноструктурного анализа, известна лишь для одной ДНК-полимеразы эукариот – полимеразы β-типа, которая заметно отличается по строению от других эукариотических ДНК-полимераз. Сводные данные об основных полимеразах эукариот приведены в таблице 3.
4.3.1.3. ДНК-полимераза α – праймаза
В клетках эукариот синтез ДНК происходит, в основном, в специфических плотных структурах ("репликативных фабриках"), присоединенных к диффузному ядерному матриксу. Предполагается, что в молекулярной организации ядерного матрикса играют некоторую роль фосфолипиды и что ДНК связана с ядерным скелетом гидрофобными взаимодействиями. "Репликативные фабрики" или 21S репликативные комплексы, включают в себя группу ферментов, состоящую не менее чем из 30 белков с молекулярной массой от 15 до 300 кДа, и содержат помимо ДНК-полимеразы α – праймазы еще и 3'-5'-экзонуклеазу, ДНК-лигазу I, РНКазу Н, ДНК-топоизомеразу I, ДНК-геликазу, РСNA и ряд других факторов. Также этот комплекс содержит RРА, специфически взаимодействующий с субъединицей р48 комплекса полимераза-праймаза. Значительный запас ДНК-полимеразы α накапливается в яйцеклетках иглокожих, амфибий, костистых рыб и дрозофилы для обеспечения интенсивной репликации ядерной ДНК в ходе раннего развития.
Как правило, ДНК-полимеразы α не обладают корректорской 3'—5'-экзонуклеазной активностью. Однако в каталитической субъединице 182 кДа ДНК-полимеразы α дрозофилы обнаружена 3'—5'-экзонуклеаза, проявляющая активность только при диссоциации субъединицы 73 кДа.
Мультибелковая форма ДНК-полимеразы α содержит также белок, который связывает динуклеотид диаденозинтетрафосфат (Ар4А). Предполагается, что Ар4А участвует в репликации ДНК и клеточном делении. Имеются данные о способности ДНК-полимеразы α использовать Ар4А в качестве праймера. Однако участие Ар4А в качестве праймера in vivo маловероятно, скорее он используется как эффектор. Интересно, что триптофанил-тРНК-синтетаза, синтезирующая этот динуклеотид, находится в том же мултибелковом комплексе.
Обычно комплекс праймаза-полимераза α состоит из четырех субъединиц: большой субъединицы с молекулярной массой 180 кДа, или семейства полипептидов с размерами от 140 до 160 кДа; субъединицы с молекулярной массой около 68–70 кДа и двух малых субъединиц с молекулярными массами 54–58 и 46–50 кДа. Субъединица р180 отвечает за полимеразную функцию. С двумя малыми субъединицами связана праймазная активность. При этом субъединица 48 кДа является каталитической и непосредственно осуществляет праймирование ДНК, а субъединица 58 кДа участвует в связывании инициирующего пуринового нуклеотида и присоединении субъединицы р48 к ДНК-полимеразе α. Она также влияет на скорость полимеризации и стабильность продукта, синтезируемого субъединицей 48 кДа. р58 также облегчает проникновение р48 из цитоплазмы в ядро. Субъединица р180 непосредственно взаимодействует с р58.
С каталитической субъединицей связана субъединица 68–70 кДа, которая необходима для транспорта каталитического полипептида в клеточное ядро. Субъединица 68–70 кДа участвует также в регуляции уровня ДНК-полимеразы α в клетке, она стимулирует синтез каталитического полипептида. Хотя комплекс ДНК-полимераза α-праймаза состоит из четырех субъединиц, количественный состав этого комплекса может быть различным. Вероятно, полимераза α и праймаза находятся в «коре» в соотношении 1: 3.
Как правило, ДНК-полимеразы α не обладают корректорской 3'—5'-экзонуклеазной активностью. Однако в каталитической субъединице 182 кДа ДНК-полимеразы α дрозофилы обнаружена 3'—5'-экзонуклеаза, проявляющая активность только при диссоциации субъединицы 73 кДа.
Мультибелковая форма ДНК-полимеразы α содержит также белок, который связывает динуклеотид диаденозинтетрафосфат (Ар4А). Предполагается, что Ар4А участвует в репликации ДНК и клеточном делении. Имеются данные о способности ДНК-полимеразы α использовать Ар4А в качестве праймера. Однако участие Ар4А в качестве праймера in vivo маловероятно, скорее он используется как эффектор. Интересно, что триптофанил-тРНК-синтетаза, синтезирующая этот динуклеотид, находится в том же мултибелковом комплексе.
Обычно комплекс праймаза-полимераза α состоит из четырех субъединиц: большой субъединицы с молекулярной массой 180 кДа, или семейства полипептидов с размерами от 140 до 160 кДа; субъединицы с молекулярной массой около 68–70 кДа и двух малых субъединиц с молекулярными массами 54–58 и 46–50 кДа. Субъединица р180 отвечает за полимеразную функцию. С двумя малыми субъединицами связана праймазная активность. При этом субъединица 48 кДа является каталитической и непосредственно осуществляет праймирование ДНК, а субъединица 58 кДа участвует в связывании инициирующего пуринового нуклеотида и присоединении субъединицы р48 к ДНК-полимеразе α. Она также влияет на скорость полимеризации и стабильность продукта, синтезируемого субъединицей 48 кДа. р58 также облегчает проникновение р48 из цитоплазмы в ядро. Субъединица р180 непосредственно взаимодействует с р58.
С каталитической субъединицей связана субъединица 68–70 кДа, которая необходима для транспорта каталитического полипептида в клеточное ядро. Субъединица 68–70 кДа участвует также в регуляции уровня ДНК-полимеразы α в клетке, она стимулирует синтез каталитического полипептида. Хотя комплекс ДНК-полимераза α-праймаза состоит из четырех субъединиц, количественный состав этого комплекса может быть различным. Вероятно, полимераза α и праймаза находятся в «коре» в соотношении 1: 3.
4.3.1.4. Реакция праймирования
Инициация репликации и прерывистый синтез ДНК на отстающей цепи происходит по РНК-праймерному механизму и является универсальным свойством репликации ДНК у про– и эукариот.
ДНК-праймаза отличается от других РНК-полимераз целым рядом присущих только ей свойств. Во-первых, матричной и субстратной специфичностью. Во-вторых, необычной процессивностью – синтезом мультимеров, кратных 10-нуклеотидным звеньям. В-третьих, низкой точностью и устойчивостью к некоторым ингибиторам РНК– и ДНК-полимераз. Здесь необходимо вернуться к проблеме синтеза РНК-праймеров. Синтез РНК-праймеров на природных матрицах начинается во множественных, но не случайных участках, его инициация происходит с АТР или GТР даже при высоких концентрациях СТР и UTР. Показано, что, например, ДНК вируса SV40 содержат предпочтительные участки инициации – 3'-dСТТТ или 3'-dССС, расположенные внутри участков из 7-25 пиримидиновых нуклеотидов. Высокое соотношение АТР/GТР повышает вероятность инициации в участках 3'-dСТТТ, а низкое – в участках 3'-dССС. Таким образом, концентрация NТР и нуклеотидная последовательность матрицы определяют участки инициации. Впрочем, участки инициации in vivo заметно отличаются от участков инициации, используемых во время репликации ДНК SV40. Во многих случаях обнаружена последовательность 5'-YYYYYYYYСТТТYYYY-3', где Y = С или Т, которая является стартовой площадкой для инициации синтеза ДНК-праймазой в составе комплекса с ДНК-полимеразой α. Минимальная длина пиримидинового кластера должна быть не менее 7 н. Замена одного из пиримидинов на 3'-конце кластера значительно понижает частоту инициации, а замены внутри и вне кластера приводят к смещению точки старта. Известно, что матрицу распознает сама ДНК-праймаза. Стартовый нуклеотид вновь синтезированного праймера всегда является пурином (чаще всего – аденином).
Этот комплекс имеет еще одну специфическую функцию – синтез теломерной отстающей цепи ДНК млекопитающих осуществляет ДНК-полимераза α-праймаза.
ДНК-праймаза – сравнительно медленный фермент. Средняя скорость включения NTP этим ферментом примерно на два порядка меньше, чем скорость включения dNТР ДНК-полимеразой α. ДНК-полимераза α способна удлинять праймеры длиной более 7-10 н. Продукты длиной 2–6 н. не являются субстратами ДНК-полимеразы α и называются абортивными, До синтеза РНК-праймера ДНК-полимераза α и ДНК-праймаза действуют независимо, а после этого их активности координируются. Синтезированный РНК-праймер перемещается в полимеразный активный центр без диссоциации в раствор. Это внутримолекулярное перемещение праймера в дуплексе с матрицей является быстрым и сравнимо по скорости с синтезом праймера. После того как ДНК-полимераза α удлинит праймер, праймаза начинает синтез нового праймера, и цикл повторяется. ДНК-праймаза эукариот отличается от других РНК-полимераз своей способностью к включению дезоксирибонуклеотида в праймер, таким же свойством обладает и праймаза прокариот. Одним из возможных объяснений необходимости включения dNТР в 3'-конец праймера является необходимость перехода от А-формы к В-форме ДНК. Поэтому понимание механизма "переключения" комплекса ДНК-полимеразы α-праймазы от синтеза РНК к ДНК имеет очень большое значение. Способность праймазы узнавать одновременно и рибо-, и дезоксириботрифосфаты представляет серьезный научный интерес.
Выбор РНК-праймера определяется гидрофобным характером белково-нуклеиновых взаимодействий. В случае гибрида РНК-ДНК дуплекс находится в А-форме, в которой обеспечивается оптимальный баланс между гидрофобными и комплементарными взаимодействиями оснований матрицы и праймера.
После инициации рост праймера сопровождается извлечением оснований матрицы из гидрофобной полости белка для спаривания с основаниями растущей цепи РНК. В условиях такой конкуренции короткие ди– и тринуклеотиды легко диссоциируют, образуя абортивные продукты. С ростом длины праймера прочность дуплекса увеличивается, ослабевает влияние гидрофобности активного центра, и пары оснований приближаются к оси спирали. При длине праймера 7 н создаются условия для включения дезоксинуклеотида и перехода в энергетически более выгодную В-форму. Здесь нужно учитывать и большее сродство к ферменту dNТР по сравнению с NТР. Предложенная концепция, по-видимому, носит универсальный характер, поскольку подобное происходит и при инициации транскрипции.
ДНК-полимераза α связывает сначала матрицу, затем праймер и субстрат. ДНК-полимераза α наиболее активна на двунитевой ДНК, содержащей бреши длиной не менее 20–30 н. Область связывания матрицы с ДНК-полимеразой α является достаточно протяженной. Она строго защищает от гидролиза 9 н праймерной цепи, 13 н двухцепочечного участка и 14 н одноцепочечной матрицы и слабо защищает несколько оснований вне этого района. Фермент связывается с 19–20 н матрицы посредством ионных и гидрофобных взаимодействий, эффективность связывания при этом коррелирует с гидрофобностью оснований матрицы.
Отличительной особенностью ДНК-полимеразы α является ее способность удлинять РНК-праймеры и прочная ассоциация с ДНК-праймазой, которая синтезирует эти праймеры.
Средняя процессивность ДНК-полимеразы α составляет 20–50 н. Праймаза редко ошибается в момент синтеза динуклеотида, но затем легко использует неправильные NТР. Хотя скорость включения ошибочных нуклеотидов зависит от нуклеотидной последовательности матрицы и самого неправильного нуклеотида, в принципе, ДНК-праймаза является самым неточным нуклеотид-полимеризующим ферментом. В некоторых случаях один неправильный нуклеотид приходится менее чем на 100 правильных. Встраивание неправильного нуклеотида не препятствует включению следующего правильного нуклеотида. Праймаза может полимеризовать сходные нуклеотиды и генерировать праймеры с множественными ошибками, котрые не ингибируют дальнейший синтез и после внутримолекулярного переноса в ДНК-полимеразный активный центр удлиняются ДНК-полимеразой в присутствии dNTP.
Существуют две модели механизма синтеза праймеров, некомплементарных матрице. Согласно первой модели, фермент просто включает некомплементарные матрице нуклеотиды. Вторая модель предполагает включение нуклеотида, комплементарного матрице, с последующим скольжением праймера относительно матрицы. Низкая точность ДНК-праймазы послужила основой гипотезы о том, почему именно РНК является затравкой при репликации ДНК. Поскольку первые нуклеотиды могут ошибочно включаться в новую растущую цепь, предполагается, что РНК-праймер отмечает "высокоошибочный" участок для последующего вырезания и более точной застройки. Эта точка зрения выглядит убедительной, но, вероятно, главная причина появления РНК-праймера связана все-таки с более эффективной инициацией синтеза ДНК при наличии А-формы РНК-ДНК дуплекса.
ДНК-праймаза отличается от других РНК-полимераз целым рядом присущих только ей свойств. Во-первых, матричной и субстратной специфичностью. Во-вторых, необычной процессивностью – синтезом мультимеров, кратных 10-нуклеотидным звеньям. В-третьих, низкой точностью и устойчивостью к некоторым ингибиторам РНК– и ДНК-полимераз. Здесь необходимо вернуться к проблеме синтеза РНК-праймеров. Синтез РНК-праймеров на природных матрицах начинается во множественных, но не случайных участках, его инициация происходит с АТР или GТР даже при высоких концентрациях СТР и UTР. Показано, что, например, ДНК вируса SV40 содержат предпочтительные участки инициации – 3'-dСТТТ или 3'-dССС, расположенные внутри участков из 7-25 пиримидиновых нуклеотидов. Высокое соотношение АТР/GТР повышает вероятность инициации в участках 3'-dСТТТ, а низкое – в участках 3'-dССС. Таким образом, концентрация NТР и нуклеотидная последовательность матрицы определяют участки инициации. Впрочем, участки инициации in vivo заметно отличаются от участков инициации, используемых во время репликации ДНК SV40. Во многих случаях обнаружена последовательность 5'-YYYYYYYYСТТТYYYY-3', где Y = С или Т, которая является стартовой площадкой для инициации синтеза ДНК-праймазой в составе комплекса с ДНК-полимеразой α. Минимальная длина пиримидинового кластера должна быть не менее 7 н. Замена одного из пиримидинов на 3'-конце кластера значительно понижает частоту инициации, а замены внутри и вне кластера приводят к смещению точки старта. Известно, что матрицу распознает сама ДНК-праймаза. Стартовый нуклеотид вновь синтезированного праймера всегда является пурином (чаще всего – аденином).
Этот комплекс имеет еще одну специфическую функцию – синтез теломерной отстающей цепи ДНК млекопитающих осуществляет ДНК-полимераза α-праймаза.
ДНК-праймаза – сравнительно медленный фермент. Средняя скорость включения NTP этим ферментом примерно на два порядка меньше, чем скорость включения dNТР ДНК-полимеразой α. ДНК-полимераза α способна удлинять праймеры длиной более 7-10 н. Продукты длиной 2–6 н. не являются субстратами ДНК-полимеразы α и называются абортивными, До синтеза РНК-праймера ДНК-полимераза α и ДНК-праймаза действуют независимо, а после этого их активности координируются. Синтезированный РНК-праймер перемещается в полимеразный активный центр без диссоциации в раствор. Это внутримолекулярное перемещение праймера в дуплексе с матрицей является быстрым и сравнимо по скорости с синтезом праймера. После того как ДНК-полимераза α удлинит праймер, праймаза начинает синтез нового праймера, и цикл повторяется. ДНК-праймаза эукариот отличается от других РНК-полимераз своей способностью к включению дезоксирибонуклеотида в праймер, таким же свойством обладает и праймаза прокариот. Одним из возможных объяснений необходимости включения dNТР в 3'-конец праймера является необходимость перехода от А-формы к В-форме ДНК. Поэтому понимание механизма "переключения" комплекса ДНК-полимеразы α-праймазы от синтеза РНК к ДНК имеет очень большое значение. Способность праймазы узнавать одновременно и рибо-, и дезоксириботрифосфаты представляет серьезный научный интерес.
Выбор РНК-праймера определяется гидрофобным характером белково-нуклеиновых взаимодействий. В случае гибрида РНК-ДНК дуплекс находится в А-форме, в которой обеспечивается оптимальный баланс между гидрофобными и комплементарными взаимодействиями оснований матрицы и праймера.
После инициации рост праймера сопровождается извлечением оснований матрицы из гидрофобной полости белка для спаривания с основаниями растущей цепи РНК. В условиях такой конкуренции короткие ди– и тринуклеотиды легко диссоциируют, образуя абортивные продукты. С ростом длины праймера прочность дуплекса увеличивается, ослабевает влияние гидрофобности активного центра, и пары оснований приближаются к оси спирали. При длине праймера 7 н создаются условия для включения дезоксинуклеотида и перехода в энергетически более выгодную В-форму. Здесь нужно учитывать и большее сродство к ферменту dNТР по сравнению с NТР. Предложенная концепция, по-видимому, носит универсальный характер, поскольку подобное происходит и при инициации транскрипции.
ДНК-полимераза α связывает сначала матрицу, затем праймер и субстрат. ДНК-полимераза α наиболее активна на двунитевой ДНК, содержащей бреши длиной не менее 20–30 н. Область связывания матрицы с ДНК-полимеразой α является достаточно протяженной. Она строго защищает от гидролиза 9 н праймерной цепи, 13 н двухцепочечного участка и 14 н одноцепочечной матрицы и слабо защищает несколько оснований вне этого района. Фермент связывается с 19–20 н матрицы посредством ионных и гидрофобных взаимодействий, эффективность связывания при этом коррелирует с гидрофобностью оснований матрицы.
Отличительной особенностью ДНК-полимеразы α является ее способность удлинять РНК-праймеры и прочная ассоциация с ДНК-праймазой, которая синтезирует эти праймеры.
Средняя процессивность ДНК-полимеразы α составляет 20–50 н. Праймаза редко ошибается в момент синтеза динуклеотида, но затем легко использует неправильные NТР. Хотя скорость включения ошибочных нуклеотидов зависит от нуклеотидной последовательности матрицы и самого неправильного нуклеотида, в принципе, ДНК-праймаза является самым неточным нуклеотид-полимеризующим ферментом. В некоторых случаях один неправильный нуклеотид приходится менее чем на 100 правильных. Встраивание неправильного нуклеотида не препятствует включению следующего правильного нуклеотида. Праймаза может полимеризовать сходные нуклеотиды и генерировать праймеры с множественными ошибками, котрые не ингибируют дальнейший синтез и после внутримолекулярного переноса в ДНК-полимеразный активный центр удлиняются ДНК-полимеразой в присутствии dNTP.
Существуют две модели механизма синтеза праймеров, некомплементарных матрице. Согласно первой модели, фермент просто включает некомплементарные матрице нуклеотиды. Вторая модель предполагает включение нуклеотида, комплементарного матрице, с последующим скольжением праймера относительно матрицы. Низкая точность ДНК-праймазы послужила основой гипотезы о том, почему именно РНК является затравкой при репликации ДНК. Поскольку первые нуклеотиды могут ошибочно включаться в новую растущую цепь, предполагается, что РНК-праймер отмечает "высокоошибочный" участок для последующего вырезания и более точной застройки. Эта точка зрения выглядит убедительной, но, вероятно, главная причина появления РНК-праймера связана все-таки с более эффективной инициацией синтеза ДНК при наличии А-формы РНК-ДНК дуплекса.
Конец бесплатного ознакомительного фрагмента
