Страница:
Н. А. Мухин, Л. В. Козловская, Е. М. Пальцева, В. В. Фомин
Нефрология: неотложные состояния
Введение
Неотложными принято считать состояния, которые при отсутствии соответствующих экстренных терапевтических мероприятий способны очень быстро приводить к угрожающим жизни осложнениям и/или смерти. Варианты неотложных состояний, возможных в ряде разделов клиники внутренних болезней (пульмонологии, кардиологии), в настоящее время четко определены, подходы к обследованию и лечению таких пациентов алгоритмизированы, при этом выбор диагностических и лечебных вмешательств, как правило, осуществляется с учетом данных медицины, основанной на доказательствах, позволяющих не только обоснованно соотнести риск и пользу от их применения, но и предсказать долгосрочное влияние на прогноз.
В отличие от этого в нефрологии понятие о неотложных состояниях в настоящее время сформировано менее четко. Нередко в качестве неотложного нефрологического состояния называют только различные варианты острой почечной недостаточности, стратегия ведения которой при этом ограничивается до соответствующей инфузионной терапии и проведения экстренного гемодиализа. Вместе с тем именно в нефрологии рассмотрение проблемы неотложных состояний, по-видимому, должно осуществляться по нозологическому принципу, поскольку особенности заболевания почек часто становятся определяющими при выборе тактики ведения, иногда отличающейся радикально при относительно стереотипных клинических и лабораторных проявлениях.
Основными особенностями неотложных состояний в нефрологии следует считать:
• возможность бурного развития при отсутствии заболевания почек, исходно сохранной функции почек или умеренном почечном поражении (типично для лекарственных и сосудистых нефропатий);
• нередкое отсутствие или малую демонстративность клинических проявлений, затрудняющие раннюю диагностику и выделение достоверных предвестников. При этом ориентация на жалобы практически не может быть использована для распознавания нефрологических неотложных состояний в отличие от того, что наблюдается при других заболеваниях: например, боль за грудиной является основным диагностическим признаком острого коронарного синдрома;
• стереотипность лабораторных изменений (например, рост креатининемии и калиемии как интегральный маркер быстро ухудшающейся почечной функции);
• кроме того, риск необратимого ухудшения почечной функции, как правило, дополняется драматически возрастающей вероятностью сердечно-сосудистых осложнений, что дополнительно ухудшает прогноз.
Как уже было сказано, клинические проявления неотложных нефрологических состояний зачастую мало заметны, в связи с чем решающее значение в их выявлении приобретает анализ динамики лабораторных показателей. Маркерами неотложных состояний в нефрологии можно считать:
• быстрый рост АД: формирование артериальной гипертензии de novo или снижение/утрату эффективности антигипертензивной терапии;
• ускоренно развивающееся поражение органов-мишеней артериальной гипертензии – острую левожелудочковую недостаточность, ухудшение зрения вплоть до слепоты (отек диска зрительного нерва – маркер «озлокачествления» артериальной гипертензии, возможны также эмболии и тромбозы сосудов сетчатки), общемозговую симптоматику (заторможенность, нарушения сознания);
• быстро нарастающие гиперкреатининемию и снижение скорости клубочковой фильтрации (определяемой расчетными методами – с помощью формул Cockroft-Gault или MDRD);
• рост плазменной концентрации калия (одно из наиболее угрожающих жизни проявлений);
• рост или снижение плазменной концентрации натрия;
• снижение плазменной концентрации альбумина (особенно при нефротическом синдроме);
• развитие артериальной гипотензии (прежде всего при нефротическом синдроме, при котором оно указывает на развитие нефротического криза);
• появление неврологической симптоматики (может свидетельствовать как о нарушениях мозгового кровообращения, так и о нарушениях электролитного гомеостаза).
Нефрологические неотложные состояния возникают особенно часто в следующих клинических ситуациях:
• при первом назначении любого лекарственного препарата;
• у пожилых больных;
• при исходной хронической почечной недостаточности (феномен acute on chronic – развитие острого ухудшения функции почек при исходном стойком ее снижении представляет собой одну из наиболее прогностически неблагоприятных ситуаций) и/или хроническом заболевании почек;
• при сахарном диабете II типа;
• при хронической сердечной недостаточности;
• при распространенном атеросклерозе;
• при нестабильных гемодинамических показателях;
• при вмешательстве на сосудах;
• при применении рентген-контрастных агентов.
Опыт любой многопрофильной клиники свидетельствует о реальной возможности возникновения у больного той или другой нефрологической ситуации, в том числе требующей неотложной помощи, включая перевод больного в отделение интенсивного наблюдения. Своевременная расшифровка этих неотложных состояний позволяет во многих случаях не только сохранить жизнь, но и во многом повлиять на долгосрочный прогноз тяжелых больных. Еще более четко реальность подобных ситуаций подтверждает опыт работы нефрологических отделений таких многопрофильных клиник, нозологический профиль которых включает не только «первичные» заболевания почек (различные варианты гломерулонефрита и др.), но и поражение почек при системных заболеваниях (системной красной волчанке, васкулитах, «склеродермической почке», нарушениях внутрисосудистого свертывания с тромбозами, тромбоэмболиями, тромботической микроангиопатией), а также поражение почек у больных с прогрессирующими заболеваниями печени (такими, как тяжелые варианты криоглобулинемического васкулита у больных с хроническим вирусным гепатитом C, гепаторенальным синдромом), гипертоническим кризом, тяжелой хронической сердечной недостаточностью.
«Первичные» поражения почек также могут быть причиной развития неотложной ситуации: тяжелый нефротический синдром с нефротическим кризом, быстропрогрессирующий нефрит с постоянной опасностью различных ургентных состояний, острый тубулоинтерстициальный нефрит различной этиологии, поражение почек при миоглобинурии и гемоглобинурии, а также почечные осложнения проводимого патогенетического лечения (например, при лечении больного нефритом циклоспорином).
В настоящее время хорошо известны остро возникающие нефрологические осложнения при проведении исследований с введением контрастных препаратов (рентгенконтрастные нефропатии), а также при манипуляциях на сосудах, например при стентировании коронарных артерий (холестериновые эмболии сосудов почек).
Современная активная терапия различных заболеваний не лишена целого ряда нежелательных явлений, предвидеть и предупредить которые возможно (например, острую уратную нефропатию, возникающую в результате синдрома лизиса опухоли при химиотерапии).
Серьезные неотложные ситуации возникают при нарушениях электролитного гомеостаза, что может наблюдаться при самых различных заболеваниях и их лечении.
Специального внимания заслуживают проблемы острой и хронической почечной недостаточности, в том числе так называемой «тихой уремии». Ее клинические признаки в течение длительного периода выражены минимально, и потому «дебютом» становится терминальная стадия уремии, проявляющаяся остро отеком легкого, одышкой, вызванной тяжелой анемией, или … первым в жизни приступом подагрического артрита (выраженная гиперурикемия в рамках терминальной азотемии). Однако названные проблемы, как и возможные осложнения у больных, находящихся на лечении хроническим гемодиализом, детально обсуждаются в специальных изданиях.
Такого же отдельного подробного обсуждения требует и проблема поражения почек в рамках полиорганной недостаточности, в том числе при ДВС-синдроме, детально представленная в соответствующих руководствах. Необходимо подчеркнуть, что неотложное нефрологическое состояние может быть отмечено в практике клинициста любой специальности. Нередко оно сочетается с поражением других органов: например, холестериновая эмболия почечных артерий приводит к одновременному поражению артериальной системы нижних конечностей, а также ветви брюшной аорты. Одной из наиболее четких эпидемиологических тенденций является неуклонное увеличение числа случаев ятрогенной острой почечной недостаточности, в том числе обусловленной неадекватным применением лекарственных препаратов или рентген-контрастных агентов.
Независимо от этиологической и патогенетической природы неотложных нефрологических состояний, во всех случаях обосновано соблюдение некоторых общих принципов ведения, позволяющих предсказать и предупредупредить их развитие:
• строгий мониторинг показателей, характеризующих функцию почек, электролитный гомеостаз, а также изменение мочи;
• контроль и при необходимости коррекция гемодинамических показателей;
• максимально возможное уменьшение числа лекарственных препаратов с отменой тех, которые способны провоцировать дальнейшее ухудшение почечной функции;
• своевременное применение ультрафильтрации и экстренного гемодиализа.
Все пациенты, у которых констатировано неотложное нефрологическое состояние, должны находиться в отделении реанимации и интенсивной терапии, располагающем возможностями заместительной почечной терапии, желательно под постоянным наблюдением нефролога. Обоснован учет подобных пациентов в региональных регистрах хронических болезней почек.
В отличие от этого в нефрологии понятие о неотложных состояниях в настоящее время сформировано менее четко. Нередко в качестве неотложного нефрологического состояния называют только различные варианты острой почечной недостаточности, стратегия ведения которой при этом ограничивается до соответствующей инфузионной терапии и проведения экстренного гемодиализа. Вместе с тем именно в нефрологии рассмотрение проблемы неотложных состояний, по-видимому, должно осуществляться по нозологическому принципу, поскольку особенности заболевания почек часто становятся определяющими при выборе тактики ведения, иногда отличающейся радикально при относительно стереотипных клинических и лабораторных проявлениях.
Основными особенностями неотложных состояний в нефрологии следует считать:
• возможность бурного развития при отсутствии заболевания почек, исходно сохранной функции почек или умеренном почечном поражении (типично для лекарственных и сосудистых нефропатий);
• нередкое отсутствие или малую демонстративность клинических проявлений, затрудняющие раннюю диагностику и выделение достоверных предвестников. При этом ориентация на жалобы практически не может быть использована для распознавания нефрологических неотложных состояний в отличие от того, что наблюдается при других заболеваниях: например, боль за грудиной является основным диагностическим признаком острого коронарного синдрома;
• стереотипность лабораторных изменений (например, рост креатининемии и калиемии как интегральный маркер быстро ухудшающейся почечной функции);
• кроме того, риск необратимого ухудшения почечной функции, как правило, дополняется драматически возрастающей вероятностью сердечно-сосудистых осложнений, что дополнительно ухудшает прогноз.
Как уже было сказано, клинические проявления неотложных нефрологических состояний зачастую мало заметны, в связи с чем решающее значение в их выявлении приобретает анализ динамики лабораторных показателей. Маркерами неотложных состояний в нефрологии можно считать:
• быстрый рост АД: формирование артериальной гипертензии de novo или снижение/утрату эффективности антигипертензивной терапии;
• ускоренно развивающееся поражение органов-мишеней артериальной гипертензии – острую левожелудочковую недостаточность, ухудшение зрения вплоть до слепоты (отек диска зрительного нерва – маркер «озлокачествления» артериальной гипертензии, возможны также эмболии и тромбозы сосудов сетчатки), общемозговую симптоматику (заторможенность, нарушения сознания);
• быстро нарастающие гиперкреатининемию и снижение скорости клубочковой фильтрации (определяемой расчетными методами – с помощью формул Cockroft-Gault или MDRD);
• рост плазменной концентрации калия (одно из наиболее угрожающих жизни проявлений);
• рост или снижение плазменной концентрации натрия;
• снижение плазменной концентрации альбумина (особенно при нефротическом синдроме);
• развитие артериальной гипотензии (прежде всего при нефротическом синдроме, при котором оно указывает на развитие нефротического криза);
• появление неврологической симптоматики (может свидетельствовать как о нарушениях мозгового кровообращения, так и о нарушениях электролитного гомеостаза).
Нефрологические неотложные состояния возникают особенно часто в следующих клинических ситуациях:
• при первом назначении любого лекарственного препарата;
• у пожилых больных;
• при исходной хронической почечной недостаточности (феномен acute on chronic – развитие острого ухудшения функции почек при исходном стойком ее снижении представляет собой одну из наиболее прогностически неблагоприятных ситуаций) и/или хроническом заболевании почек;
• при сахарном диабете II типа;
• при хронической сердечной недостаточности;
• при распространенном атеросклерозе;
• при нестабильных гемодинамических показателях;
• при вмешательстве на сосудах;
• при применении рентген-контрастных агентов.
Опыт любой многопрофильной клиники свидетельствует о реальной возможности возникновения у больного той или другой нефрологической ситуации, в том числе требующей неотложной помощи, включая перевод больного в отделение интенсивного наблюдения. Своевременная расшифровка этих неотложных состояний позволяет во многих случаях не только сохранить жизнь, но и во многом повлиять на долгосрочный прогноз тяжелых больных. Еще более четко реальность подобных ситуаций подтверждает опыт работы нефрологических отделений таких многопрофильных клиник, нозологический профиль которых включает не только «первичные» заболевания почек (различные варианты гломерулонефрита и др.), но и поражение почек при системных заболеваниях (системной красной волчанке, васкулитах, «склеродермической почке», нарушениях внутрисосудистого свертывания с тромбозами, тромбоэмболиями, тромботической микроангиопатией), а также поражение почек у больных с прогрессирующими заболеваниями печени (такими, как тяжелые варианты криоглобулинемического васкулита у больных с хроническим вирусным гепатитом C, гепаторенальным синдромом), гипертоническим кризом, тяжелой хронической сердечной недостаточностью.
«Первичные» поражения почек также могут быть причиной развития неотложной ситуации: тяжелый нефротический синдром с нефротическим кризом, быстропрогрессирующий нефрит с постоянной опасностью различных ургентных состояний, острый тубулоинтерстициальный нефрит различной этиологии, поражение почек при миоглобинурии и гемоглобинурии, а также почечные осложнения проводимого патогенетического лечения (например, при лечении больного нефритом циклоспорином).
В настоящее время хорошо известны остро возникающие нефрологические осложнения при проведении исследований с введением контрастных препаратов (рентгенконтрастные нефропатии), а также при манипуляциях на сосудах, например при стентировании коронарных артерий (холестериновые эмболии сосудов почек).
Современная активная терапия различных заболеваний не лишена целого ряда нежелательных явлений, предвидеть и предупредить которые возможно (например, острую уратную нефропатию, возникающую в результате синдрома лизиса опухоли при химиотерапии).
Серьезные неотложные ситуации возникают при нарушениях электролитного гомеостаза, что может наблюдаться при самых различных заболеваниях и их лечении.
Специального внимания заслуживают проблемы острой и хронической почечной недостаточности, в том числе так называемой «тихой уремии». Ее клинические признаки в течение длительного периода выражены минимально, и потому «дебютом» становится терминальная стадия уремии, проявляющаяся остро отеком легкого, одышкой, вызванной тяжелой анемией, или … первым в жизни приступом подагрического артрита (выраженная гиперурикемия в рамках терминальной азотемии). Однако названные проблемы, как и возможные осложнения у больных, находящихся на лечении хроническим гемодиализом, детально обсуждаются в специальных изданиях.
Такого же отдельного подробного обсуждения требует и проблема поражения почек в рамках полиорганной недостаточности, в том числе при ДВС-синдроме, детально представленная в соответствующих руководствах. Необходимо подчеркнуть, что неотложное нефрологическое состояние может быть отмечено в практике клинициста любой специальности. Нередко оно сочетается с поражением других органов: например, холестериновая эмболия почечных артерий приводит к одновременному поражению артериальной системы нижних конечностей, а также ветви брюшной аорты. Одной из наиболее четких эпидемиологических тенденций является неуклонное увеличение числа случаев ятрогенной острой почечной недостаточности, в том числе обусловленной неадекватным применением лекарственных препаратов или рентген-контрастных агентов.
Независимо от этиологической и патогенетической природы неотложных нефрологических состояний, во всех случаях обосновано соблюдение некоторых общих принципов ведения, позволяющих предсказать и предупредупредить их развитие:
• строгий мониторинг показателей, характеризующих функцию почек, электролитный гомеостаз, а также изменение мочи;
• контроль и при необходимости коррекция гемодинамических показателей;
• максимально возможное уменьшение числа лекарственных препаратов с отменой тех, которые способны провоцировать дальнейшее ухудшение почечной функции;
• своевременное применение ультрафильтрации и экстренного гемодиализа.
Все пациенты, у которых констатировано неотложное нефрологическое состояние, должны находиться в отделении реанимации и интенсивной терапии, располагающем возможностями заместительной почечной терапии, желательно под постоянным наблюдением нефролога. Обоснован учет подобных пациентов в региональных регистрах хронических болезней почек.
Глава 1
Нарушение электролитного гомеостаза
Нарушение электролитного гомеостаза – выраженное и нередко очень быстрое изменение плазменной концентрации натрия и/или калия – может стать фатальным даже тогда, когда другие гомеостатические показатели сохранны, а фильтрационная функция почек остается нормальной или ухудшена лишь умеренно. Расстройство электролитного гомеостаза, как правило, устраняют рациональными терапевтическими мероприятиями, но лишь в том случае, если тщательно учтено влияние предрасполагающих к их возникновению факторов, часто имеющих ятрогенное происхождение (передозировка салуретиков, инфузия гипоосмолярных растворов в чрезмерных количествах, прием блокаторов ренин-ангиотензин-альдостероновой системы).
Нарушение натриевого гомеостаза
Рост или снижение плазменной концентрации натрия – одни из наиболее часто встречающихся форм нарушения электролитного гомеостаза. Следует тем не менее подчеркнуть, что плазменная концентрация натрия далеко не полностью характеризует общее содержание натрия в организме человека, но в целом достаточно адекватно отражает соотношение содержания натрия и воды, а также их распределение между плазмой крови и тканями.
Плазменная концентрация натрия – основной показатель, определяющий величину осмоляльности плазмы крови.
Осмоляльность плазмы крови = 2 (плазменная концентрация натрия) + гликемия/18+азот мочевины/2,8
На практике для расчета осмоляльности плазмы крови используют упрощенную формулу.
Осмоляльность плазмы крови = 2 (плазменная концентрация натрия) + 10 мосмоль
Гипонатриемия
Гипонатриемию констатируют при снижении плазменной концентрации натрия ниже 135 мЭкв/л; при снижении до 130 мЭкв/л она становится особенно опасной.
Патологические последствия гипонатриемии включают:
• артериальную гипотензию со снижением органной перфузии;
• неврологическую симптоматику (подавленность, слабость, ухудшение памяти, сонливость, при выраженной гипонатриемии кому);
• отек головного мозга, нередко фатальный;
• значительное ухудшение общего прогноза, отмечаемое уже при умеренной бессимптомной гипонатриемии (например, у больных хронической сердечной недостаточностью снижение плазменной концентрации натрия сопряжено с увеличением смертности в период госпитализации и на амбулаторном этапе ведения).
Опасность гипонатриемии заключается также и в том, что в процессе чрезмерно быстрой ее коррекции, особенно при инфузии гипертонических растворов пациентам, у которых снижение плазменной концентрации натрия наблюдалось длительно, возможна острая дегидратация головного мозга с появлением в его белом веществе очагов демиелинизации. «Осмотическое» демиелинизирующее повреждение головного мозга, наблюдающееся в процессе инфузионной коррекции гипонатриемии, как правило, проявляется после непродолжительного улучшения состояния и регресса неврологической симптоматики (в том числе нарушений сознания), обусловленных непосредственно снижением концентрации натрия в плазме крови. Клинические признаки демиелинизации белого вещества головного мозга, обусловленной резкой дегидратацией и отмечаемой у лиц с исходной гипонатриемией при ее неадекватной инфузионной коррекции, включают:
• двигательные нарушения, иногда вплоть до тетраплегии и паралича дыхательной мускулатуры;
• нарастающие нарушения сознания;
• псевдобульбарный синдром.
Очаги демиелинизации белого вещества головного мозга могут быть выявлены у таких пациентов с помощью компьютерной или магнитно-резонансной томографии. Вместе с тем клинические проявления демиелинизирующего повреждения головного мозга, возникающего после коррекции гипонатриемии, нередко отмечаются намного раньше, чем его удается выявить с помощью лучевых методов исследования. Большинство подобных больных погибают в течение 3–5 недель.
С позиций клинической практики следует выделять два основных патогенетических варианта гипонатриемии:
• гипонатриемию, характеризующуюся истинным снижением суммарного содержания натрия в организме человека;
• гипонатриемию, возникающую при увеличении количества осмотически свободной воды (гипонатриемия разведения, «отравление водой»).
Выяснение причин гипонатриемии (табл. 1.1) необходимо, прежде всего, потому, что позволяет определить эффективную тактику ведения больных. Многие причины снижения плазменной концентрации натрия могут быть полностью устранены.
Таблица 1.1
Причины снижения плазменной концентрации натрия
 Частота обнаружения гипонатриемии изучена у пациентов различных возрастных групп. Так, при обследовании бегунов – участников марафона в Цюрихе в 2006 году (продолжительность состязания, проводившегося в холодную погоду, – около 5 часов) было выявлено, что у 3 % соревновавшихся произошло бессимптомное снижение плазменной концентрации натрия. Была обнаружена зависимость между динамикой плазменной концентрации натрия, массой тела и суммарным количеством жидкости, употребленной во время марафонского бега.
Частота обнаружения гипонатриемии изучена у пациентов различных возрастных групп. Так, при обследовании бегунов – участников марафона в Цюрихе в 2006 году (продолжительность состязания, проводившегося в холодную погоду, – около 5 часов) было выявлено, что у 3 % соревновавшихся произошло бессимптомное снижение плазменной концентрации натрия. Была обнаружена зависимость между динамикой плазменной концентрации натрия, массой тела и суммарным количеством жидкости, употребленной во время марафонского бега.
Ретроспективный анализ 7965 случаев внебольничной пневмонии у госпитализированных больных продемонстрировал, что у 8,1 % этих больных развилась гипонатриемия (содержание натрия в плазме крови менее 135 мЭкв/л). Больные с гипонатриемией оказались достоверно старше, характеризовались большим числом сопутствующих заболеваний и достоверно чаще оказывались в отделениях интенсивной терапии. При внебольничной пневмонии гипонатриемия обусловливала достоверное увеличение смертности в период госпитализации, продолжительности пребывания в стационаре, частоты возникновения потребности в переводе в отделение интенсивной терапии, искусственной вентиляции легких, а также стоимости стационарного ведения пациентов.
Изучение анамнеза 8142 пациентов, в течение 6 лет (2000–2006 годы) оказывавшихся в отделениях хирургической реанимации, показало, что у 11 % из них снижена плазменная концентрация натрия.
Снижение сывороточной концентрации натрия наблюдается достаточно часто – в первую очередь у пациентов пожилого возраста и/или находящихся в критическом состоянии. Гипонатриемия чаще возникает на амбулаторном этапе ведения пациентов.
В процессе исследований удалось выяснить как причины возникновения гипонатриемии в различных группах пациентов, так и факторы риска ее появления. Амбулаторная гипонатриемия, сопровождающаяся клиническими проявлениями и требующая госпитализации (плазменная концентрация натрия при поступлении – 118,8 ммоль/л), ассоциирована с одновременной гиповолемией (32,6 % случаев), хронической сердечной недостаточностью (26 %), синдромом неадекватной секреции антидиуретического гормона (26 %), приемом тиазидовых диуретиков (26 %) и селективных ингибиторов обратного захвата серотонина (26 %). Более чем у 20 % пациентов удается выделить несколько предрасполагающих факторов. У 71 % пациентов, госпитализированных в связи с клинически очевидной гипонатриемией, снижение плазменной концентрации натрия удавалось выявить уже на амбулаторном этапе. Гипонатриемия, развивающаяся у госпитализированных пациентов, также ассоциирована с приемом тиазидовых диуретиков, препаратов, стимулирующих секрецию антидиуретического гормона, хирургическим вмешательством и внутривенной инфузией гипотонических растворов.
Прием салуретиков, в первую очередь тиазидовых диуретиков, представляет особой одну из основных детерминант гипонатриемии, особенно возникающей амбулаторно и зачастую амбулаторно интерпретируемой. У пожилых больных, которым их назначают для лечения артериальной гипертензии или хронической сердечной недостаточности, тиазидовые диуретики провоцируют снижение плазменной концентрации натрия достаточно часто, но далеко не всегда ее удается своевременно распознать (предложен термин «тихой эпидемии» тиазид-индуцированной гипонатриемии у пожилых). Тиазид-индуцированная гипонатриемия возникает чаще у пожилых людей, особенно с дефицитом массы тела (в том числе синдромом mal-nutrition), нередко одновременно с гипокалиемией. Увеличение возраста на каждые 10 лет сопряжено с ростом риска провоцируемой тиазидами гипонатриемии в 2 раза; повышение массы тела на каждые 5 кг ассоциировано со снижением вероятности гипонатриемии на 27 %. Коррекцию спровоцированной тиазидовыми диуретиками гипонатриемии, проводимую с использованием гипертонических растворов натрия, следует осуществлять осторожно: рост плазменной концентрации натрия на 20 мЭкв/л и более опасен развитием демиелинизации.
Гипонатриемия разведения нередко развивается при декомпенсированном циррозе печени (см. «Гепаторенальный синдром»), а также у больных хронической сердечной недостаточностью, особенно в стадии, близкой к декомпенсации. Снижение сывороточной концентрации натрия у пациентов с хронической сердечной недостаточностью нередко бывает связано с задержкой осмотически свободной воды, но решающим фактором, обусловливающим ее возникновение, почти всегда становится прием салуретиков, особенно тиазидовых диуретиков.
Синдром неадекватной секреции антидиуретического гормона – наиболее демонстративный пример гипонатриемии разведения, развивающейся вследствие снижения клиренса осмотически свободной воды, обусловленного гиперпродукцией вазопрессина и последствиями его взаимодействия с V2-рецепторами. Причины синдрома неадекватной секреции антидиуретического гормона разнообразны и включают прием определенных лекарственных препаратов, стимулирующих секрецию вазопрессина, а также заболевания, при которых развивающаяся гипонатриемия всегда обусловливает дальнейшее ухудшение прогноза (табл. 1.2).
Таблица 1.2
Причины синдрома неадекватной секреции антидиуретического гормона

 Гипонатриемия всегда приводит к значительному ухудшению общего прогноза, независимо от исходной тяжести состояния больных. Снижение плазменной концентрации натрия в период госпитализации сопряжено с достоверным увеличением смертности и частоты перевода в отделение интенсивной терапии. Так, у больных хронической сердечной недостаточностью снижение плазменной концентрации натрия на каждые 3 мкмоль/л сопровождается увеличением риска смерти во время пребывания в стационаре на 19,5 % и риска смерти в течение последующих 3 месяцев на 10 %. Cнижение плазменной концентрации натрия на 1 мкмоль/л ассоциировано с ростом смертности лиц, находящихся в листе ожидания трансплантации печени, на 5 %. Обусловленная гипонатриемией энцефалопатия у пожилых приводит к увеличению риска падений и их последствий, например переломов. Именно этим можно объяснить установленный в эпидемиологических исследованиях более чем 4-кратный рост риска переломов у пожилых пациентов со сниженным сывороточным уровнем натрия. В свою очередь, частота гипонатриемии у пожилых больных с переломами более чем в 4 раза выше, чем у пожилых людей без переломов.
Гипонатриемия всегда приводит к значительному ухудшению общего прогноза, независимо от исходной тяжести состояния больных. Снижение плазменной концентрации натрия в период госпитализации сопряжено с достоверным увеличением смертности и частоты перевода в отделение интенсивной терапии. Так, у больных хронической сердечной недостаточностью снижение плазменной концентрации натрия на каждые 3 мкмоль/л сопровождается увеличением риска смерти во время пребывания в стационаре на 19,5 % и риска смерти в течение последующих 3 месяцев на 10 %. Cнижение плазменной концентрации натрия на 1 мкмоль/л ассоциировано с ростом смертности лиц, находящихся в листе ожидания трансплантации печени, на 5 %. Обусловленная гипонатриемией энцефалопатия у пожилых приводит к увеличению риска падений и их последствий, например переломов. Именно этим можно объяснить установленный в эпидемиологических исследованиях более чем 4-кратный рост риска переломов у пожилых пациентов со сниженным сывороточным уровнем натрия. В свою очередь, частота гипонатриемии у пожилых больных с переломами более чем в 4 раза выше, чем у пожилых людей без переломов.
Неотложные терапевтические мероприятия необходимы в первую очередь при гипонатриемии, сопровождающейся клиническими проявлениями; при бессимптомной гипонатриемии достаточным может оказаться только устранение факторов риска.
Острая гипонатриемия (возникшая в течение менее 48 часов) требует осторожной инфузии изотонических или гипертонических растворов натрия и контроля динамики его плазменной концентрации: во избежание демиелинизирующего поражения белого вещества головного мозга ее прирост должен составлять не более 2 мЭкв/л/час.
При хронической гипонатриемии (возникшей в течение более 48 часов) темп начального прироста плазменной концентрации натрия может достигать 10 мЭкв/л/час. После устранения неврологической симптоматики темп инфузии должен быть уменьшен таким образом, чтобы скорость увеличения плазменной концентрации натрия составляла не более 1,5 мЭкв/л/час.
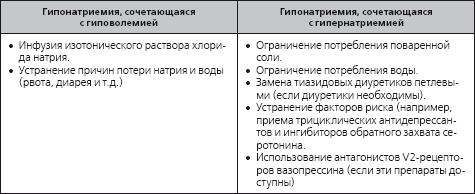
Коррекцию бессимптомной гипонатриемии осуществляют в зависимости от того, сочетается ли она со снижением объема циркулирующей крови или с его увеличением (табл. 1.3). Решающее значение в лечении подобных пациентов имеет устранение выявленных факторов риска. Ближайшие перспективы в терапии гипонатриемии разведения связывают с внедрением в клиническую практику антагонистов V2-рецепторов вазопрессина.
Таблица 1.3
Лечение гипонатриемии, сочетающейся с изменением объема циркулирующей крови
 Гипернатриемия
Гипернатриемия
Гипернатриемию констатируют, если плазменная концентрация натрия превышает 145 мЭкв/л. Как и гипонатриемия, гипернатриемия может обусловливать быстрое развитие фатальных осложнений. Гипернатриемия особенно часто встречается у госпитализированных больных, в первую очередь пожилых; так, ее удается выявить у 26 % пациентов, находящихся в отделениях интенсивной терапии. Смертность пациентов с гипернатриемией оказывается в 2 раза выше, чем смертность тех больных, у кого плазменная концентрация натрия остается в пределах нормы. Гипернатриемию, сочетающуюся с дегидратацией и гиповолемией, обнаруживают у 2,9 % пациентов, госпитализируемых в специализированный геронтологический клинический центр. Распространенность гиповолемической гипернатриемии существенно увеличивается с возрастом, составляя 1,6 % у людей моложе 65 лет и достигая 5,3 % у пациентов старше 85 лет. Среди пацентов многопрофильной терапевтической клиники не менее 1,2 % больных относятся к группе риска развития гипернатриемии.
Гипернатриемия опасна развитием дегидратации головного мозга и одновременных расстройств церебральной микроциркуляции, в том числе нарастающего клеточного сладжа, формирования микротромбов и кровоизлияний. С прогностической точки зрения, гипернатриемия всегда приводит к значительному увеличению риска смерти, в том числе в период пребывания пациента в стационаре. Установлено, что по мере увеличения гипернатриемии у пожилых пациентов в период госпитализации достоверно возрастает смертность: от 33,3 % в группе больных с концентрацией натрия в плазме от 151 до 153 мЭкв/л до 71,4 % при концентрации натрия >154 мЭкв/л. У больных, госпитализируемых в неврологические отделения интенсивной терапии, гипернатриемия сопряжена с более выраженными нарушениями сознания, оцениваемыми по шкале комы Glasgow большей частотой возникновения потребности в искусственной вентиляции легких (80,5 % против 41,5 в группе без гипернатриемии, p<0,001), большей частотой развития почечной недостаточности (10,3 % против 0,9 %, p<0,001) и значительно более высокой смертностью (30,1 % против 10,2 %, p<0,001).
Повышение плазменной концентрации натрия удается зарегистрировать у 7,9 % пациентов, требующих пребывания в отделении интенсивной терапии неврологического профиля, при этом гипернатриемия у них нередко бывает спровоцирована резким снижением объема циркулирующей крови, связанным с применением маннитола (у получавших этот осмотический диуретик частота гипернатриемии достигает 24,3 %). Ятрогенная гипернатриемия, по-видимому, наиболее опасна прогностичеcки. Так, ориентируясь на данные, полученные при обследовании пациентов многопрофильного терапевтического стационара, смертность больных с гипернатриемией, возникшей в период госпитализации, достоверно превосходит таковую у тех, у кого повышение плазменной концентрации натрия возникло на амбулаторном этапе (47,6 и 28 %, соответственно, р=0,03).
Нарушение натриевого гомеостаза
Рост или снижение плазменной концентрации натрия – одни из наиболее часто встречающихся форм нарушения электролитного гомеостаза. Следует тем не менее подчеркнуть, что плазменная концентрация натрия далеко не полностью характеризует общее содержание натрия в организме человека, но в целом достаточно адекватно отражает соотношение содержания натрия и воды, а также их распределение между плазмой крови и тканями.
Плазменная концентрация натрия – основной показатель, определяющий величину осмоляльности плазмы крови.
Осмоляльность плазмы крови = 2 (плазменная концентрация натрия) + гликемия/18+азот мочевины/2,8
На практике для расчета осмоляльности плазмы крови используют упрощенную формулу.
Осмоляльность плазмы крови = 2 (плазменная концентрация натрия) + 10 мосмоль
Гипонатриемия
Гипонатриемию констатируют при снижении плазменной концентрации натрия ниже 135 мЭкв/л; при снижении до 130 мЭкв/л она становится особенно опасной.
Патологические последствия гипонатриемии включают:
• артериальную гипотензию со снижением органной перфузии;
• неврологическую симптоматику (подавленность, слабость, ухудшение памяти, сонливость, при выраженной гипонатриемии кому);
• отек головного мозга, нередко фатальный;
• значительное ухудшение общего прогноза, отмечаемое уже при умеренной бессимптомной гипонатриемии (например, у больных хронической сердечной недостаточностью снижение плазменной концентрации натрия сопряжено с увеличением смертности в период госпитализации и на амбулаторном этапе ведения).
Опасность гипонатриемии заключается также и в том, что в процессе чрезмерно быстрой ее коррекции, особенно при инфузии гипертонических растворов пациентам, у которых снижение плазменной концентрации натрия наблюдалось длительно, возможна острая дегидратация головного мозга с появлением в его белом веществе очагов демиелинизации. «Осмотическое» демиелинизирующее повреждение головного мозга, наблюдающееся в процессе инфузионной коррекции гипонатриемии, как правило, проявляется после непродолжительного улучшения состояния и регресса неврологической симптоматики (в том числе нарушений сознания), обусловленных непосредственно снижением концентрации натрия в плазме крови. Клинические признаки демиелинизации белого вещества головного мозга, обусловленной резкой дегидратацией и отмечаемой у лиц с исходной гипонатриемией при ее неадекватной инфузионной коррекции, включают:
• двигательные нарушения, иногда вплоть до тетраплегии и паралича дыхательной мускулатуры;
• нарастающие нарушения сознания;
• псевдобульбарный синдром.
Очаги демиелинизации белого вещества головного мозга могут быть выявлены у таких пациентов с помощью компьютерной или магнитно-резонансной томографии. Вместе с тем клинические проявления демиелинизирующего повреждения головного мозга, возникающего после коррекции гипонатриемии, нередко отмечаются намного раньше, чем его удается выявить с помощью лучевых методов исследования. Большинство подобных больных погибают в течение 3–5 недель.
С позиций клинической практики следует выделять два основных патогенетических варианта гипонатриемии:
• гипонатриемию, характеризующуюся истинным снижением суммарного содержания натрия в организме человека;
• гипонатриемию, возникающую при увеличении количества осмотически свободной воды (гипонатриемия разведения, «отравление водой»).
Выяснение причин гипонатриемии (табл. 1.1) необходимо, прежде всего, потому, что позволяет определить эффективную тактику ведения больных. Многие причины снижения плазменной концентрации натрия могут быть полностью устранены.
Таблица 1.1
Причины снижения плазменной концентрации натрия

Ретроспективный анализ 7965 случаев внебольничной пневмонии у госпитализированных больных продемонстрировал, что у 8,1 % этих больных развилась гипонатриемия (содержание натрия в плазме крови менее 135 мЭкв/л). Больные с гипонатриемией оказались достоверно старше, характеризовались большим числом сопутствующих заболеваний и достоверно чаще оказывались в отделениях интенсивной терапии. При внебольничной пневмонии гипонатриемия обусловливала достоверное увеличение смертности в период госпитализации, продолжительности пребывания в стационаре, частоты возникновения потребности в переводе в отделение интенсивной терапии, искусственной вентиляции легких, а также стоимости стационарного ведения пациентов.
Изучение анамнеза 8142 пациентов, в течение 6 лет (2000–2006 годы) оказывавшихся в отделениях хирургической реанимации, показало, что у 11 % из них снижена плазменная концентрация натрия.
Снижение сывороточной концентрации натрия наблюдается достаточно часто – в первую очередь у пациентов пожилого возраста и/или находящихся в критическом состоянии. Гипонатриемия чаще возникает на амбулаторном этапе ведения пациентов.
В процессе исследований удалось выяснить как причины возникновения гипонатриемии в различных группах пациентов, так и факторы риска ее появления. Амбулаторная гипонатриемия, сопровождающаяся клиническими проявлениями и требующая госпитализации (плазменная концентрация натрия при поступлении – 118,8 ммоль/л), ассоциирована с одновременной гиповолемией (32,6 % случаев), хронической сердечной недостаточностью (26 %), синдромом неадекватной секреции антидиуретического гормона (26 %), приемом тиазидовых диуретиков (26 %) и селективных ингибиторов обратного захвата серотонина (26 %). Более чем у 20 % пациентов удается выделить несколько предрасполагающих факторов. У 71 % пациентов, госпитализированных в связи с клинически очевидной гипонатриемией, снижение плазменной концентрации натрия удавалось выявить уже на амбулаторном этапе. Гипонатриемия, развивающаяся у госпитализированных пациентов, также ассоциирована с приемом тиазидовых диуретиков, препаратов, стимулирующих секрецию антидиуретического гормона, хирургическим вмешательством и внутривенной инфузией гипотонических растворов.
Прием салуретиков, в первую очередь тиазидовых диуретиков, представляет особой одну из основных детерминант гипонатриемии, особенно возникающей амбулаторно и зачастую амбулаторно интерпретируемой. У пожилых больных, которым их назначают для лечения артериальной гипертензии или хронической сердечной недостаточности, тиазидовые диуретики провоцируют снижение плазменной концентрации натрия достаточно часто, но далеко не всегда ее удается своевременно распознать (предложен термин «тихой эпидемии» тиазид-индуцированной гипонатриемии у пожилых). Тиазид-индуцированная гипонатриемия возникает чаще у пожилых людей, особенно с дефицитом массы тела (в том числе синдромом mal-nutrition), нередко одновременно с гипокалиемией. Увеличение возраста на каждые 10 лет сопряжено с ростом риска провоцируемой тиазидами гипонатриемии в 2 раза; повышение массы тела на каждые 5 кг ассоциировано со снижением вероятности гипонатриемии на 27 %. Коррекцию спровоцированной тиазидовыми диуретиками гипонатриемии, проводимую с использованием гипертонических растворов натрия, следует осуществлять осторожно: рост плазменной концентрации натрия на 20 мЭкв/л и более опасен развитием демиелинизации.
Гипонатриемия разведения нередко развивается при декомпенсированном циррозе печени (см. «Гепаторенальный синдром»), а также у больных хронической сердечной недостаточностью, особенно в стадии, близкой к декомпенсации. Снижение сывороточной концентрации натрия у пациентов с хронической сердечной недостаточностью нередко бывает связано с задержкой осмотически свободной воды, но решающим фактором, обусловливающим ее возникновение, почти всегда становится прием салуретиков, особенно тиазидовых диуретиков.
Синдром неадекватной секреции антидиуретического гормона – наиболее демонстративный пример гипонатриемии разведения, развивающейся вследствие снижения клиренса осмотически свободной воды, обусловленного гиперпродукцией вазопрессина и последствиями его взаимодействия с V2-рецепторами. Причины синдрома неадекватной секреции антидиуретического гормона разнообразны и включают прием определенных лекарственных препаратов, стимулирующих секрецию вазопрессина, а также заболевания, при которых развивающаяся гипонатриемия всегда обусловливает дальнейшее ухудшение прогноза (табл. 1.2).
Таблица 1.2
Причины синдрома неадекватной секреции антидиуретического гормона


Неотложные терапевтические мероприятия необходимы в первую очередь при гипонатриемии, сопровождающейся клиническими проявлениями; при бессимптомной гипонатриемии достаточным может оказаться только устранение факторов риска.
Острая гипонатриемия (возникшая в течение менее 48 часов) требует осторожной инфузии изотонических или гипертонических растворов натрия и контроля динамики его плазменной концентрации: во избежание демиелинизирующего поражения белого вещества головного мозга ее прирост должен составлять не более 2 мЭкв/л/час.
При хронической гипонатриемии (возникшей в течение более 48 часов) темп начального прироста плазменной концентрации натрия может достигать 10 мЭкв/л/час. После устранения неврологической симптоматики темп инфузии должен быть уменьшен таким образом, чтобы скорость увеличения плазменной концентрации натрия составляла не более 1,5 мЭкв/л/час.
Коррекцию бессимптомной гипонатриемии осуществляют в зависимости от того, сочетается ли она со снижением объема циркулирующей крови или с его увеличением (табл. 1.3). Решающее значение в лечении подобных пациентов имеет устранение выявленных факторов риска. Ближайшие перспективы в терапии гипонатриемии разведения связывают с внедрением в клиническую практику антагонистов V2-рецепторов вазопрессина.
Таблица 1.3
Лечение гипонатриемии, сочетающейся с изменением объема циркулирующей крови

Гипернатриемию констатируют, если плазменная концентрация натрия превышает 145 мЭкв/л. Как и гипонатриемия, гипернатриемия может обусловливать быстрое развитие фатальных осложнений. Гипернатриемия особенно часто встречается у госпитализированных больных, в первую очередь пожилых; так, ее удается выявить у 26 % пациентов, находящихся в отделениях интенсивной терапии. Смертность пациентов с гипернатриемией оказывается в 2 раза выше, чем смертность тех больных, у кого плазменная концентрация натрия остается в пределах нормы. Гипернатриемию, сочетающуюся с дегидратацией и гиповолемией, обнаруживают у 2,9 % пациентов, госпитализируемых в специализированный геронтологический клинический центр. Распространенность гиповолемической гипернатриемии существенно увеличивается с возрастом, составляя 1,6 % у людей моложе 65 лет и достигая 5,3 % у пациентов старше 85 лет. Среди пацентов многопрофильной терапевтической клиники не менее 1,2 % больных относятся к группе риска развития гипернатриемии.
Гипернатриемия опасна развитием дегидратации головного мозга и одновременных расстройств церебральной микроциркуляции, в том числе нарастающего клеточного сладжа, формирования микротромбов и кровоизлияний. С прогностической точки зрения, гипернатриемия всегда приводит к значительному увеличению риска смерти, в том числе в период пребывания пациента в стационаре. Установлено, что по мере увеличения гипернатриемии у пожилых пациентов в период госпитализации достоверно возрастает смертность: от 33,3 % в группе больных с концентрацией натрия в плазме от 151 до 153 мЭкв/л до 71,4 % при концентрации натрия >154 мЭкв/л. У больных, госпитализируемых в неврологические отделения интенсивной терапии, гипернатриемия сопряжена с более выраженными нарушениями сознания, оцениваемыми по шкале комы Glasgow большей частотой возникновения потребности в искусственной вентиляции легких (80,5 % против 41,5 в группе без гипернатриемии, p<0,001), большей частотой развития почечной недостаточности (10,3 % против 0,9 %, p<0,001) и значительно более высокой смертностью (30,1 % против 10,2 %, p<0,001).
Повышение плазменной концентрации натрия удается зарегистрировать у 7,9 % пациентов, требующих пребывания в отделении интенсивной терапии неврологического профиля, при этом гипернатриемия у них нередко бывает спровоцирована резким снижением объема циркулирующей крови, связанным с применением маннитола (у получавших этот осмотический диуретик частота гипернатриемии достигает 24,3 %). Ятрогенная гипернатриемия, по-видимому, наиболее опасна прогностичеcки. Так, ориентируясь на данные, полученные при обследовании пациентов многопрофильного терапевтического стационара, смертность больных с гипернатриемией, возникшей в период госпитализации, достоверно превосходит таковую у тех, у кого повышение плазменной концентрации натрия возникло на амбулаторном этапе (47,6 и 28 %, соответственно, р=0,03).
