Функции. Переводит глюкозу в гликоген и усиливает транспорт глюкозы из крови в клетки. Гликоген – углевод, в форме которого у животных хранится запас углеводов, т. е. основного источника энергии, которая расходуется для жизнедеятельности клеток, в том числе мышечных и нервных. В случае необходимости гликоген способен распадаться до глюкозы. В мышечных клетках энергия может получаться непосредственно из гликогена (см. раздел «Обмен углеводов»). Переводя глюкозу в гликоген и транспортируя глюкозу в клетки, инсулин уменьшает содержание глюкозы в крови. Это вызывает чувство голода. Быстрое повышение инсулина в крови может вызывать ухудшение функций ЦНС из-за снижения содержания в крови глюкозы, являющейся единственным источником энергии для клеток ЦНС. Ухудшение функций ЦНС может проявляться в плохом самочувствии, общей слабости, потере сознания и смерти.
Регуляция. Гуморальная регуляция многообразна. Стимулируют секрецию инсулина в первую очередь высокий уровень глюкозы в крови, а также АКТГ и глюкокортикоиды (см. ниже); тормозят – адреналин и норадреналин. Парасимпатическая нервная система стимулирует, а симпатическая тормозит секрецию инсулина.
Функции и регуляция глюкагона в целом противоположны функциям и регуляции инсулина. Глюкагон увеличивает содержание глюкозы в крови, ускоряя распад гликогена до глюкозы и замедляя транспорт глюкозы в клетки. Уровень глюкозы является основным фактором, влияющим на синтез и секрецию глюкагона. Высокое содержание глюкозы в крови тормозит синтез и секрецию глюкагона, а низкое их стимулирует.
Функции. Активация обмена веществ. Недостаточность щитовидной железы приводит к торможению психических функций, утомляемости, замедлению работы сердца, утрате эластичности кожи, облысению. Помимо организующего влияния гормоны щитовидной железы благодаря своему стимулирующему эффекту на общий обмен веществ в организме[44] влияют на психику и поведение вторично.
Регуляция. Тиреотропин (ТТГ) стимулирует синтез и секрецию гормонов щитовидной железы. Стимулирующие нервные влияния на щитовидную железу осуществляются симпатической нервной системой.
В отличие от почти всех прочих гормонов, упоминаемых в этой книге, секреция тироксина и трийодтиронина очень мало меняется при изменениях во внешней и внутренней среде (если йод поступает в организм в достаточном количестве). Подобно парасимпатическому отделу автономной нервной системы, гормоны щитовидной железы осуществляют тоническое влияние на функции, поддерживая их на определенном уровне.
Адреналин и норадреналин синтезируются в мозговом слое надпочечников. Они являются производными аминокислоты тирозина.
Функции адреналина. Он увеличивает частоту сердечных сокращений, систолический выброс (объем крови, выталкиваемой желудочком при одном сокращении), повышает возбудимость и проводимость сердечной мышцы, расширяет бронхиолы, тормозит пищеварительные функции, как секреторную, так и двигательную, расширяет зрачок, расслабляет мышцы мочевого пузыря. Не имеет психотропного действия. Вторично усиливает чувство тревоги (см. раздел «Психотропные эффекты стрессорных гормонов»).
Регуляция. Только нервная – веточками чревного нерва, который является частью симпатической нервной системы. Мозговой слой надпочечника представляет собой видоизмененный симпатический ганглий.
В регуляции этих двух гормонов отмечаются некоторые различия. Секреция адреналина выше в ситуациях, связанных с неуверенностью, ожиданием неприятностей, боли, страха или с состоянием тревоги, т. е. при формировании мотивации, когда программа действия еще не выработана. Секреция норадреналина выше в ситуациях, сопровождающихся агрессией, гневом, яростью, т. е. при эмоциональном, физическом и умственном напряжении, необходимом для реализации выработанной программы действия – программы «борьбы». Соответственно, несколько различаются и биологические эффекты двух гормонов.
Стероидные гормоны
Мелатонин
Принципы гормональной регуляции
Передача гормонального сигнала: синтез, секреция, транспорт гормонов, их действие на клетки-мишени и инактивация
Регуляция. Гуморальная регуляция многообразна. Стимулируют секрецию инсулина в первую очередь высокий уровень глюкозы в крови, а также АКТГ и глюкокортикоиды (см. ниже); тормозят – адреналин и норадреналин. Парасимпатическая нервная система стимулирует, а симпатическая тормозит секрецию инсулина.
В поджелудочной железе синтезируются инсулин и глюкагонГлюкагон синтезируется в А-клетках островков Лангерганса поджелудочной железы.
Функции и регуляция глюкагона в целом противоположны функциям и регуляции инсулина. Глюкагон увеличивает содержание глюкозы в крови, ускоряя распад гликогена до глюкозы и замедляя транспорт глюкозы в клетки. Уровень глюкозы является основным фактором, влияющим на синтез и секрецию глюкагона. Высокое содержание глюкозы в крови тормозит синтез и секрецию глюкагона, а низкое их стимулирует.
В щитовидной железе синтезируются тироксин и трийодтиронинТироксин и трийодтиронин синтезируются в фолликулах щитовидной железы, лежащей на передней поверхности шеи.
Функции. Активация обмена веществ. Недостаточность щитовидной железы приводит к торможению психических функций, утомляемости, замедлению работы сердца, утрате эластичности кожи, облысению. Помимо организующего влияния гормоны щитовидной железы благодаря своему стимулирующему эффекту на общий обмен веществ в организме[44] влияют на психику и поведение вторично.
Регуляция. Тиреотропин (ТТГ) стимулирует синтез и секрецию гормонов щитовидной железы. Стимулирующие нервные влияния на щитовидную железу осуществляются симпатической нервной системой.
В отличие от почти всех прочих гормонов, упоминаемых в этой книге, секреция тироксина и трийодтиронина очень мало меняется при изменениях во внешней и внутренней среде (если йод поступает в организм в достаточном количестве). Подобно парасимпатическому отделу автономной нервной системы, гормоны щитовидной железы осуществляют тоническое влияние на функции, поддерживая их на определенном уровне.
Секреция гормонов щитовидной железы мало меняется при изменениях во внешней или внутренней среде. В норме гормоны щитовидной железы осуществляют только тоническое влияние на функции организмаСекреция всех других гормонов меняется в соответствии с возникающими потребностями, так же как это происходит с активностью симпатического отдела автономной нервной системы.
Адреналин и норадреналин синтезируются в мозговом слое надпочечников. Они являются производными аминокислоты тирозина.
Функции адреналина. Он увеличивает частоту сердечных сокращений, систолический выброс (объем крови, выталкиваемой желудочком при одном сокращении), повышает возбудимость и проводимость сердечной мышцы, расширяет бронхиолы, тормозит пищеварительные функции, как секреторную, так и двигательную, расширяет зрачок, расслабляет мышцы мочевого пузыря. Не имеет психотропного действия. Вторично усиливает чувство тревоги (см. раздел «Психотропные эффекты стрессорных гормонов»).
В мозговом слое надпочечников синтезируются адреналин и норадреналинФункции норадреналина те же, что и у адреналина, за исключением влияния на пищеварительный тракт, мышцы зрачка, углеводный обмен и потребление кислорода тканями. Увеличивает работоспособность утомленных мышц, выделяясь из окончаний симпатических нервов. Не обладает психотропным эффектом. Основной источник норадреналина в крови – не мозговой слой надпочечников, а окончания симпатических нервов в мышцах.
Регуляция. Только нервная – веточками чревного нерва, который является частью симпатической нервной системы. Мозговой слой надпочечника представляет собой видоизмененный симпатический ганглий.
В регуляции этих двух гормонов отмечаются некоторые различия. Секреция адреналина выше в ситуациях, связанных с неуверенностью, ожиданием неприятностей, боли, страха или с состоянием тревоги, т. е. при формировании мотивации, когда программа действия еще не выработана. Секреция норадреналина выше в ситуациях, сопровождающихся агрессией, гневом, яростью, т. е. при эмоциональном, физическом и умственном напряжении, необходимом для реализации выработанной программы действия – программы «борьбы». Соответственно, несколько различаются и биологические эффекты двух гормонов.
Стероидные гормоны
Все вышеперечисленные гормоны относятся к пептидам. Периферические гормоны, продуцируемые корой надпочечников и половыми железами, относятся к химическому классу стероидов.
Стероиды отличаются от пептидов не только химически, но и физиологически. Во-первых, увеличение концентрации пептидных гормонов в крови можно зарегистрировать через несколько секунд после стимулирующего воздействия. Рост концентрации стероидов в крови отмечается только через несколько минут после стимуляции. Во-вторых, время полужизни пептидов в крови составляет от одной до двух минут, а стероидов – десятки минут. Это связано с тем, что распад пептидов происходит с помощью ферментов крови, а метаболизм стероидов протекает главным образом в печени. Большая химическая стабильность стероидов позволяет определять их содержание не только в крови, но и в слюне, моче и экскрементах, что очень удобно для полевых исследований физиологии диких животных. В-третьих, пептиды неэффективны при введении в рот, так как разрушаются пищеварительными ферментами, а стероиды, поступая в организм с пищей, всасываются в кровь в желудочно-кишечном тракте. Наконец, и это самое важное, стероиды свободно проникают в ЦНС, а пептидные гормоны – с трудом. Это связано с наличием гемато-энцефалического барьера, обеспечивающего постоянство химической среды ЦНС. Некоторые гормоны (например, адреналин) совершенно не проникают в ЦНС из крови, а для других (например, окситоцина) существуют специальные системы транспортных белков, которые работают с ограниченной скоростью.
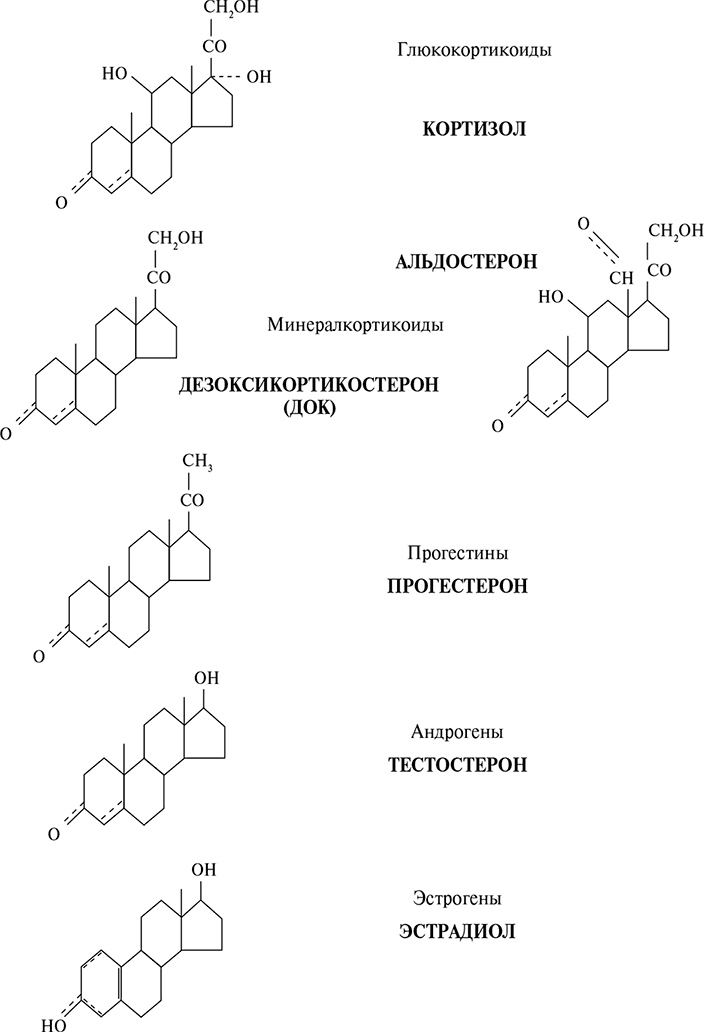 Рис. 2.4. Пять семейств стероидов. На основании строения молекул все стероиды разделены на пять семейств, биологические свойства которых тоже различны. Приведены химические формулы представителей пяти семейств стероидных гормонов. Следует обратить внимание на большое сходство строения гормонов, сильно различающихся по своему биологическому эффекту
Рис. 2.4. Пять семейств стероидов. На основании строения молекул все стероиды разделены на пять семейств, биологические свойства которых тоже различны. Приведены химические формулы представителей пяти семейств стероидных гормонов. Следует обратить внимание на большое сходство строения гормонов, сильно различающихся по своему биологическому эффекту
Стероиды синтезируются из общего предшественника – холестерина – и делятся на пять семейств: глюкокортикоиды, минералокортикоиды, прогестины, андрогены (мужские половые гормоны) и эстрогены (женские половые гормоны) (рис. 2.4 и 2.5). Несмотря на общий план строения стероидов, почти каждое семейство является функциональным антагонистом остальных. Например, прогестины препятствуют проявлению эффектов всех остальных четырех групп стероидов.
 Рис. 2.5. Схема биосинтеза стероидов. Заглавными буквами выделены основные представители семейств. Следует обратить внимание на метаболическую близость стероидов с различным биологическим действием, т. е. на потенциальную легкость превращения одного стероида в другой. Эта метаболическая близость имеет практическое следствие: при стрессе увеличивается секреция не только глюкокортикоидов, но и других стероидов. У разных индивидуумов при стрессе увеличивается секреция стероидов разных семейств
Рис. 2.5. Схема биосинтеза стероидов. Заглавными буквами выделены основные представители семейств. Следует обратить внимание на метаболическую близость стероидов с различным биологическим действием, т. е. на потенциальную легкость превращения одного стероида в другой. Эта метаболическая близость имеет практическое следствие: при стрессе увеличивается секреция не только глюкокортикоидов, но и других стероидов. У разных индивидуумов при стрессе увеличивается секреция стероидов разных семейств
Стероидные гормоны синтезируются в двух железах: корковом слое надпочечников и гонадах (половых железах). В коре надпочечников синтезируются главным образом минералокортикоиды и глюкокортикоиды. Поэтому эти два семейства вместе называют кортикостероидами. Прогестины, андрогены и эстрогены в основном синтезируются в гонадах.
В коре надпочечников отсутствуют нервные окончания, соответственно, синтез гормонов в этом органе регулируется только гуморальным путем. Кора надпочечников делится на три слоя, в каждом из них синтезируется особый тип стероидных гормонов.
В клубочковой зоне синтезируются минералокортикоиды – альдостерон (основной у человека) и дезоксикортикостерон (с меньшим влиянием на солевой обмен, но с психотропной активностью).
Функции: как следует из названия, регуляция водно-солевого обмена (задерживают в организме натрий и увеличивают выделение калия); усиление воспалительных процессов.
Регуляция: основной регулятор содержание калия и натрия в крови. Стимуляция синтеза при снижении концентрации натрия в диете. Кроме того, в регуляции секреции минералокортикоидов участвуют и другие гуморальные агенты: факторы, синтезируемые в печени (ренин-ангиотензиновая система, которая активируется при стрессе), вазопрессин, окситоцин. Торможение минералокортикоидной активности коры надпочечников осуществляется эндорфинами.
В пучковой зоне синтезируются глюкокортикоиды, главными из которых у человека является кортизол, а у крыс и мышей – основных лабораторных животных – кортикостерон.
Регуляция: АКТГ – основной стимулятор. Кроме того, синтез кортизола увеличивается вазопрессином и факторами, секретируемыми в мозговом слое надпочечников. Гуморальные факторы, тормозящие синтез и секрецию кортизола, неизвестны.
Уровень глюкокортикоидов в крови – самый распространенный показатель стресса.
Адаптивное значение глюкокортикоидов было показано Гансом Селье в 1930-е гг. (см. главу 4). Уже в годы Второй мировой войны экстракты коры надпочечников использовались в немецкой армии в качестве стимуляторов (например, летчиками перед пикированием). Материал – бычьи надпочечники – вывозили подводными лодками из Аргентины.
В сетчатой зоне коры надпочечников синтезируются мужские и женские половые гормоны. Половые стероиды делятся на три группы, которые удобнее рассмотреть отдельно – для мужского и женского организма.
На тестостерон приходится 90 % общей продукции андрогенов. Основное место синтеза – мужские гонады (половые железы). Под влиянием тестостерона идет созревание сперматозоидов, формируются вторичные половые признаки, проявляется половое поведение. Тестостерон усиливает обмен веществ, в частности синтез белка, в первую очередь в нервной и мышечной ткани. Тестостерон играет ключевую роль в процессе формирования организма – на эмбриональном этапе, в детстве и во время полового созревания. Секреция тестостерона усиливается под действием ЛГ.
В женском организме прогестерон является основным гормоном, который вырабатывается во время беременности, в частности он расслабляет мускулатуру матки. Прогестерон усиливает основной обмен веществ и повышает температуру тела. Основной психотропный эффект прогестерона (точнее, его метаболитов) – противотревожное действие.
Эстрадиол, помимо влияния на женскую репродуктивную систему, воздействует на обмен веществ, в частности на рост костной ткани, усиливает задержку азота в организме, участвуя в водно-солевом обмене, обладает противовоспалительной активностью и стабилизирует работу сердечно-сосудистой системы. Психотропные эффекты эстрадиола у женщин обусловлены в первую очередь его организующим влиянием на созревающий мозг женского организма (см. главу 8). Основной регулятор, стимулирующий секрецию эстрадиола, – лютеинизирующий гормон.
Тестостерон обеспечивает у женщин половое влечение, стимулирует рост волос на лобке и в подмышечных впадинах, а также увеличение мышечной массы.
Стероиды отличаются от пептидов не только химически, но и физиологически. Во-первых, увеличение концентрации пептидных гормонов в крови можно зарегистрировать через несколько секунд после стимулирующего воздействия. Рост концентрации стероидов в крови отмечается только через несколько минут после стимуляции. Во-вторых, время полужизни пептидов в крови составляет от одной до двух минут, а стероидов – десятки минут. Это связано с тем, что распад пептидов происходит с помощью ферментов крови, а метаболизм стероидов протекает главным образом в печени. Большая химическая стабильность стероидов позволяет определять их содержание не только в крови, но и в слюне, моче и экскрементах, что очень удобно для полевых исследований физиологии диких животных. В-третьих, пептиды неэффективны при введении в рот, так как разрушаются пищеварительными ферментами, а стероиды, поступая в организм с пищей, всасываются в кровь в желудочно-кишечном тракте. Наконец, и это самое важное, стероиды свободно проникают в ЦНС, а пептидные гормоны – с трудом. Это связано с наличием гемато-энцефалического барьера, обеспечивающего постоянство химической среды ЦНС. Некоторые гормоны (например, адреналин) совершенно не проникают в ЦНС из крови, а для других (например, окситоцина) существуют специальные системы транспортных белков, которые работают с ограниченной скоростью.

Стероиды синтезируются из общего предшественника – холестерина – и делятся на пять семейств: глюкокортикоиды, минералокортикоиды, прогестины, андрогены (мужские половые гормоны) и эстрогены (женские половые гормоны) (рис. 2.4 и 2.5). Несмотря на общий план строения стероидов, почти каждое семейство является функциональным антагонистом остальных. Например, прогестины препятствуют проявлению эффектов всех остальных четырех групп стероидов.

Стероидные гормоны синтезируются в двух железах: корковом слое надпочечников и гонадах (половых железах). В коре надпочечников синтезируются главным образом минералокортикоиды и глюкокортикоиды. Поэтому эти два семейства вместе называют кортикостероидами. Прогестины, андрогены и эстрогены в основном синтезируются в гонадах.
В коре надпочечников отсутствуют нервные окончания, соответственно, синтез гормонов в этом органе регулируется только гуморальным путем. Кора надпочечников делится на три слоя, в каждом из них синтезируется особый тип стероидных гормонов.
В клубочковой зоне синтезируются минералокортикоиды – альдостерон (основной у человека) и дезоксикортикостерон (с меньшим влиянием на солевой обмен, но с психотропной активностью).
Функции: как следует из названия, регуляция водно-солевого обмена (задерживают в организме натрий и увеличивают выделение калия); усиление воспалительных процессов.
Регуляция: основной регулятор содержание калия и натрия в крови. Стимуляция синтеза при снижении концентрации натрия в диете. Кроме того, в регуляции секреции минералокортикоидов участвуют и другие гуморальные агенты: факторы, синтезируемые в печени (ренин-ангиотензиновая система, которая активируется при стрессе), вазопрессин, окситоцин. Торможение минералокортикоидной активности коры надпочечников осуществляется эндорфинами.
В пучковой зоне синтезируются глюкокортикоиды, главными из которых у человека является кортизол, а у крыс и мышей – основных лабораторных животных – кортикостерон.
В коре надпочечников синтезируются минералокортикоиды и глюкокортикоиды. Синтезируются и все другие стероидыФункции: обмен углеводов; противовоспалительное и противоаллергическое действие; множественные влияния на эффекты других гормонов, в первую очередь гормонов гипоталамо-гипофизарной системы. Кортизол – функциональный антагонист прогестерона.
Регуляция: АКТГ – основной стимулятор. Кроме того, синтез кортизола увеличивается вазопрессином и факторами, секретируемыми в мозговом слое надпочечников. Гуморальные факторы, тормозящие синтез и секрецию кортизола, неизвестны.
Уровень глюкокортикоидов в крови – самый распространенный показатель стресса.
Адаптивное значение глюкокортикоидов было показано Гансом Селье в 1930-е гг. (см. главу 4). Уже в годы Второй мировой войны экстракты коры надпочечников использовались в немецкой армии в качестве стимуляторов (например, летчиками перед пикированием). Материал – бычьи надпочечники – вывозили подводными лодками из Аргентины.
В сетчатой зоне коры надпочечников синтезируются мужские и женские половые гормоны. Половые стероиды делятся на три группы, которые удобнее рассмотреть отдельно – для мужского и женского организма.
В мужских гонадах синтезируются андрогены, в женских – эстрогены и прогестиныВ мужском организме прогестерон, который относится к прогестинам, синтезируется только в надпочечниках; его функции и регуляция его синтеза изучены плохо. Известен только лишь противотревожный эффект прогестерона. Секреция эстрадиола, основного женского полового гормона, тоже происходит только в надпочечниках. Помимо влияния на обмен веществ, эстрадиол, возможно, участвует в организации родительского поведения.
На тестостерон приходится 90 % общей продукции андрогенов. Основное место синтеза – мужские гонады (половые железы). Под влиянием тестостерона идет созревание сперматозоидов, формируются вторичные половые признаки, проявляется половое поведение. Тестостерон усиливает обмен веществ, в частности синтез белка, в первую очередь в нервной и мышечной ткани. Тестостерон играет ключевую роль в процессе формирования организма – на эмбриональном этапе, в детстве и во время полового созревания. Секреция тестостерона усиливается под действием ЛГ.
В женском организме прогестерон является основным гормоном, который вырабатывается во время беременности, в частности он расслабляет мускулатуру матки. Прогестерон усиливает основной обмен веществ и повышает температуру тела. Основной психотропный эффект прогестерона (точнее, его метаболитов) – противотревожное действие.
Эстрадиол, помимо влияния на женскую репродуктивную систему, воздействует на обмен веществ, в частности на рост костной ткани, усиливает задержку азота в организме, участвуя в водно-солевом обмене, обладает противовоспалительной активностью и стабилизирует работу сердечно-сосудистой системы. Психотропные эффекты эстрадиола у женщин обусловлены в первую очередь его организующим влиянием на созревающий мозг женского организма (см. главу 8). Основной регулятор, стимулирующий секрецию эстрадиола, – лютеинизирующий гормон.
Тестостерон обеспечивает у женщин половое влечение, стимулирует рост волос на лобке и в подмышечных впадинах, а также увеличение мышечной массы.
Мелатонин
Мелатонин[45] синтезируется в эпифизе – маленькой железе, примыкающей к эпиталамусу. В XVII в. Рене Декарт считал эпифиз «седалищем души». Гормоны эпифиза, главным из которых является мелатонин, секретируются как в системный кровоток, так и в спинномозговую жидкость, поскольку эпифиз находится в полости третьего желудочка.
Особенностью регуляции функций эпифиза является прямая связь с гипоталамическими ядрами, непосредственно соединенными с сетчаткой. Таким образом, эпифиз получает от глаза сигналы об изменении освещенности. Секреция эпифизарных гормонов усиливается в темноте. Кроме нервных влияний, секреторная функция эпифиза находится под контролем многообразных гуморальных факторов, содержащихся в спинномозговой жидкости.
Подробнее о мелатонине в связи с его ролью в формировании депрессии будет сказано в главе 5.
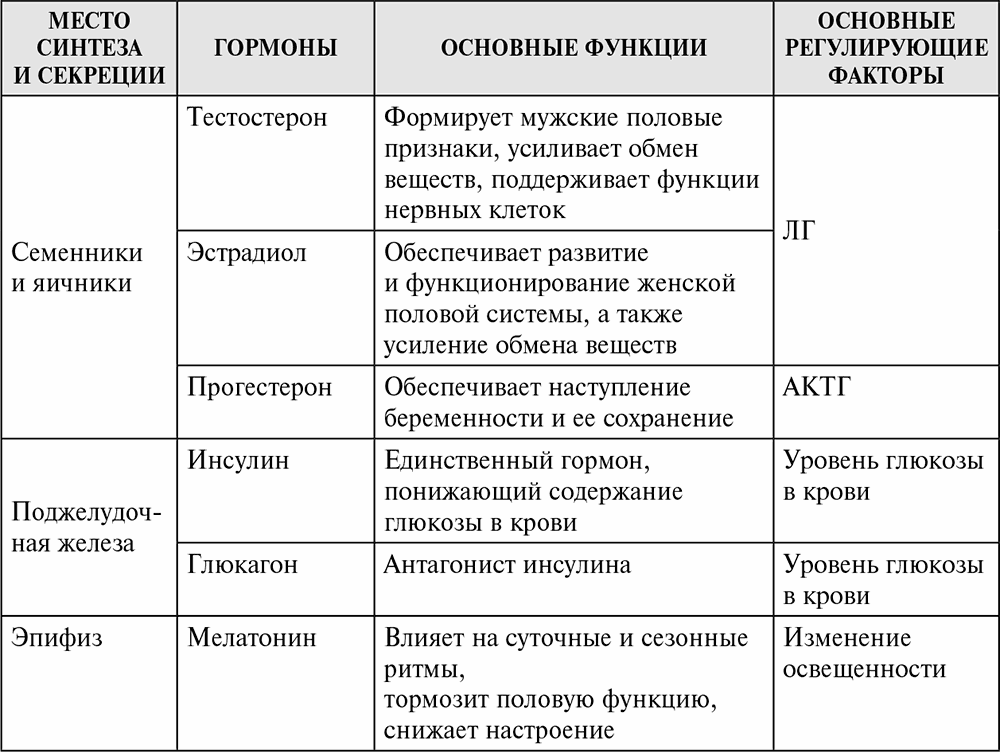
Сведения об основных периферических гормонах суммированы в табл. 2.2.
Таблица 2.2. Основные периферические гормоны

В эпифизе синтезируется мелатонинМелатонин – это производное аминокислоты триптофана. Основная функция мелатонина – обеспечение ритмических процессов в организме, связанных с циклическим изменением освещенности на протяжении суток и в течение года. Помимо организации биологических ритмов мелатонин при повышенной секреции тормозит синтез гонадолиберина и, как следствие, половую функцию и вызывает депрессивно-подобные состояния.
Особенностью регуляции функций эпифиза является прямая связь с гипоталамическими ядрами, непосредственно соединенными с сетчаткой. Таким образом, эпифиз получает от глаза сигналы об изменении освещенности. Секреция эпифизарных гормонов усиливается в темноте. Кроме нервных влияний, секреторная функция эпифиза находится под контролем многообразных гуморальных факторов, содержащихся в спинномозговой жидкости.
Подробнее о мелатонине в связи с его ролью в формировании депрессии будет сказано в главе 5.
Сведения об основных периферических гормонах суммированы в табл. 2.2.
Таблица 2.2. Основные периферические гормоны


Принципы гормональной регуляции
В предыдущем разделе было показано, что гормоны относятся к различным химическим классам соединений, в основном к пептидам и стероидам. Гормоны синтезируются в различных железах. Механизмы регуляции и, естественно, функции разных гормонов также различны. Тем не менее действие всех гуморальных факторов, в том числе и гормонов, имеет определенные общие черты. Рассмотрению этих общих принципов и посвящен данный раздел.
Передача гормонального сигнала: синтез, секреция, транспорт гормонов, их действие на клетки-мишени и инактивация
В определении понятия «гормон» было указано несколько этапов распространения гормонального сигнала (рис. 2.6).
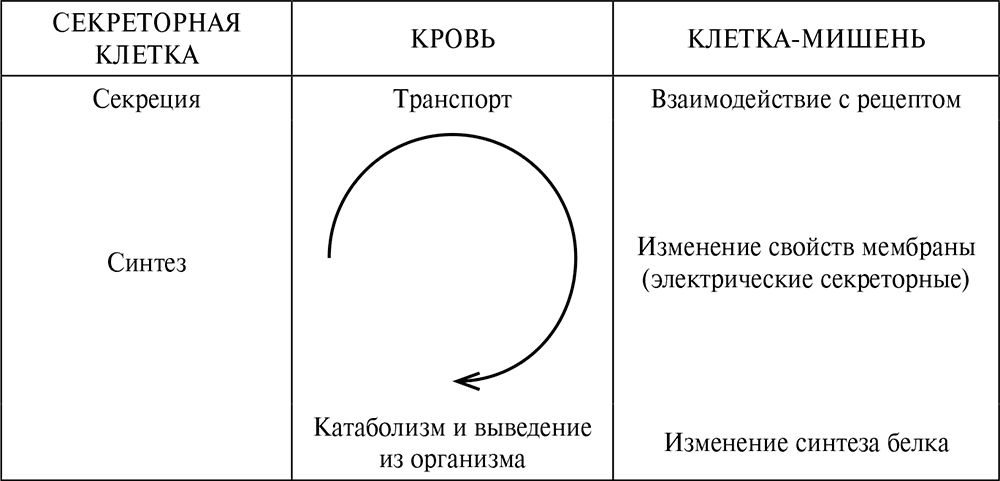 Рис. 2.6. Этапы распространения гормонального сигнала. Внутри клетки происходит синтез гормона. Секреция – не пассивное выделение вещества в окружающее пространство, а активный процесс, на который могут влиять факторы, не изменяющие интенсивность синтеза. В крови гормоны связываются с белками-носителями. В связанной форме гормоны неактивны. Таким образом, их биологический эффект зависит и от содержания в крови транспортных белков. Для реализации биологического эффекта гормон должен связаться с клеточным рецептором – сложной структурой, расположенной внутри клеточной мембраны или внутри клетки, в ее цитозоле. После связывания молекулы гормона с рецептором следует целый каскад химических реакций, которые приводят к изменению активности клетки. Это проявляется в изменении синтеза белка в клетке, а также в изменении свойств ее мембраны, которые происходят при передаче нервного импульса, сокращении мышечных клеток и секреции из них различных веществ. Освободившись из комплекса с рецептором, молекула гормона инактивируется в крови (пептиды) или в печени (стероиды). К изменению гормонального эффекта приводят изменения не только синтеза молекул гормона в эндокринной железе, но и на любом этапе передачи гормонального сигнала
Рис. 2.6. Этапы распространения гормонального сигнала. Внутри клетки происходит синтез гормона. Секреция – не пассивное выделение вещества в окружающее пространство, а активный процесс, на который могут влиять факторы, не изменяющие интенсивность синтеза. В крови гормоны связываются с белками-носителями. В связанной форме гормоны неактивны. Таким образом, их биологический эффект зависит и от содержания в крови транспортных белков. Для реализации биологического эффекта гормон должен связаться с клеточным рецептором – сложной структурой, расположенной внутри клеточной мембраны или внутри клетки, в ее цитозоле. После связывания молекулы гормона с рецептором следует целый каскад химических реакций, которые приводят к изменению активности клетки. Это проявляется в изменении синтеза белка в клетке, а также в изменении свойств ее мембраны, которые происходят при передаче нервного импульса, сокращении мышечных клеток и секреции из них различных веществ. Освободившись из комплекса с рецептором, молекула гормона инактивируется в крови (пептиды) или в печени (стероиды). К изменению гормонального эффекта приводят изменения не только синтеза молекул гормона в эндокринной железе, но и на любом этапе передачи гормонального сигнала
Следует различать этапы синтеза и секреции как два независимых процесса. В этой книге выражения «изменение (увеличение, снижение) секреции» и «изменение синтеза» обычно употребляются как синонимы, но это сделано только для облегчения восприятия. В действительности секреция не является пассивным процессом выделения из клетки вещества вследствие его накопления. Это многостадийный процесс, на который влияют как внутри-, так и внеклеточные регуляторы. Зачастую эти два процесса – синтез и секреция – оказываются несогласованными, и при увеличении синтеза не происходит увеличения секреции. Таким образом, некое воздействие, о котором известно, что оно приводит к увеличению синтеза гормона, не обязательно ведет к увеличению содержания этого гормона в крови.
Гормон, поступивший в кровь, переносится к тканям-мишеням в разных формах. Определенная доля молекул находится в том виде, в котором они были секретированы, но бόльшая часть связывается с белками крови. Некоторые из этих белков связывают многие гормоны (альбумин), а другие обладают высокой специфичностью по отношению к определенным гормонам, т. е. связывают только один или строго ограниченный круг гормонов. (Так, кортикостероид-связывающий глобулин связывает глюкокортикоиды, минералокортикоиды и прогестины, но не связывает эстрогены; белок, который связывает пролактин и гормон роста, не присоединяет другие пептидные гормоны.) Связывание гормонов белками крови имеет три функции.
Первая функция – регуляторная. Связанный гормон не взаимодействует с тканями-мишенями, т. е. та часть молекул секретированного гормона, которая связалась с белком, биологически не активна.
Вторая – запасающая — функция связывания гормонов с белками крови определяется тем, что в крови имеется постоянный запас гормона, который может быть легко переведен в активное состояние. При снижении концентрации свободного гормона часть связанного высвобождается из комплекса с белком.
Третья функция связывания молекул гормона белками крови – транспортная. В некоторых случаях гормон, связанный с транспортным белком, быстрее проникает в клетку-мишень.
После синтеза, секреции и транспорта начинается взаимодействие гормона с клеткой-мишенью. Оно обеспечивается клеточными рецепторами. Они представляют собой сложные белки и расположены в клеточной мембране (рецепторы пептидных гормонов), в цитоплазме клетки (рецепторы стероидных гормонов) и в клеточном ядре (рецепторы трийодтиронина и тироксина).
Основная характеристика рецепторов – их специфичность. Благодаря этому свойству рецепторов гормоны, распространяясь по всему организму, действуют не на все ткани и органы, а только на те, клетки которых содержат рецепторы данного гормона. Рецепторы обладают гораздо более высокой специфичностью, чем транспортные белки крови. Почти все рецепторы связывают только один определенный гормон, причем в гораздо большей степени, чем его ближайшие химические аналоги. В то же время большинство гормонов связываются с несколькими подтипами рецепторов, и специфичность этих подтипов различна. Таким образом достигается тонкое регулирование функций клетки-мишени.
Связывание гормона с рецептором вызывает цепь сложных биохимических реакций, конечным итогом которых является изменение синтеза определенных белков, что и принято считать биологическим эффектом данного гормона. Поскольку гормональный эффект проявляется только в результате взаимодействия с рецептором, некоторые исследователи полагают, что ключевая молекула в системе гуморальной регуляции – рецептор, а не гормон. Не останавливаясь здесь на критике этой концепции (неполное соответствие гормонального эффекта и количества рецептора в ткани и т. п.), отметим, что мы будем рассматривать именно гормоны как основное звено в системах гуморальной регуляции по следующим причинам.
Во-первых, методически определить гормоны гораздо легче, чем рецепторы. Финансовые затраты на приобретение реактивов для определения гормонов значительно меньше, чем на покупку реактивов для установления содержания рецепторов. Самые сложные из гормонов представляют собой цепочку из нескольких десятков аминокислот. В то же время рецепторы – это сложные белки, которые могут состоять из десятков тысяч аминокислот, обладают сложной структурой и легко разрушаются при биохимических манипуляциях. Концентрация гормонов в тканях организма значительно выше концентрации рецепторов в тех же тканях. Часто для определения содержания гормона достаточно одной сотой миллилитра крови, а для анализа рецепторов требуется порой несколько граммов ткани. Гормоны находятся в крови, часть которой можно взять для анализа почти безболезненно и без существенных последствий для живого организма. Рецепторы находятся в тканях, что требует более серьезного вторжения в организм. В некоторых случаях вовсе невозможно определить содержание рецепторов у живого организма, например в структурах головного мозга человека.
Во-вторых, мы не можем в процессе эксперимента менять содержание рецепторов в тканях, тогда как изменить уровень гормона удается легко и с незначительными финансовыми затратами. Довольно просто ввести дополнительное количество гормона, сделав инъекцию, а уменьшить его количество можно введением вещества, блокирующего синтез или секрецию гормона, а также удалив отдельную железу (в эксперименте на животном). Молекулярно-генетические методы, позволяющие изменить количество рецепторов в тканях, появились только в последние годы. Они остаются еще очень дорогими и громоздкими, а кроме того, имеют существенные методические ограничения.
Таким образом, экспериментальных данных о содержании гормонов в крови при разных состояниях организма в тысячи раз больше, чем о содержании рецепторов в тканях. Что же касается работ, выполненных на человеке, то количество исследований рецепторов в миллионы раз меньше, чем количество исследований уровня гормонов. Таким образом, в этой книге основное внимание уделено изменению уровня гормона в крови, а не активности рецепторного аппарата клетки.
Итак, первые четыре этапа передачи гормонального сигнала – это синтез, секреция, транспорт белками крови и связывание с рецепторным аппаратом в клетках тканей. Заключительным, пятым, этапом передачи гуморального сигнала является инактивация гормона и вывод его из организма. Нарушение метаболизма гормона может привести к изменениям в работе всей эндокринной системы. При замедленной инактивации однократное введение гормона способно вызвать длительный или же неожиданно сильный эффект. В норме время полужизни пептидных гормонов составляет несколько минут, а стероидных – несколько часов. Многие синтетические производные гормонов значительно эффективнее природных аналогов именно потому, что они медленно подвергаются инактивации в процессе обмена веществ.

Следует различать этапы синтеза и секреции как два независимых процесса. В этой книге выражения «изменение (увеличение, снижение) секреции» и «изменение синтеза» обычно употребляются как синонимы, но это сделано только для облегчения восприятия. В действительности секреция не является пассивным процессом выделения из клетки вещества вследствие его накопления. Это многостадийный процесс, на который влияют как внутри-, так и внеклеточные регуляторы. Зачастую эти два процесса – синтез и секреция – оказываются несогласованными, и при увеличении синтеза не происходит увеличения секреции. Таким образом, некое воздействие, о котором известно, что оно приводит к увеличению синтеза гормона, не обязательно ведет к увеличению содержания этого гормона в крови.
Гормон, поступивший в кровь, переносится к тканям-мишеням в разных формах. Определенная доля молекул находится в том виде, в котором они были секретированы, но бόльшая часть связывается с белками крови. Некоторые из этих белков связывают многие гормоны (альбумин), а другие обладают высокой специфичностью по отношению к определенным гормонам, т. е. связывают только один или строго ограниченный круг гормонов. (Так, кортикостероид-связывающий глобулин связывает глюкокортикоиды, минералокортикоиды и прогестины, но не связывает эстрогены; белок, который связывает пролактин и гормон роста, не присоединяет другие пептидные гормоны.) Связывание гормонов белками крови имеет три функции.
Первая функция – регуляторная. Связанный гормон не взаимодействует с тканями-мишенями, т. е. та часть молекул секретированного гормона, которая связалась с белком, биологически не активна.
Реализация гормонального сигнала происходит в пять этапов: 1) синтез гормона 2) секреция гормона 3) транспорт гормона 4) взаимодействие гормона с клеточным рецептором 5) инактивация гормона и вывод его из организмаВ результате эффективная концентрация гормона всегда меньше, чем его общая концентрация в крови. Чем выше в ней содержание белка, связывающего молекулы гормона, тем меньше эффективная концентрация гормона, т. е. возможный биологический эффект. Следовательно, биологическая активность гормона регулируется содержанием в крови белков, которые связывают этот гормон. Например, при беременности возрастает количество белка, связывающего кортизол. При возникновении потребности тканей в гормоне увеличиваются расщепление гормон-белкового комплекса и эффективная концентрация, а содержание биологически активного гормона в крови возрастает. Таким образом, регулирующая функция белков, связывающих гормоны, тесно связана со второй функцией – запасающей.
Вторая – запасающая — функция связывания гормонов с белками крови определяется тем, что в крови имеется постоянный запас гормона, который может быть легко переведен в активное состояние. При снижении концентрации свободного гормона часть связанного высвобождается из комплекса с белком.
Третья функция связывания молекул гормона белками крови – транспортная. В некоторых случаях гормон, связанный с транспортным белком, быстрее проникает в клетку-мишень.
После синтеза, секреции и транспорта начинается взаимодействие гормона с клеткой-мишенью. Оно обеспечивается клеточными рецепторами. Они представляют собой сложные белки и расположены в клеточной мембране (рецепторы пептидных гормонов), в цитоплазме клетки (рецепторы стероидных гормонов) и в клеточном ядре (рецепторы трийодтиронина и тироксина).
Основная характеристика рецепторов – их специфичность. Благодаря этому свойству рецепторов гормоны, распространяясь по всему организму, действуют не на все ткани и органы, а только на те, клетки которых содержат рецепторы данного гормона. Рецепторы обладают гораздо более высокой специфичностью, чем транспортные белки крови. Почти все рецепторы связывают только один определенный гормон, причем в гораздо большей степени, чем его ближайшие химические аналоги. В то же время большинство гормонов связываются с несколькими подтипами рецепторов, и специфичность этих подтипов различна. Таким образом достигается тонкое регулирование функций клетки-мишени.
Связывание гормона с рецептором вызывает цепь сложных биохимических реакций, конечным итогом которых является изменение синтеза определенных белков, что и принято считать биологическим эффектом данного гормона. Поскольку гормональный эффект проявляется только в результате взаимодействия с рецептором, некоторые исследователи полагают, что ключевая молекула в системе гуморальной регуляции – рецептор, а не гормон. Не останавливаясь здесь на критике этой концепции (неполное соответствие гормонального эффекта и количества рецептора в ткани и т. п.), отметим, что мы будем рассматривать именно гормоны как основное звено в системах гуморальной регуляции по следующим причинам.
Во-первых, методически определить гормоны гораздо легче, чем рецепторы. Финансовые затраты на приобретение реактивов для определения гормонов значительно меньше, чем на покупку реактивов для установления содержания рецепторов. Самые сложные из гормонов представляют собой цепочку из нескольких десятков аминокислот. В то же время рецепторы – это сложные белки, которые могут состоять из десятков тысяч аминокислот, обладают сложной структурой и легко разрушаются при биохимических манипуляциях. Концентрация гормонов в тканях организма значительно выше концентрации рецепторов в тех же тканях. Часто для определения содержания гормона достаточно одной сотой миллилитра крови, а для анализа рецепторов требуется порой несколько граммов ткани. Гормоны находятся в крови, часть которой можно взять для анализа почти безболезненно и без существенных последствий для живого организма. Рецепторы находятся в тканях, что требует более серьезного вторжения в организм. В некоторых случаях вовсе невозможно определить содержание рецепторов у живого организма, например в структурах головного мозга человека.
Во-вторых, мы не можем в процессе эксперимента менять содержание рецепторов в тканях, тогда как изменить уровень гормона удается легко и с незначительными финансовыми затратами. Довольно просто ввести дополнительное количество гормона, сделав инъекцию, а уменьшить его количество можно введением вещества, блокирующего синтез или секрецию гормона, а также удалив отдельную железу (в эксперименте на животном). Молекулярно-генетические методы, позволяющие изменить количество рецепторов в тканях, появились только в последние годы. Они остаются еще очень дорогими и громоздкими, а кроме того, имеют существенные методические ограничения.
Таким образом, экспериментальных данных о содержании гормонов в крови при разных состояниях организма в тысячи раз больше, чем о содержании рецепторов в тканях. Что же касается работ, выполненных на человеке, то количество исследований рецепторов в миллионы раз меньше, чем количество исследований уровня гормонов. Таким образом, в этой книге основное внимание уделено изменению уровня гормона в крови, а не активности рецепторного аппарата клетки.
Итак, первые четыре этапа передачи гормонального сигнала – это синтез, секреция, транспорт белками крови и связывание с рецепторным аппаратом в клетках тканей. Заключительным, пятым, этапом передачи гуморального сигнала является инактивация гормона и вывод его из организма. Нарушение метаболизма гормона может привести к изменениям в работе всей эндокринной системы. При замедленной инактивации однократное введение гормона способно вызвать длительный или же неожиданно сильный эффект. В норме время полужизни пептидных гормонов составляет несколько минут, а стероидных – несколько часов. Многие синтетические производные гормонов значительно эффективнее природных аналогов именно потому, что они медленно подвергаются инактивации в процессе обмена веществ.
