Клинические проявления. Характерен отягощенный аллергоанамнез, эпизоды одышки, свистящих хрипов, кашля, в том числе в ночное время. Обострения провоцируются контактом с аллергенами, инфекциями, физической нагрузкой и прочим, после применения бронходилататоров происходит исчезновение симптомов. В течении приступа выделяют следующие периоды.
1. Период предвестников. Характерны заложенность носа или отделяемое из него, чихание, кашель, зуд и першение в горле, конъюнктивит, полиморфная сыпь, изменения поведения и настроения, нарушения аппетита и сна, симптомы ОРВИ.
2. Приступный период. Характеризуется рядом симптомов.
Симптомы удушья — дыхательный дискомфорт, субъективные ощущения нехватки воздуха, сжатия грудной клетки, возникающие внезапно.
Синдром дыхательной недостаточности — одышка экспираторная с участием вспомогательной мускулатуры, раздувание крыльев носа, набухание шейных вен, сухой приступообразный или малопродуктивный влажный кашель с трудно отходящей вязкой мокротой, дистанционные хрипы, ортопноэ, бледность кожи, периоральный и акроцианоз.
Бронхолегочный синдром — коробочный перкуторный звук, нижние границы легких опущены, подвижность легочных краев ограничена, дыхание с удлиненным выдохом или ослабленное, сухие свистящие хрипы, разнокалиберные влажные хрипы (особенно у детей раннего возраста) по всем легочным полям.
Изменения со стороны сердечно-сосудистой системы — тахикардия, пульс слабого наполнения, повышение артериального давления, тоны сердца приглушены, уменьшение относительной сердечной тупости вследствие эмфиземы.
3. Послеприступный период проявляется продуктивным кашлем, исчезновением одышки.
Диагностика. Основана на анамнестических данных, характерной клинической картине и результатах дополнительных методов обследования, которые включают:
1) оценку функции внешнего дыхания (ФВД). Выявляется обструктивный тип нарушений вентиляции легких;
2) функциональные тесты: положительный ответ на ингаляцию бета-агониста (прирост основных показателей ФВД > 20 %); проба с физической нагрузкой (снижение показателей проходимости бронхов через 3–5 мин после стандартной физической нагрузки > 20 %);
3) пикфлоуметрию — отмечается суточный разброс пиковой скорости выдоха, измеряемый в течение 2–3 недель > 20 %;
4) рентгенографическое исследование легких в период обострения — обнаруживается вздутие легких (повышение прозрачности по периферии легочных полей, низкое стояние куполов диафрагмы, расширение межреберных промежутков), усиление корневого рисунка;
5) исследование крови и мокроты — характерна эозинофилия крови и мокроты;
6) отмечается увеличение общего и специфических IgE в крови и биологических жидкостях;
7) положительные кожные пробы со специфическими аллергенами;
8) пробное лечение — высокая эффективность бета-агонистов.
Классификация. В 1997 г. утверждена национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика», согласно которой отменено разделение астмы на аллергическую, инфекционно-аллергическую и смешанную формы. С практической точки зрения на первый план выдвигается классификация бронхиальной астмы по степени тяжести, что определяет современную стратегию ее терапии. Выделяют легкое, среднетяжелое и тяжелое течение заболевания.
Степень тяжести определяется по следующим показателям:
1) количество ночных приступов в неделю;
2) количество дневных симптомов в день и неделю;
3) кратность применения (потребность) бета-2-агонистов короткого действия;
4) выраженность нарушений физической активности и сна;
5) значение пиковой скорости выдоха (ПСВ) и ее процентное соотношение с должным или наилучшим значением;
6) суточные колебания ПСВ.
При диссоциации отдельных показателей тяжести (редкие, но тяжелые приступы) бронхиальную астму следует характеризовать по более тяжелому признаку.
Таблица 1. Критерии тяжести бронхиальной астмы у детей
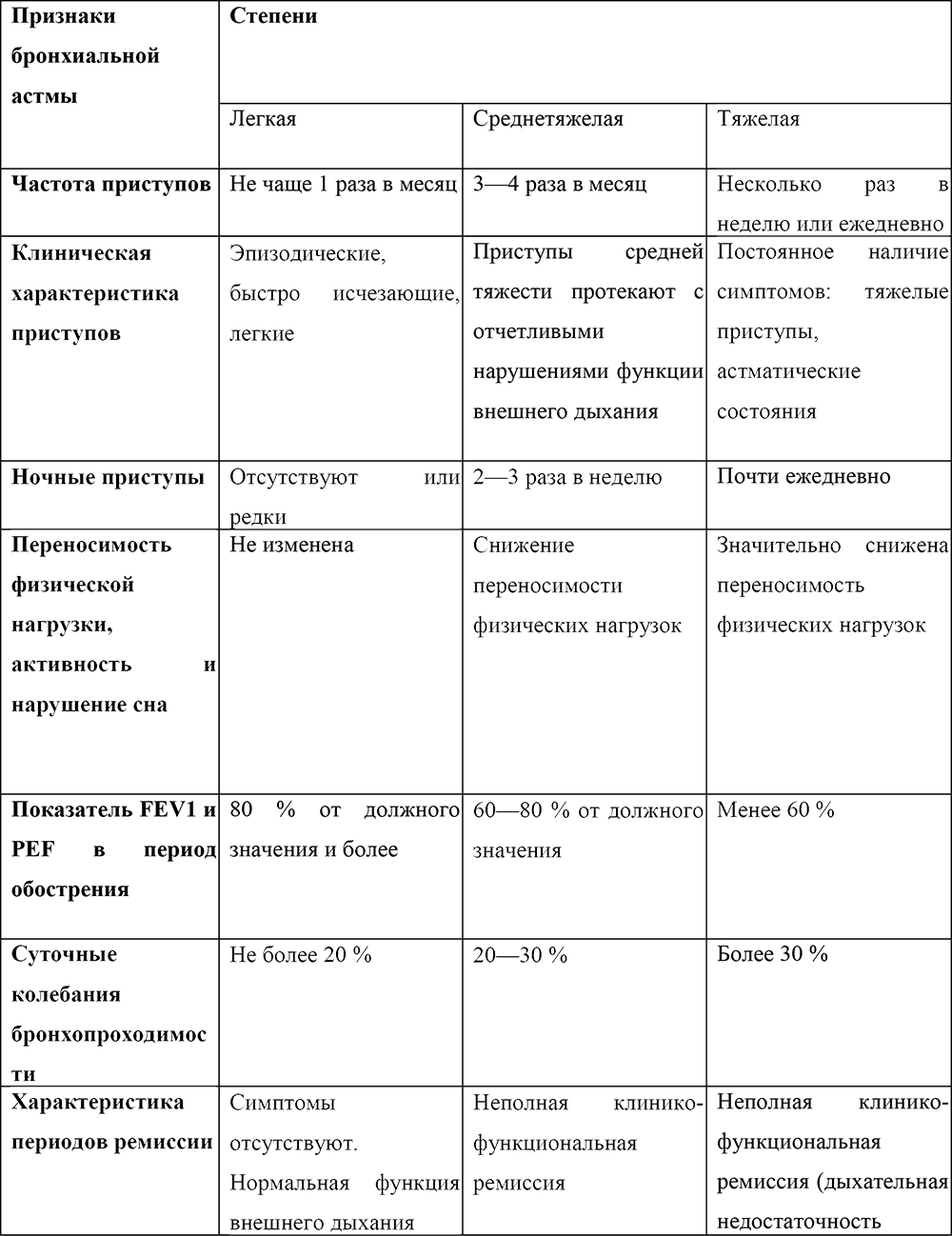
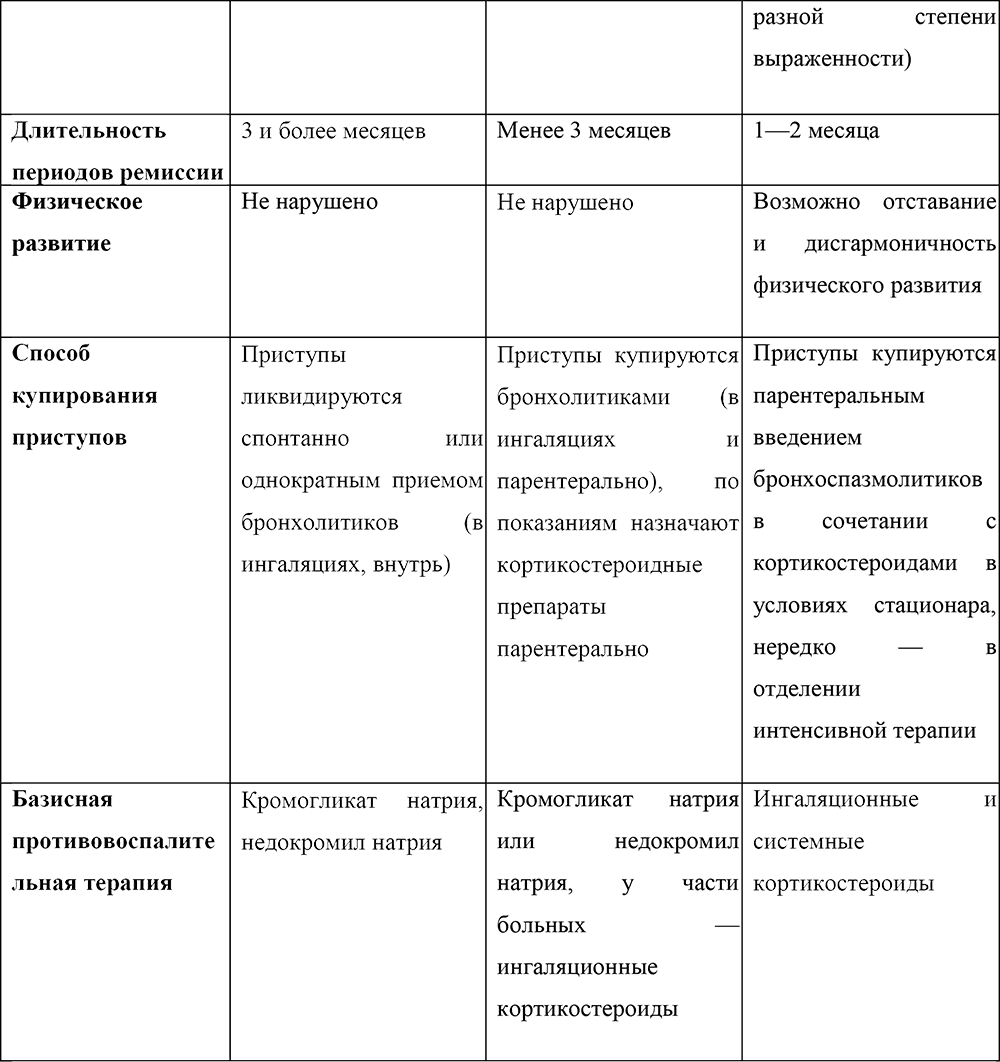
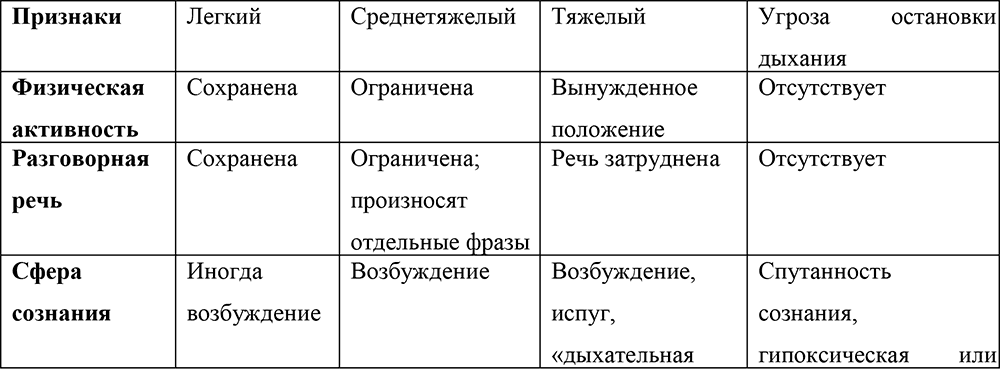
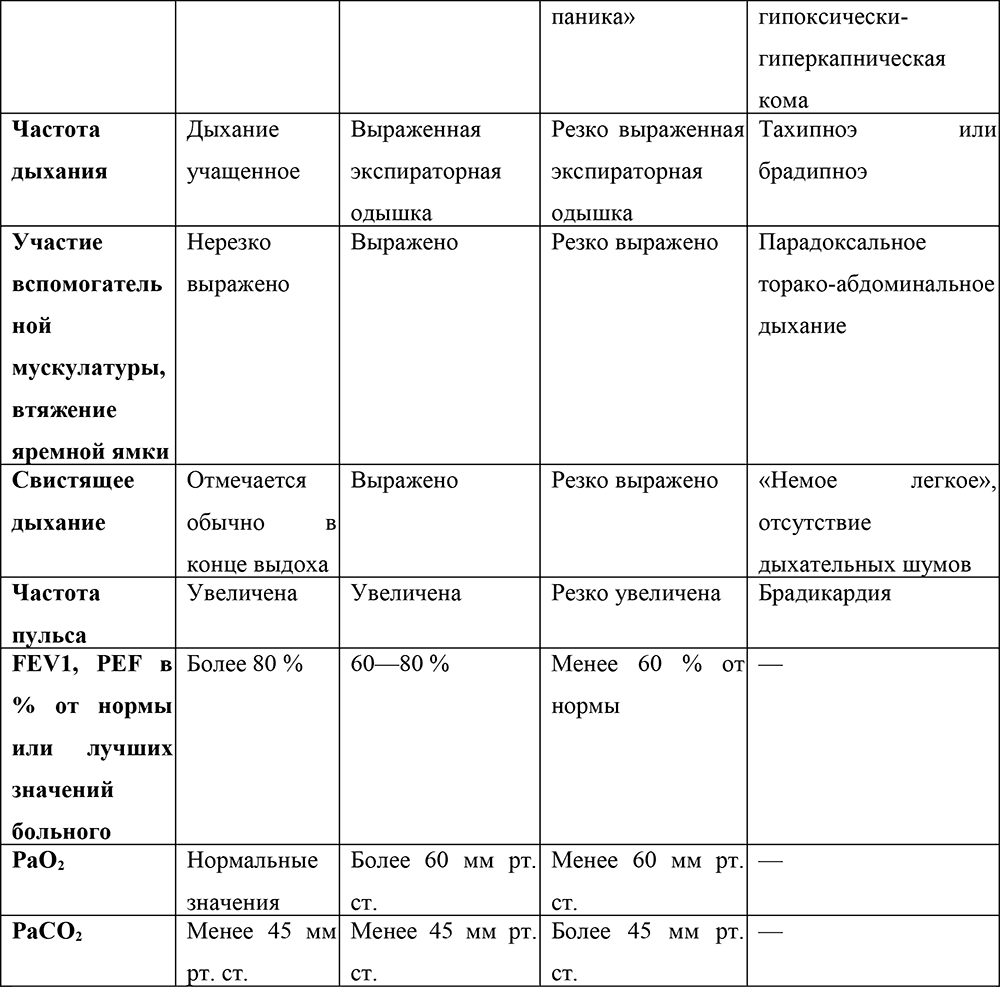
Таблица 2. Критерии оценки тяжести приступа бронхиальной астмы у детей
Астматический статус (АС) — тяжелый затяжной приступ с прогрессирующей дыхательной недостаточностью, резистентный к обычной терапии бронходилататорами, вследствие функционального блока бета-адренергических рецепторов бронхов.
Факторы, приводящие к развитию астматического статуса:
1) массивное воздействие аллергенов, бронхиальная или инфекция ЛОР-органов;
2) передозировка ингаляционных бета-2-агонистов;
3) неоправданная или быстрая отмена глюкокортикостероидного препарата у больных гормонзависимой астмой.
Критерии астматического статуса:
1) длительность некупирующегося приступа бронхиальной астмы не менее 6 ч;
2) нарушение дренажной функции бронхов;
3) гипоксемия и гиперкапния;
4) резистентность к симпатомиметикам.
По степени тяжести различают три стадии астматического статуса (А. Г. Чучалин, 1997 г.).
I стадия — относительная компенсация — характеризуется развитием длительно не купирующегося приступа удушья. Больные в сознании, адекватны, принимают вынужденное сидячее положение. Одышка с выраженным участием вспомогательной мускулатуры. Кашель непродуктивен. Перкуторно — коробочный звук, аускультативно — дыхание ослабленное, проводится во все отделы, обилие сухих свистящих хрипов. Лабораторно — дыхательный алкалоз.
II стадия — декомпенсация — характеризуется нарастанием бронхообструкции. В легких дыхание проводится «мозаично» или резко ослаблено («немое» легкое) при сохранении дистанционных хрипов. Грудная клетка эмфизематозно вздута, экскурсия ее незаметна. Пульс слабый, систолическое и пульсовое артериальное давление снижены. Лабораторно — гиперкапния, смешанный ацидоз, гемоконцентрация.
III стадия — гипоксическая гиперкапническая кома — характеризуется крайне тяжелым состоянием, нарушением сознания, церебральными неврологическими расстройствами. Дыхание редкое, поверхностное, парадоксальное. Пульс нитевидный, гипотония, коллапс. Лабораторно — декомпенсированный метаболический ацидоз.
Фазы течения бронхиальной астмы: обострение, ремиссия.
Обострение может протекать в виде острого приступа или затяжного состояния бронхиальной обструкции. Приступ бронхиальной астмы — острый эпизод экспираторного удушья, затрудненного и (или) свистящего дыхания и спастического кашля при резком снижении показателя пиковой скорости выдоха, четко отмечаемый пациентом и его окружающими.
Обострение в виде затяжного состояния бронхиальной обструкции характеризуется длительным (дни, недели, месяцы) затруднением дыхания с клинически выраженным синдромом бронхиальной обструкции, на фоне которого могут повторяться острые приступы различной тяжести.
Период ремиссии — межприступный период. Ремиссия может быть полной или неполной, что определяется характером клинико-функциональных показателей.
Осложнения бронхиальной астмы: легочное сердце (острое, подострое и хроническое); эмфизема легких; пневмосклероз; ателектаз легких (сегментарный, полисегментарный); интерстициальная, медиастинальная и подкожная эмфизема; спонтанный пневмоторакс; неврологические и эндокринные расстройства.
Дифференциальный диагноз проводится с хронической пневмонией, муковисцидозом, врожденными аномалиями развития бронхов (бронхопульмональная дисплазия, недоразвитие легких), экзогенным аллергическим альвеолитом, инородным телом трахеобронхиального дерева, дыхательными нарушениями нейрогенного и психогенного генеза.
Лечение. Основные цели терапии бронхиальной астмы у детей:
1) предотвращение развития угрожающих жизни состояний и летальных исходов;
2) ликвидация или смягчение клинических проявлений заболевания;
3) уменьшение частоты и выраженности обострений;
4) нормализация или улучшение показателей ФВД;
5) восстановление и поддержание жизненной активности, включая переносимость физических нагрузок;
6) отмена или снижение потребности в бронхолитической терапии;
7) предотвращение побочных эффектов лекарственной терапии;
8) предупреждение инвалидизации.
Лекарственные препараты, используемые для терапии бронхиальной астмы, выпускаются в различных формах и с различными устройствами для доставки в дыхательные пути. Предпочтителен ингаляционный путь введения препаратов, при котором быстро наступает клинический эффект с минимальным побочным действием. Широко используются дозированные ингаляторы. Их недостатком является необходимость синхронизировать вдох с нажатием на дно баллончика. Для детей, испытывающих затруднения с применением дозированных ингаляторов, рекомендуют спейсеры (пластиковые камеры для объемного распыления аэрозоля). В последнее время используются ингаляторы с синхронизатором («Легкое дыхание») или ингаляторы, в которых препарат находится в виде порошка, активизирующиеся за счет вдоха больного (дискхалеры, турбохалеры, спинхалеры). Для терапии обострений рекомендуется использовать небулайзер-ингалятор с компрессором для распыления аэрозоля с особо мелкодисперсными частицами, не требующий синхронизации с дыханием и позволяющий создать высокие концентрации лекарства в легких, может применяться с первых месяцев жизни ребенка.
Бронходилататоры
Противовоспалительные препараты
Неотложная терапия приступа бронхиальной астмы
Базисная терапия бронхиальной астмы
1. Период предвестников. Характерны заложенность носа или отделяемое из него, чихание, кашель, зуд и першение в горле, конъюнктивит, полиморфная сыпь, изменения поведения и настроения, нарушения аппетита и сна, симптомы ОРВИ.
2. Приступный период. Характеризуется рядом симптомов.
Симптомы удушья — дыхательный дискомфорт, субъективные ощущения нехватки воздуха, сжатия грудной клетки, возникающие внезапно.
Синдром дыхательной недостаточности — одышка экспираторная с участием вспомогательной мускулатуры, раздувание крыльев носа, набухание шейных вен, сухой приступообразный или малопродуктивный влажный кашель с трудно отходящей вязкой мокротой, дистанционные хрипы, ортопноэ, бледность кожи, периоральный и акроцианоз.
Бронхолегочный синдром — коробочный перкуторный звук, нижние границы легких опущены, подвижность легочных краев ограничена, дыхание с удлиненным выдохом или ослабленное, сухие свистящие хрипы, разнокалиберные влажные хрипы (особенно у детей раннего возраста) по всем легочным полям.
Изменения со стороны сердечно-сосудистой системы — тахикардия, пульс слабого наполнения, повышение артериального давления, тоны сердца приглушены, уменьшение относительной сердечной тупости вследствие эмфиземы.
3. Послеприступный период проявляется продуктивным кашлем, исчезновением одышки.
Диагностика. Основана на анамнестических данных, характерной клинической картине и результатах дополнительных методов обследования, которые включают:
1) оценку функции внешнего дыхания (ФВД). Выявляется обструктивный тип нарушений вентиляции легких;
2) функциональные тесты: положительный ответ на ингаляцию бета-агониста (прирост основных показателей ФВД > 20 %); проба с физической нагрузкой (снижение показателей проходимости бронхов через 3–5 мин после стандартной физической нагрузки > 20 %);
3) пикфлоуметрию — отмечается суточный разброс пиковой скорости выдоха, измеряемый в течение 2–3 недель > 20 %;
4) рентгенографическое исследование легких в период обострения — обнаруживается вздутие легких (повышение прозрачности по периферии легочных полей, низкое стояние куполов диафрагмы, расширение межреберных промежутков), усиление корневого рисунка;
5) исследование крови и мокроты — характерна эозинофилия крови и мокроты;
6) отмечается увеличение общего и специфических IgE в крови и биологических жидкостях;
7) положительные кожные пробы со специфическими аллергенами;
8) пробное лечение — высокая эффективность бета-агонистов.
Классификация. В 1997 г. утверждена национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика», согласно которой отменено разделение астмы на аллергическую, инфекционно-аллергическую и смешанную формы. С практической точки зрения на первый план выдвигается классификация бронхиальной астмы по степени тяжести, что определяет современную стратегию ее терапии. Выделяют легкое, среднетяжелое и тяжелое течение заболевания.
Степень тяжести определяется по следующим показателям:
1) количество ночных приступов в неделю;
2) количество дневных симптомов в день и неделю;
3) кратность применения (потребность) бета-2-агонистов короткого действия;
4) выраженность нарушений физической активности и сна;
5) значение пиковой скорости выдоха (ПСВ) и ее процентное соотношение с должным или наилучшим значением;
6) суточные колебания ПСВ.
При диссоциации отдельных показателей тяжести (редкие, но тяжелые приступы) бронхиальную астму следует характеризовать по более тяжелому признаку.
Таблица 1. Критерии тяжести бронхиальной астмы у детей


Таблица 2. Критерии оценки тяжести приступа бронхиальной астмы у детей


Астматический статус (АС) — тяжелый затяжной приступ с прогрессирующей дыхательной недостаточностью, резистентный к обычной терапии бронходилататорами, вследствие функционального блока бета-адренергических рецепторов бронхов.
Факторы, приводящие к развитию астматического статуса:
1) массивное воздействие аллергенов, бронхиальная или инфекция ЛОР-органов;
2) передозировка ингаляционных бета-2-агонистов;
3) неоправданная или быстрая отмена глюкокортикостероидного препарата у больных гормонзависимой астмой.
Критерии астматического статуса:
1) длительность некупирующегося приступа бронхиальной астмы не менее 6 ч;
2) нарушение дренажной функции бронхов;
3) гипоксемия и гиперкапния;
4) резистентность к симпатомиметикам.
По степени тяжести различают три стадии астматического статуса (А. Г. Чучалин, 1997 г.).
I стадия — относительная компенсация — характеризуется развитием длительно не купирующегося приступа удушья. Больные в сознании, адекватны, принимают вынужденное сидячее положение. Одышка с выраженным участием вспомогательной мускулатуры. Кашель непродуктивен. Перкуторно — коробочный звук, аускультативно — дыхание ослабленное, проводится во все отделы, обилие сухих свистящих хрипов. Лабораторно — дыхательный алкалоз.
II стадия — декомпенсация — характеризуется нарастанием бронхообструкции. В легких дыхание проводится «мозаично» или резко ослаблено («немое» легкое) при сохранении дистанционных хрипов. Грудная клетка эмфизематозно вздута, экскурсия ее незаметна. Пульс слабый, систолическое и пульсовое артериальное давление снижены. Лабораторно — гиперкапния, смешанный ацидоз, гемоконцентрация.
III стадия — гипоксическая гиперкапническая кома — характеризуется крайне тяжелым состоянием, нарушением сознания, церебральными неврологическими расстройствами. Дыхание редкое, поверхностное, парадоксальное. Пульс нитевидный, гипотония, коллапс. Лабораторно — декомпенсированный метаболический ацидоз.
Фазы течения бронхиальной астмы: обострение, ремиссия.
Обострение может протекать в виде острого приступа или затяжного состояния бронхиальной обструкции. Приступ бронхиальной астмы — острый эпизод экспираторного удушья, затрудненного и (или) свистящего дыхания и спастического кашля при резком снижении показателя пиковой скорости выдоха, четко отмечаемый пациентом и его окружающими.
Обострение в виде затяжного состояния бронхиальной обструкции характеризуется длительным (дни, недели, месяцы) затруднением дыхания с клинически выраженным синдромом бронхиальной обструкции, на фоне которого могут повторяться острые приступы различной тяжести.
Период ремиссии — межприступный период. Ремиссия может быть полной или неполной, что определяется характером клинико-функциональных показателей.
Осложнения бронхиальной астмы: легочное сердце (острое, подострое и хроническое); эмфизема легких; пневмосклероз; ателектаз легких (сегментарный, полисегментарный); интерстициальная, медиастинальная и подкожная эмфизема; спонтанный пневмоторакс; неврологические и эндокринные расстройства.
Дифференциальный диагноз проводится с хронической пневмонией, муковисцидозом, врожденными аномалиями развития бронхов (бронхопульмональная дисплазия, недоразвитие легких), экзогенным аллергическим альвеолитом, инородным телом трахеобронхиального дерева, дыхательными нарушениями нейрогенного и психогенного генеза.
Лечение. Основные цели терапии бронхиальной астмы у детей:
1) предотвращение развития угрожающих жизни состояний и летальных исходов;
2) ликвидация или смягчение клинических проявлений заболевания;
3) уменьшение частоты и выраженности обострений;
4) нормализация или улучшение показателей ФВД;
5) восстановление и поддержание жизненной активности, включая переносимость физических нагрузок;
6) отмена или снижение потребности в бронхолитической терапии;
7) предотвращение побочных эффектов лекарственной терапии;
8) предупреждение инвалидизации.
Лекарственные препараты, используемые для терапии бронхиальной астмы, выпускаются в различных формах и с различными устройствами для доставки в дыхательные пути. Предпочтителен ингаляционный путь введения препаратов, при котором быстро наступает клинический эффект с минимальным побочным действием. Широко используются дозированные ингаляторы. Их недостатком является необходимость синхронизировать вдох с нажатием на дно баллончика. Для детей, испытывающих затруднения с применением дозированных ингаляторов, рекомендуют спейсеры (пластиковые камеры для объемного распыления аэрозоля). В последнее время используются ингаляторы с синхронизатором («Легкое дыхание») или ингаляторы, в которых препарат находится в виде порошка, активизирующиеся за счет вдоха больного (дискхалеры, турбохалеры, спинхалеры). Для терапии обострений рекомендуется использовать небулайзер-ингалятор с компрессором для распыления аэрозоля с особо мелкодисперсными частицами, не требующий синхронизации с дыханием и позволяющий создать высокие концентрации лекарства в легких, может применяться с первых месяцев жизни ребенка.
Бронходилататоры
I. Селективные бета-2-адреномиметики (агонисты) являются наиболее щадящими и высокоэффективными адреномиметиками, рекомендуются вместо ранее используемых неселективных бета-агонистов (орципреналина).
1. Бета-2-агонисты короткого действия: применяются для купирования приступа бронхиальной астмы:
1) сальбутамол; таблетки: вентолин (2 мг), сальгим (4 мг). Дозы препаратов: до 2 лет — 100 мкг/кг 4 раза в день, старше 2 лет — 1–2 мг 3–4 раза в день.
Ингаляционные формы: дозированные ингаляторы — сальбутамол (100 мкг в 1 дозе), вентолин (100 мкг), вентолин «Легкое дыхание» (100 мкг), вентодиск — порошок для ингаляций в ротадисках, ротадиск содержит 8 доз по 200 или 400 мкг в комплекте с дисковым ингалятором дискхалером, Сальбен — сухой порошок для ингаляций по 200 мкг, вводится при помощи индивидуального ингалятора циклохалера, вентолин-небулы (пластиковые ампулы) по 2,5 мл (2,5 мг) для ингаляции через небулайзер. Дозы препаратов — 100–200 мкг не чаще 3–4 раз в день;
2) фенотерол: дозированный ингалятор беротек (100 мкг и 200 мкг), раствор беротека для небулайзера (1 мг фенотерола в 1 мл);
3) тербуталин: дозированный ингалятор бриканил (250 мкг в 1 дозе), таблетки бриканил (2,5 мг). Доза — по 1 вдоху или 1 таблетке каждые 6 ч;
4) гексопреналин: дозированный ингалятор ипрадол 200 мкг в 1 дозе, таблетки по 500 мкг.
2. Бета-2-агонисты длительного действия: используются для базисной терапии:
1) сальбутамол пролонгированного действия, обусловленного осмотически управляемым механизмом постепенного высвобождения лекарственного вещества из ядра таблетки в течение 9—12 ч (вольмакс — 4 мг, сальтос — 7,23 мг сальбутамола в таблетке). Доза детям 3 —12 лет — по 4 мг 2 раза в день, старше 12 лет при необходимости до 8 мг 2 раза в день. Таблетки проглатываются целиком;
2) сальметерол: дозированные ингаляторы серевент, сальметер по 25 мкг в 1 дозе, порошок для ингаляций в ротадисках серевент, сальметер по 4 дозы в ротадиске, 1 доза 50 мкг. Доза детям старше 3 лет — по 25–50 мкг 2 раза в сутки;
3) формотерол: дозирующий ингалятор оксис в турбухалере, 4,5 мкг в 1 дозе, доза детям старше 6 лет — по 4,5–9 мкг 1–2 раза в сутки;
4) кленбутерол (спиропент): таблетки по 0, 02 мг, сироп — в 1 мл 0, 005 мг кленбутерола. Дозы: таблетки детям старше 12 лет — по 1 таблетке 2 раза в день, сироп детям младше 2 лет — 5 мл 2 раза в сутки, 2–4 лет — 5 мл 3 раза в сутки, 4–6 лет — 10 мл 2 раза в сутки, 6—12 лет — 15 мл 2 раза в сутки.
Другие адреномиметики в настоящее время не рекомендуются к использованию из-за побочных эффектов.
II. Блокаторы М-холинорецепторов. Ипратропиум бромид (атровент); дозированный ингалятор 20 мкг в 1 дозе по 1–2 вдоха 3–4 раза в сутки; порошок для ингаляций в капсулах, 200 мкг в 1 капсуле, детям старше 7 лет — по 1 капсуле 3–4 раза в сутки; раствор для ингаляций через небулайзер, 250 мкг в 1 мл.
III. Комбинированные препараты.
1. Беродуал (бета-2-агонист + ипратропиума бромид); дозированный ингалятор (20 мкг ипратропиума и 50 мкг фенотерола) детям старше 3 лет — по 1–2 дозы 3 раза в сутки; раствор для небулайзера во флаконах по 20 мл (в 1 мл 500 мкг фенотерола и 250 мкг ипратропиума).
2. Комбивент; дозированный аэрозольный ингалятор (20 мкг ипратропиума и 100 мкг сальбутамола), применяется для детей после 12 лет.
3. Дитек (бета-2-агонист + кромогликат натрия); дозированный ингалятор, в 1 дозе 50 мкг фенотерола и 1 мг кромогликата натрия, детям 4–6 лет — по 1 дозе 4 раза в сутки, старше 6 лет — по 2 дозы 3 раза в сутки.
4. Интал плюс (бета-2-агонист + кромогликат натрия); дозированный ингалятор, в 1 дозе 100 мкг сальбутамола и 1 мг кромогликата натрия, детям с 6 лет — по 1–2 ингаляции 4 раза в сутки, возможно увеличение дозы до 6–8 ингаляций в сутки.
IV. Метилксантины.
1. Короткого действия (эуфиллин, аминофиллин) — таблетки по 150 мг, раствор для внутривенного введения 2,4 %-ный по 10 мл в ампуле. Эуфиллин в свечах и внутримышечно не применяется. Доза: нагрузочная при внутривенном введении 4,5–5 мг/кг в течение 30 мин, в дальнейшем при непрерывной инфузии в дозе 0,6–0,8 мг/кг/ч или дробно через 4–5 ч под контролем концентрации теофиллина в крови. Пероральная суточная доза — 7—10 мг/кг.
2. Пролонгированного действия (теофиллин): теопек (таблетки по 100, 200, 300 мг теофиллина), ретафил (таблетки по 200, 300 мг), теотард (капсулы по 200, 350, 500 мг), эуфилонг (капсулы по 250, 375 мг), вентакс (капсулы по 100, 200, 300 мг), спофиллин-ретард (таблетки по 100, 250 мг), суточная доза 10–15 мг/кг.
1. Бета-2-агонисты короткого действия: применяются для купирования приступа бронхиальной астмы:
1) сальбутамол; таблетки: вентолин (2 мг), сальгим (4 мг). Дозы препаратов: до 2 лет — 100 мкг/кг 4 раза в день, старше 2 лет — 1–2 мг 3–4 раза в день.
Ингаляционные формы: дозированные ингаляторы — сальбутамол (100 мкг в 1 дозе), вентолин (100 мкг), вентолин «Легкое дыхание» (100 мкг), вентодиск — порошок для ингаляций в ротадисках, ротадиск содержит 8 доз по 200 или 400 мкг в комплекте с дисковым ингалятором дискхалером, Сальбен — сухой порошок для ингаляций по 200 мкг, вводится при помощи индивидуального ингалятора циклохалера, вентолин-небулы (пластиковые ампулы) по 2,5 мл (2,5 мг) для ингаляции через небулайзер. Дозы препаратов — 100–200 мкг не чаще 3–4 раз в день;
2) фенотерол: дозированный ингалятор беротек (100 мкг и 200 мкг), раствор беротека для небулайзера (1 мг фенотерола в 1 мл);
3) тербуталин: дозированный ингалятор бриканил (250 мкг в 1 дозе), таблетки бриканил (2,5 мг). Доза — по 1 вдоху или 1 таблетке каждые 6 ч;
4) гексопреналин: дозированный ингалятор ипрадол 200 мкг в 1 дозе, таблетки по 500 мкг.
2. Бета-2-агонисты длительного действия: используются для базисной терапии:
1) сальбутамол пролонгированного действия, обусловленного осмотически управляемым механизмом постепенного высвобождения лекарственного вещества из ядра таблетки в течение 9—12 ч (вольмакс — 4 мг, сальтос — 7,23 мг сальбутамола в таблетке). Доза детям 3 —12 лет — по 4 мг 2 раза в день, старше 12 лет при необходимости до 8 мг 2 раза в день. Таблетки проглатываются целиком;
2) сальметерол: дозированные ингаляторы серевент, сальметер по 25 мкг в 1 дозе, порошок для ингаляций в ротадисках серевент, сальметер по 4 дозы в ротадиске, 1 доза 50 мкг. Доза детям старше 3 лет — по 25–50 мкг 2 раза в сутки;
3) формотерол: дозирующий ингалятор оксис в турбухалере, 4,5 мкг в 1 дозе, доза детям старше 6 лет — по 4,5–9 мкг 1–2 раза в сутки;
4) кленбутерол (спиропент): таблетки по 0, 02 мг, сироп — в 1 мл 0, 005 мг кленбутерола. Дозы: таблетки детям старше 12 лет — по 1 таблетке 2 раза в день, сироп детям младше 2 лет — 5 мл 2 раза в сутки, 2–4 лет — 5 мл 3 раза в сутки, 4–6 лет — 10 мл 2 раза в сутки, 6—12 лет — 15 мл 2 раза в сутки.
Другие адреномиметики в настоящее время не рекомендуются к использованию из-за побочных эффектов.
II. Блокаторы М-холинорецепторов. Ипратропиум бромид (атровент); дозированный ингалятор 20 мкг в 1 дозе по 1–2 вдоха 3–4 раза в сутки; порошок для ингаляций в капсулах, 200 мкг в 1 капсуле, детям старше 7 лет — по 1 капсуле 3–4 раза в сутки; раствор для ингаляций через небулайзер, 250 мкг в 1 мл.
III. Комбинированные препараты.
1. Беродуал (бета-2-агонист + ипратропиума бромид); дозированный ингалятор (20 мкг ипратропиума и 50 мкг фенотерола) детям старше 3 лет — по 1–2 дозы 3 раза в сутки; раствор для небулайзера во флаконах по 20 мл (в 1 мл 500 мкг фенотерола и 250 мкг ипратропиума).
2. Комбивент; дозированный аэрозольный ингалятор (20 мкг ипратропиума и 100 мкг сальбутамола), применяется для детей после 12 лет.
3. Дитек (бета-2-агонист + кромогликат натрия); дозированный ингалятор, в 1 дозе 50 мкг фенотерола и 1 мг кромогликата натрия, детям 4–6 лет — по 1 дозе 4 раза в сутки, старше 6 лет — по 2 дозы 3 раза в сутки.
4. Интал плюс (бета-2-агонист + кромогликат натрия); дозированный ингалятор, в 1 дозе 100 мкг сальбутамола и 1 мг кромогликата натрия, детям с 6 лет — по 1–2 ингаляции 4 раза в сутки, возможно увеличение дозы до 6–8 ингаляций в сутки.
IV. Метилксантины.
1. Короткого действия (эуфиллин, аминофиллин) — таблетки по 150 мг, раствор для внутривенного введения 2,4 %-ный по 10 мл в ампуле. Эуфиллин в свечах и внутримышечно не применяется. Доза: нагрузочная при внутривенном введении 4,5–5 мг/кг в течение 30 мин, в дальнейшем при непрерывной инфузии в дозе 0,6–0,8 мг/кг/ч или дробно через 4–5 ч под контролем концентрации теофиллина в крови. Пероральная суточная доза — 7—10 мг/кг.
2. Пролонгированного действия (теофиллин): теопек (таблетки по 100, 200, 300 мг теофиллина), ретафил (таблетки по 200, 300 мг), теотард (капсулы по 200, 350, 500 мг), эуфилонг (капсулы по 250, 375 мг), вентакс (капсулы по 100, 200, 300 мг), спофиллин-ретард (таблетки по 100, 250 мг), суточная доза 10–15 мг/кг.
Противовоспалительные препараты
I. Нестероидные противовоспалительные препараты контролируют высвобождение медиаторов воспаления из тучных клеток, предупреждая их либерацию, угнетают неиммунологические изменения нейрофизиологического происхождения, уменьшают гиперреактивность бронхов и предупреждают рефлекторно обусловленную бронхообструкцию.
1. Кромогликат натрия (интал) — дозированный ингалятор (1 мг в 1 дозе), порошок для ингаляций в капсулах (в 1 капсуле — 20 мг) с ингалятором спинхалером; кропоз — дозированный ингалятор (5 мг в 1 дозе); комбинированные препараты — дитек, интал плюс (см. выше).
2. Недокромил натрия (тайлед) — дозированный ингалятор (2 мг в 1 дозе); тайлед минт — дозированный аэрозоль во флаконе с синхронером (2 мг в 1 дозе).
3. Антигистаминные препараты: кетотифен (задитен) — таблетки по 1 мг; кларитин — таблетки по 10 мг, сироп.
II. Ингаляционные кортикостероиды
1. Бекламетазон дипропионат, альдецин, бекотид, бекломет, беклазон — дозированные ингаляторы (1 доза — 50 мкг); бекотид «Легкое дыхание» — ингалятор с синхронером (1 доза — 100 мкг, 250 мкг); Бекодиск — порошок для ингаляций в ротадисках (1 доза — 100 мкг, 200 мкг). Режим дозирования — по 100 мкг 2–4 раза в сутки.
2. Будесонид, будесонид форте — дозированный аэрозоль (1 доза — 200 мкг); пульмикорт турбухалер — сухой порошок (в 1 дозе — 100 мкг, 200 мкг). Режим дозирования — 200–400 мкг 1 раз в день или 100–200 мкг 2 раза в день.
3. Флутиказона пропионат, фликсотид — дозированный аэрозоль, порошок для ингаляций в ротадисках (в 1 дозе — 50 мкг, 125 мкг, 250 мкг). Режим дозирования — по 50—100 мкг 2 раза в день.
4. Флунисолид, Ингакорт — дозированный ингалятор (1 доза — 250 мкг).
III. Антилейкотриеновые препараты
1. Ингибиторы синтеза лейкотриенов (зилетон).
2. Блокаторы рецепторов к лейкотриенам: зафирлукаст (аколат), монтелукаст — назначаются детям старше 12 лет по 1 таблетке (20 мг) 2 раза в сутки.
3. Противоаллергический иммуноглобулин, гистоглобулин в настоящее время не рекомендуются большинством руководств в качестве стандартного метода терапии бронхиальной астмы.
4. Специфическая аллерговакцинация (гипосенсибилизация) проводится детям с легкой и среднетяжелой формой бронхиальной астмы при четкой доказанности причинно значимого аллергена, в случаях малой эффективности проводимой фармакотерапии и невозможности элиминировать причинно-значимые аллергены из окружающей среды больного. Проводится только аллергологом.
1. Кромогликат натрия (интал) — дозированный ингалятор (1 мг в 1 дозе), порошок для ингаляций в капсулах (в 1 капсуле — 20 мг) с ингалятором спинхалером; кропоз — дозированный ингалятор (5 мг в 1 дозе); комбинированные препараты — дитек, интал плюс (см. выше).
2. Недокромил натрия (тайлед) — дозированный ингалятор (2 мг в 1 дозе); тайлед минт — дозированный аэрозоль во флаконе с синхронером (2 мг в 1 дозе).
3. Антигистаминные препараты: кетотифен (задитен) — таблетки по 1 мг; кларитин — таблетки по 10 мг, сироп.
II. Ингаляционные кортикостероиды
1. Бекламетазон дипропионат, альдецин, бекотид, бекломет, беклазон — дозированные ингаляторы (1 доза — 50 мкг); бекотид «Легкое дыхание» — ингалятор с синхронером (1 доза — 100 мкг, 250 мкг); Бекодиск — порошок для ингаляций в ротадисках (1 доза — 100 мкг, 200 мкг). Режим дозирования — по 100 мкг 2–4 раза в сутки.
2. Будесонид, будесонид форте — дозированный аэрозоль (1 доза — 200 мкг); пульмикорт турбухалер — сухой порошок (в 1 дозе — 100 мкг, 200 мкг). Режим дозирования — 200–400 мкг 1 раз в день или 100–200 мкг 2 раза в день.
3. Флутиказона пропионат, фликсотид — дозированный аэрозоль, порошок для ингаляций в ротадисках (в 1 дозе — 50 мкг, 125 мкг, 250 мкг). Режим дозирования — по 50—100 мкг 2 раза в день.
4. Флунисолид, Ингакорт — дозированный ингалятор (1 доза — 250 мкг).
III. Антилейкотриеновые препараты
1. Ингибиторы синтеза лейкотриенов (зилетон).
2. Блокаторы рецепторов к лейкотриенам: зафирлукаст (аколат), монтелукаст — назначаются детям старше 12 лет по 1 таблетке (20 мг) 2 раза в сутки.
3. Противоаллергический иммуноглобулин, гистоглобулин в настоящее время не рекомендуются большинством руководств в качестве стандартного метода терапии бронхиальной астмы.
4. Специфическая аллерговакцинация (гипосенсибилизация) проводится детям с легкой и среднетяжелой формой бронхиальной астмы при четкой доказанности причинно значимого аллергена, в случаях малой эффективности проводимой фармакотерапии и невозможности элиминировать причинно-значимые аллергены из окружающей среды больного. Проводится только аллергологом.
Неотложная терапия приступа бронхиальной астмы
Общие принципы:
1) при первичном осмотре оценивается тяжесть приступа, проводится пикфлоуметрия;
2) удаление причинно-значимых аллергенов или триггерных факторов;
3) уточнение ранее проводимого лечения (количество доз бронхолитиков, пути введения; время, прошедшее с момента последнего приема бронхолитика; применялись ли кортикостероиды, в каких дозах);
4) оказание неотложной помощи в зависимости от тяжести приступа. В процессе терапии и наблюдения тяжесть может быть пересмотрена;
5) наблюдение в динамике.
Терапия легкого приступа: ингаляция бронхолитика короткого действия (1–2 дозы). Оптимально использование спейсера, возможно приспособление типа пластикового стаканчика с отверстием в дне для ингалятора.
После купирования приступа продолжают введение бета-2-агонистов каждые 4–6 ч в течение 24–48 ч или эуфиллина перорально 10–15 мг/кг в сутки. При увеличении частоты использования бета-2-агонистов более 3 раз в сутки необходимо усиление базисной терапии.
Терапия среднетяжелого приступа: ингаляция 1–2 доз бронхолитика (с помощью дозирующего ингалятора со спейсером или небулайзера); эуфиллин внутривенно на физрастворе 5 мг/кг; при неэффективности этих мероприятий — глюкокортикоиды (1–2 мг/кг преднизолона парентерально).
После купирования приступа продолжают введение бронхолитиков ингаляционно 1–2 дня с последующим переводом на пролонгированные бронхолитики (бета-2-агонисты, метилксантины), увеличивают дозу базисной противовоспалительной терапии.
Терапия тяжелого приступа: терапия тяжелого приступа включает мероприятия, направленные на устранение бронхоспазма, уменьшение вазосекреторных расстройств, разжижение и удаление мокроты, ликвидацию дыхательной и сердечной недостаточности, гипоксии, метаболических нарушений и надпочечниковой недостаточности.
Проводятся следующие мероприятия:
1) оксигенотерапия через маску или носовой катетер;
2) регидратационная терапия (5 %-ный физраствор глюкозы, реополиглюкин в общем объеме 10–20 мл на 1 кг массы);
3) эуфиллин (аминофиллин) 2,4 %-ный 4,5–5 мг/кг на физрастворе в течение 20–30 мин. В последующем проводится непрерывная инфузия в дозе 0,6–0,8 мг/кг/ч или дробно каждые 4–5 ч. Пролонгированные препараты теофиллина в терапии острого приступа не используются;
4) глюкокортикоиды парентерально в дозе 2—10 мг/кг/сут по преднизолону каждые 4–6 ч до выведения ребенка из приступа;
5) бета-2-агонисты используются на начальных этапах купирования приступа при отсутствии признаков их передозировки по 1 дозе с интервалом 20 мин в течение часа, предпочтительно через небулайзер или спейсер. При астматическом статусе бета-2-агонисты не применяются в связи с блокадой бета-2-адренорецепторов.
При отсутствии эффекта от терапии при астматическом статусе используется поднаркозная бронхоскопия с санацией трахеобронхиального дерева в условиях реанимационного отделения.
После ликвидации тяжелого приступа необходимо продолжить пикфлоуметрию, введение бронхоспазмолитиков короткого действия 3–5 дней через 4 ч, затем произвести перевод на пролонгированные бронхолитики (бета-2-агонисты, метилксантины), системные кортикостероиды парентерально или перорально в течение 3–5 дней в дозе 1–2 мг/кг/сут до купирования бронхиальной обструкции. Если ребенок получает базисную терапию, необходимо увеличить дозу на 7—10 дней. При необходимости производится коррекция базисной терапии.
Не используются для терапии приступа бронхиальной астмы антигистаминные препараты, седативные, фитопрепараты, горчичники, банки, препараты кальция, муколитики, пролонгированные бронхолитики. Антибиотики назначаются при наличии пневмонии или другой бактериальной инфекции с учетом чувствительности микрофлоры.
1) при первичном осмотре оценивается тяжесть приступа, проводится пикфлоуметрия;
2) удаление причинно-значимых аллергенов или триггерных факторов;
3) уточнение ранее проводимого лечения (количество доз бронхолитиков, пути введения; время, прошедшее с момента последнего приема бронхолитика; применялись ли кортикостероиды, в каких дозах);
4) оказание неотложной помощи в зависимости от тяжести приступа. В процессе терапии и наблюдения тяжесть может быть пересмотрена;
5) наблюдение в динамике.
Терапия легкого приступа: ингаляция бронхолитика короткого действия (1–2 дозы). Оптимально использование спейсера, возможно приспособление типа пластикового стаканчика с отверстием в дне для ингалятора.
После купирования приступа продолжают введение бета-2-агонистов каждые 4–6 ч в течение 24–48 ч или эуфиллина перорально 10–15 мг/кг в сутки. При увеличении частоты использования бета-2-агонистов более 3 раз в сутки необходимо усиление базисной терапии.
Терапия среднетяжелого приступа: ингаляция 1–2 доз бронхолитика (с помощью дозирующего ингалятора со спейсером или небулайзера); эуфиллин внутривенно на физрастворе 5 мг/кг; при неэффективности этих мероприятий — глюкокортикоиды (1–2 мг/кг преднизолона парентерально).
После купирования приступа продолжают введение бронхолитиков ингаляционно 1–2 дня с последующим переводом на пролонгированные бронхолитики (бета-2-агонисты, метилксантины), увеличивают дозу базисной противовоспалительной терапии.
Терапия тяжелого приступа: терапия тяжелого приступа включает мероприятия, направленные на устранение бронхоспазма, уменьшение вазосекреторных расстройств, разжижение и удаление мокроты, ликвидацию дыхательной и сердечной недостаточности, гипоксии, метаболических нарушений и надпочечниковой недостаточности.
Проводятся следующие мероприятия:
1) оксигенотерапия через маску или носовой катетер;
2) регидратационная терапия (5 %-ный физраствор глюкозы, реополиглюкин в общем объеме 10–20 мл на 1 кг массы);
3) эуфиллин (аминофиллин) 2,4 %-ный 4,5–5 мг/кг на физрастворе в течение 20–30 мин. В последующем проводится непрерывная инфузия в дозе 0,6–0,8 мг/кг/ч или дробно каждые 4–5 ч. Пролонгированные препараты теофиллина в терапии острого приступа не используются;
4) глюкокортикоиды парентерально в дозе 2—10 мг/кг/сут по преднизолону каждые 4–6 ч до выведения ребенка из приступа;
5) бета-2-агонисты используются на начальных этапах купирования приступа при отсутствии признаков их передозировки по 1 дозе с интервалом 20 мин в течение часа, предпочтительно через небулайзер или спейсер. При астматическом статусе бета-2-агонисты не применяются в связи с блокадой бета-2-адренорецепторов.
При отсутствии эффекта от терапии при астматическом статусе используется поднаркозная бронхоскопия с санацией трахеобронхиального дерева в условиях реанимационного отделения.
После ликвидации тяжелого приступа необходимо продолжить пикфлоуметрию, введение бронхоспазмолитиков короткого действия 3–5 дней через 4 ч, затем произвести перевод на пролонгированные бронхолитики (бета-2-агонисты, метилксантины), системные кортикостероиды парентерально или перорально в течение 3–5 дней в дозе 1–2 мг/кг/сут до купирования бронхиальной обструкции. Если ребенок получает базисную терапию, необходимо увеличить дозу на 7—10 дней. При необходимости производится коррекция базисной терапии.
Не используются для терапии приступа бронхиальной астмы антигистаминные препараты, седативные, фитопрепараты, горчичники, банки, препараты кальция, муколитики, пролонгированные бронхолитики. Антибиотики назначаются при наличии пневмонии или другой бактериальной инфекции с учетом чувствительности микрофлоры.
Базисная терапия бронхиальной астмы
Основные принципы:
1) рациональное использование лекарств с учетом путей их введения (предпочтителен ингаляционный способ);
2) ступенчатый (в зависимости от тяжести заболевания) подход к лечению;
3) у детей старше 5 лет базисная терапия проводится под контролем функции внешнего дыхания (пикфлоуметрия);
4) базисная терапия определяется с учетом исходной степени тяжести заболевания на момент осмотра больного, проводится длительно, отменяется при достижении стойкой ремиссии.
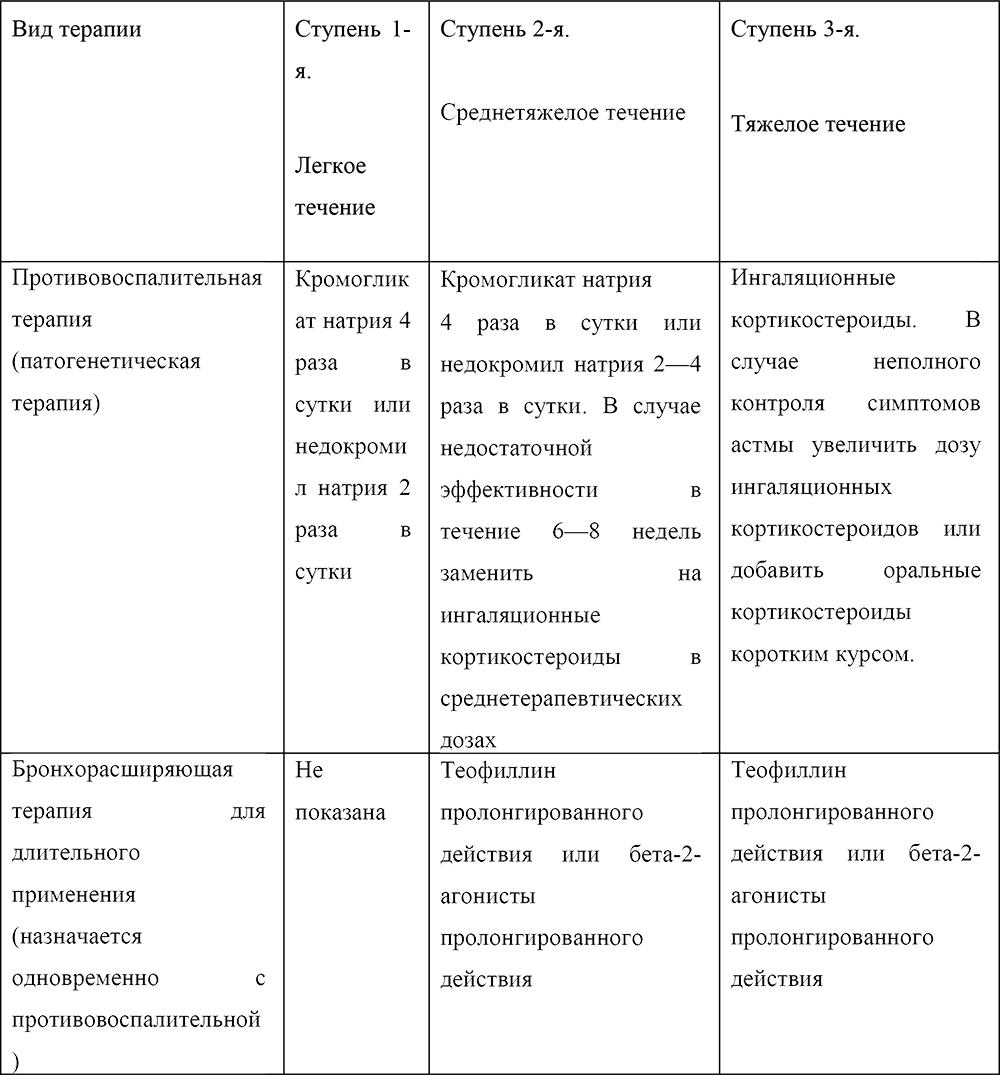
Таблица 3. Ступенчатый подход к базисному (длительному) лечению бронхиальной астмы у детей.
Примечания:
1) при астме легкого течения с редкими приступами и длительной ремиссией базисная терапия кромогликатом натрия или недокромилом натрия проводится для профилактики сезонных обострений;
2) прием кромогликата натрия или недокромила натрия с профилактической целью показан также при постнагрузочном бронхоспазме или контакте с аллергеном;
3) бета-2-агонисты пролонгированного действия (сальметерол, формотерол) используются в комбинации с противовоспалительными препаратами при их недостаточной эффективности;
4) при легком течении атопической астмы у детей раннего возраста и в случаях сочетанных проявлений бронхиальной астмы и атопического дерматита также может быть рекомендован кетотифен;
5) по завершении курса лечения стероидами per os необходим переход на ингаляционные стероиды;
6) при отсутствии выраженных клинико-функциональных проявлений заболевания у детей с тяжелой астмой в течение 6 месяцев возможно снижение суточной дозы ингаляционных стероидов с их постепенной заменой на недокромил натрия или кромогликат натрия.
1) рациональное использование лекарств с учетом путей их введения (предпочтителен ингаляционный способ);
2) ступенчатый (в зависимости от тяжести заболевания) подход к лечению;
3) у детей старше 5 лет базисная терапия проводится под контролем функции внешнего дыхания (пикфлоуметрия);
4) базисная терапия определяется с учетом исходной степени тяжести заболевания на момент осмотра больного, проводится длительно, отменяется при достижении стойкой ремиссии.
Таблица 3. Ступенчатый подход к базисному (длительному) лечению бронхиальной астмы у детей.

Примечания:
1) при астме легкого течения с редкими приступами и длительной ремиссией базисная терапия кромогликатом натрия или недокромилом натрия проводится для профилактики сезонных обострений;
2) прием кромогликата натрия или недокромила натрия с профилактической целью показан также при постнагрузочном бронхоспазме или контакте с аллергеном;
3) бета-2-агонисты пролонгированного действия (сальметерол, формотерол) используются в комбинации с противовоспалительными препаратами при их недостаточной эффективности;
4) при легком течении атопической астмы у детей раннего возраста и в случаях сочетанных проявлений бронхиальной астмы и атопического дерматита также может быть рекомендован кетотифен;
5) по завершении курса лечения стероидами per os необходим переход на ингаляционные стероиды;
6) при отсутствии выраженных клинико-функциональных проявлений заболевания у детей с тяжелой астмой в течение 6 месяцев возможно снижение суточной дозы ингаляционных стероидов с их постепенной заменой на недокромил натрия или кромогликат натрия.
Конец бесплатного ознакомительного фрагмента
