Страница:
Боли при кардиоспазме обычно возникают при глотании и локализуются за грудиной. Они связаны с растяжением стенок пищевода при нераскрытой НПС и исчезают после срыгивания или прохождения пищи в желудок. Иногда боли, напротив, появляются натощак или после рвоты. В этих случаях они вызваны эзофагитом и уменьшаются после приема пищи. У некоторых пациентов болевые ощущения могут быть довольно интенсивными, не связанными с актом глотания, возникать при волнении, физической нагрузке или даже в покое, в ночное время, вследствие некоординированных, спастических сокращений пищеводной мускулатуры.
Регургитация происходит на высоте затрудненного глотания после нескольких глотков. При этом сначала возникает ощущение «комка» в верхней части пищевода, а затем пищевые массы непроизвольно поступают в полость рта или наружу. При выраженной дилатации пищевода регургитация бывает реже, но обильнее. Иногда ее провоцирует перемена положения тела, чаще, когда пациент ложится или наклоняется кпереди. У большинства больных отмечается ночная регургитация, проявляющаяся вытеканием содержимого пищевода на подушку («симптом мокрой подушки»). В более тяжелых случаях возникает обильная регургитация с поперхиванием и приступами сильного кашля вследствие затекания пищевых масс в дыхательные пути, что может привести к аспирационной пневмонии.
Потеря массы тела в начале болезни выражена нерезко и отмечается примерно у половины больных. При прогрессировании дисфагии и регургитации наблюдается заметное похудание. У небольшой части пациентов развивается истощение.
Данные объективного исследования при кардиоспазме малоинформативны ввиду их неспецифичности. Общее состояние в I–II стадиях кардиоспазма хорошее. При III–IV стадиях наблюдается более выраженное понижение питания. У пациентов со значительной дилатацией пищевода может быть неприятный запах изо рта на почве гниения и брожения застаивающихся пищевых масс. Старыми авторами описывались расширение границ срединного притупления при перкуссии (ввиду расширения пищевода и смещения его вправо) и изменения аускультативных данных (шум плеска при наличии резко выраженного расширения пищевода).
Лабораторная и инструментальная диагностика
Дифференциальная диагностика
Лечение
Рубцовые стриктуры пищевода
Этиология и патогенез
Классификация
Регургитация происходит на высоте затрудненного глотания после нескольких глотков. При этом сначала возникает ощущение «комка» в верхней части пищевода, а затем пищевые массы непроизвольно поступают в полость рта или наружу. При выраженной дилатации пищевода регургитация бывает реже, но обильнее. Иногда ее провоцирует перемена положения тела, чаще, когда пациент ложится или наклоняется кпереди. У большинства больных отмечается ночная регургитация, проявляющаяся вытеканием содержимого пищевода на подушку («симптом мокрой подушки»). В более тяжелых случаях возникает обильная регургитация с поперхиванием и приступами сильного кашля вследствие затекания пищевых масс в дыхательные пути, что может привести к аспирационной пневмонии.
Потеря массы тела в начале болезни выражена нерезко и отмечается примерно у половины больных. При прогрессировании дисфагии и регургитации наблюдается заметное похудание. У небольшой части пациентов развивается истощение.
Данные объективного исследования при кардиоспазме малоинформативны ввиду их неспецифичности. Общее состояние в I–II стадиях кардиоспазма хорошее. При III–IV стадиях наблюдается более выраженное понижение питания. У пациентов со значительной дилатацией пищевода может быть неприятный запах изо рта на почве гниения и брожения застаивающихся пищевых масс. Старыми авторами описывались расширение границ срединного притупления при перкуссии (ввиду расширения пищевода и смещения его вправо) и изменения аускультативных данных (шум плеска при наличии резко выраженного расширения пищевода).
Лабораторная и инструментальная диагностика
Лабораторные методы при кардиоспазме малоинформативны, поскольку при этом заболевании не бывает специфических патологических изменений. При развитии осложнений (например, аспирационной пневмонии, дисфагии III–IV степени) могут быть лейкоцитоз, электролитные нарушения и т. д. Диагностика кардиоспазма, прежде всего, основывается на рентгенологическом и эндоскопическом исследованиях.
Главный рентгенологический симптом кардиоспазма – выявление конического сужения дистального отдела пищевода, которое описывается как симптом «мышиного хвоста», «птичьего клюва» и т. д. Вышележащие отделы пищевода при этом обычно расширены соответственно стадии заболевания. Дилатация пищевода может быть выражена очень значительно. При рентгеноскопии выявляют нераскрытое кардии при акте глотания, нарушение перистальтики пищевода. Нередко обнаруживают отсутствие газового пузыря желудка и рентгенологические признаки аспирационных легочных осложнений кардиоспазма (рис. 19).
Эндоскопическое исследование пищевода позволяет выявить степень расширения его проксимальных сегментов, характер и выраженность эзофагита и метапластических изменений. Почти всегда при кардиоспазме удается пройти эндоскопом в желудок, в отличие от рака кардии и органических рубцовых стенозов (симптом Мельцера).
Манометрия пищевода позволяет подтвердить диагноз кардиоспазма и дифференцировать его от других нейромышечных заболеваний. Основной манометрический признак кардиоспазма – полное или частичное нерасслабление НПС при глотании. Часто наблюдаются повышение «давления покоя» НПС и ослабление перистальтики гладкой мускулатуры пищевода.
За рубежом для исследования опорожнения пищевода при подозрении на кардиоспазм широко применяют радионуклидное исследование (сцинтиграфию). Для этого больным дают выпить специальный раствор, содержащий радиофармпрепарат, а затем в динамике регистрируют интенсивность вызванного им гамма-излучения в гамма-камере. Это позволяет уточнить время частичного или полного опорожнения пищевода, которое при кардиоспазме, как правило, в значительной степени замедлено.

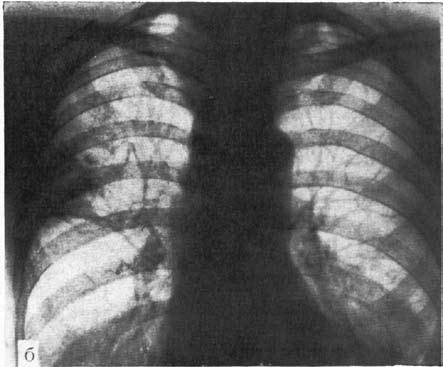
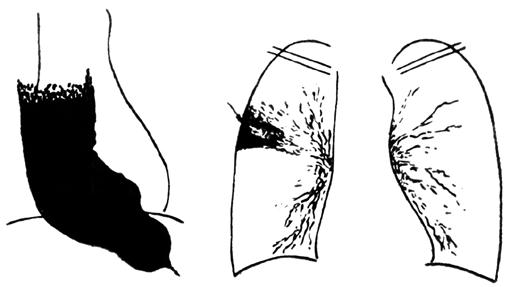
Рис. 19. Рентгенологические симптомы кардиоспазма: А – пищевод значительно расширен, удлинен и смещен вправо; дистальный его отрезок резко сужен, газовый пузырь желудка отсутствует; Б – справа в верхней доле легкого явления пневмосклероза как следствие многократных аспирационных пневмоний. (Приводится по: Е.М. Каган. Рентгенодиагностика заболеваний пищевода. М., 1968)
Главный рентгенологический симптом кардиоспазма – выявление конического сужения дистального отдела пищевода, которое описывается как симптом «мышиного хвоста», «птичьего клюва» и т. д. Вышележащие отделы пищевода при этом обычно расширены соответственно стадии заболевания. Дилатация пищевода может быть выражена очень значительно. При рентгеноскопии выявляют нераскрытое кардии при акте глотания, нарушение перистальтики пищевода. Нередко обнаруживают отсутствие газового пузыря желудка и рентгенологические признаки аспирационных легочных осложнений кардиоспазма (рис. 19).
Эндоскопическое исследование пищевода позволяет выявить степень расширения его проксимальных сегментов, характер и выраженность эзофагита и метапластических изменений. Почти всегда при кардиоспазме удается пройти эндоскопом в желудок, в отличие от рака кардии и органических рубцовых стенозов (симптом Мельцера).
Манометрия пищевода позволяет подтвердить диагноз кардиоспазма и дифференцировать его от других нейромышечных заболеваний. Основной манометрический признак кардиоспазма – полное или частичное нерасслабление НПС при глотании. Часто наблюдаются повышение «давления покоя» НПС и ослабление перистальтики гладкой мускулатуры пищевода.
За рубежом для исследования опорожнения пищевода при подозрении на кардиоспазм широко применяют радионуклидное исследование (сцинтиграфию). Для этого больным дают выпить специальный раствор, содержащий радиофармпрепарат, а затем в динамике регистрируют интенсивность вызванного им гамма-излучения в гамма-камере. Это позволяет уточнить время частичного или полного опорожнения пищевода, которое при кардиоспазме, как правило, в значительной степени замедлено.



Рис. 19. Рентгенологические симптомы кардиоспазма: А – пищевод значительно расширен, удлинен и смещен вправо; дистальный его отрезок резко сужен, газовый пузырь желудка отсутствует; Б – справа в верхней доле легкого явления пневмосклероза как следствие многократных аспирационных пневмоний. (Приводится по: Е.М. Каган. Рентгенодиагностика заболеваний пищевода. М., 1968)
Дифференциальная диагностика
Кардиоспазм дифференцируют с опухолями пищевода и кардиального отдела желудка, рубцовыми стенозами и дивертикулами пищевода, грыжей пищеводного отверстия диафрагмы (ГПОД). Все эти заболевания имеют сходную клиническую симптоматику, а в качестве ведущего симптома выступает дисфагия.
Злокачественные опухоли пищевода и кардии встречаются значительно чаще кардиоспазма. Обычно заболевают люди старше 50–60 лет, тогда как ахалазией страдают более молодые пациенты. Рак развивается в течение нескольких месяцев и сопровождается прогрессирующей дисфагией, параллельным ухудшением общего состояния (нарастанием слабости, потери массы тела, вплоть до истощения, анемии), тогда как кардиоспазм – длительное заболевание с медленным течением и годами сохраняющимся хорошим общим состоянием пациентов.
Сужение кардии при раке может сопровождаться супрастенотическим расширением пищевода, что бывает и при кардиоспазме. Однако для рака характерно нарушение целости контура стенки пищевода и желудка с образованием дефекта наполнения. Стенозированный участок при этом бывает неровным, нечетким, как бы изъеденным. Эвакуация бария в желудок происходит непрерывной суженной струйкой. Газовый пузырь желудка при раке, в отличие от кардиоспазма, хорошо выявляется (рис. 20).

Рис. 20. Сужение пищеводножелудочного перехода при раке кардиального отдела желудка. Газовый пузырь желудка виден отчетливо. (Приводится по: Б. Е. Петерсон. Рак проксимального отдела желудка. 1972)
При ГПОД более выражен болевой синдром, жгучие боли локализуются за грудиной и в эпигастрии. Дисфагия редко бывает тяжелой, регургитация обычно отсутствует. В рентгенологической картине может быть сходство с кардиоспазмом I стадии. Для дифференциальной диагностики необходимо провести исследование в горизонтальном положении, при котором легко можно увидеть скользящую ГПОД. У некоторых больных симптомы дивертикула пищевода сходны с таковыми при кардиоспазме. Точный диагноз можно поставить на основании рентгенологического исследования.
В сложных и диагностически неясных случаях для уточнения диагноза показано проведение КТ грудной и брюшной полости, а также эндосонографии пищевода.
Злокачественные опухоли пищевода и кардии встречаются значительно чаще кардиоспазма. Обычно заболевают люди старше 50–60 лет, тогда как ахалазией страдают более молодые пациенты. Рак развивается в течение нескольких месяцев и сопровождается прогрессирующей дисфагией, параллельным ухудшением общего состояния (нарастанием слабости, потери массы тела, вплоть до истощения, анемии), тогда как кардиоспазм – длительное заболевание с медленным течением и годами сохраняющимся хорошим общим состоянием пациентов.
Сужение кардии при раке может сопровождаться супрастенотическим расширением пищевода, что бывает и при кардиоспазме. Однако для рака характерно нарушение целости контура стенки пищевода и желудка с образованием дефекта наполнения. Стенозированный участок при этом бывает неровным, нечетким, как бы изъеденным. Эвакуация бария в желудок происходит непрерывной суженной струйкой. Газовый пузырь желудка при раке, в отличие от кардиоспазма, хорошо выявляется (рис. 20).

Рис. 20. Сужение пищеводножелудочного перехода при раке кардиального отдела желудка. Газовый пузырь желудка виден отчетливо. (Приводится по: Б. Е. Петерсон. Рак проксимального отдела желудка. 1972)
При ГПОД более выражен болевой синдром, жгучие боли локализуются за грудиной и в эпигастрии. Дисфагия редко бывает тяжелой, регургитация обычно отсутствует. В рентгенологической картине может быть сходство с кардиоспазмом I стадии. Для дифференциальной диагностики необходимо провести исследование в горизонтальном положении, при котором легко можно увидеть скользящую ГПОД. У некоторых больных симптомы дивертикула пищевода сходны с таковыми при кардиоспазме. Точный диагноз можно поставить на основании рентгенологического исследования.
В сложных и диагностически неясных случаях для уточнения диагноза показано проведение КТ грудной и брюшной полости, а также эндосонографии пищевода.
Лечение
При I–II стадиях кардиоспазма проводят консервативное лечение. Ведущее место в лечении III–IV стадии заболевания принадлежит хирургическим методам.
Консервативное лечение. Для лечения кардиоспазма применяли множество лекарственных препаратов из самых разных фармакологических групп. Однако более или менее клинически успешным оказалось использование только двух из них: нитратов и блокаторов кальциевых каналов. Эти препараты снижают тонус НПС и облегчают глотание. Считается, что нитраты более эффективны, но имеют труднопереносимый побочный эффект – сильную головную боль. Блокаторы кальциевых каналов (нифедипин, дилтиазем) переносятся больными существенно лучше. Новейшие исследования доказывают перспективность использования силденафила (виагры) в терапии нейромышечных заболеваний пищевода.
Лекарственное лечение кардиоспазма лучше применять на ранних стадиях и при так называемом первом типе болезни, когда перистальтика гладкой мускулатуры пищевода еще сохранена.
На практике, когда лекарственное лечение не дает должного клинического эффекта (а это бывает нередко), «стартовым» методом лечения наиболее часто является кардиодилатация (КД). Сущность ее заключается в насильственном растяжении и частичном разрыве мускулатуры дистального сегмента пищевода.
В прошлом широко применялся металлический кардиодилататор Штарка, в котором есть 4 расширяющиеся бранши, присоединенные к металлическому стержню. На противоположном конце укреплена рукоятка с кремальерой, обеспечивающей дозированное раскрытие браншей (рис. 21).
Современные кардиодилататоры состоят из резинового или полихлорвинилового зонда с укрепленным на его конце баллоном (рис. 22).
Дилататор вводят под рентгенологическим или эндоскопическим контролем. Баллон наполняют воздухом или водой; при этом достигают определенного уровня давления. Технические детали вмешательства (вид анестезии, длительность экспозиции дилататора, режим повторных КД) широко варьируют в разных клиниках. Так, в нашей клинике в течение многих лет с успехом применялась КД резиновым гидродилататором под давлением 300 мм рт. ст. с экспозицией 1 час. Вмешательство осуществлялось под общей анестезией.

Рис. 21. Кардиодилататор Штарка. (Приводится по: 0. Д. Федорова. Кардиоспазм. М., 1973)
В большинстве случаев после КД наблюдается улучшение в виде облегчения глотания и регресса других симптомов заболевания. В поздних стадиях кардиоспазма (III–IV) нередко возникают показания к операции, поскольку КД малоэффективна или опасна ввиду высокого риска разрыва пищевода.
Наиболее распространенными операциями при кардиоспазме являются эзофагокардиомиотомия (операция Геллера) и ее многочисленные модификации. Рассечение мышечной оболочки дистального отрезка пищевода устраняет нерасслабление НПС при глотании. Современный вариант операции Геллера предусматривает рассечение мышечной оболочки вертикальным разрезом на передней стенке пищевода с небольшим (1–2 см) заходом на кардию (рис. 23).

Рис. 22. Баллонный пневмокардиодилататор, надеваемый на дистальную часть эндоскопа.
(Приводится по: Ю.И. Галлингера, Э.А. Годжелло. Оперативная эндоскопия пищевода. М., 1999)
Многие хирурги для достижения более надежного результата иссекают полоску пищеводной стенки. Эзофагокардиомиотомию можно выполнять как абдоминальным, так и торакальным доступом.
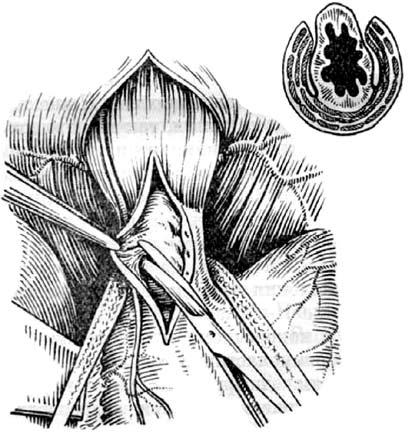
Рис. 23. Эзофагокардиомиотомия по Геллеру. Этап отделения слизистой оболочки от мышечного слоя пищевода и кардии. (Приводится по: А. А. Шалимов и соавт. Хирургия пищевода. М., 1975)
Однако технически безупречное производство операции Геллера возможно далеко не всегда. При значительных склеротических изменениях стенки пищевода полноценную миотомию выполнить трудно. Высок риск случайного повреждения слизистой, что приводит к развитию после операции медиастинита и/или перитонита. В отдаленном периоде может образоваться эпифренальный дивертикул пищевода вследствие пролабирования слизистой через миотомическое отверстие. Нередко возникает ретракция рассеченных тканей с дальнейшим рубцеванием, что ведет к рецидиву дисфагии. Избыточная миотомия влечет за собой развитие тяжелого рефлюкс-эзофагита. Для устранения недостатков оригинальной операции были предложены ее модификации, которые предусматривали укрытие миотомического отверстия: при способе Б. В. Петровского – лоскутом, выкроенным из диафрагмы, В. И. Колесова – сальником на ножке (рис. 24 и 25).
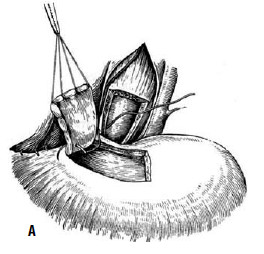
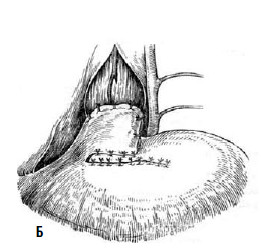
Рис. 24. Эзофагокардиопластика диафрагмальным лоскутом по Б.В. Петровскому: А – иссечен участок мышечного слоя пищевода, сформирован диафрагмальный лоскут, начато подшивание последнего к мышечным краям пищевода; Б – лоскут фиксирован, дефект в диафрагме ушит. (Приводится по: О. Д. Федорова. Кардиоспазм. М., 1973)
Однако отдаленные исходы и таких операций оказались не очень хорошими – в первую очередь, вследствие грубого рубцевания перемещенных лоскутов. Гораздо лучшим способом оказалось укрытие линии разреза передней стенкой дна желудка, которую поворачивают на 180♦ (рис. 26).

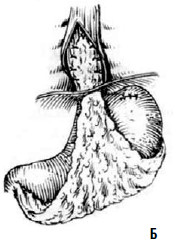
Рис. 25. Эзофагокардиомиотомия с оментопластикой по В. И. Колесову:
А – подшивание сальника к краям рассеченных мышц пищевода; Б – окончательный вид операции. (Приводится по: А.А. Шалимов и соавт. Хирургия пищевода. М., 1975)
Эта операция позволяет сделать угол Гиса более острым и тем самым уменьшить риск развития недостаточности кардии и пептического эзофагита в послеоперационном периоде.
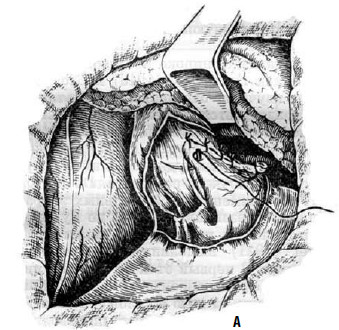
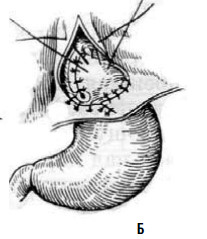
Рис. 26. Эзофагокардиомиотомия с частичной фундопликацией по методике Т. А. Суворовой: А – подшивание дна желудка к краям рассеченных мышц пищевода; Б – окончательный вид операции. (Приводится по: А. А. Шалимов и соавт. Хирургия пищевода. М., 1975)
Очень серьезным достижением последних десятилетий явилась разработка методики выполнения такой операции при помощи эндовидеохирургической техники. Во многих зарубежных клиниках в настоящее время лапароскопическая эзофагокардиомиотомия с частичной фундопликацией является «золотым стандартом» хирургического вмешательства при кардиоспазме.
Однако на поздних стадиях заболевания (III–IV) эзофагомиотомию выполнять не следует, поскольку у таких больных весь пищевод патологически изменен, а перистальтика его резко ослаблена или отсутствует. Тогда патогенетически обоснованным методом лечения является субтотальная резекция или экстирпация пищевода с его одноэтапной пластикой, как правило, желудочным трансплантатом. Резекционное вмешательство показано также после неэффективной миотомии и при развитии пептической стриктуры пищевода (как осложнение рефлюкс-эзофагита). Опыт нашей клиники показал хорошие непосредственные и отдаленные результаты таких операций.
Таким образом, как уже указывалось, в самых общих чертах можно сформулировать зависимость метода лечения кардиоспазма от стадии заболевания: в I стадии – применяют лекарственное лечение, во II–III – КД, в III–IV – хирургическое вмешательство.
Консервативное лечение. Для лечения кардиоспазма применяли множество лекарственных препаратов из самых разных фармакологических групп. Однако более или менее клинически успешным оказалось использование только двух из них: нитратов и блокаторов кальциевых каналов. Эти препараты снижают тонус НПС и облегчают глотание. Считается, что нитраты более эффективны, но имеют труднопереносимый побочный эффект – сильную головную боль. Блокаторы кальциевых каналов (нифедипин, дилтиазем) переносятся больными существенно лучше. Новейшие исследования доказывают перспективность использования силденафила (виагры) в терапии нейромышечных заболеваний пищевода.
Лекарственное лечение кардиоспазма лучше применять на ранних стадиях и при так называемом первом типе болезни, когда перистальтика гладкой мускулатуры пищевода еще сохранена.
На практике, когда лекарственное лечение не дает должного клинического эффекта (а это бывает нередко), «стартовым» методом лечения наиболее часто является кардиодилатация (КД). Сущность ее заключается в насильственном растяжении и частичном разрыве мускулатуры дистального сегмента пищевода.
В прошлом широко применялся металлический кардиодилататор Штарка, в котором есть 4 расширяющиеся бранши, присоединенные к металлическому стержню. На противоположном конце укреплена рукоятка с кремальерой, обеспечивающей дозированное раскрытие браншей (рис. 21).
Современные кардиодилататоры состоят из резинового или полихлорвинилового зонда с укрепленным на его конце баллоном (рис. 22).
Дилататор вводят под рентгенологическим или эндоскопическим контролем. Баллон наполняют воздухом или водой; при этом достигают определенного уровня давления. Технические детали вмешательства (вид анестезии, длительность экспозиции дилататора, режим повторных КД) широко варьируют в разных клиниках. Так, в нашей клинике в течение многих лет с успехом применялась КД резиновым гидродилататором под давлением 300 мм рт. ст. с экспозицией 1 час. Вмешательство осуществлялось под общей анестезией.

Рис. 21. Кардиодилататор Штарка. (Приводится по: 0. Д. Федорова. Кардиоспазм. М., 1973)
В большинстве случаев после КД наблюдается улучшение в виде облегчения глотания и регресса других симптомов заболевания. В поздних стадиях кардиоспазма (III–IV) нередко возникают показания к операции, поскольку КД малоэффективна или опасна ввиду высокого риска разрыва пищевода.
Наиболее распространенными операциями при кардиоспазме являются эзофагокардиомиотомия (операция Геллера) и ее многочисленные модификации. Рассечение мышечной оболочки дистального отрезка пищевода устраняет нерасслабление НПС при глотании. Современный вариант операции Геллера предусматривает рассечение мышечной оболочки вертикальным разрезом на передней стенке пищевода с небольшим (1–2 см) заходом на кардию (рис. 23).

Рис. 22. Баллонный пневмокардиодилататор, надеваемый на дистальную часть эндоскопа.
(Приводится по: Ю.И. Галлингера, Э.А. Годжелло. Оперативная эндоскопия пищевода. М., 1999)
Многие хирурги для достижения более надежного результата иссекают полоску пищеводной стенки. Эзофагокардиомиотомию можно выполнять как абдоминальным, так и торакальным доступом.

Рис. 23. Эзофагокардиомиотомия по Геллеру. Этап отделения слизистой оболочки от мышечного слоя пищевода и кардии. (Приводится по: А. А. Шалимов и соавт. Хирургия пищевода. М., 1975)
Однако технически безупречное производство операции Геллера возможно далеко не всегда. При значительных склеротических изменениях стенки пищевода полноценную миотомию выполнить трудно. Высок риск случайного повреждения слизистой, что приводит к развитию после операции медиастинита и/или перитонита. В отдаленном периоде может образоваться эпифренальный дивертикул пищевода вследствие пролабирования слизистой через миотомическое отверстие. Нередко возникает ретракция рассеченных тканей с дальнейшим рубцеванием, что ведет к рецидиву дисфагии. Избыточная миотомия влечет за собой развитие тяжелого рефлюкс-эзофагита. Для устранения недостатков оригинальной операции были предложены ее модификации, которые предусматривали укрытие миотомического отверстия: при способе Б. В. Петровского – лоскутом, выкроенным из диафрагмы, В. И. Колесова – сальником на ножке (рис. 24 и 25).


Рис. 24. Эзофагокардиопластика диафрагмальным лоскутом по Б.В. Петровскому: А – иссечен участок мышечного слоя пищевода, сформирован диафрагмальный лоскут, начато подшивание последнего к мышечным краям пищевода; Б – лоскут фиксирован, дефект в диафрагме ушит. (Приводится по: О. Д. Федорова. Кардиоспазм. М., 1973)
Однако отдаленные исходы и таких операций оказались не очень хорошими – в первую очередь, вследствие грубого рубцевания перемещенных лоскутов. Гораздо лучшим способом оказалось укрытие линии разреза передней стенкой дна желудка, которую поворачивают на 180♦ (рис. 26).


Рис. 25. Эзофагокардиомиотомия с оментопластикой по В. И. Колесову:
А – подшивание сальника к краям рассеченных мышц пищевода; Б – окончательный вид операции. (Приводится по: А.А. Шалимов и соавт. Хирургия пищевода. М., 1975)
Эта операция позволяет сделать угол Гиса более острым и тем самым уменьшить риск развития недостаточности кардии и пептического эзофагита в послеоперационном периоде.


Рис. 26. Эзофагокардиомиотомия с частичной фундопликацией по методике Т. А. Суворовой: А – подшивание дна желудка к краям рассеченных мышц пищевода; Б – окончательный вид операции. (Приводится по: А. А. Шалимов и соавт. Хирургия пищевода. М., 1975)
Очень серьезным достижением последних десятилетий явилась разработка методики выполнения такой операции при помощи эндовидеохирургической техники. Во многих зарубежных клиниках в настоящее время лапароскопическая эзофагокардиомиотомия с частичной фундопликацией является «золотым стандартом» хирургического вмешательства при кардиоспазме.
Однако на поздних стадиях заболевания (III–IV) эзофагомиотомию выполнять не следует, поскольку у таких больных весь пищевод патологически изменен, а перистальтика его резко ослаблена или отсутствует. Тогда патогенетически обоснованным методом лечения является субтотальная резекция или экстирпация пищевода с его одноэтапной пластикой, как правило, желудочным трансплантатом. Резекционное вмешательство показано также после неэффективной миотомии и при развитии пептической стриктуры пищевода (как осложнение рефлюкс-эзофагита). Опыт нашей клиники показал хорошие непосредственные и отдаленные результаты таких операций.
Таким образом, как уже указывалось, в самых общих чертах можно сформулировать зависимость метода лечения кардиоспазма от стадии заболевания: в I стадии – применяют лекарственное лечение, во II–III – КД, в III–IV – хирургическое вмешательство.
Рубцовые стриктуры пищевода
Рубцовые стриктуры (сужения) пищевода (РСП) являются осложнением острых и хронических воспалительных процессов пищевода различной природы. Наиболее часто они развиваются в исходе коррозивного эзофагита, обусловленного химическим ожогом, и рефлюкс-эзофагита, вызванного забросом агрессивного желудочного и/или кишечного содержимого на фоне несостоятельности пищеводно-желудочного замыкательного механизма. Нередко наблюдаются и послеоперационные стриктуры пищевода, а точнее – пищеводных анастомозов.
Эзофагиты другой этиологии как причина РСП встречаются значительно реже (при туберкулезе, сифилисе, дифтерии, системных заболеваниях соединительной ткани – чаще склеродермии, радиационном поражении и др.).
Эзофагиты другой этиологии как причина РСП встречаются значительно реже (при туберкулезе, сифилисе, дифтерии, системных заболеваниях соединительной ткани – чаще склеродермии, радиационном поражении и др.).
Этиология и патогенез
Послеожоговые РСП являются осложнением химических ожогов пищевода. Последние возникают в результате случайного или преднамеренного (например, с целью самоубийства) приема едких веществ (кислот, щелочей и других химически агрессивных субстанций), обычно в жидком виде. В прошлом нередко встречались ожоги пищевода каустической содой, уксусной эссенцией, серной кислотой. В настоящее время чаще наблюдаются ожоги чистящими жидкостями, раствором аммиака, электролитом для заправки аккумуляторных батарей. Ожоги щелочами протекают в целом более тяжело, так как при этом формируется глубокий колликвационный (влажный) некроз, поражающий не только всю толщу пищеводной стенки, но и нередко распространяющийся на окружающую клетчатку и соседние органы. При ожогах кислотами образуется коагуляционный (сухой) некроз в виде плотного струпа, который в какой-то мере ограничивает дальнейшее проникновение кислоты в более глубоко лежащие ткани.
В течении ожоговой болезни выделяют IV периода. Первые 3 периода продолжаются по 2 недели, IV период от 2 недель до 2 лет:
I период – гиперемия, отек, некроз;
II период – формирование ожогового струпа;
III период – отторжение ожогового струпа;
IV период – формирование рубцовой стриктуры.
Различают три степени тяжести химического ожога пищевода.
I степень характеризуется поражением поверхностных слоев эпителия слизистой пищевода. Вследствие ожога развивается десквамативный эзофагит, в исходе которого, как правило, происходит полное выздоровление. При II степени ожога слизистая поражается на всю глубину с частичным вовлечением подслизистого слоя. Развивается язвенно-некротический эзофагит, а впоследствии – послеожоговая РСП. При III степени наблюдается поражение всех слоев стенки пищевода, нередко некроз распространяется на параэзофагеальную клетчатку, трахею, плевру, перикард и другие органы. Иногда наступает перфорация пищевода как следствие деструкции стенки органа. Тяжесть ожога зависит от характера, концентрации и количества выпитой агрессивной жидкости.
В клинической картине ожога пищевода преобладают сильные жгучие боли в полости рта, за грудиной и в эпигастрии, осиплость голоса, одышка, сильное слюнотечение. Вскоре после приема агрессивной жидкости развивается тяжелая дисфагия; попытка проглатывания жидкости резко болезненна. Часто бывает многократная болезненная рвота. Развивается картина интоксикации, вызванная резорбтивным действием яда. Нарастают гипертермия, олигоанурия. Ряд больных погибает именно от нарастания полиорганной недостаточности в первые часы после ожоговой травмы. Перфорация пищевода (или желудка) при III степени ожога резко ухудшает прогноз.
Если осложнения не развились, состояние больных к концу первой недели после ожоговой травмы заметно улучшается. Уменьшается интенсивность болей, саливация и жажда, улучшаются самочувствие и сон. Больные начинают глотать жидкую и густую пищу. Лишь с шестой-седьмой недели дисфагия возникает вновь, свидетельствуя о формировании РСП.
Задача инструментальных методов диагностики в первые дни после ожога пищевода состоит в том, чтобы исключить развитие жизнеопасных осложнений. Рентгеноскопия пищевода осуществляется, как правило, с водорастворимым контрастом и служит для диагностики перфорации пищевода и пищеводно-респираторных свищей. Эндоскопическое исследование многие специалисты считают противопоказанным (значительный риск перфорации!), хотя в ряде клиник оно используется для диагностики III степени ожога пищевода и особенно желудка, когда ранняя операция может предупредить развитие перфоративного медиастинита и/или перитонита. Обзорная рентгенография и ультразвуковое сканирование грудной клетки помогают установить диагноз плеврита и перикардита.
Первая помощь при химическом ожоге пищевода направлена на уменьшение агрессивных свойств токсического вещества. До прибытия «скорой помощи» больной должен прополоскать рот большим количеством воды, затем выпить воды и вызвать рвоту, повторяя эти действия несколько раз. Врачебная помощь заключается во введении анальгетиков (при возможности наркотических), седативных средств и промывании желудка через тонкий резиновый зонд, введенный через нос. Пациенты с химической травмой пищевода нуждаются в госпитализации, оптимально – в токсикологическое или реанимационное отделение. Там им проводят комплексное консервативное лечение (форсированный диурез, при необходимости – аппаратные методики детоксикации, антибактериальную терапию, введение кортикостероидов и т. д). По мере выведения больного из тяжелого состояния и формирования РСП к лечению подключается хирург.
Чтобы предупредить развитие РСП и уменьшить выраженность рубцового процесса, возможно применение раннего (профилактического) бужирования пищевода, начиная с 5 по 10 сутки после ожога. Определенный эффект оказывают протеолитические ферменты (лидаза), кортикостероиды и гипербарическая оксигенация.
Пептические стриктуры пищевода являются осложнением рефлюкс-эзофагита. В свою очередь, рефлюкс-эзофагит вызывается различными нарушениями замыкательного аппарата пищеводнокардиальной области, среди которых наиболее часто встречаются грыжи пищеводного отверстия диафрагмы (ГПОД). У ряда больных рефлюкс-эзофагит развивается после операций на пищеводе и желудке (гастрэктомии, проксимальной резекции желудка, резекции пищевода, эзофагокардиомиотомии и др.). При длительном течении эзофагита воспалительный процесс распространяется на мышечный слой и даже на параэзофагеальную клетчатку с формированием РСП. Кроме того, стриктура может развиться при заживлении пептической язвы пищевода.
Обычно образование пептической РСП – процесс довольно длительный (в сравнении с послеожоговым сужением), растянутый на месяцы и годы. Однако в ряде случаев он развивается стремительно, например, при длительном стояния назогастрального зонда, обычно у больных, перенесших операции на органах брюшной полости с тяжелым, осложненным течением послеоперационного периода.
Послеоперационные рубцовые стриктуры чаще всего являются сужениями не самого пищевода, а анастомозов пищевода с желудком или кишкой, накладываемых при гастрэктомии, проксимальной резекции желудка или резекции пищевода. Причины их развития разнообразны: технические погрешности при формировании анастомоза (избыточная или недостаточная мобилизация сшиваемых органов, вовлечение в шов большого массива тканей, применение слишком толстых и грубых нитей и т. д.), вторичное заживление несостоятельности швов, значительная ишемия тканей в зоне соустья, индивидуальная реакция на шовный материал.
Нередко в клинической практике встречаются ситуации, когда в патогенезе РСП участвуют различные факторы. Так, в процессе формирования дистальной послеожоговой стриктуры пищевода вследствие вторичного укорочения пищевода развивается ГПОД. После проведенного бужирования просвет пищевода восстанавливается, но очень скоро стриктура рецидивирует, но уже не как ожоговая, а как пептическая, поскольку антирефлюксный механизм, ввиду повреждения дистального сегмента пищевода, резко нарушен.
В течении ожоговой болезни выделяют IV периода. Первые 3 периода продолжаются по 2 недели, IV период от 2 недель до 2 лет:
I период – гиперемия, отек, некроз;
II период – формирование ожогового струпа;
III период – отторжение ожогового струпа;
IV период – формирование рубцовой стриктуры.
Различают три степени тяжести химического ожога пищевода.
I степень характеризуется поражением поверхностных слоев эпителия слизистой пищевода. Вследствие ожога развивается десквамативный эзофагит, в исходе которого, как правило, происходит полное выздоровление. При II степени ожога слизистая поражается на всю глубину с частичным вовлечением подслизистого слоя. Развивается язвенно-некротический эзофагит, а впоследствии – послеожоговая РСП. При III степени наблюдается поражение всех слоев стенки пищевода, нередко некроз распространяется на параэзофагеальную клетчатку, трахею, плевру, перикард и другие органы. Иногда наступает перфорация пищевода как следствие деструкции стенки органа. Тяжесть ожога зависит от характера, концентрации и количества выпитой агрессивной жидкости.
В клинической картине ожога пищевода преобладают сильные жгучие боли в полости рта, за грудиной и в эпигастрии, осиплость голоса, одышка, сильное слюнотечение. Вскоре после приема агрессивной жидкости развивается тяжелая дисфагия; попытка проглатывания жидкости резко болезненна. Часто бывает многократная болезненная рвота. Развивается картина интоксикации, вызванная резорбтивным действием яда. Нарастают гипертермия, олигоанурия. Ряд больных погибает именно от нарастания полиорганной недостаточности в первые часы после ожоговой травмы. Перфорация пищевода (или желудка) при III степени ожога резко ухудшает прогноз.
Если осложнения не развились, состояние больных к концу первой недели после ожоговой травмы заметно улучшается. Уменьшается интенсивность болей, саливация и жажда, улучшаются самочувствие и сон. Больные начинают глотать жидкую и густую пищу. Лишь с шестой-седьмой недели дисфагия возникает вновь, свидетельствуя о формировании РСП.
Задача инструментальных методов диагностики в первые дни после ожога пищевода состоит в том, чтобы исключить развитие жизнеопасных осложнений. Рентгеноскопия пищевода осуществляется, как правило, с водорастворимым контрастом и служит для диагностики перфорации пищевода и пищеводно-респираторных свищей. Эндоскопическое исследование многие специалисты считают противопоказанным (значительный риск перфорации!), хотя в ряде клиник оно используется для диагностики III степени ожога пищевода и особенно желудка, когда ранняя операция может предупредить развитие перфоративного медиастинита и/или перитонита. Обзорная рентгенография и ультразвуковое сканирование грудной клетки помогают установить диагноз плеврита и перикардита.
Первая помощь при химическом ожоге пищевода направлена на уменьшение агрессивных свойств токсического вещества. До прибытия «скорой помощи» больной должен прополоскать рот большим количеством воды, затем выпить воды и вызвать рвоту, повторяя эти действия несколько раз. Врачебная помощь заключается во введении анальгетиков (при возможности наркотических), седативных средств и промывании желудка через тонкий резиновый зонд, введенный через нос. Пациенты с химической травмой пищевода нуждаются в госпитализации, оптимально – в токсикологическое или реанимационное отделение. Там им проводят комплексное консервативное лечение (форсированный диурез, при необходимости – аппаратные методики детоксикации, антибактериальную терапию, введение кортикостероидов и т. д). По мере выведения больного из тяжелого состояния и формирования РСП к лечению подключается хирург.
Чтобы предупредить развитие РСП и уменьшить выраженность рубцового процесса, возможно применение раннего (профилактического) бужирования пищевода, начиная с 5 по 10 сутки после ожога. Определенный эффект оказывают протеолитические ферменты (лидаза), кортикостероиды и гипербарическая оксигенация.
Пептические стриктуры пищевода являются осложнением рефлюкс-эзофагита. В свою очередь, рефлюкс-эзофагит вызывается различными нарушениями замыкательного аппарата пищеводнокардиальной области, среди которых наиболее часто встречаются грыжи пищеводного отверстия диафрагмы (ГПОД). У ряда больных рефлюкс-эзофагит развивается после операций на пищеводе и желудке (гастрэктомии, проксимальной резекции желудка, резекции пищевода, эзофагокардиомиотомии и др.). При длительном течении эзофагита воспалительный процесс распространяется на мышечный слой и даже на параэзофагеальную клетчатку с формированием РСП. Кроме того, стриктура может развиться при заживлении пептической язвы пищевода.
Обычно образование пептической РСП – процесс довольно длительный (в сравнении с послеожоговым сужением), растянутый на месяцы и годы. Однако в ряде случаев он развивается стремительно, например, при длительном стояния назогастрального зонда, обычно у больных, перенесших операции на органах брюшной полости с тяжелым, осложненным течением послеоперационного периода.
Послеоперационные рубцовые стриктуры чаще всего являются сужениями не самого пищевода, а анастомозов пищевода с желудком или кишкой, накладываемых при гастрэктомии, проксимальной резекции желудка или резекции пищевода. Причины их развития разнообразны: технические погрешности при формировании анастомоза (избыточная или недостаточная мобилизация сшиваемых органов, вовлечение в шов большого массива тканей, применение слишком толстых и грубых нитей и т. д.), вторичное заживление несостоятельности швов, значительная ишемия тканей в зоне соустья, индивидуальная реакция на шовный материал.
Нередко в клинической практике встречаются ситуации, когда в патогенезе РСП участвуют различные факторы. Так, в процессе формирования дистальной послеожоговой стриктуры пищевода вследствие вторичного укорочения пищевода развивается ГПОД. После проведенного бужирования просвет пищевода восстанавливается, но очень скоро стриктура рецидивирует, но уже не как ожоговая, а как пептическая, поскольку антирефлюксный механизм, ввиду повреждения дистального сегмента пищевода, резко нарушен.
Классификация
Классифицируют РСП по различным признакам (локализация и выраженность сужения, характер его, количество стриктур, наличие осложнений и др.).
Так, например, в классификации послеожоговых РСП Э. Н. Ванцяна и РА. Тощакова (1971) различают высокие стриктуры – глоточные, шейные, бифуркационные – и низкие – расположенные от эпифренальной части пищевода (т. е. нижнегрудного отдела) до кардии. По протяженности выделяют короткие (до 3 см) и трубчатые (более 3 см) стриктуры. Наконец, РСП бывают одиночными и множественными (двойной, тройной локализации и более).
Более подробную классификацию послеожоговых РСП предложили Г. Л. Ратнер и В. И. Белоконев (1982). Она является составной частью классификации так называемой послеожоговой непроходимости пищевода, которая бывает не только механической (обусловленной собственно стриктурой), но и функциональной (анорексия, функциональная дисфагия). Авторы классифицируют непроходимость пищевода по этиологии (ожоги кислотами, щелочами и другими агрессивными агентами); по времени развития (ранняя – до 4 недель, поздняя – позже 4 недель). Послеожоговые РСП разделяют так:
1. По степени сужения (соответственно выраженности дисфагии).
2. По локализации стриктуры:
а) высокие – устье пищевода, шейный отдел;
б) срединные – аортальные, бифуркационные;
в) низкие – эпифренальные, кардиальные;
г) комбинированные – пищевода и желудка.
3. По протяженности:
а) короткие: мембранозные, циркулярные (менее 3 см);
б) трубчатые (более 3 см);
в) четкообразные;
г) тотальные.
4. По форме супрастенотического расширения:
а) коническая;
б) мешотчатая.
5. По наличию осложнений:
а) ложные ходы в средостение;
б) дивертикулы пищевода;
в) рубцовое укорочение пищевода;
г) пищеводно-респираторные свищи.
Классификация пептических стриктур пищевода, по сравнению с послеожоговыми, значительно проще. Так, А. Ф. Черноусов и соавт. (1999) считают принципиально важным деление пептических стриктур на короткие (до 3 см) и протяженные (более 3 см), а также на первичные (развиваются как осложнение рефлюкс-эзофагита на почве ГПОД) и вторичные (являются осложнением безуспешных, часто повторных, хирургических вмешательств на кардии).
Так, например, в классификации послеожоговых РСП Э. Н. Ванцяна и РА. Тощакова (1971) различают высокие стриктуры – глоточные, шейные, бифуркационные – и низкие – расположенные от эпифренальной части пищевода (т. е. нижнегрудного отдела) до кардии. По протяженности выделяют короткие (до 3 см) и трубчатые (более 3 см) стриктуры. Наконец, РСП бывают одиночными и множественными (двойной, тройной локализации и более).
Более подробную классификацию послеожоговых РСП предложили Г. Л. Ратнер и В. И. Белоконев (1982). Она является составной частью классификации так называемой послеожоговой непроходимости пищевода, которая бывает не только механической (обусловленной собственно стриктурой), но и функциональной (анорексия, функциональная дисфагия). Авторы классифицируют непроходимость пищевода по этиологии (ожоги кислотами, щелочами и другими агрессивными агентами); по времени развития (ранняя – до 4 недель, поздняя – позже 4 недель). Послеожоговые РСП разделяют так:
1. По степени сужения (соответственно выраженности дисфагии).
2. По локализации стриктуры:
а) высокие – устье пищевода, шейный отдел;
б) срединные – аортальные, бифуркационные;
в) низкие – эпифренальные, кардиальные;
г) комбинированные – пищевода и желудка.
3. По протяженности:
а) короткие: мембранозные, циркулярные (менее 3 см);
б) трубчатые (более 3 см);
в) четкообразные;
г) тотальные.
4. По форме супрастенотического расширения:
а) коническая;
б) мешотчатая.
5. По наличию осложнений:
а) ложные ходы в средостение;
б) дивертикулы пищевода;
в) рубцовое укорочение пищевода;
г) пищеводно-респираторные свищи.
Классификация пептических стриктур пищевода, по сравнению с послеожоговыми, значительно проще. Так, А. Ф. Черноусов и соавт. (1999) считают принципиально важным деление пептических стриктур на короткие (до 3 см) и протяженные (более 3 см), а также на первичные (развиваются как осложнение рефлюкс-эзофагита на почве ГПОД) и вторичные (являются осложнением безуспешных, часто повторных, хирургических вмешательств на кардии).
