Функция: моноциты мигрируют в соединительную ткань, где дифференцируются в макрофаги и фагоцитируют чужеродные агенты и вещества;
– влияют на иммунные процессы, способствуя продукции антител иммунокомпетентными клетками (плазмоцитами);
– осуществляют захват и внутриклеточное переваривание различных стареющих и погибших клеток и постклеточных структур (в том числе форменных элементов крови), а также их фрагментов;
– секретирует различные вещества, регулирующие состояние межклеточного вещества (лизосомальные протеазы, коллагеназы, эластазы и др.) и функциональную активность и пролиферацию клеток других типов (монокины).
Лимфоцит (lymphocytus) – это сферическая мелкая клетка диаметром 8—10 мкм; окрашенное ядро занимает большую часть клетки, оставляя узкий ободок светлой голубой цитоплазмы на периферии (рис. 5.2).
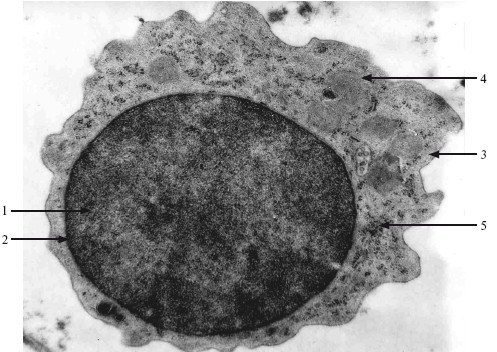
Рис. 5.2. Лимфоцит. ТЭМ. ×18 000.
1 – ядро; 2 – гетерохроматин; 3 – цитоплазма; 4 – митохондрия; 5 – рибосомы.
Ультраструктура: небольшое количество митохондрий, слаборазвитый комплекс Гольджи, почти нет гранулярной эндоплазматической сети, но большое количество свободных рибосом. Присутствует также некоторое количество лизосом (азурофильные гранулы диаметром 0,5 мкм).
Лимфоциты – единственные клетки крови, способные при определенных условиях митотически делиться.
Лимфоциты – весьма гетерогенная (неоднородная) популяция клеток.
Классификация лимфоцитов: 1) по размерам и морфологии; 2) по генезису (особенностям развития); 3) по функции; 4) по рецепторам к антигенам; 5) по продолжительности жизни.
По размерам лимфоциты подразделяются на малые – 4,5–6 мкм; средние – 7—10 мкм и большие – более 10 мкм.
В крови около 90 % малых (зрелые) и 10–12 % средних лимфоцитов. Большие (бластные) лимфоциты в нормальных условиях в крови не встречаются.
В крови взрослого человека наблюдаются также большие гранулярные лимфоциты (5—10 % от всех лимфоцитов крови) с бобовидным асимметрическим ядром и цитоплазмой, содержащей крупные азурофильные гранулы с перфорином и гранзимами, обеспечивающими цитотоксическую активность этих клеток. Они выполняют функцию NK-клеток, или естественных киллеров, – особой разновидности эффекторных клеток иммунной системы.
По особенностям ультраструктуры малые лимфоциты подразделяются на светлые (70–75 %) и темные (12–13 %). По источникам развития выделяют:
– Т-лимфоциты: их образование и дальнейшее развитие связано с тимусом;
– В-лимфоциты: их развитие у птиц связано со специальным органом в области задней кишки – фабрициевой сумкой, а у млекопитающих и человека – пока точно не установленным ее аналогом (скорее всего, с красным костным мозгом).
По функции:
I. Т-лимфоциты, обеспечивающие клеточный, или врожденный, иммунитет, подразделяют на субпопуляции: 1) киллеры, 2) хелперы, 3) супрессоры, 4) клетки памяти, 5) амплифайеры, 6) дифференцирующие и др.;
– Т-киллеры, или цитотоксические лимфоциты, обеспечивают защиту организма от чужеродных клеток или генетически измененных собственных клеток;
– Т-хелперы регулируют гуморальный иммунитет, усиливая деятельность В-лимфоцитов;
– Т-супрессоры также участвуют в регуляции гуморального иммунитета, угнетая функцию плазмоцитов;
– Т-клетки памяти: короткоживущие (месяцы) и долгоживущие (годы);
– Т-амплифайеры (усилители) усиливают функции Т-киллеров, хелперов, супрессоров и других иммунокомпетентных клеток;
– Т-дифференцирующие клетки оказывают влияние на пролиферацию и дифференцировку стволовых клеток.
II. В-лимфоциты, обеспечивающие гуморальный, или приобретенный, иммунитет;
– защиту организма от чужеродных корпускулярных антигенов: бактерий, вирусов, токсинов, белков и др. Среди В-лимфоцитов выделяют:
– рецепторные (нулевые) В-лимфоциты, которые выполняют только рецепторные функции, т. е. распознают соответствующий их рецепторам антиген;
– эффекторные В-лимфоциты (плазмоциты), трансформирующиеся из «нулевых» клеток под влиянием антигена в присутствии Т-хелперов и макрофагов и активно продуцирующие антитела;
– В-клетки памяти: короткоживущие (недели) и долгоживущие (месяцы).
В пределах своих субпопуляций Т– и В-лимфоциты различаются между собой по типам рецепторов к разным антигенам, образуя группы (клоны) клеток, имеющие одинаковые рецепторы. При встрече лимфоцита с антигеном, к которому у него есть рецептор, лимфоцит стимулируется, превращается в лимфобласт, а затем пролиферирует и дифференцируется, в результате чего образуется клон новых лимфоцитов с одинаковыми рецепторами.
Количество: это вторая по многочисленности популяция агранулоцитов крови – в 1 мкл от 1500 до 2500 (20–25 % от всех лейкоцитов).
Продолжительность жизни: Т-лимфоциты могут жить несколько лет, В-лимфоциты погибают через несколько месяцев.
Функция: Т-лимфоциты ответственны в первую очередь за клеточный (врожденный) иммунитет, В-лимфоциты обеспечивают гуморальный (приобретенный) иммунитет.
Тромбоцит (thrombocytus), или кровяная пластинка, – это округлый или овальный фрагмент клетки диаметром 2–4 мкм. Тромбоциты происходят от мегакариоцитов в красном костном мозге.
Кровяные пластинки имеют прозрачный периферический участок (гиаломер) и более плотный гранулярный центр (грануломер).
Гиаломер содержит актиновые микрофиламенты цитоскелета и микротрубочки, а также промежуточные филаменты; систему трубочек, соединенную с поверхностью (открытая система канальцев), обеспечивающую экзоцитоз содержимого гранул тромбоцитов, и плотную систему трубочек (которая, вероятно, накапливает и выделяет ионы кальция, а также вырабатывает простагландины);
– микротрубочки (4—15) формируют краевое кольцо по периферии цитоплазмы, служащее для поддержания формы тромбоцита;
– промежуточные филаменты образованы белком виментином.
Грануломер состоит из α-гранул (диаметр от 300 до 500 нм), плотных телец, или 5-гранул (диаметр от 250 до 300 нм), 1-гранул, редко встречающихся митохондрий, некоторого количества лизосом и частиц гликогена;
– плазмолемму покрывает гликокаликс, состоящий из гликозаминогликанов и гликопротеинов. В присутствии ионов кальция и АДФ он способствует слипанию кровяных пластинок, так что в случае необходимости они могут приклеиваться друг к другу и к стенке сосуда;
– α-гранулы содержат фибриноген, фибронектин, тромбопластин кровяных пластинок, тромбоцитарный фактор роста, тромбоглобулин, тромбоспондин и фактор свертывания V;
– плотные тельца (с плотным матриксом) содержат АДФ, АТФ, ионы кальция, магния, пирофосфат, гистамин, серотонин;
– l-гранулы (диаметр 200–250 нм) содержат гидролитические ферменты и рассматриваются как лизосомы.
Количество тромбоцитов в 1 мкл от 200 000 до 300 000 (200–300 109/л).
Продолжительность жизни менее 2 нед, ежедневно обновляется около 15 % от всех тромбоцитов.
Функция: остановка кровотечения при повреждении стенки сосудов путем свертывания крови (гемокоагуляция);
– участие в реакциях заживления ран и воспаления;
– обеспечение нормальной функции эндотелия сосудов (ангиотрофическая функция).
Анализ крови определяется такими понятиями, как гемограмма и лейкоцитарная формула.
Гемограмма – количественное содержание форменных элементов крови в 1 л или 1 мкл.
Гемограмма взрослого человека
Эритроциты:
у мужчин – 3,9–5,5 1012/л (3,9–5,5 106 в 1 мкл);
у женщин – 3,7–4,7 1012/л (3,7–4,7 106 в 1 мкл).
Лейкоциты – 3,8–9,0 109/л (3,8–9 103 в 1 мкл).
Тромбоциты: – 200–300 109 (200–300 103 в 1 мкл).
Лейкоцитарная формула – процентное содержание различный форм лейкоцитов (от общего числа лейкоцитов, принимаемого за 100 %).
Лейкоцитарная формула взрослого человека
Базофилы – 0,5–1 %.
Эозинофилы – 1–5 %.
Нейтрофилы – 65–75 %:
юные – 0–0,5 %;
палочкоядерные – 3–5 %;
сегментоядерные – 60–65 %.
Лимфоциты – 20–35 %.
Моноциты – 6–8 %.
5.1.3. Возрастные особенности крови
5.2. кроветворение
5.2.1. Гранулоцитопоэз
5.2.2. Лимфоцитопоэз
– влияют на иммунные процессы, способствуя продукции антител иммунокомпетентными клетками (плазмоцитами);
– осуществляют захват и внутриклеточное переваривание различных стареющих и погибших клеток и постклеточных структур (в том числе форменных элементов крови), а также их фрагментов;
– секретирует различные вещества, регулирующие состояние межклеточного вещества (лизосомальные протеазы, коллагеназы, эластазы и др.) и функциональную активность и пролиферацию клеток других типов (монокины).
Лимфоцит (lymphocytus) – это сферическая мелкая клетка диаметром 8—10 мкм; окрашенное ядро занимает большую часть клетки, оставляя узкий ободок светлой голубой цитоплазмы на периферии (рис. 5.2).

Рис. 5.2. Лимфоцит. ТЭМ. ×18 000.
1 – ядро; 2 – гетерохроматин; 3 – цитоплазма; 4 – митохондрия; 5 – рибосомы.
Ультраструктура: небольшое количество митохондрий, слаборазвитый комплекс Гольджи, почти нет гранулярной эндоплазматической сети, но большое количество свободных рибосом. Присутствует также некоторое количество лизосом (азурофильные гранулы диаметром 0,5 мкм).
Лимфоциты – единственные клетки крови, способные при определенных условиях митотически делиться.
Лимфоциты – весьма гетерогенная (неоднородная) популяция клеток.
Классификация лимфоцитов: 1) по размерам и морфологии; 2) по генезису (особенностям развития); 3) по функции; 4) по рецепторам к антигенам; 5) по продолжительности жизни.
По размерам лимфоциты подразделяются на малые – 4,5–6 мкм; средние – 7—10 мкм и большие – более 10 мкм.
В крови около 90 % малых (зрелые) и 10–12 % средних лимфоцитов. Большие (бластные) лимфоциты в нормальных условиях в крови не встречаются.
В крови взрослого человека наблюдаются также большие гранулярные лимфоциты (5—10 % от всех лимфоцитов крови) с бобовидным асимметрическим ядром и цитоплазмой, содержащей крупные азурофильные гранулы с перфорином и гранзимами, обеспечивающими цитотоксическую активность этих клеток. Они выполняют функцию NK-клеток, или естественных киллеров, – особой разновидности эффекторных клеток иммунной системы.
По особенностям ультраструктуры малые лимфоциты подразделяются на светлые (70–75 %) и темные (12–13 %). По источникам развития выделяют:
– Т-лимфоциты: их образование и дальнейшее развитие связано с тимусом;
– В-лимфоциты: их развитие у птиц связано со специальным органом в области задней кишки – фабрициевой сумкой, а у млекопитающих и человека – пока точно не установленным ее аналогом (скорее всего, с красным костным мозгом).
По функции:
I. Т-лимфоциты, обеспечивающие клеточный, или врожденный, иммунитет, подразделяют на субпопуляции: 1) киллеры, 2) хелперы, 3) супрессоры, 4) клетки памяти, 5) амплифайеры, 6) дифференцирующие и др.;
– Т-киллеры, или цитотоксические лимфоциты, обеспечивают защиту организма от чужеродных клеток или генетически измененных собственных клеток;
– Т-хелперы регулируют гуморальный иммунитет, усиливая деятельность В-лимфоцитов;
– Т-супрессоры также участвуют в регуляции гуморального иммунитета, угнетая функцию плазмоцитов;
– Т-клетки памяти: короткоживущие (месяцы) и долгоживущие (годы);
– Т-амплифайеры (усилители) усиливают функции Т-киллеров, хелперов, супрессоров и других иммунокомпетентных клеток;
– Т-дифференцирующие клетки оказывают влияние на пролиферацию и дифференцировку стволовых клеток.
II. В-лимфоциты, обеспечивающие гуморальный, или приобретенный, иммунитет;
– защиту организма от чужеродных корпускулярных антигенов: бактерий, вирусов, токсинов, белков и др. Среди В-лимфоцитов выделяют:
– рецепторные (нулевые) В-лимфоциты, которые выполняют только рецепторные функции, т. е. распознают соответствующий их рецепторам антиген;
– эффекторные В-лимфоциты (плазмоциты), трансформирующиеся из «нулевых» клеток под влиянием антигена в присутствии Т-хелперов и макрофагов и активно продуцирующие антитела;
– В-клетки памяти: короткоживущие (недели) и долгоживущие (месяцы).
В пределах своих субпопуляций Т– и В-лимфоциты различаются между собой по типам рецепторов к разным антигенам, образуя группы (клоны) клеток, имеющие одинаковые рецепторы. При встрече лимфоцита с антигеном, к которому у него есть рецептор, лимфоцит стимулируется, превращается в лимфобласт, а затем пролиферирует и дифференцируется, в результате чего образуется клон новых лимфоцитов с одинаковыми рецепторами.
Количество: это вторая по многочисленности популяция агранулоцитов крови – в 1 мкл от 1500 до 2500 (20–25 % от всех лейкоцитов).
Продолжительность жизни: Т-лимфоциты могут жить несколько лет, В-лимфоциты погибают через несколько месяцев.
Функция: Т-лимфоциты ответственны в первую очередь за клеточный (врожденный) иммунитет, В-лимфоциты обеспечивают гуморальный (приобретенный) иммунитет.
Тромбоцит (thrombocytus), или кровяная пластинка, – это округлый или овальный фрагмент клетки диаметром 2–4 мкм. Тромбоциты происходят от мегакариоцитов в красном костном мозге.
Кровяные пластинки имеют прозрачный периферический участок (гиаломер) и более плотный гранулярный центр (грануломер).
Гиаломер содержит актиновые микрофиламенты цитоскелета и микротрубочки, а также промежуточные филаменты; систему трубочек, соединенную с поверхностью (открытая система канальцев), обеспечивающую экзоцитоз содержимого гранул тромбоцитов, и плотную систему трубочек (которая, вероятно, накапливает и выделяет ионы кальция, а также вырабатывает простагландины);
– микротрубочки (4—15) формируют краевое кольцо по периферии цитоплазмы, служащее для поддержания формы тромбоцита;
– промежуточные филаменты образованы белком виментином.
Грануломер состоит из α-гранул (диаметр от 300 до 500 нм), плотных телец, или 5-гранул (диаметр от 250 до 300 нм), 1-гранул, редко встречающихся митохондрий, некоторого количества лизосом и частиц гликогена;
– плазмолемму покрывает гликокаликс, состоящий из гликозаминогликанов и гликопротеинов. В присутствии ионов кальция и АДФ он способствует слипанию кровяных пластинок, так что в случае необходимости они могут приклеиваться друг к другу и к стенке сосуда;
– α-гранулы содержат фибриноген, фибронектин, тромбопластин кровяных пластинок, тромбоцитарный фактор роста, тромбоглобулин, тромбоспондин и фактор свертывания V;
– плотные тельца (с плотным матриксом) содержат АДФ, АТФ, ионы кальция, магния, пирофосфат, гистамин, серотонин;
– l-гранулы (диаметр 200–250 нм) содержат гидролитические ферменты и рассматриваются как лизосомы.
Количество тромбоцитов в 1 мкл от 200 000 до 300 000 (200–300 109/л).
Продолжительность жизни менее 2 нед, ежедневно обновляется около 15 % от всех тромбоцитов.
Функция: остановка кровотечения при повреждении стенки сосудов путем свертывания крови (гемокоагуляция);
– участие в реакциях заживления ран и воспаления;
– обеспечение нормальной функции эндотелия сосудов (ангиотрофическая функция).
Анализ крови определяется такими понятиями, как гемограмма и лейкоцитарная формула.
Гемограмма – количественное содержание форменных элементов крови в 1 л или 1 мкл.
Гемограмма взрослого человека
Эритроциты:
у мужчин – 3,9–5,5 1012/л (3,9–5,5 106 в 1 мкл);
у женщин – 3,7–4,7 1012/л (3,7–4,7 106 в 1 мкл).
Лейкоциты – 3,8–9,0 109/л (3,8–9 103 в 1 мкл).
Тромбоциты: – 200–300 109 (200–300 103 в 1 мкл).
Лейкоцитарная формула – процентное содержание различный форм лейкоцитов (от общего числа лейкоцитов, принимаемого за 100 %).
Лейкоцитарная формула взрослого человека
Базофилы – 0,5–1 %.
Эозинофилы – 1–5 %.
Нейтрофилы – 65–75 %:
юные – 0–0,5 %;
палочкоядерные – 3–5 %;
сегментоядерные – 60–65 %.
Лимфоциты – 20–35 %.
Моноциты – 6–8 %.
5.1.3. Возрастные особенности крови
У новорожденных и детей гемограмма и лейкоцитарная формула отличаются от таковых у взрослых.
Гемограмма новорожденных: 1) эритроцитов 6–7 1012/л (эритроцитоз); 2) лейкоцитов 10–30 109/л (лейкоцитоз); 3) тромбоцитов 200–300 109/л, т. е. как у взрослых. Через 2 нед содержание эритроцитов приближается к показателям взрослых (около 5,0 • 1012/л). Спустя 3–6 мес число эритроцитов уменьшается (менее 4–5 • 1012/л) – физиологическая анемия, а затем постепенно достигает показателей у взрослых к периоду полового созревания.
Содержание лейкоцитов у детей через 2 нед после рождения снижается до 9—15 109/л и к периоду полового созревания достигает показателя у взрослых.
Лейкоцитарная формула новорожденных. Наибольшие изменения в лейкоцитарной формуле отмечаются в содержании нейтрофилов и лимфоцитов. Остальные показатели существенно не отличаются от показателей у взрослых (табл. 5.1).
Таблица 5.1. Лейкоцитарная формула

Гемограмма новорожденных: 1) эритроцитов 6–7 1012/л (эритроцитоз); 2) лейкоцитов 10–30 109/л (лейкоцитоз); 3) тромбоцитов 200–300 109/л, т. е. как у взрослых. Через 2 нед содержание эритроцитов приближается к показателям взрослых (около 5,0 • 1012/л). Спустя 3–6 мес число эритроцитов уменьшается (менее 4–5 • 1012/л) – физиологическая анемия, а затем постепенно достигает показателей у взрослых к периоду полового созревания.
Содержание лейкоцитов у детей через 2 нед после рождения снижается до 9—15 109/л и к периоду полового созревания достигает показателя у взрослых.
Лейкоцитарная формула новорожденных. Наибольшие изменения в лейкоцитарной формуле отмечаются в содержании нейтрофилов и лимфоцитов. Остальные показатели существенно не отличаются от показателей у взрослых (табл. 5.1).
Таблица 5.1. Лейкоцитарная формула

5.2. кроветворение
Кроветворение (гемоцитопоэз) – процесс образования форменных элементов крови. Различают два вида кроветворения: миелоидное и лимфоидное. В свою очередь в миелоидном кроветворении выделяют: а) эритроцитопоэз; б) гранулоцитопоэз; в) тромбоцитопоэз; г) моноцитопоэз, а в лимфоидном: а) Т-лимфоцитопоэз; б) В-лимфоцитопоэз; в) NK-цитопоэз.
Кроме того, гемоцитопоэз подразделяется на два периода: эмбриональный и постэмбриональный. В эмбриональном периоде гемоцитопоэза происходит образование крови как ткани, поэтому он представляет собой гистогенез крови. Постэмбриональный гемоцитопоэз – это процесс физиологической регенерации крови.
Эмбриональный период гемоцитопоэза осуществляется в эмбриогенезе поэтапно, сменяя разные органы кроветворения. Этапы перекрывают друг друга, обеспечивая тем самым непрерывность процесса. В соответствии с этим эмбриональный гемоцитопоэз подразделяется на три этапа: 1) желточный, 2) гепатотимоли-енальный, 3) медуллярный (медуллолимфоидный).
Желточное кроветворение начинается со 2—3-й недели эмбриогенеза: в мезенхиме желточного мешка в результате пролиферации мезенхимных клеток образуются «кровяные островки». Периферические клетки островков уплощаются (эндотелий сосуда), центральные клетки округляются и превращаются в стволовые клетки крови.
Интраваскулярно (в сосудах) образуются первичные эритробласты, первичные эритроциты (мегалобласты, мегалоциты). Экстраваскулярно из части стволовых клеток начинают развиваться в небольшом количестве зернистые лейкоциты.
В конце 3-й недели желточная сосудистая сеть соединяется с эмбриональной (в тельце зародыша), устанавливается желточный круг кровообращения. Кровь и стволовые клетки крови поступают в сосуды зародыша, стволовые клетки заселяют закладки будущих кроветворных органов. К 12-й неделе желточное кроветворение прекращается.
Гепатотимолиенальный этап характеризуется следующим:
– определенной органной локализацией;
– возросшими количественными и качественными параметрами крови (появляется гранулоцитопоэз, тромбоцитопоэз, моноцитопоэз и лимфоцитопоэз);
– экстраваскулярным характером;
– переходом на нормобластический тип кроветворения.
В печени с 5-й недели до конца 5-го месяца происходит в основном экстраваскулярное миелоидное кроветворение, которое постепенно снижается и к рождению полностью прекращается. С 7-й недели в печени впервые появляются NK-клетки, которые в крови обнаруживаются только с 27—28-й недели.
Тимус очень быстро (9—12 нед) из универсального кроветворного органа становится лимфоидным, в нем начинается Т-лимфоцитопоэз, который продолжается и после рождения до его инволюции (25–30 лет).
Селезенка с 7—8-й недели заселяется стволовыми клетками, в ней начинается универсальное экстраваскулярное кроветворение (миело– и лимфоцитопоэз), особенно активное с 5-го по 7-й месяц. С 7-го месяца миелопоэз угнетается и к рождению прекращается. Лимфоидное кроветворение локализуется вокруг артериальных сосудов органа, нарастает и продолжается в постнатальном периоде.
Медуллярный этап. Источником стволовых клеток крови со 2—3-го месяца становится красный костный мозг. Закладка красного костного мозга появляется на 2-м месяце эмбриогенеза, кроветворение в нем начинается с 3-го месяца, а с 6—10-го месяца он становится основным органом миелоидного и частично лимфоидного кроветворения, т. е. универсальным кроветворным органом. В тимусе, лимфатических узлах, селезенке в этот период осуществляется лимфоидное кроветворение. В результате последовательной смены органов кроветворения и совершенствования процесса кроветворения формируется кровь как ткань.
Постэмбриональный период гемоцитопоэза осуществляется в красном костном мозге и лимфоидных органах (тимус, лимфоидные органы, лимфатические узлы, селезенка).
Сущность процесса кроветворения заключается в пролиферации и поэтапной дифференцировке стволовых клеток в зрелые форменные элементы крови.
Общепринятой является унипотентная теория кроветворения [Максимов А. А., 1909], согласно которой все форменные элементы крови развиваются из единого предшественника – стволовой клетки.
Кроветворение в постнатальном периоде онтогенеза представлено прежде всего двумя видами кроветворения: миелоидным и лимфоидным. Каждый вид кроветворения подразделяется на разновидности или ряды кроветворения (диффероны).
Миелопоэз: а) эритроцитопоэз, или эритроцитарный ряд; б) гранулоцитопоэз, или гранулоцитарный ряд; в) моноцитопоэз, или моноцитарный ряд; г) тромбоцитопоэз, или тромбоцитарный ряд.
Лимфоцитопоэз: а) Т-лимфоцитопоэз, или Т-лимфоцитарный ряд; б) В-лимфоцитопоэз, или плазмоцитопоэз.
В процессе поэтапной дифференцировки стволовых клеток в зрелые форменные элементы крови в каждом ряду кроветворения образуются промежуточные типы клеток, которые в схеме кроветворения составляют классы клеток. Всего в схеме кроветворения различают VI классов клеток: I – стволовые кроветворные клетки (СКК); II – полустволовые; III – унипотентные; IV – бластные; V – созревающие; VI – зрелые форменные элементы.
Морфологическая и функциональная характеристика клеток различных классов схемы кроветворения
Класс I – стволовая тотипотентная (плюрипотентная, полипотентная) клетка, способная к поддержанию своей популяции. По морфологии соответствует малому лимфоциту:
– обладает способностью к самоподдержанию своей популяции без притока клеток извне;
– редко делится. Деление СКК стимулируется фактором стволовых клеток, вырабатываемым стромальными клетками костного мозга;
– способна образовывать все виды форменных элементов крови;
– устойчива к действию повреждающих факторов;
– располагается в хорошо защищенных от внешних воздействий и обладающих обильным кровоснабжением местах (ячейки костной ткани);
– циркулирует в крови, мигрируя в другие органы кроветворения.
Направление дифференцировки стволовой клетки определяется содержанием в крови данного форменного элемента, а также влиянием микроокружения стволовых клеток, индуктивным влиянием стромальных (ретикулярных) клеток красного костного мозга или другого кроветворного органа, вырабатывающего гемопоэтические факторы роста (гемопоэтины).
Поддержание численности популяции стволовых клеток обеспечивается тем, что после митоза стволовой клетки одна из дочерних клеток становится на путь дифференцировки, а другая принимает морфологию малого лимфоцита и остается стволовой.
Делятся стволовые клетки редко (их интерфаза составляет 1–2 года): 80 % стволовых клеток находятся в состоянии покоя и только 20 % – в митозе и последующей дифференцировке.
В процессе пролиферации в культуре костного мозга или селезенке каждая стволовая клетка образует группу, или клон, клеток, поэтому стволовые клетки в литературе нередко называют колониеобразующими единицами – КОЕ-С.
Класс II – полустволовые, ограниченно полипотентные или мультипотентные (частично коммитированные) клетки – предшественницы: а) миелопоэза – КОЕ-ГЭММ; б) лимфоцитопоэза – КОЕ-Л, или Лск; в) NK-цитопоэза. Имеют морфологию малого лимфоцита. Каждая из них дает клон клеток, но только миелоидных или лимфоидных. Делятся чаще (через 3–4 нед) и также поддерживают численность своей популяции.
Класс III – олигопотентные (КОЕ-ГМ) и унипотентные (прогениторные) поэтинчувствительные клетки – предшественницы своего ряда кроветворения: КОЕ-М, КОЕ-Гн, КОЕ-Эо, КОЕ-Б, КОЕ-Мег и КОЕ-Э. Морфология их также соответствует морфологии малого лимфоцита. Способны дифференцироваться только в один тип форменного элемента.
Делятся часто, но одни потомки этих клеток вступают на путь дифференцировки, а другие сохраняют численность популяции клеток данного класса.
Частота деления этих клеток и способность дифференцироваться дальше зависят от содержания в крови особых биологически активных веществ – поэтинов, специфичных для каждого ряда кроветворения (эритропоэтины, тромбоцитопоэтины и др.).
Первые три класса клеток объединяются в класс морфологически неидентифицируемых клеток, так как все они имеют морфологию малого лимфоцита, но потенции их к развитию различны.
Класс IV – бластные (молодые) клетки, или бласты (эритробласты, лимфобласты и т. д.). Отличаются по морфологии как от трех предшествующих, так и от последующих классов клеток.
Эти клетки крупные, имеют большое рыхлое богатое эухроматином ядро с 2–4 ядрышками, цитоплазма базофильная за счет большого числа свободных рибосом. Часто делятся, но дочерние клетки все вступают на путь дальнейшей дифференцировки. По цитохимическим свойствам можно идентифицировать бласты разных рядов кроветворения.
Класс V – класс созревающих (дифференцирующихся) клеток, характерных для своего ряда кроветворения. В этом классе может быть несколько разновидностей переходных клеток – от одной (пролимфоцит, промоноцит) до пяти – в эритроцитарном ряду. Некоторые созревающие клетки в небольшом количестве (см. лейкоцитарную формулу гранулоцитов) могут попадать в кровь (например, ретикулоциты, юные и палочкоядерные гранулоциты).
Класс VI – зрелые форменные элементы крови. Следует отметить, что только эритроциты, тромбоциты и сегментоядерные гранулоциты являются зрелыми конечными дифференцированными форменными элементами или их фрагментами.
Моноциты – не окончательно дифференцированные клетки. Покидая кровеносное русло, они дифференцируются в тканях в конечные клетки – макрофаги. Лимфоциты при встрече с антигенами превращаются в бласты и снова делятся.
Совокупность клеток, составляющих линию дифференцировки стволовой клетки в определенный форменный элемент, образует его дифферон, или гистогенетический ряд. Например, эритроцитарный дифферон (эритрон) составляют: I класс – стволовая клетка (СК); II класс – полустволовая клетка (ПСК) – предшественница миелопоэза; III класс – унипотентная эритропоэтин-чувствительная клетка – КОЕ-Э, сюда же относят бурстобразующую единицу – БОЕ-Э, способную быстро (взрывоподобно) образовывать колонию эритроидных клеток численностью в несколько сотен элементов; IV класс – проэритробласт; V класс – созревающие клетки: базофильный, полихроматофильный, оксифильный нормоцит; VI класс – эритроцит.
В процессе созревания эритроцитов в V классе происходят: а) синтез и накопление гемоглобина, б) редукция органелл, в) редукция ядра.
В норме пополнение эритроцитов происходит в основном за счет деления и дифференцировки созревающих клеток – пронормоцитов, базофильных и полихроматофильных нормоцитов. Такой тип кроветворения носит название гомопластического кроветворения. Клеточные элементы, составляющие диффероны других форменных элементов крови, каждый студент должен уметь перечислить по схеме кроветворения.
Кроме того, гемоцитопоэз подразделяется на два периода: эмбриональный и постэмбриональный. В эмбриональном периоде гемоцитопоэза происходит образование крови как ткани, поэтому он представляет собой гистогенез крови. Постэмбриональный гемоцитопоэз – это процесс физиологической регенерации крови.
Эмбриональный период гемоцитопоэза осуществляется в эмбриогенезе поэтапно, сменяя разные органы кроветворения. Этапы перекрывают друг друга, обеспечивая тем самым непрерывность процесса. В соответствии с этим эмбриональный гемоцитопоэз подразделяется на три этапа: 1) желточный, 2) гепатотимоли-енальный, 3) медуллярный (медуллолимфоидный).
Желточное кроветворение начинается со 2—3-й недели эмбриогенеза: в мезенхиме желточного мешка в результате пролиферации мезенхимных клеток образуются «кровяные островки». Периферические клетки островков уплощаются (эндотелий сосуда), центральные клетки округляются и превращаются в стволовые клетки крови.
Интраваскулярно (в сосудах) образуются первичные эритробласты, первичные эритроциты (мегалобласты, мегалоциты). Экстраваскулярно из части стволовых клеток начинают развиваться в небольшом количестве зернистые лейкоциты.
В конце 3-й недели желточная сосудистая сеть соединяется с эмбриональной (в тельце зародыша), устанавливается желточный круг кровообращения. Кровь и стволовые клетки крови поступают в сосуды зародыша, стволовые клетки заселяют закладки будущих кроветворных органов. К 12-й неделе желточное кроветворение прекращается.
Гепатотимолиенальный этап характеризуется следующим:
– определенной органной локализацией;
– возросшими количественными и качественными параметрами крови (появляется гранулоцитопоэз, тромбоцитопоэз, моноцитопоэз и лимфоцитопоэз);
– экстраваскулярным характером;
– переходом на нормобластический тип кроветворения.
В печени с 5-й недели до конца 5-го месяца происходит в основном экстраваскулярное миелоидное кроветворение, которое постепенно снижается и к рождению полностью прекращается. С 7-й недели в печени впервые появляются NK-клетки, которые в крови обнаруживаются только с 27—28-й недели.
Тимус очень быстро (9—12 нед) из универсального кроветворного органа становится лимфоидным, в нем начинается Т-лимфоцитопоэз, который продолжается и после рождения до его инволюции (25–30 лет).
Селезенка с 7—8-й недели заселяется стволовыми клетками, в ней начинается универсальное экстраваскулярное кроветворение (миело– и лимфоцитопоэз), особенно активное с 5-го по 7-й месяц. С 7-го месяца миелопоэз угнетается и к рождению прекращается. Лимфоидное кроветворение локализуется вокруг артериальных сосудов органа, нарастает и продолжается в постнатальном периоде.
Медуллярный этап. Источником стволовых клеток крови со 2—3-го месяца становится красный костный мозг. Закладка красного костного мозга появляется на 2-м месяце эмбриогенеза, кроветворение в нем начинается с 3-го месяца, а с 6—10-го месяца он становится основным органом миелоидного и частично лимфоидного кроветворения, т. е. универсальным кроветворным органом. В тимусе, лимфатических узлах, селезенке в этот период осуществляется лимфоидное кроветворение. В результате последовательной смены органов кроветворения и совершенствования процесса кроветворения формируется кровь как ткань.
Постэмбриональный период гемоцитопоэза осуществляется в красном костном мозге и лимфоидных органах (тимус, лимфоидные органы, лимфатические узлы, селезенка).
Сущность процесса кроветворения заключается в пролиферации и поэтапной дифференцировке стволовых клеток в зрелые форменные элементы крови.
Общепринятой является унипотентная теория кроветворения [Максимов А. А., 1909], согласно которой все форменные элементы крови развиваются из единого предшественника – стволовой клетки.
Кроветворение в постнатальном периоде онтогенеза представлено прежде всего двумя видами кроветворения: миелоидным и лимфоидным. Каждый вид кроветворения подразделяется на разновидности или ряды кроветворения (диффероны).
Миелопоэз: а) эритроцитопоэз, или эритроцитарный ряд; б) гранулоцитопоэз, или гранулоцитарный ряд; в) моноцитопоэз, или моноцитарный ряд; г) тромбоцитопоэз, или тромбоцитарный ряд.
Лимфоцитопоэз: а) Т-лимфоцитопоэз, или Т-лимфоцитарный ряд; б) В-лимфоцитопоэз, или плазмоцитопоэз.
В процессе поэтапной дифференцировки стволовых клеток в зрелые форменные элементы крови в каждом ряду кроветворения образуются промежуточные типы клеток, которые в схеме кроветворения составляют классы клеток. Всего в схеме кроветворения различают VI классов клеток: I – стволовые кроветворные клетки (СКК); II – полустволовые; III – унипотентные; IV – бластные; V – созревающие; VI – зрелые форменные элементы.
Морфологическая и функциональная характеристика клеток различных классов схемы кроветворения
Класс I – стволовая тотипотентная (плюрипотентная, полипотентная) клетка, способная к поддержанию своей популяции. По морфологии соответствует малому лимфоциту:
– обладает способностью к самоподдержанию своей популяции без притока клеток извне;
– редко делится. Деление СКК стимулируется фактором стволовых клеток, вырабатываемым стромальными клетками костного мозга;
– способна образовывать все виды форменных элементов крови;
– устойчива к действию повреждающих факторов;
– располагается в хорошо защищенных от внешних воздействий и обладающих обильным кровоснабжением местах (ячейки костной ткани);
– циркулирует в крови, мигрируя в другие органы кроветворения.
Направление дифференцировки стволовой клетки определяется содержанием в крови данного форменного элемента, а также влиянием микроокружения стволовых клеток, индуктивным влиянием стромальных (ретикулярных) клеток красного костного мозга или другого кроветворного органа, вырабатывающего гемопоэтические факторы роста (гемопоэтины).
Поддержание численности популяции стволовых клеток обеспечивается тем, что после митоза стволовой клетки одна из дочерних клеток становится на путь дифференцировки, а другая принимает морфологию малого лимфоцита и остается стволовой.
Делятся стволовые клетки редко (их интерфаза составляет 1–2 года): 80 % стволовых клеток находятся в состоянии покоя и только 20 % – в митозе и последующей дифференцировке.
В процессе пролиферации в культуре костного мозга или селезенке каждая стволовая клетка образует группу, или клон, клеток, поэтому стволовые клетки в литературе нередко называют колониеобразующими единицами – КОЕ-С.
Класс II – полустволовые, ограниченно полипотентные или мультипотентные (частично коммитированные) клетки – предшественницы: а) миелопоэза – КОЕ-ГЭММ; б) лимфоцитопоэза – КОЕ-Л, или Лск; в) NK-цитопоэза. Имеют морфологию малого лимфоцита. Каждая из них дает клон клеток, но только миелоидных или лимфоидных. Делятся чаще (через 3–4 нед) и также поддерживают численность своей популяции.
Класс III – олигопотентные (КОЕ-ГМ) и унипотентные (прогениторные) поэтинчувствительные клетки – предшественницы своего ряда кроветворения: КОЕ-М, КОЕ-Гн, КОЕ-Эо, КОЕ-Б, КОЕ-Мег и КОЕ-Э. Морфология их также соответствует морфологии малого лимфоцита. Способны дифференцироваться только в один тип форменного элемента.
Делятся часто, но одни потомки этих клеток вступают на путь дифференцировки, а другие сохраняют численность популяции клеток данного класса.
Частота деления этих клеток и способность дифференцироваться дальше зависят от содержания в крови особых биологически активных веществ – поэтинов, специфичных для каждого ряда кроветворения (эритропоэтины, тромбоцитопоэтины и др.).
Первые три класса клеток объединяются в класс морфологически неидентифицируемых клеток, так как все они имеют морфологию малого лимфоцита, но потенции их к развитию различны.
Класс IV – бластные (молодые) клетки, или бласты (эритробласты, лимфобласты и т. д.). Отличаются по морфологии как от трех предшествующих, так и от последующих классов клеток.
Эти клетки крупные, имеют большое рыхлое богатое эухроматином ядро с 2–4 ядрышками, цитоплазма базофильная за счет большого числа свободных рибосом. Часто делятся, но дочерние клетки все вступают на путь дальнейшей дифференцировки. По цитохимическим свойствам можно идентифицировать бласты разных рядов кроветворения.
Класс V – класс созревающих (дифференцирующихся) клеток, характерных для своего ряда кроветворения. В этом классе может быть несколько разновидностей переходных клеток – от одной (пролимфоцит, промоноцит) до пяти – в эритроцитарном ряду. Некоторые созревающие клетки в небольшом количестве (см. лейкоцитарную формулу гранулоцитов) могут попадать в кровь (например, ретикулоциты, юные и палочкоядерные гранулоциты).
Класс VI – зрелые форменные элементы крови. Следует отметить, что только эритроциты, тромбоциты и сегментоядерные гранулоциты являются зрелыми конечными дифференцированными форменными элементами или их фрагментами.
Моноциты – не окончательно дифференцированные клетки. Покидая кровеносное русло, они дифференцируются в тканях в конечные клетки – макрофаги. Лимфоциты при встрече с антигенами превращаются в бласты и снова делятся.
Совокупность клеток, составляющих линию дифференцировки стволовой клетки в определенный форменный элемент, образует его дифферон, или гистогенетический ряд. Например, эритроцитарный дифферон (эритрон) составляют: I класс – стволовая клетка (СК); II класс – полустволовая клетка (ПСК) – предшественница миелопоэза; III класс – унипотентная эритропоэтин-чувствительная клетка – КОЕ-Э, сюда же относят бурстобразующую единицу – БОЕ-Э, способную быстро (взрывоподобно) образовывать колонию эритроидных клеток численностью в несколько сотен элементов; IV класс – проэритробласт; V класс – созревающие клетки: базофильный, полихроматофильный, оксифильный нормоцит; VI класс – эритроцит.
В процессе созревания эритроцитов в V классе происходят: а) синтез и накопление гемоглобина, б) редукция органелл, в) редукция ядра.
В норме пополнение эритроцитов происходит в основном за счет деления и дифференцировки созревающих клеток – пронормоцитов, базофильных и полихроматофильных нормоцитов. Такой тип кроветворения носит название гомопластического кроветворения. Клеточные элементы, составляющие диффероны других форменных элементов крови, каждый студент должен уметь перечислить по схеме кроветворения.
5.2.1. Гранулоцитопоэз
Гранулоциты существуют трех типов, каждый из которых происходит от собственной унипотентной стволовой клетки, производной КОЕ-ГЭММ (колониеобразующей единицы гранулоцитов, эритроцитов, моноцитов и мегакариоцитов), образующей гистологически определенный миелобласт.
Образование нейтрофилов: I класс (СК) II класс (ПСК)
III класс (унипотентная лейкопоэтинчувствительная клетка – КОЕ-Гн) IV класс (нейтрофильный миелобласт) V класс (нейтрофильный промиелоцит, нейтрофильный миелоцит, нейтрофильный метамиелоцит, палочкоядерный нейтрофил)
VI класс (зрелый нейтрофил).
Нейтрофильный миелобласт (IV класс) диаметром от 12 до 14 мкм, его крупное округлое красновато-синее ядро имеет тонкую сеть хроматина, присутствуют два или три бледно-серых ядрышка, цитоплазма не имеет гранул;
– на периферии клетки часто имеются цитоплазматические выпячивания, похожие на псевдоподии (определяются на электронных микрофотографиях);
– в цитоплазме присутствуют гранулярная эндоплазматическая сеть, небольшой комплекс Гольджи, множество митохондрий и свободных рибосом.
Нейтрофильный промиелоцит (V класс) крупнее миелобласта (диаметр 16–24 мкм). Ядро имеет грубую сеть хроматина и 1–2 ядрышка;
– цитоплазма голубоватого оттенка, содержит множество азурофильных гранул (неспецифических), периферия клетки больше не имеет похожих на псевдоподии цитоплазматических выпячиваний. На электронных микрофотографиях видны хорошо развитый комплекс Гольджи, гранулярная эндоплазматическая сеть и множество митохондрий;
– азурофильные гранулы диаметром примерно 0,5 мкм, формируются на поверхности созревающего комплекса Гольджи. Это лизосомы, содержащие гидролитические ферменты и пероксидазу.
Нейтрофильный миелоцит диаметром 10–12 мкм; имеет немного уплощенное ацентричное ядро с грубой сетью хроматина. Ядрышки могут быть, а могут отсутствовать;
– специфические гранулы диаметром 0,1 мкм, содержат лизоцим, щелочную фосфатазу, коллагеназу и фагоцитин, ясно видны, как и азурофильные гранулы;
– комплекс Гольджи хорошо развит, выглядит как прозрачный чистый участок в бледно-голубой цитоплазме;
– на поверхности формирования комплекса Гольджи образуются специфические нейтрофильные гранулы;
– все еще происходит клеточное деление. Это единственная стадия, на которой формируются специфические нейтрофильные гранулы.
Нейтрофильный метамиелоцит похож на нейтрофильный миелоцит, за исключением того, что ядро бобовидное и грубая сеть хроматина не имеет ядрышек (рис. 5.3);
– гетерохроматин указывает на уменьшение синтеза белка, что отражается в редукции органелл в клетке.
Палочкоядерный нейтрофил похож на зрелый нейтрофил, за исключением подковообразного ядра. Палочкоядерные клетки часто находят в циркулирующей крови, а в случаях инфицирования организма их число резко увеличивается.

Рис. 5.3. Мазок красного костного мозга. ×1200.
1 – мегакариобласт; 2 – метамиелоцит.
Количество нейтрофилов, продуцируемый: в организме здорового взрослого человека, около 800 000 в день.
Образование эозинофилов и базофилов: стадии развития эозинофилов и базофилов похожи на стадии, описанные для нейтрофилов, за исключением того, что типы гранул, формирующихся на стадии миелоцита, специфичны для каждого типа клеток. Кроме того, морфология ядра зрелой клетки напоминает таковую на поздней стадии палочкоядерного гранулоцита.
Моноцитопоэз: I класс (СК) → II класс (ПСК) → III класс (унипотентная клетка – КОЕ-М) – общая предшественница моноцитов и нейтрофилов (дает начало монобластам) → IV класс (монобласты) → V класс (промоноцит) → VI класс (моноцит).
Промоноцит – крупная клетка (диаметр 16–18 мкм) с несколько бобовидным ядром, расположенным эксцентрично в светло-голубой цитоплазме, которая содержит также множество азурофильных гранул (лизосом), продуцируемых хорошо развитым комплексом Гольджи, многочисленные митохондрии и довольно развитую гранулярную эндоплазматическую сеть.
Деление промоноцитов приводит к формированию моноцитов (VI класс), которые покидают костный мозг, поступают в кровоток, а затем после проникновения в соединительную ткань периферических органов дифференцируются в макрофаги, а также в дендритные антигенпредставляющие клетки.
Количество моноцитов, образующихся ежедневно в организме здорового взрослого человека, составляет около 1 1010.
Образование кровяных пластинок (тромбоцитопоэз): I класс (СК) → II класс (ПСК) → III класс (унипотентная тромбопоэтинчувствительная клетка – КОЕ-мег) → IV класс (мегакариобласт) → V класс (промегакариоцит) → VI класс (тромбоцитах).
Мегакариобласт – крупная клетка (диаметр 25–40 мкм), единственное крупное ядро с выемками (либо дольчатое) имеет тонкую сеть хроматина. Деление мегакариобласта происходит путем эндомитоза, в его ходе не образуется дочерних клеток. Вместо этого клетка приобретает гигантские размеры, плоидность ядра может достигать 64 (см. рис. 5.2);
– цитоплазма слабобазофильная, без гранул, на электронных микрофотографиях видны крупные митохондрии, многочисленные полисомы, некоторое количество гранулярной эндоплазматической сети и довольно хорошо развитый комплекс Гольджи.
Промегакариоцит – крупная округлая клетка диаметром 42–45 мкм с объемным дольчатым полиплоидным ядром и резко базофильной цитоплазмой;
– помимо обычных органелл, цитоплазма содержит сложную систему гладких пузырьков, тубул, плоских цистерн, которые, сливаясь, формируют тромбоцитарные демаркационные каналы;
– в процессе дальнейшей дифференцировки промегакариоциты становятся либо резервными, либо тромбоцитпродуцирующими мегакариоцитами.
Мегакариоцит – необычайно крупная клетка (диаметр 40– 100 мкм) с одним многодольчатым крупным полиплоидным ядром. На электронных микрофотографиях видны хорошо развитый комплекс Гольджи, активно формирующий α-гранулы, лизосомы и плотные тельца, многочисленные митохондрии и довольно развитая гранулярная эндоплазматическая сеть.
Мегакариоциты расположены в окружности синусоидов, в поры стенки которых проникают их отростки. Отростки распадаются вдоль определенных демаркационных каналов, формируя группы соединенных кровяных пластинок, которые затем разделяются на отдельные тромбоциты.
После полного отделения тромбоцитов остаточные мегакариоциты подвергаются дегенерации, фагоцитируются и замещаются новыми.
Образование нейтрофилов: I класс (СК) II класс (ПСК)
III класс (унипотентная лейкопоэтинчувствительная клетка – КОЕ-Гн) IV класс (нейтрофильный миелобласт) V класс (нейтрофильный промиелоцит, нейтрофильный миелоцит, нейтрофильный метамиелоцит, палочкоядерный нейтрофил)
VI класс (зрелый нейтрофил).
Нейтрофильный миелобласт (IV класс) диаметром от 12 до 14 мкм, его крупное округлое красновато-синее ядро имеет тонкую сеть хроматина, присутствуют два или три бледно-серых ядрышка, цитоплазма не имеет гранул;
– на периферии клетки часто имеются цитоплазматические выпячивания, похожие на псевдоподии (определяются на электронных микрофотографиях);
– в цитоплазме присутствуют гранулярная эндоплазматическая сеть, небольшой комплекс Гольджи, множество митохондрий и свободных рибосом.
Нейтрофильный промиелоцит (V класс) крупнее миелобласта (диаметр 16–24 мкм). Ядро имеет грубую сеть хроматина и 1–2 ядрышка;
– цитоплазма голубоватого оттенка, содержит множество азурофильных гранул (неспецифических), периферия клетки больше не имеет похожих на псевдоподии цитоплазматических выпячиваний. На электронных микрофотографиях видны хорошо развитый комплекс Гольджи, гранулярная эндоплазматическая сеть и множество митохондрий;
– азурофильные гранулы диаметром примерно 0,5 мкм, формируются на поверхности созревающего комплекса Гольджи. Это лизосомы, содержащие гидролитические ферменты и пероксидазу.
Нейтрофильный миелоцит диаметром 10–12 мкм; имеет немного уплощенное ацентричное ядро с грубой сетью хроматина. Ядрышки могут быть, а могут отсутствовать;
– специфические гранулы диаметром 0,1 мкм, содержат лизоцим, щелочную фосфатазу, коллагеназу и фагоцитин, ясно видны, как и азурофильные гранулы;
– комплекс Гольджи хорошо развит, выглядит как прозрачный чистый участок в бледно-голубой цитоплазме;
– на поверхности формирования комплекса Гольджи образуются специфические нейтрофильные гранулы;
– все еще происходит клеточное деление. Это единственная стадия, на которой формируются специфические нейтрофильные гранулы.
Нейтрофильный метамиелоцит похож на нейтрофильный миелоцит, за исключением того, что ядро бобовидное и грубая сеть хроматина не имеет ядрышек (рис. 5.3);
– гетерохроматин указывает на уменьшение синтеза белка, что отражается в редукции органелл в клетке.
Палочкоядерный нейтрофил похож на зрелый нейтрофил, за исключением подковообразного ядра. Палочкоядерные клетки часто находят в циркулирующей крови, а в случаях инфицирования организма их число резко увеличивается.

Рис. 5.3. Мазок красного костного мозга. ×1200.
1 – мегакариобласт; 2 – метамиелоцит.
Количество нейтрофилов, продуцируемый: в организме здорового взрослого человека, около 800 000 в день.
Образование эозинофилов и базофилов: стадии развития эозинофилов и базофилов похожи на стадии, описанные для нейтрофилов, за исключением того, что типы гранул, формирующихся на стадии миелоцита, специфичны для каждого типа клеток. Кроме того, морфология ядра зрелой клетки напоминает таковую на поздней стадии палочкоядерного гранулоцита.
Моноцитопоэз: I класс (СК) → II класс (ПСК) → III класс (унипотентная клетка – КОЕ-М) – общая предшественница моноцитов и нейтрофилов (дает начало монобластам) → IV класс (монобласты) → V класс (промоноцит) → VI класс (моноцит).
Промоноцит – крупная клетка (диаметр 16–18 мкм) с несколько бобовидным ядром, расположенным эксцентрично в светло-голубой цитоплазме, которая содержит также множество азурофильных гранул (лизосом), продуцируемых хорошо развитым комплексом Гольджи, многочисленные митохондрии и довольно развитую гранулярную эндоплазматическую сеть.
Деление промоноцитов приводит к формированию моноцитов (VI класс), которые покидают костный мозг, поступают в кровоток, а затем после проникновения в соединительную ткань периферических органов дифференцируются в макрофаги, а также в дендритные антигенпредставляющие клетки.
Количество моноцитов, образующихся ежедневно в организме здорового взрослого человека, составляет около 1 1010.
Образование кровяных пластинок (тромбоцитопоэз): I класс (СК) → II класс (ПСК) → III класс (унипотентная тромбопоэтинчувствительная клетка – КОЕ-мег) → IV класс (мегакариобласт) → V класс (промегакариоцит) → VI класс (тромбоцитах).
Мегакариобласт – крупная клетка (диаметр 25–40 мкм), единственное крупное ядро с выемками (либо дольчатое) имеет тонкую сеть хроматина. Деление мегакариобласта происходит путем эндомитоза, в его ходе не образуется дочерних клеток. Вместо этого клетка приобретает гигантские размеры, плоидность ядра может достигать 64 (см. рис. 5.2);
– цитоплазма слабобазофильная, без гранул, на электронных микрофотографиях видны крупные митохондрии, многочисленные полисомы, некоторое количество гранулярной эндоплазматической сети и довольно хорошо развитый комплекс Гольджи.
Промегакариоцит – крупная округлая клетка диаметром 42–45 мкм с объемным дольчатым полиплоидным ядром и резко базофильной цитоплазмой;
– помимо обычных органелл, цитоплазма содержит сложную систему гладких пузырьков, тубул, плоских цистерн, которые, сливаясь, формируют тромбоцитарные демаркационные каналы;
– в процессе дальнейшей дифференцировки промегакариоциты становятся либо резервными, либо тромбоцитпродуцирующими мегакариоцитами.
Мегакариоцит – необычайно крупная клетка (диаметр 40– 100 мкм) с одним многодольчатым крупным полиплоидным ядром. На электронных микрофотографиях видны хорошо развитый комплекс Гольджи, активно формирующий α-гранулы, лизосомы и плотные тельца, многочисленные митохондрии и довольно развитая гранулярная эндоплазматическая сеть.
Мегакариоциты расположены в окружности синусоидов, в поры стенки которых проникают их отростки. Отростки распадаются вдоль определенных демаркационных каналов, формируя группы соединенных кровяных пластинок, которые затем разделяются на отдельные тромбоциты.
После полного отделения тромбоцитов остаточные мегакариоциты подвергаются дегенерации, фагоцитируются и замещаются новыми.
5.2.2. Лимфоцитопоэз
Клетка-предшественница лимфоцитов берет начало от популяции СК (тотипотентные гемопоэтические стволовые клетки), находится в костном мозге, как и в циркулирующей крови, как член популяции «нулевых» клеток.
Конец бесплатного ознакомительного фрагмента
