Страница:
Рудольф Павлович Самусев, Марина Юрьевна Капитонова
Общая и частная гистология
Предисловие
В настоящем пособии в краткой форме изложены сведения по общей и частной гистологии в соответствии с учебной программой по гистологии, цитологии и эмбриологии. Материал иллюстрирован снимками с оригинальных гистологических препаратов, а также электронограммами.
С позиций современной морфологической науки даны основные понятия по цитологии, типам тканей, приведены особенности микроскопического строения органов и систем человеческого организма.
Пособие может быть использовано для повторения материала при подготовке к занятиям, зачетам и экзамену по дисциплине.
Для студентов медицинского и биологического профилей высших учебных заведений, а также для молодых ученых-морфологов.
С позиций современной морфологической науки даны основные понятия по цитологии, типам тканей, приведены особенности микроскопического строения органов и систем человеческого организма.
Пособие может быть использовано для повторения материала при подготовке к занятиям, зачетам и экзамену по дисциплине.
Для студентов медицинского и биологического профилей высших учебных заведений, а также для молодых ученых-морфологов.
Список сокращений
АДГ – антидиуретический гормон
АКТГ – адренокортикотрогшый гормон
АТФ – аденозинтрифосфат
ГМК – гладко-мышечные клетки
ГМТ – гладкая мышечная ткань
ДНК – дезоксирибонуклеиновая кислота
ДЭС – диффузная эндокринная система
КЦ – клеточный цикл
КЯП – комплекс ядерной поры
ЛГ – лютеинизирующий гормон
ОП – окаймленный пузырек
ПНС – периферическая нервная система
иРНК – информационная рибонуклеиновая кислота
рРНК – рибосомная рибонуклеиновая кислота
тРНК – транспортная рибонуклеиновая кислота
РТК – рецепторные Т-клетки
СКК – стволовые кроветворные клетки
ТТГ – тиреотропный гормон
ТЭМ – трансмиссионная электронная микроскопия
ФК – фузогенный комплекс
ФСГ – фолликулостимулирующий гормон
ЦНС – центральная нервная система
ЭПС – эндоплазматическая сеть
АКТГ – адренокортикотрогшый гормон
АТФ – аденозинтрифосфат
ГМК – гладко-мышечные клетки
ГМТ – гладкая мышечная ткань
ДНК – дезоксирибонуклеиновая кислота
ДЭС – диффузная эндокринная система
КЦ – клеточный цикл
КЯП – комплекс ядерной поры
ЛГ – лютеинизирующий гормон
ОП – окаймленный пузырек
ПНС – периферическая нервная система
иРНК – информационная рибонуклеиновая кислота
рРНК – рибосомная рибонуклеиновая кислота
тРНК – транспортная рибонуклеиновая кислота
РТК – рецепторные Т-клетки
СКК – стволовые кроветворные клетки
ТТГ – тиреотропный гормон
ТЭМ – трансмиссионная электронная микроскопия
ФК – фузогенный комплекс
ФСГ – фолликулостимулирующий гормон
ЦНС – центральная нервная система
ЭПС – эндоплазматическая сеть
Глава 1
Гистологическая техника
Гистология, как и любая другая наука, имеет свои задачи и специфические методы исследования материала. Основным методом является изучение фиксированных и окрашенных гистологических препаратов под микроскопом в проходящем свете.
Традиционный способ подготовки материала для получения гистологического препарата включает следующее: 1) фиксацию материала; 2) промывку фиксированного материала; 3) обезвоживание и уплотнение материала; 4) приготовление блоков; 5) изготовление срезов (резка); 6) окрашивание срезов; 7) заключение и маркировку срезов.
Традиционный способ подготовки материала для получения гистологического препарата включает следующее: 1) фиксацию материала; 2) промывку фиксированного материала; 3) обезвоживание и уплотнение материала; 4) приготовление блоков; 5) изготовление срезов (резка); 6) окрашивание срезов; 7) заключение и маркировку срезов.
1.1. Фиксация материала
Цель фиксации – максимально закрепить и сохранить в обрабатываемой ткани или органе его прижизненную структуру. После фиксации материал разрезают или расщепляют, чтобы получить срезы толщиной 5—20 мкм. Затем полученные срезы окрашивают или обрабатывают соответствующими способами для приготовления постоянных гистологических препаратов, способных сохраняться длительное время.
Фиксатор (фиксирующая жидкость) должен обладать следующими качествами: быстро проникать в ткани и коагулировать белки исследуемого материала – ткани или органа для исключения аутолиза; сводить до минимума деформацию (сморщивание или набухание) объекта; легко удаляться при промывке водой и не мешать дальнейшей обработке (уплотнению и окрашиванию) изучаемого материала.
Количество фиксатора по объему должно быть, как правило, в 100 раз больше объема фиксируемого материала. Используют фиксатор только один раз. Величина фиксируемого кусочка должна быть минимальной – не более 1 см3 или 1 см в одном измерении, а в особых случаях не превышать 1 мм3.
Продолжительность фиксации – не менее 24 ч, при других методиках и экспресс-диагностике – от 3–5 мин до 6 ч. Большие колебания времени фиксации зависят от применяемых методик, специфики материала и фиксатора.
Из наиболее распространенных фиксаторов чаще всего применяют следующие:
1) формалин (10–20 % водный раствор);
2) этиловый спирт (этанол) 80–96 %;
3) смесь спирта с формалином (спирт-формол): 70 % этилового спирта 10 мл и 10–20 % раствора формалина 4 мл;
4) жидкость Мюллера: калия двухромовокислого 2,5 г, натрия сульфата 1 г, воды 100 мл;
5) жидкость Ценкера: жидкости Мюллера 100 мл, сулемы 5 г, ледяной уксусной кислоты (добавляют сразу перед употреблением фиксатора) 5 мл;
6) жидкость Максимова (ценкер-формол): жидкости Ценкера 90 мл, формалина 10–20 % 10 мл.
Фиксатор (фиксирующая жидкость) должен обладать следующими качествами: быстро проникать в ткани и коагулировать белки исследуемого материала – ткани или органа для исключения аутолиза; сводить до минимума деформацию (сморщивание или набухание) объекта; легко удаляться при промывке водой и не мешать дальнейшей обработке (уплотнению и окрашиванию) изучаемого материала.
Количество фиксатора по объему должно быть, как правило, в 100 раз больше объема фиксируемого материала. Используют фиксатор только один раз. Величина фиксируемого кусочка должна быть минимальной – не более 1 см3 или 1 см в одном измерении, а в особых случаях не превышать 1 мм3.
Продолжительность фиксации – не менее 24 ч, при других методиках и экспресс-диагностике – от 3–5 мин до 6 ч. Большие колебания времени фиксации зависят от применяемых методик, специфики материала и фиксатора.
Из наиболее распространенных фиксаторов чаще всего применяют следующие:
1) формалин (10–20 % водный раствор);
2) этиловый спирт (этанол) 80–96 %;
3) смесь спирта с формалином (спирт-формол): 70 % этилового спирта 10 мл и 10–20 % раствора формалина 4 мл;
4) жидкость Мюллера: калия двухромовокислого 2,5 г, натрия сульфата 1 г, воды 100 мл;
5) жидкость Ценкера: жидкости Мюллера 100 мл, сулемы 5 г, ледяной уксусной кислоты (добавляют сразу перед употреблением фиксатора) 5 мл;
6) жидкость Максимова (ценкер-формол): жидкости Ценкера 90 мл, формалина 10–20 % 10 мл.
1.2. Промывка фиксированного материала
Промывка материала (кусочки органов, тканей или небольшие органы целиком, особенно от мелких экспериментальных животных) в водопроводной проточной воде, как правило, продолжается столько же, сколько длилась фиксация, чаще 18–24 ч. Затем фиксированные ткани и органы должны быть подготовлены для получения срезов различного типа: целлоидиновых, парафиновых или замороженных.
1.3. Обезвоживание и уплотнение фиксированного материала
Этот этап необходим в случаях, если нужно получить целлоидиновые или парафиновые блоки. Перед заливкой материала в целлоидин или парафин из изучаемых объектов удаляют воду и уплотняют их. Для этого материал последовательно переносят в спирты возрастающей крепости, начиная с 70 % до абсолютного (100 %) включительно, т. е. проводят через батарею спиртов возрастающей крепости. Время пребывания в каждом спирте колеблется в зависимости от характера ткани от 4–6 до 24 ч.
1.4. Приготовление блоков
Целлоидиновые блоки. Материал из абсолютного спирта перекладывают в две порции (на 24 ч в каждую) смеси из равных количеств абсолютного спирта и эфира. Затем кусочки тканей последовательно помещают от 2 до 7 дней в растворы целлоидина: I (2 %), II (4 %), III (8 %), IV (8 %). Последний целлоидиновый раствор вместе с помещенными в него кусочками ткани подсушивают в эксикаторе наполовину, т. е. до получения 16 % раствора.
На поверхность целлоидина наливают 70 % спирт и через 1 сут вырезают из уплотненной массы кусочки материала, отступя от их краев на 3–5 мм, и с помощью густого раствора целлоидина наклеивают на деревянные кубики, предварительно обезжиренные спиртом или эфиром.
Целлоидиновые блоки до изготовления из них срезов хранят в 70 % этиловом спирте в банках с притертой пробкой.
Парафиновые блоки. Производят такие же обезвоживание и уплотнение изучаемого объекта, как и при целлоидиновой заливке, т. е. проводку через батарею спиртов возрастающей крепости. После этого кусочки перемещают в смесь равных частей абсолютного спирта и ксилола на 1–3 ч (или спирта и хлороформа на 6—12 ч), затем последовательно переносят в первый чистый ксилол на 1–3 ч (или хлороформ на 6—12 ч), во второй чистый ксилол на 1–3 ч (или хлороформ на 6—12 ч), насыщенный раствор парафина в ксилоле в термостате при температуре 37 °C на 2 ч (или хлороформе на 6—12 ч). Для этих целей применяется легкоплавкий парафин.
Далее кусочки тканей переносят в термостате в «чистый» тугоплавкий парафин при температуре 54–57 °C на 1,5–2 ч, во второй «чистый» парафин при той же температуре и на такой же срок. Наконец, материал (по объектам, органам или тканям) заливают расплавленным парафином в бумажные или металлические формочки и охлаждают водой низкой температуры в холодильнике, охлаждающих термосах, криостате и т. д. Эта процедура преследует определенную цель – равномерное затвердевание парафина и находящихся в нем тканей при постепенном снижении температуры скрепляющего субстрата.
Каждый из залитых в парафин комплексов в дальнейшем прикрепляют к деревянным кубикам, обработанным по той же методике, что и для целлоидиновых блоков, путем скрепления нижней, расплавленной прикосновением нагретого шпателя поверхности препарата с верхней поверхностью деревянного кубика.
Хранят парафиновые блоки в сухих банках с притертой пробкой в прохладных и недоступных солнечным лучам местах или шкафах, удаленных от нагревательных приборов и аппаратуры.
Необходимый блок извлекают непосредственно перед приготовлением срезов, а его остатки, если это необходимо для дальнейшего исследования, сразу после изготовления нужного количества срезов помещают в прежнее хранилище.
На поверхность целлоидина наливают 70 % спирт и через 1 сут вырезают из уплотненной массы кусочки материала, отступя от их краев на 3–5 мм, и с помощью густого раствора целлоидина наклеивают на деревянные кубики, предварительно обезжиренные спиртом или эфиром.
Целлоидиновые блоки до изготовления из них срезов хранят в 70 % этиловом спирте в банках с притертой пробкой.
Парафиновые блоки. Производят такие же обезвоживание и уплотнение изучаемого объекта, как и при целлоидиновой заливке, т. е. проводку через батарею спиртов возрастающей крепости. После этого кусочки перемещают в смесь равных частей абсолютного спирта и ксилола на 1–3 ч (или спирта и хлороформа на 6—12 ч), затем последовательно переносят в первый чистый ксилол на 1–3 ч (или хлороформ на 6—12 ч), во второй чистый ксилол на 1–3 ч (или хлороформ на 6—12 ч), насыщенный раствор парафина в ксилоле в термостате при температуре 37 °C на 2 ч (или хлороформе на 6—12 ч). Для этих целей применяется легкоплавкий парафин.
Далее кусочки тканей переносят в термостате в «чистый» тугоплавкий парафин при температуре 54–57 °C на 1,5–2 ч, во второй «чистый» парафин при той же температуре и на такой же срок. Наконец, материал (по объектам, органам или тканям) заливают расплавленным парафином в бумажные или металлические формочки и охлаждают водой низкой температуры в холодильнике, охлаждающих термосах, криостате и т. д. Эта процедура преследует определенную цель – равномерное затвердевание парафина и находящихся в нем тканей при постепенном снижении температуры скрепляющего субстрата.
Каждый из залитых в парафин комплексов в дальнейшем прикрепляют к деревянным кубикам, обработанным по той же методике, что и для целлоидиновых блоков, путем скрепления нижней, расплавленной прикосновением нагретого шпателя поверхности препарата с верхней поверхностью деревянного кубика.
Хранят парафиновые блоки в сухих банках с притертой пробкой в прохладных и недоступных солнечным лучам местах или шкафах, удаленных от нагревательных приборов и аппаратуры.
Необходимый блок извлекают непосредственно перед приготовлением срезов, а его остатки, если это необходимо для дальнейшего исследования, сразу после изготовления нужного количества срезов помещают в прежнее хранилище.
1.5. Изготовление срезов
Ткань, которую необходимо подвергнуть микроскопическому исследованию, режут на срезы на специальных аппаратах, получивших название микротомов (санные или роторные), с помощью особых стальных ножей.
Наиболее распространенным из них является санный микротом (рис. 1.1). Этот аппарат состоит из массивной металлической подставки – основания с вертикальной и боковой, расположенной под острым углом пластинами с хорошо отшлифованными полосками – полозьями, по которым скользят в горизонтальном положении ножевые салазки с отшлифованными поверхностями – ножедержатель. На каждой поверхности имеется специальный паз с винтом для крепления микротомного ножа из прочной стали, заточку лезвия которого производят под контролем микроскопа.
С помощью винта можно регулировать наклон ножа к горизонтальной плоскости, а за счет барашкового зажима – угол поворота ножа, что позволяет наиболее удобно ориентировать его к блоку и приготовлять оптимально тонкие срезы.
С левой стороны микротома располагается приспособление для равномерного поднятия подлежащего резанию объекта. Зажим с препаратом – объектодержатель продвигается по наклонной плоскости с помощью горизонтального микрометрического винта. На дужке винта нанесена шкала, указывающая, на какое расстояние вверх поднимается блок соответственно повороту винта (цена одного деления 1 мкм). Объектодержатель с помощью винтов можно установить за счет шарнира в любом направлении и отрегулировать тем самым расположение тканевых элементов в получаемых срезах.
Приготовление среза: блок устанавливают в объектодержателе микротома в соответствии с заданным наклоном и поворотом, прочно фиксируют микротомный нож в ножедержателе, причем лезвие его должно находиться выше верхней поверхности блока. Затем последний с помощью винта подводят до соприкосновения с режущей частью ножа, который отодвигается за объект. Микрометрический винт поворачивают на желаемую толщину и плавным движением ножевых салазок к себе делают срез. Полученный срез снимают с поверхности ножа мягкой беличьей или колонковой кистью и переносят в чашку Петри с водой (для парафиновых срезов воду подогревают).
Для изготовления серийных срезов используют ротационные микротомы с вертикально установленным ножом, неподвижно закрепленным в ножедержателе (рис. 1.2). Блокодержатель подвижен и перемещается с помощью шарнирного винта. Срезы одинаковой толщины подаются на движущуюся ленту и могут быть легко пронумерованы. Подобные микротомы применяют для тотального посрезного изучения отдельных объектов, особенно в эмбриологии.

Рис. 1.1. Санный микротом.
1 – объектодержатель; 2 – стальной нож; 3 – полозья.
Широкое распространение приобрели микротомы, в которых исследуемый материал может быть разрезан на срезы без предварительной заливки в среды благодаря замораживанию. Это позволяет не только сократить время процедуры получения срезов, но и устранить влияние всякого рода реактивов на тканевые элементы, что особенно важно и даже необходимо для микрохимического и гистохимического исследований.
К такому типу аппаратов относятся замораживающий микротом и криостат. Оба имеют объектные столики, микротомные ножи и подающие механизмы, т. е. основные части, характерные для описанного санного микротома.
В замораживающем микротоме к объектному столику подведен шланг от баллона со сжиженной углекислотой.
На поверхность объектного столика с предварительно замороженной водяной подушкой-основой помещают исследуемый материал, смоченный и залитый вокруг отстойной водопроводной водой. Затем кусочки медленно замораживают, пуская прерывистую струю углекислоты, и делают срезы необходимой толщины.

Рис. 1.2. Ротационный микротом.
1 – объектодержатель; 2 – держатель сменных лезвий.
В криостате используется тот же принцип замораживания тканей и одновременного ингибирования (блокировки) их ферментов. Это позволяет получить приближенные до максимума к прижизненным состояние и содержание их в тканевых элементах.
Охлаждение в криостате осуществляется с помощью либо углекислоты, либо мощных холодильных агрегатов, способных быстро заморозить изучаемый материал.
Наиболее распространенным из них является санный микротом (рис. 1.1). Этот аппарат состоит из массивной металлической подставки – основания с вертикальной и боковой, расположенной под острым углом пластинами с хорошо отшлифованными полосками – полозьями, по которым скользят в горизонтальном положении ножевые салазки с отшлифованными поверхностями – ножедержатель. На каждой поверхности имеется специальный паз с винтом для крепления микротомного ножа из прочной стали, заточку лезвия которого производят под контролем микроскопа.
С помощью винта можно регулировать наклон ножа к горизонтальной плоскости, а за счет барашкового зажима – угол поворота ножа, что позволяет наиболее удобно ориентировать его к блоку и приготовлять оптимально тонкие срезы.
С левой стороны микротома располагается приспособление для равномерного поднятия подлежащего резанию объекта. Зажим с препаратом – объектодержатель продвигается по наклонной плоскости с помощью горизонтального микрометрического винта. На дужке винта нанесена шкала, указывающая, на какое расстояние вверх поднимается блок соответственно повороту винта (цена одного деления 1 мкм). Объектодержатель с помощью винтов можно установить за счет шарнира в любом направлении и отрегулировать тем самым расположение тканевых элементов в получаемых срезах.
Приготовление среза: блок устанавливают в объектодержателе микротома в соответствии с заданным наклоном и поворотом, прочно фиксируют микротомный нож в ножедержателе, причем лезвие его должно находиться выше верхней поверхности блока. Затем последний с помощью винта подводят до соприкосновения с режущей частью ножа, который отодвигается за объект. Микрометрический винт поворачивают на желаемую толщину и плавным движением ножевых салазок к себе делают срез. Полученный срез снимают с поверхности ножа мягкой беличьей или колонковой кистью и переносят в чашку Петри с водой (для парафиновых срезов воду подогревают).
Для изготовления серийных срезов используют ротационные микротомы с вертикально установленным ножом, неподвижно закрепленным в ножедержателе (рис. 1.2). Блокодержатель подвижен и перемещается с помощью шарнирного винта. Срезы одинаковой толщины подаются на движущуюся ленту и могут быть легко пронумерованы. Подобные микротомы применяют для тотального посрезного изучения отдельных объектов, особенно в эмбриологии.

Рис. 1.1. Санный микротом.
1 – объектодержатель; 2 – стальной нож; 3 – полозья.
Широкое распространение приобрели микротомы, в которых исследуемый материал может быть разрезан на срезы без предварительной заливки в среды благодаря замораживанию. Это позволяет не только сократить время процедуры получения срезов, но и устранить влияние всякого рода реактивов на тканевые элементы, что особенно важно и даже необходимо для микрохимического и гистохимического исследований.
К такому типу аппаратов относятся замораживающий микротом и криостат. Оба имеют объектные столики, микротомные ножи и подающие механизмы, т. е. основные части, характерные для описанного санного микротома.
В замораживающем микротоме к объектному столику подведен шланг от баллона со сжиженной углекислотой.
На поверхность объектного столика с предварительно замороженной водяной подушкой-основой помещают исследуемый материал, смоченный и залитый вокруг отстойной водопроводной водой. Затем кусочки медленно замораживают, пуская прерывистую струю углекислоты, и делают срезы необходимой толщины.

Рис. 1.2. Ротационный микротом.
1 – объектодержатель; 2 – держатель сменных лезвий.
В криостате используется тот же принцип замораживания тканей и одновременного ингибирования (блокировки) их ферментов. Это позволяет получить приближенные до максимума к прижизненным состояние и содержание их в тканевых элементах.
Охлаждение в криостате осуществляется с помощью либо углекислоты, либо мощных холодильных агрегатов, способных быстро заморозить изучаемый материал.
1.6. Окрашивание гистологических срезов
При различных микроскопических методах, за исключением электронной микроскопии, полученные срезы подвергают окраске, выявляющей различные структурные элементы тканей и клеток. Для этого применяют красители – основные или ядерные: например, гематоксилин, окрашивающий ядра клеток в цвета от синего до черного; кислые или цитоплазматические: например, эозин, тонирующий цитоплазму в красный цвет, пикриновую кислоту, окрашивающую ее в желтый цвет, и др.; нейтральные: например, нейтральный красный для прижизненной окраски клеточных элементов и др.
В зависимости от цели исследования используют многочисленные красители для выявления общей морфологии клетки, контрастирования кариоплазмы (ядра) и цитоплазмы (для окраски ядра в красный цвет применяют кармин, сафранин и т. д.). Специфическими красителями являются орсеин, окрашивающий эластические волокна в коричневый цвет, судан III окрашивает жир в желтый цвет, а четырехокись осмия – в черный цвет, нитрат серебра импрегнирует нервные клетки и волокна в цвета от коричневого до черного, метиленовый синий окрашивает нервные элементы в синий цвет.
Из множества различных красителей и их комбинаций, применяемых в современной общегистологической технике, наиболее распространенной является окраска гематоксилином и эозином.
Перед окраской срез подвергают депарафинированию, т. е. срезы последовательно проводят через растворитель парафина (ксилол), спирты нисходящей концентрации и помещают в чашку Петри с водой. Затем срезы обрабатывают в следующем порядке:
1) в растворе гематоксилина 5—10 мин;
2) в проточной воде 5—10 мин;
3) в дистиллированной воде 1–2 мин;
4) в растворе эозина 1—10 мин;
5) в дистиллированной воде 1–3 мин;
6) в 70 % спирте 1–2 мин;
7) в 96 % спирте 1–2 мин;
8) в 100 % спирте (абсолютный) 1–2 мин;
9) в карболксилоле 1–3 мин;
10) в ксилоле 1–3 мин;
11) в кедровом или канадском бальзаме (срез помещают в каплю бальзама между предварительно обезжиренными предметным и покровным стеклами).
В зависимости от цели исследования используют многочисленные красители для выявления общей морфологии клетки, контрастирования кариоплазмы (ядра) и цитоплазмы (для окраски ядра в красный цвет применяют кармин, сафранин и т. д.). Специфическими красителями являются орсеин, окрашивающий эластические волокна в коричневый цвет, судан III окрашивает жир в желтый цвет, а четырехокись осмия – в черный цвет, нитрат серебра импрегнирует нервные клетки и волокна в цвета от коричневого до черного, метиленовый синий окрашивает нервные элементы в синий цвет.
Из множества различных красителей и их комбинаций, применяемых в современной общегистологической технике, наиболее распространенной является окраска гематоксилином и эозином.
Перед окраской срез подвергают депарафинированию, т. е. срезы последовательно проводят через растворитель парафина (ксилол), спирты нисходящей концентрации и помещают в чашку Петри с водой. Затем срезы обрабатывают в следующем порядке:
1) в растворе гематоксилина 5—10 мин;
2) в проточной воде 5—10 мин;
3) в дистиллированной воде 1–2 мин;
4) в растворе эозина 1—10 мин;
5) в дистиллированной воде 1–3 мин;
6) в 70 % спирте 1–2 мин;
7) в 96 % спирте 1–2 мин;
8) в 100 % спирте (абсолютный) 1–2 мин;
9) в карболксилоле 1–3 мин;
10) в ксилоле 1–3 мин;
11) в кедровом или канадском бальзаме (срез помещают в каплю бальзама между предварительно обезжиренными предметным и покровным стеклами).
1.7. Заключение и этикетирование (маркировка) препаратов
После заключения среза в бальзам и под предметное стекло, т. е. после приготовления так называемого постоянного препарата, он подлежит обозначению – маркировке. Для этого справа и слева от покровного стекла наклеивают этикетки с надписями: слева – описание ткани или органа, объекта, из которого получен материал, справа – метод окрашивания; в необходимых случаях указывают фиксацию материала и дату изготовления препарата.
1.8. Микроскоп и правила работы с ним
Микроскоп – сложный и самый распространенный в биологии и медицине прибор для изучения мелких органов, клеток и тканей организма (рис. 1.3). Наиболее важное значение в нем имеют объективы. Они находятся в непосредственной близости от рассматриваемого объекта, отчего и получили свое название. Объектив состоит из ряда линз, закрепленных в оправе с международной стандартной резьбой в 36 витков в тубусе микроскопа любой оптической фирмы.
Увеличение микроскопа равно произведению цифровых значений объектива и окуляра, скоординированных на тубусе микроскопа, т. е. поставленных друг против друга.
Цена увеличения нанесена на обойме объектива и в верхней линзовой плашке окуляра [в рабочих студенческих микроскопах значения таковы: объектив ×8, ×40, ×90 (иммерсионный); окуляр ×7, ×10].
Общее увеличение светооптического микроскопа равно 2000–2500, однако полезное увеличение, способствующее выявлению деталей объекта, составляет 1500–1600.
Изображение, полученное от простой сферической линзы, направленной непосредственно на рассматриваемый объект, имеет два недостатка: сферическую и хроматическую аберрации, суть которых заключается в следующем.
Известно, что в двояковыпуклой линзе лучи, более удаленные от центра, т. е. центральной оптической оси, сильнее преломляются и пересекают главную оптическую ось на сравнительно близких расстояниях от центра линзы. Лучи, расположенные недалеко от оси, будут преломляться меньше и отдаляются от центра линзы. Таким образом, вместо стигматического точечного изображения возникает расплывчатое пятно. Такая погрешность оптической линзы получила название сферической аберрации.
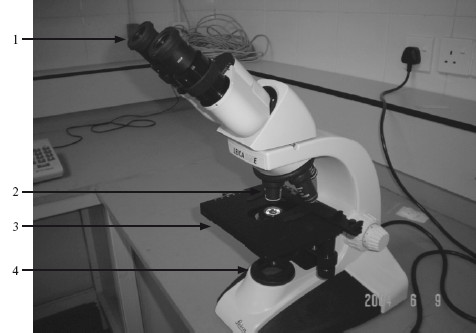
Рис. 1.3. Световой микроскоп.
1 – окуляр; 2 – объектив; 3 – предметный столик; 4 – источник света.
Количественно сферическая аберрация характеризуется продольной аберрацией – линейным расстоянием между точками пересечения крайних и центральных лучей с главной оптической осью.
Продольные аберрации обусловлены материалом линзы и ее кривизной. В последнем случае аберрации собирательной и рассеивающей линз противоположны по знаку, что позволяет, комбинируя такие линзы в объективе, уменьшить сферическую аберрацию. Это в микроскопах достигается путем набора линз разной значимости в одном объективе.
Кроме сферической, существует хроматическая аберрация, связанная с тем, что волны различной длины преломляются неодинаково: фиолетовые сильнее, красные меньше всего. В результате этого белое пятно будет цветным, окрашенным во все цвета спектра на усредненном экране. Такая наслойка дополнительного цвета на окрашенные гистологические препараты нежелательна и должна быть сведена до минимума. Это достигается комбинацией линз из стекла специального состава. Такая система называется ахроматической и в простом варианте состоит из выпуклой линзы, изготовленной из кронгласа (легкий сорт стекла), склеенной с двояковыпуклой линзой из флинтгласса (тяжелый сорт стекла).
Все объективы микроскопа делятся на ахроматы, в которых устранена аберрация двух наиболее ярких цветов спектра – желтого и зеленого, апохроматы, в которых хроматическая аберрация устранена почти полностью, и полуахроматы; так называемые флюоритовые, занимающие среднее положение между названными объективами.
Для исследования мелких деталей, особенно при цитологических наблюдениях, используют иммерсионные объективы с высокой разрешающей силой.
Чтобы усилить освещенность, в таких системах применяют жидкости, уменьшающие рассеивание света (водная и масляная иммерсия) и заполняющие пространство между верхней поверхностью покровного стекла и передней линзой объектива.
Использование иммерсионного масла, имеющего одинаковый со стеклом и канадским бальзамом коэффициент преломления, создает идеальную гомогенную среду, обеспечивающую возможность различать мельчайшие детали клеток и тканей.
Разрешающей способностью называется способность объектива «разрешить», т. е. показать, наименьшее расстояние между двумя близлежащими деталями предмета, при котором они еще видны раздельно. Она выражается формулой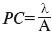 , где λ – длина световой волны, А – числовая апертура.
, где λ – длина световой волны, А – числовая апертура.
Числовая апертура – произведение показателя преломления среды, находящейся между предметом и объективом, и синуса половины угла, образованного двумя крайними лучами, которые еще проходят объектив. Формула ее такова: А = n · sin а, где n – коэффициент преломления среды, α – значение угла. В цифровом выражении показатель А выгравирован на обойме каждого объектива ниже знака линейного увеличения более мелким шрифтом. Таким образом, исследователь освобожден от необходимости вычисления апертуры по приведенной формуле. При подборе объективов для практических целей необходимо всегда обращать внимание на этот показатель: чем больше числовая апертура, тем выше разрешающая способность объектива, следовательно, и всего микроскопа как прибора, так как окуляр на значение разрешающей силы не влияет, что видно из ранее приведенных формул. Теоретически разрешение светового микроскопа составляет 0,2 мкм, практически оно обычно равно 0,4 мкм.
Приступая к микроскопированию гистологических препаратов, необходимо помнить следующее: всякое исследование надо начинать при малом увеличении для ознакомления с общим видом препарата, расположением тканевых структур различного характера, особенностями их окраски, сочетанием комплексов клеточных структур в различных слоях органа.
При рассеянном искусственном и естественном освещении пользуются вогнутым зеркалом, при точечном источнике света – плоской его поверхностью, регулируя конденсором, особенно при работе с иммерсионными объективами, степень освещенности поля зрения.
Перед переходом на большое увеличение нужную деталь, подлежащую изучению, надо установить при малом увеличении в центре зрения и, не поднимая тубуса микроскопа макрометрическим винтом, плавным движением перевести револьвер на большое увеличение; дальнейшую юстировку (отработка четкости изображения) надо проводить с помощью только микрометрического винта.
Микроскоп нужно содержать в чистоте, после работы вытирать от пыли фланелевой или марлевой салфеткой и предохранять от механических повреждений, не оставлять в местах солнечного освещения или теплового прогревания.
По окончании работы необходимо перевести револьвер микроскопа на малое увеличение, снять с предметного столика препарат, очистить от пыли и грязи сначала оптические, а затем механические части и сдать лаборанту свое рабочее место и все, что было принято перед лабораторной работой.
Увеличение микроскопа равно произведению цифровых значений объектива и окуляра, скоординированных на тубусе микроскопа, т. е. поставленных друг против друга.
Цена увеличения нанесена на обойме объектива и в верхней линзовой плашке окуляра [в рабочих студенческих микроскопах значения таковы: объектив ×8, ×40, ×90 (иммерсионный); окуляр ×7, ×10].
Общее увеличение светооптического микроскопа равно 2000–2500, однако полезное увеличение, способствующее выявлению деталей объекта, составляет 1500–1600.
Изображение, полученное от простой сферической линзы, направленной непосредственно на рассматриваемый объект, имеет два недостатка: сферическую и хроматическую аберрации, суть которых заключается в следующем.
Известно, что в двояковыпуклой линзе лучи, более удаленные от центра, т. е. центральной оптической оси, сильнее преломляются и пересекают главную оптическую ось на сравнительно близких расстояниях от центра линзы. Лучи, расположенные недалеко от оси, будут преломляться меньше и отдаляются от центра линзы. Таким образом, вместо стигматического точечного изображения возникает расплывчатое пятно. Такая погрешность оптической линзы получила название сферической аберрации.

Рис. 1.3. Световой микроскоп.
1 – окуляр; 2 – объектив; 3 – предметный столик; 4 – источник света.
Количественно сферическая аберрация характеризуется продольной аберрацией – линейным расстоянием между точками пересечения крайних и центральных лучей с главной оптической осью.
Продольные аберрации обусловлены материалом линзы и ее кривизной. В последнем случае аберрации собирательной и рассеивающей линз противоположны по знаку, что позволяет, комбинируя такие линзы в объективе, уменьшить сферическую аберрацию. Это в микроскопах достигается путем набора линз разной значимости в одном объективе.
Кроме сферической, существует хроматическая аберрация, связанная с тем, что волны различной длины преломляются неодинаково: фиолетовые сильнее, красные меньше всего. В результате этого белое пятно будет цветным, окрашенным во все цвета спектра на усредненном экране. Такая наслойка дополнительного цвета на окрашенные гистологические препараты нежелательна и должна быть сведена до минимума. Это достигается комбинацией линз из стекла специального состава. Такая система называется ахроматической и в простом варианте состоит из выпуклой линзы, изготовленной из кронгласа (легкий сорт стекла), склеенной с двояковыпуклой линзой из флинтгласса (тяжелый сорт стекла).
Все объективы микроскопа делятся на ахроматы, в которых устранена аберрация двух наиболее ярких цветов спектра – желтого и зеленого, апохроматы, в которых хроматическая аберрация устранена почти полностью, и полуахроматы; так называемые флюоритовые, занимающие среднее положение между названными объективами.
Для исследования мелких деталей, особенно при цитологических наблюдениях, используют иммерсионные объективы с высокой разрешающей силой.
Чтобы усилить освещенность, в таких системах применяют жидкости, уменьшающие рассеивание света (водная и масляная иммерсия) и заполняющие пространство между верхней поверхностью покровного стекла и передней линзой объектива.
Использование иммерсионного масла, имеющего одинаковый со стеклом и канадским бальзамом коэффициент преломления, создает идеальную гомогенную среду, обеспечивающую возможность различать мельчайшие детали клеток и тканей.
Разрешающей способностью называется способность объектива «разрешить», т. е. показать, наименьшее расстояние между двумя близлежащими деталями предмета, при котором они еще видны раздельно. Она выражается формулой
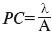 , где λ – длина световой волны, А – числовая апертура.
, где λ – длина световой волны, А – числовая апертура.Числовая апертура – произведение показателя преломления среды, находящейся между предметом и объективом, и синуса половины угла, образованного двумя крайними лучами, которые еще проходят объектив. Формула ее такова: А = n · sin а, где n – коэффициент преломления среды, α – значение угла. В цифровом выражении показатель А выгравирован на обойме каждого объектива ниже знака линейного увеличения более мелким шрифтом. Таким образом, исследователь освобожден от необходимости вычисления апертуры по приведенной формуле. При подборе объективов для практических целей необходимо всегда обращать внимание на этот показатель: чем больше числовая апертура, тем выше разрешающая способность объектива, следовательно, и всего микроскопа как прибора, так как окуляр на значение разрешающей силы не влияет, что видно из ранее приведенных формул. Теоретически разрешение светового микроскопа составляет 0,2 мкм, практически оно обычно равно 0,4 мкм.
Приступая к микроскопированию гистологических препаратов, необходимо помнить следующее: всякое исследование надо начинать при малом увеличении для ознакомления с общим видом препарата, расположением тканевых структур различного характера, особенностями их окраски, сочетанием комплексов клеточных структур в различных слоях органа.
При рассеянном искусственном и естественном освещении пользуются вогнутым зеркалом, при точечном источнике света – плоской его поверхностью, регулируя конденсором, особенно при работе с иммерсионными объективами, степень освещенности поля зрения.
Перед переходом на большое увеличение нужную деталь, подлежащую изучению, надо установить при малом увеличении в центре зрения и, не поднимая тубуса микроскопа макрометрическим винтом, плавным движением перевести револьвер на большое увеличение; дальнейшую юстировку (отработка четкости изображения) надо проводить с помощью только микрометрического винта.
Микроскоп нужно содержать в чистоте, после работы вытирать от пыли фланелевой или марлевой салфеткой и предохранять от механических повреждений, не оставлять в местах солнечного освещения или теплового прогревания.
По окончании работы необходимо перевести револьвер микроскопа на малое увеличение, снять с предметного столика препарат, очистить от пыли и грязи сначала оптические, а затем механические части и сдать лаборанту свое рабочее место и все, что было принято перед лабораторной работой.
Глава 2
Строение клетки
Клетка (cellula) – наименьшая структурная единица живого, способная к независимому существованию. Она является основой развития, строения и жизнедеятельности всех животных и растительных организмов.
Главные функции клетки: возбудимость, проводимость, сократимость, поглощение и ассимиляция, дыхание, секреция, экскреция, рост и репродукция.
Клетка состоит из трех основных частей: ядра, цитоплазмы и плазматической мембраны (цитолемма).
Ядро (nucleus) – система генетической детерминации и регуляции белкового синтеза в клетке (рис. 2.1).
Структурные компоненты ядра: хроматин (хромосомы), ядерная оболочка (кариолемма), ядрышко, нуклеоплазма (ядерный сок).

Рис. 2.1. Фибробласт. Ядро. ТЭМ. ×22 000.
1 – ядро; 2 – гетерохроматин; 3 – эухроматин; 4 – ядерное тельце; 5 – кариолемма; 6 – комплекс Гольджи; 7 – митохондрии; 8 – лизосомы; 9 – цистерны гранулярной ЭПС.
Функции ядра: воспроизведение, накопление, хранение и распределение генетического материала (содержит 23 пары ДНК хромосом); регуляция синтеза белка в цитоплазме посредством макромолекул рибосомной РНК (рРНК), информационной РНК (иРНК) и транспортной РНК (тРНК).
Различают эухроматин (слабоокрашиваемый, диспергированный, менее конденсированный, активно участвует в процессах транскрипции), соответствует сегментам хромосом, которые деспирализованы и открыты для транскрипции, и гетерохроматин (хорошо окрашиваемый, конденсированный, не постоянно участвует в процессах транскрипции), соответствующий конденсированным, плотно скрученным сегментам хромосом.
Тельце Бара – скопление гетерохроматина, соответствующее неактивной Х-хромосоме у особей женского пола.
Организация хромосом сложная. Они состоят из спиралей, которые сформированы из гистоновых нуклеосом, образующих сердечники, вокруг которых обернута двойная спираль ДНК.
Молекула ДНК построена из двух антипараллельных цепей с комплементарной последовательностью нуклеотидов. Участок молекулы ДНК, кодирующий последовательность аминокислотных остатков в полипептидной цепи, называется геномом.
Ядерная оболочка (nucleolemma) состоит из наружной и внутренней параллельных мембран, разделенных узким перинуклеарным пространством – цистерной, диаметром 10–30 нм. Мембраны продолжаются друг в друга вокруг ядерных пор.
К наружной ядерной мембране прикреплены рибосомы. Наружная мембрана переходит в гранулярную эндоплазматическую сеть (ГЭПС).
Внутренняя ядерная мембрана содержит сеть переплетающихся промежуточных (виментиновых) филаментов, связанных с ядерной пластинкой, к которой прикрепляются интерфазные хромосомы. Ядерная пластинка состоит из переплетенных промежуточных филаментов (ламинов) толщиной 80—100 нм, образующих кариоскелет.
Ядерные поры – это каналы связи диаметром 70—100 нм между ядром и цитоплазмой, их число и распределение изменчивы. Двусторонний транспорт через пору обеспечивается белками экспортинами (транспортируют РНК из ядра) и импортинами (переносят белковые субъединицы рибосом).
Ядерная пора изнутри выстлана специализированными структурами, образующими комплекс ядерной поры.
Комплекс ядерной поры (КЯП) состоит из немембранных структур: белка-рецептора на сигналы ядерного импорта, а также крупных белковых гранул, определяющих границы поры.
Главные функции клетки: возбудимость, проводимость, сократимость, поглощение и ассимиляция, дыхание, секреция, экскреция, рост и репродукция.
Клетка состоит из трех основных частей: ядра, цитоплазмы и плазматической мембраны (цитолемма).
Ядро (nucleus) – система генетической детерминации и регуляции белкового синтеза в клетке (рис. 2.1).
Структурные компоненты ядра: хроматин (хромосомы), ядерная оболочка (кариолемма), ядрышко, нуклеоплазма (ядерный сок).

Рис. 2.1. Фибробласт. Ядро. ТЭМ. ×22 000.
1 – ядро; 2 – гетерохроматин; 3 – эухроматин; 4 – ядерное тельце; 5 – кариолемма; 6 – комплекс Гольджи; 7 – митохондрии; 8 – лизосомы; 9 – цистерны гранулярной ЭПС.
Функции ядра: воспроизведение, накопление, хранение и распределение генетического материала (содержит 23 пары ДНК хромосом); регуляция синтеза белка в цитоплазме посредством макромолекул рибосомной РНК (рРНК), информационной РНК (иРНК) и транспортной РНК (тРНК).
Различают эухроматин (слабоокрашиваемый, диспергированный, менее конденсированный, активно участвует в процессах транскрипции), соответствует сегментам хромосом, которые деспирализованы и открыты для транскрипции, и гетерохроматин (хорошо окрашиваемый, конденсированный, не постоянно участвует в процессах транскрипции), соответствующий конденсированным, плотно скрученным сегментам хромосом.
Тельце Бара – скопление гетерохроматина, соответствующее неактивной Х-хромосоме у особей женского пола.
Организация хромосом сложная. Они состоят из спиралей, которые сформированы из гистоновых нуклеосом, образующих сердечники, вокруг которых обернута двойная спираль ДНК.
Молекула ДНК построена из двух антипараллельных цепей с комплементарной последовательностью нуклеотидов. Участок молекулы ДНК, кодирующий последовательность аминокислотных остатков в полипептидной цепи, называется геномом.
Ядерная оболочка (nucleolemma) состоит из наружной и внутренней параллельных мембран, разделенных узким перинуклеарным пространством – цистерной, диаметром 10–30 нм. Мембраны продолжаются друг в друга вокруг ядерных пор.
К наружной ядерной мембране прикреплены рибосомы. Наружная мембрана переходит в гранулярную эндоплазматическую сеть (ГЭПС).
Внутренняя ядерная мембрана содержит сеть переплетающихся промежуточных (виментиновых) филаментов, связанных с ядерной пластинкой, к которой прикрепляются интерфазные хромосомы. Ядерная пластинка состоит из переплетенных промежуточных филаментов (ламинов) толщиной 80—100 нм, образующих кариоскелет.
Ядерные поры – это каналы связи диаметром 70—100 нм между ядром и цитоплазмой, их число и распределение изменчивы. Двусторонний транспорт через пору обеспечивается белками экспортинами (транспортируют РНК из ядра) и импортинами (переносят белковые субъединицы рибосом).
Ядерная пора изнутри выстлана специализированными структурами, образующими комплекс ядерной поры.
Комплекс ядерной поры (КЯП) состоит из немембранных структур: белка-рецептора на сигналы ядерного импорта, а также крупных белковых гранул, определяющих границы поры.
