Страница:
На сегодняшний момент существует несколько гипотез, пытающихся объяснить влияние тренировки на синтез белка в мышце. Но все эти гипотезы можно объединить в два конкурирующих направления – теория накопления и теория разрушения.
Суть теории накопления состоит в том, что во время мышечной деятельности в клетке вырабатываются некие факторы-регуляторы, оказывающие влияние на процессы считывания информации с ДНК. Некоторые ученые относят к этим факторам повышение кислотности среды в результате мышечной деятельности, влияющее на спирилизацию ДНК. Некоторые относят к факторам-регуляторам свободный креатин – при интенсивной деятельности креатинфосфат, содержащийся в клетке, в целях восполнения энергии передает свою фосфатную группу на АДФ, превращаясь в креатин, и именно креатин, по мнению ученых, оказывает регулирующее воздействие на ДНК.
Думаю, что подобные процессы должны иметь место в регуляции интенсивности белкового обмена, – как известно в случае обездвиживания мышцы интенсивность синтеза белка в клетках снижается, то есть движение само по себе является фактором-регулятором белкового синтеза. Между тем я не могу отвести существенную роль этим процессам в гипертрофии мышц, так как свое регулирующее воздействие данные факторы оказывают непосредственно во время работы мышц, а синтез белка идет в основном после прекращения нагрузки во время отдыха, когда концентрация факторов-регуляторов уже возвращается к уровню, характерному для состояния покоя.
Я полагаю, что более полную картину способна сформировать теория разрушения, суть которой заключается в нижеследующем.
Как я уже упоминал выше – организм это саморегулируемая система, настроенная миллионами лет эволюции на поддержание постоянства внутренней среды. Разрушение внутренних структур организма автоматически запускает процессы, стремящиеся восстановить утраченное равновесие. Так разрушение белковых структур клетки должно тут активизировать восстановительные процессы синтеза белка, создав все необходимые условия для их протекания. То, что активность синтеза белка в поврежденной ткани в несколько раз выше, чем в нормальных условиях – это факт. Интенсивные восстановительные процессы не могут затихнуть сразу по завершению восстановления поврежденных структур. Как и все прочие процессы, процессы синтеза белка имеют некоторую инерцию, поэтому, в результате восстановления будет наблюдаться некоторый избыточный анаболизм, приводящий к превышению уровня белка в клетке над исходным. Другими словами, будет наблюдаться хорошо известная нам по восстановлению энергетических ресурсов суперкомпенсация. То есть восстановление белковых структур клетки подчиняется тем же общим законам адаптации, с которыми вы уже знакомы.
Обычно регулирующую роль тренировки в гипертрофии мышц сводят лишь к интенсификации процессов синтеза РНК в ядрах клеток. Между тем общий объем мышцы зависит от количества в ней мышечных клеток/волокон и от количества ядер в мышечных клетках/волокнах (напоминаю, что мышечная клетка и волокно это один и тоже объект). Согласно утвердившимся в среде спортивных физиологов представлениям число мышечных клеток/волокон задается генетически и не меняется в ходе тренировок, – об этом свидетельствуют большинство экспериментов, проводившихся в данном направлении (Шекман Б.С.), хотя имеется и ряд экспериментальных данных заставляющих усомнится в этом постулате (об этом чуть позже). Объясняется неизменность количества клеток/волокон в мышце тем, что мышечная клетка представляет из себя сложный многоядерный объект, ядра которого утрачивают способность к делению, как и вся клетка, еще на этапе эмбрионального развития. Между тем потенциальный объем клетки/волокна зависит от количества в ней клеточных ядер – источников РНК. При прочих равных условиях волокно с большим количеством ядер будет иметь больший объем.
А теперь внимание! Как показывает ряд экспериментов (M Cabric и N.T.James) в ходе тренировок в мышечных клетках увеличивается количество клеточных ядер. Но ядра мышечных клеток не способны к делению! Так откуда же взялись новые ядра?
Ответ на этот вопрос можно найти в работах ученых, занимающихся проблемами регенерации травмированной ткани. Как оказалось, на этапе эмбрионального развития, не все клетки эмбриона, из которых развивается мышечная ткань, сливаются в мышечные волокна и утрачивают способность к делению, часть из них (около 10%) остается в оболочке волокон в виде клеток-сателлитов. Клетки-сателлиты сохраняют способность к делению на протяжении всей жизни и являются резервом восстановления мышечной ткани. Только клетки сателлиты способны быть источником новых ядер в волокне. Как показывают эксперименты (Володина А.В., Женевская Р.П., Климов А.А. и Данилов Р.К., Улумбеков Э.Г. и Челышев Ю.А.) повреждение волокна приводит к активации клеток-сателлитов, которые, освободившись из оболочки, вступают в цикл деления, затем сливаются вместе, восстанавливая поврежденные волокна. Логично предположить, что к активации клеток-сателлитов после тренировки приводят процессы аналогичные травмам волокон. Многие знают на собственном опыте, что интенсивная тренировка, особенно после продолжительного перерыва, отзывается болью в последующие несколько дней отдыха. Боль явно свидетельствует о разрушениях внутренней структуры мышц. Микроскопические исследования показывают, что в результате тренировок в ряде мышечных волокон нарушается упорядоченное расположение миофибрилл, наблюдается распад митохондрий, а в крови повышается уровень лейкоцитов, как при травмах или инфекционном воспалении (Морозов В.И., Штерлинг М.Д. с соавторами). Разрушение внутренней структуры мышечного волокна во время тренировки, назовем его микротравмой, приводит к появлению в волокне обрывков белковых молекул, что активизирует лизосомы, «переваривающие», с помощью содержащихся в них ферментов, белковые структуры, подлежащие уничтожению. Если лизосомы не справляются с объемом повреждений, то через сутки наблюдается пик активности боле мощных «чистильщиков» – фагоцитов. Фагоциты – клетки, живущие в межклеточном веществе и крови, основная задача которых уничтожение поврежденных тканей и чужеродных микроорганизмов. Именно продукты жизнедеятельности фагоцитов вызывают воспалительные процессы и боль в мышцах, через сутки после тренировки. Но между тем, по-видимому, именно благодаря деятельности лизосом и фагоцитов повреждается оболочка мышечного волокна, и из нее высвобождаются клетки-сателлиты. Освободившись, клетки-сателлиты начинают цикл деления и сливаются с поврежденным волокном, увеличивая в нем количество ядер, тем самым, повышая его потенциальную возможность в синтезе белка.
В свете выше сказанного, я бы не стал полностью исключать возможность высвобождения клеток-сателлит в межклеточное пространство и слияние их в новые волокна, что достоверно наблюдалось в случае обширных повреждений мышечной ткани, правда, новые волокна в этих случаях образовывались в замен утраченных, что вовсе не приводило у общему увеличению количества волокон в мышце. Но, если предположить, что повреждения волокна не столь обширны, чтобы привести к его гибели, а клетки сателлиты пошли по пути слияния в новое волокно, то гиперплазия становится не таким уж невероятным фактом, как это принято считать. Тем более что есть ряд экспериментов выбивающихся из общих представлений о невозможности гиперплазии. Так Goneya W, удалось на 19-20% увеличить количество мышечных волокон в лапах кошек, которых он заставлял тренироваться с прогрессирующей нагрузкой. А Yamada S, Buffinger N, Dimario J&Strohman R (1989) и Larson L&Tesch PA (1986) проводили взятия проб из мышечной ткани у элитных бодибилдеров, и контрольной группы людей, не обладающих значительной мускулатурой, анализ проб показал, что поперечное сечение волокон у элитных бодибилдеров лишь незначительно больше чем у представителей контрольной группы, в то время как поперечное сечение мышц различалось существенно, то есть бодибилдеры обладают большим количеством волокон по сравнению с контрольной группой, что может быть либо следствием гиперплазии волокон, либо элитные бодибилдеры от рождения обладали значительно большим количеством волокон, чем обычные люди, но эти волокна были крайне тонкими (так как до тренировки элитные бодибилдеры обладали мускулатурой обычных размеров). В последнее хочется верить меньше всего, так как эта теория ставит крест на возможности обычных людей добиться сколько-нибудь значительной гипертрофии мышц. Однако не будем зацикливаться на вопросах гиперплазии, и так как возможность последней у человека считается недоказанной, будем по-прежнему исходить из того, что рост мышц происходит исключительно по причине гипертрофии уже существующих волокон. Но вот одной из причин гипертрофии самих волокон, как раз и является увеличение в них количества клеточных ядер, что по оказываемому эффекту практически равносильно гиперплазии.
Вернемся к рассмотрению процессов происходящих в мышце во время восстановления после тренировки. По завершении катаболического этапа саморазрушения поврежденных структур начинается этап компенсации – восстановления внутренней структуры волокон, который, ради справедливости должен заметить, не всегда может завершиться суперкомпенсацией. При слишком обширных травмах или отсутствии условий для восстановления результат может быть прямо противоположным.
Против теории разрушения чаще всего приводят следующие аргументы: «Если причиной роста являются микротравмы, то почему же мышца не растет, если ее бить палками?»
Ответ на этот вопрос можно найти в работе Володиной А.В., целью ее докторской диссертации является изучение процессов, препятствующих реализации регенерационного потенциала, заложенного в мышечном волокне. Эксперименты показали, что, в условиях обширного повреждения волокон, сопровождающегося ишемией (нарушением кровоснабжения) поврежденных тканей, вызывающей дефицит в снабжении волокна кислородом и питательными веществами, часть клеток-сателлит гибнет и поглощается фагоцитами, а часть идет по пути превращения не в мышечные клетки, а в фибробласты (клетки, производящие коллаген). В итоге место повреждения затягивается соединительной тканью, а количество волокон в мышечной ткани снижается, по причине гибели части из них от повреждений.
Очевидно, что при микротравмах волокон – разрушении внутренней структуры волокна без нарушения его целостности, в отличие от травм целой мышцы, снабжение волокон кислородом, а так же его иннервация не нарушены, поэтому условия, приводящие к гибели целых волокон и клеток-сателлитов, отсутствуют.
И так, если объем микротравм, полученных в ходе тренировки, был не слишком велик для срыва восстановительных процессов, но достаточен для активации клеток-сателлитов, то в подвергшемся тренировочной нагрузке волокне увеличивается количество клеточных ядер. Восстановление энергетических ресурсов после тренировки приводит к суперкомпенсации энергетических веществ, а лизис разрушенных тренировкой белков увеличивает содержание свободных аминокислот непосредственно в волокне, что в совокупности создает благоприятные условия для интенсификации процессов синтеза белка. При условии достаточного по времени и полноценного отдыха, отсутствия новых стрессовых нагрузок, адекватного снабжения волокна энергией и пластическими ресурсами (аминокислотами) интенсивные процессы восстановления приведут к накоплению в волокне белковых структур сверх уровня, который был до тренировки, то есть будет наблюдаться гипертрофия мышц.
Надо отметить, что последовательность протекания фаз общей неспецифической адаптационной реакции (синдрома стресса) такова, что обеспечивает поддержку описанных выше регенерационных процессов на системном уровне. Первая катаболическая фаза стресс реакции, сопровождается выбросом кортикостероидов, что приводит к мобилизации энергетических ресурсов организма и обеспечивает индукцию ферментов лизосом и фагоцитов, расщепляющих белок (кортикостероиды являются теми гормонами, которые активируют на ДНК клеток гены протеолитических ферментов), что способствует скорейшему очищению волокон от поврежденных структур. В последующей фазе стресс реакции синтез кортикостероидов сменяется синтезом анаболических гормонов, что обеспечивает на системном уровне компенсаторный анаболизм.
Как тут не вспомнить об основном законе философии – единстве и борьбе противоположностей. Анаболизм активируется катаболизмом – рост мышц есть следствие их предварительного разрушения.
Ученый и пауэрлифтер Фредерик Хетфилд, считающий роль микротравм в тренировочном процессе скорее отрицательной из-за необходимости длительного восстановления, полагает, что причиной микротравм является повреждение миофибрильных нитей во время негативных повторений. Вот как он описывает механизм этих повреждений: «Так как количество перекрестных мостиков, старающихся сократить мышцу недостаточно, они буквально „продираются“ сквозь мостики соединений нити, стараясь вызвать концентрическое сокращение. Однако сцепиться как следует им не удается, они срываются и повреждаются. Эти действия, очень напоминающие протаскивание щетины одной зубной щетки через другую, сопровождаются сильным трением, и мышечные нити разрушаются»
Не правда ли образно? Но, на мой взгляд, несколько сумбурно – так пишут когда хотят объяснить то, что до конца не понимают сами. К сожалению, мэтр ошибся дважды.
Во-первых, микротравмы возникают не только при негативных повторениях, но и при позитивном движении.
Во-вторых, использовать термин «трение» для описания взаимодействия молекул некорректно. Сила трения введена в физике для описания на макроуровне поверхностного взаимодействия тел специально, дабы абстрагироваться от истинной природы «трения» – электромагнитного взаимодействия молекул поверхностного слоя.
Механизм повреждения миофибрильных нитей носит несколько иной характер, чем описывает Хетфилд, и мне удалось его аналитически смоделировать.
Для понимания механизма повреждения миофибрильных нитей следует обратиться к рассмотрению фаз движения миозинового мостика, которые вкратце уже описаны в первой части статьи. Сейчас остановимся подробнее на этом вопросе (рис. 8).
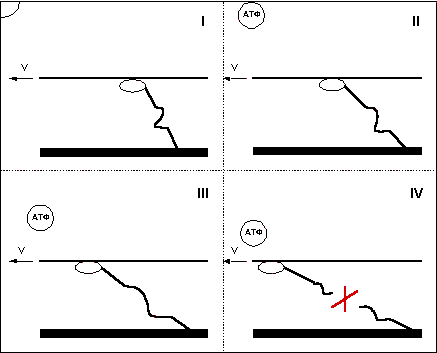
Анализируя фазы движения миозинового мостика, я сразу обратил внимание на тот факт, что для отцепления мостика от актина требуется молекула АТФ. При скольжении нитей миозина вдоль актина под действием сил тянущих мостиков (позитивное движение) или под действием внешней силы (негативное движение) сцепленные мостики растягиваются и мешают движению, этим, как вы помните, объясняется различие в силе развиваемой волокном при удлинении и сокращении и сокращении с разной скоростью. Когда АТФ в мышце находится в достаточном количестве, мостики успевают вовремя отцепиться, но что будет, если, при снижении концентрации АТФ в мышце, молекула АТФ не успеет отцепить головку миозина до того, как растяжение мостика превысит предел его прочности? Естественно сцепленный мостик разорвется! (Рис. 9).
Вы, наверное, слышали о состоянии трупного окоченения мышц? Наступает оно потому, что в мертвом организме запасы АТФ не восполняются, и мостики миозина оказываются накрепко сцепленными с актином. Представьте, что произойдет с мышцей трупа, если ее насильно растянуть. Так вот нечто подобное происходит и с отдельными волокнами живой мышцы, в которых по причине интенсивной деятельности резко снижается уровень АТФ.
Надо понимать, что изображенное мной место разрыва мостика достаточно условно, я не могу точно сказать, где находится самое слабое звено в цепи, но то, что при движении, сопровождающемся недостатком АТФ, должно происходить нефизиологическое разрушение акто-миозинового комплекса – неоспоримо.
Сомневаться в правильности «отказной» теории, меня заставил и тот факт, что проявление боли в мышцах – вестника микротравм не имеет прямой связи с работой до «отказа». С одной стороны, на начальном этапе тренинга боль в мышцах возникает при любой работе, не зависимо от того был «отказ» или нет. С другой стороны регулярные тренировки приводят к тому, что даже работа сверх «отказа» (читинг, стриптиз и др.) не вызывает боли в мышцах – боль возвращается только после продолжительного перерыва в тренировках.
Эти противоречия заставили меня заняться детальным изучением процесса «отказа».
– Увеличение времени нахождения мостиков в ригорном – сцепленном не генерирующем силу состоянии (фаза V, VI);
– Увеличение времени нахождения мостиков в разомкнутом состоянии (фаза I, II).
Вспоминая аналогию с гребцами, скажем, что скорость движения лодки и развиваемая при этом сила тем выше, чем быстрее весла вытаскиваются из воды после гребка и чем меньше гребцы сидят с поднятыми веслами без дела.
Время нахождения мостика в ригорном состоянии зависит от того, как быстро АТФ вступит в контакт с головкой миозина. Как известно частицы вещества постоянно находятся в хаотическом движении (рис. 10). Предположим что r – некий радиус, ограничивающий область пространства вокруг головки миозина, при попадании в пределы которого молекулы АТФ становится возможным реакция, приводящая к отцеплению головки от актина.
Т=h/v
Естественно чем выше концентрация АТФ в мышце, тем меньше среднее расстояние между молекулами АТФ и головками миозина и тем меньше время нахождения мостиков в ригорном состоянии.
То есть сила волокна зависит от концентрации АТФ. При прочих равных условиях волокно с высокой концентрацией АТФ сильнее такого же волокна, но с меньшей концентрацией АТФ. Известно, что воспроизводство АТФ за счет креатинфосфата происходит почти мгновенно, поэтому можно сказать, что концентрация АТФ при работе мышцы зависит и от концентрации креатинфосфата. Таким образом:
Чем выше концентрация энергетических фосфатов (АТФ и креатинфосфата) в мышечном волокне, тем выше сила, развиваемая волокном.
После зависимости силы волокна от количества и поперечного сечения миофибрилл, влияние концентрации энергетических фосфатов на силу волокна является наиболее значимым. Именно по этой причине многие атлеты отмечают некоторую прибавку в силе, повышая уровень креатинфосфата в мышцах, принимая креатин, в качестве пищевой добавки.
Надо заметить, что зависимость силы волокна от концентрации энергетических фосфатов не является линейной. При высоких концентрациях, когда время ожидания контакта АТФ с головкой миозина станет меньше или сопоставимым со временем, необходимым для протекания химической реакции, приводящей к отделению головки миозина от актина, повышение концентрации АТФ и креатинфосфата будет мало влиять на скорость переключения мостиков и соответственно силу волокна. Зато низкие концентрации АТФ и креатинфосфата существенно снизят силу волокна, что может служить одной из причин отказа.
Рассмотрим второй фактор снижения силы сокращения – увеличение времени нахождения мостиков в разомкнутом состоянии (I, II фазы), что может происходить в результате снижения скорости гидролиза АТФ (снижения активности АТФазы – фермента ускоряющего реакцию гидролиза АТФ).
Расщепление АТФ и его воспроизводство за счет креатинфосфата вызывает накопление в мышце ортофосфорной кислоты, а гликолиз ведет к накоплению молочной кислоты. Активность АТФазы – фермента, благодаря которому происходит гидролиз АТФ, сильно зависит от кислотности среды. Как показывают эксперименты, максимум АТФазной активности достигается при среде близкой к нейтральной (рН=7), а при смещении среды мышцы в кислую сторону активность АТФазы падает, и при снижении рН среды до 5 АТФазная активность стремится к нулю (Богач П.Г. с соавторами, Поглазов Б.Ф). Таким образом, при накоплении кислых продуктов метаболизма АТФаза миозина постепенно снижает скорость гидролиза АТФ, и мостики теряют способность сцепляться с актином, при этом мышца снижает силу сокращения, несмотря на поступающий от мотонейрона сигнал.
Существует и еще как минимум две причины снижения силы мышц – при длительной работе накопление продуктов метаболизма тормозит процессы передачи сигнала от мотонейрона к волокну (Романовский Д.Ю.), а в центральной нервной системе развивается охранительное торможение.
То есть «отказ» мышцы является суперпозицией различных причин и доминирование одного либо другого фактора определяется интенсивностью работы мышцы.
Для достижения максимальной мощности основных источников воспроизводства энергии (гликолиза в быстрых волокнах и окисления в медленных) требуется время.
Скорость воспроизводства АТФ за счет гликолиза достигает своего максимума только через 20 —30 секунд после начала интенсивной работы.
Для достижения максимальной скорости окислительного процесса требуется гораздо больше времени, связано это в основном с необходимостью оптимизацией процессов доставки кислорода. Скорость окисления становится максимальной лишь через 1-2 минуты работы мышц, этот эффект наверняка известен вам под названием «второе дыхание».
Между тем мышца развивает максимальную мощность с первых же долей секунд после поступления команды к сокращению, гликолиз, в совокупности с окислением, не в состоянии обеспечить необходимую скорость воспроизводства АТФ для поддержания этой мощности. Приведение в соответствие скоростей расхода и воспроизводства АТФ во время работы мышцы идет по двум направлениям. Во-первых, постепенная активизация гликолиза и окисления увеличивает количество АТФ, синтезируемого в единицу времени за счет этих источников. Во-вторых, накопление продуктов метаболизма, в результате деятельности гликолиза и окисления, снижает активность АТФазы миозина и соответственно скорость расхода АТФ. Благодаря этим двум процессам скорости расхода и воспроизводства АТФ выравниваются, и в дальнейшем движение продолжается с постепенно снижающейся мощностью, но в состоянии равновесия между количеством синтезируемого АТФ и потребностями мышцы в энергии. Отказ же мышцы наступает не из-за окончания запасов АТФ, а из-за снижения сократительной способности мышц в результате накопления кислых продуктов метаболизма.
Суть теории накопления состоит в том, что во время мышечной деятельности в клетке вырабатываются некие факторы-регуляторы, оказывающие влияние на процессы считывания информации с ДНК. Некоторые ученые относят к этим факторам повышение кислотности среды в результате мышечной деятельности, влияющее на спирилизацию ДНК. Некоторые относят к факторам-регуляторам свободный креатин – при интенсивной деятельности креатинфосфат, содержащийся в клетке, в целях восполнения энергии передает свою фосфатную группу на АДФ, превращаясь в креатин, и именно креатин, по мнению ученых, оказывает регулирующее воздействие на ДНК.
Думаю, что подобные процессы должны иметь место в регуляции интенсивности белкового обмена, – как известно в случае обездвиживания мышцы интенсивность синтеза белка в клетках снижается, то есть движение само по себе является фактором-регулятором белкового синтеза. Между тем я не могу отвести существенную роль этим процессам в гипертрофии мышц, так как свое регулирующее воздействие данные факторы оказывают непосредственно во время работы мышц, а синтез белка идет в основном после прекращения нагрузки во время отдыха, когда концентрация факторов-регуляторов уже возвращается к уровню, характерному для состояния покоя.
Я полагаю, что более полную картину способна сформировать теория разрушения, суть которой заключается в нижеследующем.
Как я уже упоминал выше – организм это саморегулируемая система, настроенная миллионами лет эволюции на поддержание постоянства внутренней среды. Разрушение внутренних структур организма автоматически запускает процессы, стремящиеся восстановить утраченное равновесие. Так разрушение белковых структур клетки должно тут активизировать восстановительные процессы синтеза белка, создав все необходимые условия для их протекания. То, что активность синтеза белка в поврежденной ткани в несколько раз выше, чем в нормальных условиях – это факт. Интенсивные восстановительные процессы не могут затихнуть сразу по завершению восстановления поврежденных структур. Как и все прочие процессы, процессы синтеза белка имеют некоторую инерцию, поэтому, в результате восстановления будет наблюдаться некоторый избыточный анаболизм, приводящий к превышению уровня белка в клетке над исходным. Другими словами, будет наблюдаться хорошо известная нам по восстановлению энергетических ресурсов суперкомпенсация. То есть восстановление белковых структур клетки подчиняется тем же общим законам адаптации, с которыми вы уже знакомы.
Обычно регулирующую роль тренировки в гипертрофии мышц сводят лишь к интенсификации процессов синтеза РНК в ядрах клеток. Между тем общий объем мышцы зависит от количества в ней мышечных клеток/волокон и от количества ядер в мышечных клетках/волокнах (напоминаю, что мышечная клетка и волокно это один и тоже объект). Согласно утвердившимся в среде спортивных физиологов представлениям число мышечных клеток/волокон задается генетически и не меняется в ходе тренировок, – об этом свидетельствуют большинство экспериментов, проводившихся в данном направлении (Шекман Б.С.), хотя имеется и ряд экспериментальных данных заставляющих усомнится в этом постулате (об этом чуть позже). Объясняется неизменность количества клеток/волокон в мышце тем, что мышечная клетка представляет из себя сложный многоядерный объект, ядра которого утрачивают способность к делению, как и вся клетка, еще на этапе эмбрионального развития. Между тем потенциальный объем клетки/волокна зависит от количества в ней клеточных ядер – источников РНК. При прочих равных условиях волокно с большим количеством ядер будет иметь больший объем.
А теперь внимание! Как показывает ряд экспериментов (M Cabric и N.T.James) в ходе тренировок в мышечных клетках увеличивается количество клеточных ядер. Но ядра мышечных клеток не способны к делению! Так откуда же взялись новые ядра?
Ответ на этот вопрос можно найти в работах ученых, занимающихся проблемами регенерации травмированной ткани. Как оказалось, на этапе эмбрионального развития, не все клетки эмбриона, из которых развивается мышечная ткань, сливаются в мышечные волокна и утрачивают способность к делению, часть из них (около 10%) остается в оболочке волокон в виде клеток-сателлитов. Клетки-сателлиты сохраняют способность к делению на протяжении всей жизни и являются резервом восстановления мышечной ткани. Только клетки сателлиты способны быть источником новых ядер в волокне. Как показывают эксперименты (Володина А.В., Женевская Р.П., Климов А.А. и Данилов Р.К., Улумбеков Э.Г. и Челышев Ю.А.) повреждение волокна приводит к активации клеток-сателлитов, которые, освободившись из оболочки, вступают в цикл деления, затем сливаются вместе, восстанавливая поврежденные волокна. Логично предположить, что к активации клеток-сателлитов после тренировки приводят процессы аналогичные травмам волокон. Многие знают на собственном опыте, что интенсивная тренировка, особенно после продолжительного перерыва, отзывается болью в последующие несколько дней отдыха. Боль явно свидетельствует о разрушениях внутренней структуры мышц. Микроскопические исследования показывают, что в результате тренировок в ряде мышечных волокон нарушается упорядоченное расположение миофибрилл, наблюдается распад митохондрий, а в крови повышается уровень лейкоцитов, как при травмах или инфекционном воспалении (Морозов В.И., Штерлинг М.Д. с соавторами). Разрушение внутренней структуры мышечного волокна во время тренировки, назовем его микротравмой, приводит к появлению в волокне обрывков белковых молекул, что активизирует лизосомы, «переваривающие», с помощью содержащихся в них ферментов, белковые структуры, подлежащие уничтожению. Если лизосомы не справляются с объемом повреждений, то через сутки наблюдается пик активности боле мощных «чистильщиков» – фагоцитов. Фагоциты – клетки, живущие в межклеточном веществе и крови, основная задача которых уничтожение поврежденных тканей и чужеродных микроорганизмов. Именно продукты жизнедеятельности фагоцитов вызывают воспалительные процессы и боль в мышцах, через сутки после тренировки. Но между тем, по-видимому, именно благодаря деятельности лизосом и фагоцитов повреждается оболочка мышечного волокна, и из нее высвобождаются клетки-сателлиты. Освободившись, клетки-сателлиты начинают цикл деления и сливаются с поврежденным волокном, увеличивая в нем количество ядер, тем самым, повышая его потенциальную возможность в синтезе белка.
В свете выше сказанного, я бы не стал полностью исключать возможность высвобождения клеток-сателлит в межклеточное пространство и слияние их в новые волокна, что достоверно наблюдалось в случае обширных повреждений мышечной ткани, правда, новые волокна в этих случаях образовывались в замен утраченных, что вовсе не приводило у общему увеличению количества волокон в мышце. Но, если предположить, что повреждения волокна не столь обширны, чтобы привести к его гибели, а клетки сателлиты пошли по пути слияния в новое волокно, то гиперплазия становится не таким уж невероятным фактом, как это принято считать. Тем более что есть ряд экспериментов выбивающихся из общих представлений о невозможности гиперплазии. Так Goneya W, удалось на 19-20% увеличить количество мышечных волокон в лапах кошек, которых он заставлял тренироваться с прогрессирующей нагрузкой. А Yamada S, Buffinger N, Dimario J&Strohman R (1989) и Larson L&Tesch PA (1986) проводили взятия проб из мышечной ткани у элитных бодибилдеров, и контрольной группы людей, не обладающих значительной мускулатурой, анализ проб показал, что поперечное сечение волокон у элитных бодибилдеров лишь незначительно больше чем у представителей контрольной группы, в то время как поперечное сечение мышц различалось существенно, то есть бодибилдеры обладают большим количеством волокон по сравнению с контрольной группой, что может быть либо следствием гиперплазии волокон, либо элитные бодибилдеры от рождения обладали значительно большим количеством волокон, чем обычные люди, но эти волокна были крайне тонкими (так как до тренировки элитные бодибилдеры обладали мускулатурой обычных размеров). В последнее хочется верить меньше всего, так как эта теория ставит крест на возможности обычных людей добиться сколько-нибудь значительной гипертрофии мышц. Однако не будем зацикливаться на вопросах гиперплазии, и так как возможность последней у человека считается недоказанной, будем по-прежнему исходить из того, что рост мышц происходит исключительно по причине гипертрофии уже существующих волокон. Но вот одной из причин гипертрофии самих волокон, как раз и является увеличение в них количества клеточных ядер, что по оказываемому эффекту практически равносильно гиперплазии.
Вернемся к рассмотрению процессов происходящих в мышце во время восстановления после тренировки. По завершении катаболического этапа саморазрушения поврежденных структур начинается этап компенсации – восстановления внутренней структуры волокон, который, ради справедливости должен заметить, не всегда может завершиться суперкомпенсацией. При слишком обширных травмах или отсутствии условий для восстановления результат может быть прямо противоположным.
Против теории разрушения чаще всего приводят следующие аргументы: «Если причиной роста являются микротравмы, то почему же мышца не растет, если ее бить палками?»
Ответ на этот вопрос можно найти в работе Володиной А.В., целью ее докторской диссертации является изучение процессов, препятствующих реализации регенерационного потенциала, заложенного в мышечном волокне. Эксперименты показали, что, в условиях обширного повреждения волокон, сопровождающегося ишемией (нарушением кровоснабжения) поврежденных тканей, вызывающей дефицит в снабжении волокна кислородом и питательными веществами, часть клеток-сателлит гибнет и поглощается фагоцитами, а часть идет по пути превращения не в мышечные клетки, а в фибробласты (клетки, производящие коллаген). В итоге место повреждения затягивается соединительной тканью, а количество волокон в мышечной ткани снижается, по причине гибели части из них от повреждений.
Очевидно, что при микротравмах волокон – разрушении внутренней структуры волокна без нарушения его целостности, в отличие от травм целой мышцы, снабжение волокон кислородом, а так же его иннервация не нарушены, поэтому условия, приводящие к гибели целых волокон и клеток-сателлитов, отсутствуют.
И так, если объем микротравм, полученных в ходе тренировки, был не слишком велик для срыва восстановительных процессов, но достаточен для активации клеток-сателлитов, то в подвергшемся тренировочной нагрузке волокне увеличивается количество клеточных ядер. Восстановление энергетических ресурсов после тренировки приводит к суперкомпенсации энергетических веществ, а лизис разрушенных тренировкой белков увеличивает содержание свободных аминокислот непосредственно в волокне, что в совокупности создает благоприятные условия для интенсификации процессов синтеза белка. При условии достаточного по времени и полноценного отдыха, отсутствия новых стрессовых нагрузок, адекватного снабжения волокна энергией и пластическими ресурсами (аминокислотами) интенсивные процессы восстановления приведут к накоплению в волокне белковых структур сверх уровня, который был до тренировки, то есть будет наблюдаться гипертрофия мышц.
Надо отметить, что последовательность протекания фаз общей неспецифической адаптационной реакции (синдрома стресса) такова, что обеспечивает поддержку описанных выше регенерационных процессов на системном уровне. Первая катаболическая фаза стресс реакции, сопровождается выбросом кортикостероидов, что приводит к мобилизации энергетических ресурсов организма и обеспечивает индукцию ферментов лизосом и фагоцитов, расщепляющих белок (кортикостероиды являются теми гормонами, которые активируют на ДНК клеток гены протеолитических ферментов), что способствует скорейшему очищению волокон от поврежденных структур. В последующей фазе стресс реакции синтез кортикостероидов сменяется синтезом анаболических гормонов, что обеспечивает на системном уровне компенсаторный анаболизм.
Как тут не вспомнить об основном законе философии – единстве и борьбе противоположностей. Анаболизм активируется катаболизмом – рост мышц есть следствие их предварительного разрушения.
Что такое микротравма
Открытым остается вопрос, что вызывает разрушение внутренней структуры волокна и является тем самым стрессом для мышцы? Прежде чем ответить на этот вопрос, рекомендую читателям вспомнить механизм сокращения мышц, описанный в I части.Ученый и пауэрлифтер Фредерик Хетфилд, считающий роль микротравм в тренировочном процессе скорее отрицательной из-за необходимости длительного восстановления, полагает, что причиной микротравм является повреждение миофибрильных нитей во время негативных повторений. Вот как он описывает механизм этих повреждений: «Так как количество перекрестных мостиков, старающихся сократить мышцу недостаточно, они буквально „продираются“ сквозь мостики соединений нити, стараясь вызвать концентрическое сокращение. Однако сцепиться как следует им не удается, они срываются и повреждаются. Эти действия, очень напоминающие протаскивание щетины одной зубной щетки через другую, сопровождаются сильным трением, и мышечные нити разрушаются»
Не правда ли образно? Но, на мой взгляд, несколько сумбурно – так пишут когда хотят объяснить то, что до конца не понимают сами. К сожалению, мэтр ошибся дважды.
Во-первых, микротравмы возникают не только при негативных повторениях, но и при позитивном движении.
Во-вторых, использовать термин «трение» для описания взаимодействия молекул некорректно. Сила трения введена в физике для описания на макроуровне поверхностного взаимодействия тел специально, дабы абстрагироваться от истинной природы «трения» – электромагнитного взаимодействия молекул поверхностного слоя.
Механизм повреждения миофибрильных нитей носит несколько иной характер, чем описывает Хетфилд, и мне удалось его аналитически смоделировать.
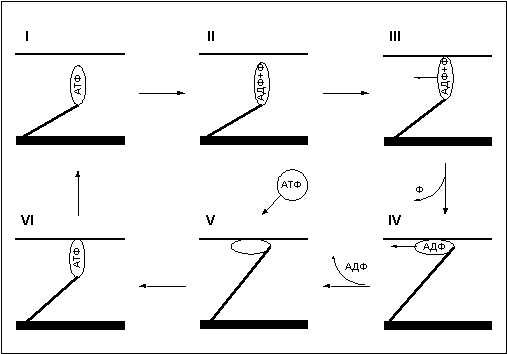
Для понимания механизма повреждения миофибрильных нитей следует обратиться к рассмотрению фаз движения миозинового мостика, которые вкратце уже описаны в первой части статьи. Сейчас остановимся подробнее на этом вопросе (рис. 8).

Рис. 8.
Итак, в первой фазе, еще до сцепления с актином, головка миозинового мостика несет в себе АТФ. Далее во второй фазе под действием фермента АТФаза АТФ гидролизуется, расщепляясь на АДФ и неорганический фосфат. Происходит это на не связанном с актином миозине, после этого миозиновая головка может соединяться с актином – третья фаза. Для совершения рабочего хода мостика используется энергия, освобождающаяся при диссоциации продуктов гидролиза АТФ. Основная доля энергии выделяется при высвобождении неорганического фосфата (переход из третей фазы в четвертую) и меньшая часть при высвобождении АДФ (переход из четвертой фазы в пятую). В пятой фазе – ригорное состояние мостика, мостик уже не генерирует силу, но по-прежнему находится в сцепленном состоянии, вывести его из этого состояния может только молекула АТФ. Поглощая АТФ, головка миозина переходит в шестую фазу, после чего отцепляется от актина, возвращаясь в исходное состояние (первая фаза).Анализируя фазы движения миозинового мостика, я сразу обратил внимание на тот факт, что для отцепления мостика от актина требуется молекула АТФ. При скольжении нитей миозина вдоль актина под действием сил тянущих мостиков (позитивное движение) или под действием внешней силы (негативное движение) сцепленные мостики растягиваются и мешают движению, этим, как вы помните, объясняется различие в силе развиваемой волокном при удлинении и сокращении и сокращении с разной скоростью. Когда АТФ в мышце находится в достаточном количестве, мостики успевают вовремя отцепиться, но что будет, если, при снижении концентрации АТФ в мышце, молекула АТФ не успеет отцепить головку миозина до того, как растяжение мостика превысит предел его прочности? Естественно сцепленный мостик разорвется! (Рис. 9).
Вы, наверное, слышали о состоянии трупного окоченения мышц? Наступает оно потому, что в мертвом организме запасы АТФ не восполняются, и мостики миозина оказываются накрепко сцепленными с актином. Представьте, что произойдет с мышцей трупа, если ее насильно растянуть. Так вот нечто подобное происходит и с отдельными волокнами живой мышцы, в которых по причине интенсивной деятельности резко снижается уровень АТФ.
Надо понимать, что изображенное мной место разрыва мостика достаточно условно, я не могу точно сказать, где находится самое слабое звено в цепи, но то, что при движении, сопровождающемся недостатком АТФ, должно происходить нефизиологическое разрушение акто-миозинового комплекса – неоспоримо.

Рис. 9.
«Эврика!» – воскликнул я. Вот оно объяснение системы Ментцера! Работа до «отказа» вызывает истощение запасов АТФ и, соответственно, разрывы в акто-миозиновом комплексе, что является стрессом для мышцы и вызывает адаптационную реакцию. Сразу спешу предупредить читателей, радость моя была преждевременной. Как оказалось «отказ» наступает вовсе не из-за исчерпания запасов АТФ, и уровень АТФ остается достаточно высоким даже в уставшей мышце. Решение задачи оказалось не таким простым, зато еще более красивым.Сомневаться в правильности «отказной» теории, меня заставил и тот факт, что проявление боли в мышцах – вестника микротравм не имеет прямой связи с работой до «отказа». С одной стороны, на начальном этапе тренинга боль в мышцах возникает при любой работе, не зависимо от того был «отказ» или нет. С другой стороны регулярные тренировки приводят к тому, что даже работа сверх «отказа» (читинг, стриптиз и др.) не вызывает боли в мышцах – боль возвращается только после продолжительного перерыва в тренировках.
Эти противоречия заставили меня заняться детальным изучением процесса «отказа».
Что такое «отказ» мышцы?
«Отказ» понятие довольно условное, это не особое состояние мышцы, а ни что иное, как неспособность развить силу, необходимую для преодоления внешней нагрузки. Причиной отказа является снижение силы, генерируемой целой мышцей и отдельными волокнами. Сила отдельного волокна зависит от количества одновременно тянущих миозиновых мостиков. Биохимических причин снижения силы, развиваемой мостиком в генерирующих силу фазах (III, IV) не существует, во всяком случае, пока об этом ничего не известно, поэтому сила волокна может снизиться только по следующим причинам:– Увеличение времени нахождения мостиков в ригорном – сцепленном не генерирующем силу состоянии (фаза V, VI);
– Увеличение времени нахождения мостиков в разомкнутом состоянии (фаза I, II).
Вспоминая аналогию с гребцами, скажем, что скорость движения лодки и развиваемая при этом сила тем выше, чем быстрее весла вытаскиваются из воды после гребка и чем меньше гребцы сидят с поднятыми веслами без дела.
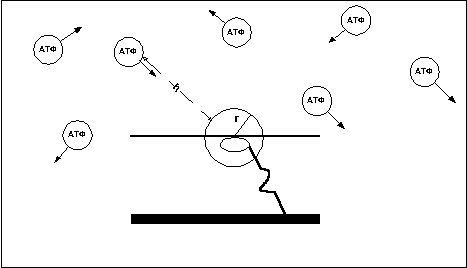
Время нахождения мостика в ригорном состоянии зависит от того, как быстро АТФ вступит в контакт с головкой миозина. Как известно частицы вещества постоянно находятся в хаотическом движении (рис. 10). Предположим что r – некий радиус, ограничивающий область пространства вокруг головки миозина, при попадании в пределы которого молекулы АТФ становится возможным реакция, приводящая к отцеплению головки от актина.

Рис. 10
В этом случае время нахождения мостика в ригорном состоянии равно частному от деления расстояния (h) от мостика до ближайшей молекулы АТФ, движущейся в направлении мостика, на скорость движения молекулы (v). Среднее же время нахождения мостиков в ригорном состоянии равно средневзвешенному расстоянию между молекулами АТФ деленному на средневзвешенную скорость движения молекул.Т=h/v
Естественно чем выше концентрация АТФ в мышце, тем меньше среднее расстояние между молекулами АТФ и головками миозина и тем меньше время нахождения мостиков в ригорном состоянии.
То есть сила волокна зависит от концентрации АТФ. При прочих равных условиях волокно с высокой концентрацией АТФ сильнее такого же волокна, но с меньшей концентрацией АТФ. Известно, что воспроизводство АТФ за счет креатинфосфата происходит почти мгновенно, поэтому можно сказать, что концентрация АТФ при работе мышцы зависит и от концентрации креатинфосфата. Таким образом:
Чем выше концентрация энергетических фосфатов (АТФ и креатинфосфата) в мышечном волокне, тем выше сила, развиваемая волокном.
После зависимости силы волокна от количества и поперечного сечения миофибрилл, влияние концентрации энергетических фосфатов на силу волокна является наиболее значимым. Именно по этой причине многие атлеты отмечают некоторую прибавку в силе, повышая уровень креатинфосфата в мышцах, принимая креатин, в качестве пищевой добавки.
Надо заметить, что зависимость силы волокна от концентрации энергетических фосфатов не является линейной. При высоких концентрациях, когда время ожидания контакта АТФ с головкой миозина станет меньше или сопоставимым со временем, необходимым для протекания химической реакции, приводящей к отделению головки миозина от актина, повышение концентрации АТФ и креатинфосфата будет мало влиять на скорость переключения мостиков и соответственно силу волокна. Зато низкие концентрации АТФ и креатинфосфата существенно снизят силу волокна, что может служить одной из причин отказа.
Рассмотрим второй фактор снижения силы сокращения – увеличение времени нахождения мостиков в разомкнутом состоянии (I, II фазы), что может происходить в результате снижения скорости гидролиза АТФ (снижения активности АТФазы – фермента ускоряющего реакцию гидролиза АТФ).
Расщепление АТФ и его воспроизводство за счет креатинфосфата вызывает накопление в мышце ортофосфорной кислоты, а гликолиз ведет к накоплению молочной кислоты. Активность АТФазы – фермента, благодаря которому происходит гидролиз АТФ, сильно зависит от кислотности среды. Как показывают эксперименты, максимум АТФазной активности достигается при среде близкой к нейтральной (рН=7), а при смещении среды мышцы в кислую сторону активность АТФазы падает, и при снижении рН среды до 5 АТФазная активность стремится к нулю (Богач П.Г. с соавторами, Поглазов Б.Ф). Таким образом, при накоплении кислых продуктов метаболизма АТФаза миозина постепенно снижает скорость гидролиза АТФ, и мостики теряют способность сцепляться с актином, при этом мышца снижает силу сокращения, несмотря на поступающий от мотонейрона сигнал.
Существует и еще как минимум две причины снижения силы мышц – при длительной работе накопление продуктов метаболизма тормозит процессы передачи сигнала от мотонейрона к волокну (Романовский Д.Ю.), а в центральной нервной системе развивается охранительное торможение.
То есть «отказ» мышцы является суперпозицией различных причин и доминирование одного либо другого фактора определяется интенсивностью работы мышцы.
Еще раз об энергетике
Резкая активизация мышечной деятельности из состояния покоя требует такого же резкого увеличения скорости производства энергии.Для достижения максимальной мощности основных источников воспроизводства энергии (гликолиза в быстрых волокнах и окисления в медленных) требуется время.
Скорость воспроизводства АТФ за счет гликолиза достигает своего максимума только через 20 —30 секунд после начала интенсивной работы.
Для достижения максимальной скорости окислительного процесса требуется гораздо больше времени, связано это в основном с необходимостью оптимизацией процессов доставки кислорода. Скорость окисления становится максимальной лишь через 1-2 минуты работы мышц, этот эффект наверняка известен вам под названием «второе дыхание».
Между тем мышца развивает максимальную мощность с первых же долей секунд после поступления команды к сокращению, гликолиз, в совокупности с окислением, не в состоянии обеспечить необходимую скорость воспроизводства АТФ для поддержания этой мощности. Приведение в соответствие скоростей расхода и воспроизводства АТФ во время работы мышцы идет по двум направлениям. Во-первых, постепенная активизация гликолиза и окисления увеличивает количество АТФ, синтезируемого в единицу времени за счет этих источников. Во-вторых, накопление продуктов метаболизма, в результате деятельности гликолиза и окисления, снижает активность АТФазы миозина и соответственно скорость расхода АТФ. Благодаря этим двум процессам скорости расхода и воспроизводства АТФ выравниваются, и в дальнейшем движение продолжается с постепенно снижающейся мощностью, но в состоянии равновесия между количеством синтезируемого АТФ и потребностями мышцы в энергии. Отказ же мышцы наступает не из-за окончания запасов АТФ, а из-за снижения сократительной способности мышц в результате накопления кислых продуктов метаболизма.
