Внутрисекреторная функция поджелудочной железы выполняется благодаря синтезу гормонов, отвечающих за регуляцию углеводного и жирового обмена.
ПЕЧЕНЬ
ОСОБЕННОСТИ ЖЕЛЧНОГО ПУЗЫРЯ
ОСОБЕННОСТИ ТОНКОЙ КИШКИ
ОСОБЕННОСТИ ТОЛСТОГО КИШЕЧНИКА
ОСОБЕННОСТИ МИКРОФЛОРЫ КИШЕЧНИКА
ОСОБЕННОСТИ ПИЩЕВАРЕНИЯ У ДЕТЕЙ РАННЕГО ВОЗРАСТА
ГЛАВА 7. АНАТОМО-ФИЗИОЛОГИЧЕСКИЕ ОСОБЕННОСТИ МОЧЕВЫДЕЛИТЕЛЬНОЙ СИСТЕМЫ
ОСОБЕННОСТЬ МОЧЕИСПУСКАНИЯ У ДЕТЕЙ
ОСОБЕННОСТИ СБОРА МОЧИ У ДЕТЕЙ
ИНСТРУМЕНТАЛЬНЫЕ ОБСЛЕДОВАНИЯ ПРИ ЗАБОЛЕВАНИЯХ ПОЧЕК
ЧАСТЬ II
ГЛАВА 1. ПОВРЕЖДЕНИЯ ПРИ РОДАХ
ТРАВМЫ МЯГКИХ ТКАНЕЙ
ПАРАЛИЧ ЛИЦЕВОГО НЕРВА
РОДОВАЯ ТРАВМА СПИННОГО МОЗГА И ПЛЕЧЕВОГО СПЛЕТЕНИЯ
ПЕЧЕНЬ
Печень новорожденного – самый большой орган, занимающий 1/3 объема брюшной полости. В 11 месяцев происходит удвоение ее массы, к 2–3 годам она утраивается, к 8 годам увеличивается в 5 раз, к 16–17 годам масса печени – в 10 раз.
Печень выполняет следующие функции:
1) вырабатывает желчь, участвующую в кишечном пищеварении;
2) стимулирует моторику кишечника, за счет действия желчи;
3) депонирует питательные вещества;
4) осуществляет барьерную функцию;
5) участвует в обмене веществ, в том числе – в преобразовании витаминов А, D, С, В12, К;
6) во внутриутробном периоде является кроветворным органом.
После рождения происходит дальнейшее формирование долек печени. Функциональные возможности печени у детей раннего возраста низкие: у новорожденных детей метаболизм непрямого билирубина осуществляется не полностью.
Печень выполняет следующие функции:
1) вырабатывает желчь, участвующую в кишечном пищеварении;
2) стимулирует моторику кишечника, за счет действия желчи;
3) депонирует питательные вещества;
4) осуществляет барьерную функцию;
5) участвует в обмене веществ, в том числе – в преобразовании витаминов А, D, С, В12, К;
6) во внутриутробном периоде является кроветворным органом.
После рождения происходит дальнейшее формирование долек печени. Функциональные возможности печени у детей раннего возраста низкие: у новорожденных детей метаболизм непрямого билирубина осуществляется не полностью.
ОСОБЕННОСТИ ЖЕЛЧНОГО ПУЗЫРЯ
Желчный пузырь располагается под правой долей печени и имеет веретенообразную форму, его длина достигает 3 см. Типичную грушевидную форму он приобретает к 7 месяцам, к 2 годам достигает края печени.
Основная функция желчного пузыря – скопление и выделение печеночной желчи. Желчь ребенка по своему составу отличается от желчи взрослого человека. В ней мало желчных кислот, холестерина, солей, много воды, муцина, пигментов. В периоде новорожденности желчь богата мочевиной. В желчи ребенка гликохолевая кислота преобладает и усиливает бактерицидный эффект желчи, а также ускоряет отделение панкреатического сока. Желчь эмульгирует жиры, растворяет жирные кислоты, улучшает перистальтику.
С возрастом размеры желчного пузыря увеличиваются, начинает выделяться желчь иного состава, чем у детей младшего возраста. Длина общего желчного протока с возрастом увеличивается.
Размеры желчного пузыря у детей (Чапова О. И., 2005 г.):
1) новорожденный – 3,5 × 1,0 × 0,68 см;
2) 1 год – 5,0 × 1,6 × 1,0 см;
3) 5 лет – 7,0 × 1,8 × 1,2 см;
4) 12 лет – 7,7 × 3,7 × 1,5 см.
Основная функция желчного пузыря – скопление и выделение печеночной желчи. Желчь ребенка по своему составу отличается от желчи взрослого человека. В ней мало желчных кислот, холестерина, солей, много воды, муцина, пигментов. В периоде новорожденности желчь богата мочевиной. В желчи ребенка гликохолевая кислота преобладает и усиливает бактерицидный эффект желчи, а также ускоряет отделение панкреатического сока. Желчь эмульгирует жиры, растворяет жирные кислоты, улучшает перистальтику.
С возрастом размеры желчного пузыря увеличиваются, начинает выделяться желчь иного состава, чем у детей младшего возраста. Длина общего желчного протока с возрастом увеличивается.
Размеры желчного пузыря у детей (Чапова О. И., 2005 г.):
1) новорожденный – 3,5 × 1,0 × 0,68 см;
2) 1 год – 5,0 × 1,6 × 1,0 см;
3) 5 лет – 7,0 × 1,8 × 1,2 см;
4) 12 лет – 7,7 × 3,7 × 1,5 см.
ОСОБЕННОСТИ ТОНКОЙ КИШКИ
Кишечник у детей относительно длиннее, чем у взрослых.
Соотношение длины тонкой кишки и длины тела у новорожденного составляет 8,3: 1, на первом году жизни – 7,6: 1, в 16 лет – 6,6: 1.
Длина тонкой кишки у ребенка первого года жизни равна 1,2–2,8 м. Площадь внутренней поверхности тонкой кишки на первой неделе жизни составляет 85 см2, у взрослого – 3,3 × 103 см2. Площадь тонкого кишечника увеличивается за счет развития эпителия и микроворсин.
Тонкая кишка анатомически делится на 3 отдела. Первый отдел – это двенадцатиперстная кишка, длина которой у новорожденного составляет 10 см, у взрослого доходит до 30 см. Она имеет три сфинктера, главная функция которых заключается в создании области пониженного давления, где происходит контакт пищи с ферментами поджелудочной железы.
Второй и третий отделы представлены тонкой и подвздошной кишками. Длина тонкой кишки составляет 2/5 длины до илеоцекального угла, остальные 3/5 составляет подвздошная кишка.
Переваривание пищи, всасывание ее ингредиентов происходит в тонком кишечнике. Слизистая оболочка кишки богата кровеносными сосудами, эпителий тонкого кишечника быстро обновляется. Кишечные железы у детей более крупные, лимфоидная ткань разбросана по всему кишечнику. По мере роста ребенка образуются пейеровы бляшки.
Соотношение длины тонкой кишки и длины тела у новорожденного составляет 8,3: 1, на первом году жизни – 7,6: 1, в 16 лет – 6,6: 1.
Длина тонкой кишки у ребенка первого года жизни равна 1,2–2,8 м. Площадь внутренней поверхности тонкой кишки на первой неделе жизни составляет 85 см2, у взрослого – 3,3 × 103 см2. Площадь тонкого кишечника увеличивается за счет развития эпителия и микроворсин.
Тонкая кишка анатомически делится на 3 отдела. Первый отдел – это двенадцатиперстная кишка, длина которой у новорожденного составляет 10 см, у взрослого доходит до 30 см. Она имеет три сфинктера, главная функция которых заключается в создании области пониженного давления, где происходит контакт пищи с ферментами поджелудочной железы.
Второй и третий отделы представлены тонкой и подвздошной кишками. Длина тонкой кишки составляет 2/5 длины до илеоцекального угла, остальные 3/5 составляет подвздошная кишка.
Переваривание пищи, всасывание ее ингредиентов происходит в тонком кишечнике. Слизистая оболочка кишки богата кровеносными сосудами, эпителий тонкого кишечника быстро обновляется. Кишечные железы у детей более крупные, лимфоидная ткань разбросана по всему кишечнику. По мере роста ребенка образуются пейеровы бляшки.
ОСОБЕННОСТИ ТОЛСТОГО КИШЕЧНИКА
Толстый кишечник состоит из различных отделов и развивается после рождения. У детей до 4 лет восходящая кишка по длине больше нисходящей. Сигмовидная кишка относительно большей длины. Постепенно эти особенности исчезают. Слепая кишка и аппендикс подвижны, аппендикс часто располагается атипично.
Прямая кишка у детей первых месяцев жизни относительно длинная. У новорожденных ампула прямой кишки неразвита, плохо развита окружающая жировая клетчатка. К 2 годам прямая кишка принимает свое окончательное положение, что способствует выпадению прямой кишки в раннем детском возрасте при натуживании, при упорных запорах и тенезмах у ослабленных детей.
Сальник у детей до 5 лет – короткий.
Сокоотделение у детей в толстом кишечнике небольшое, но при механическом раздражении резко возрастает.
В толстом кишечнике происходит всасывание воды и формирование каловых масс.
Прямая кишка у детей первых месяцев жизни относительно длинная. У новорожденных ампула прямой кишки неразвита, плохо развита окружающая жировая клетчатка. К 2 годам прямая кишка принимает свое окончательное положение, что способствует выпадению прямой кишки в раннем детском возрасте при натуживании, при упорных запорах и тенезмах у ослабленных детей.
Сальник у детей до 5 лет – короткий.
Сокоотделение у детей в толстом кишечнике небольшое, но при механическом раздражении резко возрастает.
В толстом кишечнике происходит всасывание воды и формирование каловых масс.
ОСОБЕННОСТИ МИКРОФЛОРЫ КИШЕЧНИКА
Желудочно-кишечный тракт у плода стерилен. При контакте ребенка с окружающей средой происходит заселение его микрофлорой. В желудке и двенадцатиперстной кишке микрофлора скудная. В тонком и толстом кишечнике количество микробов увеличивается и зависит от вида вскармливания. Основной микрофлорой является B. bifidum, рост которой стимулируется β-лактозой грудного молока. При искусственном вскармливании в кишечнике доминирует условно-патогенная грамотрицательная кишечная палочка. Нормальная кишечная флора выполняет две основные функции:
1) создание иммунологического барьера;
2) синтез витаминов и ферментов.
1) создание иммунологического барьера;
2) синтез витаминов и ферментов.
ОСОБЕННОСТИ ПИЩЕВАРЕНИЯ У ДЕТЕЙ РАННЕГО ВОЗРАСТА
Для детей первых месяцев жизни имеют определяющее значение питательные вещества, которые поступают с молоком матери и перевариваются за счет веществ, содержащихся в самом женском молоке. С введением прикорма стимулируются механизмы ферментных систем ребенка. Всасывание пищевых ингредиентов у детей раннего возраста имеет свои особенности. Казеин сначала створаживается в желудке под влиянием сычужного фермента. В тонкой кишке он начинает расщепляться до аминокислот, которые активизируются и всасываются.
Переваривание жира зависит от вида вскармливания. Жиры коровьего молока содержат длинноцепочечные жиры, которые расщепляются за счет панкреатической липазы в присутствии жирных кислот.
Всасывание жира происходит в конечных и средних отделах тонкой кишки. Расщепление молочного сахара у детей происходит в кайме кишечного эпителия. В женском молоке содержится β-лактоза, в коровьем – α-лактоза. В связи с этим при искусственном вскармливании углеводный состав пищи изменен. Витамины также всасываются в тонкой кишке.
Переваривание жира зависит от вида вскармливания. Жиры коровьего молока содержат длинноцепочечные жиры, которые расщепляются за счет панкреатической липазы в присутствии жирных кислот.
Всасывание жира происходит в конечных и средних отделах тонкой кишки. Расщепление молочного сахара у детей происходит в кайме кишечного эпителия. В женском молоке содержится β-лактоза, в коровьем – α-лактоза. В связи с этим при искусственном вскармливании углеводный состав пищи изменен. Витамины также всасываются в тонкой кишке.
ГЛАВА 7. АНАТОМО-ФИЗИОЛОГИЧЕСКИЕ ОСОБЕННОСТИ МОЧЕВЫДЕЛИТЕЛЬНОЙ СИСТЕМЫ
К моменту рождения созревание почек еще не закончено. Клубочки у новорожденных значительно меньше, чем у взрослых, их фильтрующая поверхность составляет 30 % нормы взрослого. Канальцы короче и уже. По сравнению со взрослыми реабсорбция мочи у детей снижена.
С возрастом органы мочевыделения меняются. У детей младшего возраста размеры почек относительно больше, отношение их массы к массе тела новорожденного составляет 1: 100, у взрослого человека – 1: 200.
Верхний полюс почки находится на уровне XI–XII грудного позвонка, нижний – на уровне IV поясничного позвонка. К 2 годам эти особенности расположения почек исчезают. В последующие годы рост почек соответствует росту тела.
Почки в первые годы жизни имеют дольчатое строение. Корковый слой развит недостаточно. Клубочки у новорожденного располагаются компактно. Количество клубочкового фильтрата у детей в первые месяцы жизни понижено по причине того, что фильтрующая поверхность у них значительно меньше, чем у взрослых (см. табл. 15).
 При росте почки наблюдается равномерное развитие нефронов.
При росте почки наблюдается равномерное развитие нефронов.
Количество мочи, образующееся у ребенка, в норме можно приблизительно рассчитать по формуле:
V = 100 × (n + 5), где V – объем мочи за сутки;
n – число лет.
Или по формуле:
V = 600 + 100 (n – 1),
где V – объем мочи за сутки;
n – число лет.
Для выведения шлаков детям требуется больше воды, чем взрослым. Обезвоживание у детей наступает значительно быстрее. Дети, получающие грудное молоко, полностью усваивают его, и продуктов, удаляемых через почки, очень мало. В связи с этим при низких функциональных возможностях, несовершенстве систем, регулирующих водно-солевой обмен, ребенок поддерживает постоянство внутренней среды. При замене грудного молока другими продуктами нагрузка на почки возрастает, увеличивается количество продуктов, подлежащих удалению, почки работают с большим напряжением, изменяется кислотность мочи.
Почки участвуют в поддержании осмотической регуляции обмена крови и внеклеточной жидкости, поддержании кислотнощелочного равновесия.
Моча образуется в результате активной функции нефрона, с помощью которой происходит ультрафильтрация плазмы в капиллярах клубочков, в канальцах происходят обратное всасывание воды, глюкозы, синтез и секреция необходимых для организма соединений. Через фильтрующую мембрану клубочков из плазмы крови проходят низкомолекулярные водорастворимые соединения. Почечный фильтр не пропускает клеточные элементы и белки.
Регуляция мочеобразования происходит через гипофиз, надпочечники, гуморальным и нервным путями. Выведение воды регулируется антидиуретическим гормоном. Альдостерон – гормон коры надпочечников – повышает обратное всасывание натрия и выведение калия. В первые 3 месяца выделяется 90 мл мочи на 1 кг веса, в возрасте 10 лет – 25–35 мл на 1 кг веса в сутки.
Мочеточники. Мочеточники у детей раннего возраста относительно шире, более извилисты, чем у взрослых. Стенки мочеточников снабжены плохо сформированными мышечными и эластичными волокнами.
Мочевой пузырь. У новорожденных мочевой пузырь – овальной формы и находится выше, чем у взрослых. Его слизистая оболочка полностью сформирована. С возрастом ребенка утолщаются его мышечный слой и эластические волокна. Емкость мочевого пузыря у новорожденного составляет 50 мл, в 1 год – 200 мл.
Мочеиспускательный канал. У мальчиков его длина составляет 5–6 см, у взрослых мужчин – 14–18 см.
С возрастом органы мочевыделения меняются. У детей младшего возраста размеры почек относительно больше, отношение их массы к массе тела новорожденного составляет 1: 100, у взрослого человека – 1: 200.
Верхний полюс почки находится на уровне XI–XII грудного позвонка, нижний – на уровне IV поясничного позвонка. К 2 годам эти особенности расположения почек исчезают. В последующие годы рост почек соответствует росту тела.
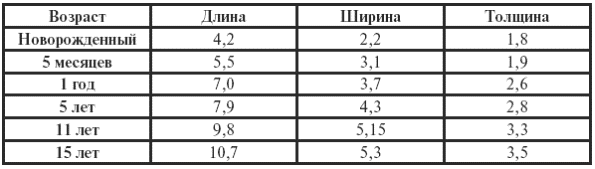
Почки в первые годы жизни имеют дольчатое строение. Корковый слой развит недостаточно. Клубочки у новорожденного располагаются компактно. Количество клубочкового фильтрата у детей в первые месяцы жизни понижено по причине того, что фильтрующая поверхность у них значительно меньше, чем у взрослых (см. табл. 15).
Таблица 15
Размеры почек у детей (см) (Фимин В. А., 2003 г.)

Количество мочи, образующееся у ребенка, в норме можно приблизительно рассчитать по формуле:
V = 100 × (n + 5), где V – объем мочи за сутки;
n – число лет.
Или по формуле:
V = 600 + 100 (n – 1),
где V – объем мочи за сутки;
n – число лет.
Для выведения шлаков детям требуется больше воды, чем взрослым. Обезвоживание у детей наступает значительно быстрее. Дети, получающие грудное молоко, полностью усваивают его, и продуктов, удаляемых через почки, очень мало. В связи с этим при низких функциональных возможностях, несовершенстве систем, регулирующих водно-солевой обмен, ребенок поддерживает постоянство внутренней среды. При замене грудного молока другими продуктами нагрузка на почки возрастает, увеличивается количество продуктов, подлежащих удалению, почки работают с большим напряжением, изменяется кислотность мочи.
Почки участвуют в поддержании осмотической регуляции обмена крови и внеклеточной жидкости, поддержании кислотнощелочного равновесия.
Моча образуется в результате активной функции нефрона, с помощью которой происходит ультрафильтрация плазмы в капиллярах клубочков, в канальцах происходят обратное всасывание воды, глюкозы, синтез и секреция необходимых для организма соединений. Через фильтрующую мембрану клубочков из плазмы крови проходят низкомолекулярные водорастворимые соединения. Почечный фильтр не пропускает клеточные элементы и белки.
Регуляция мочеобразования происходит через гипофиз, надпочечники, гуморальным и нервным путями. Выведение воды регулируется антидиуретическим гормоном. Альдостерон – гормон коры надпочечников – повышает обратное всасывание натрия и выведение калия. В первые 3 месяца выделяется 90 мл мочи на 1 кг веса, в возрасте 10 лет – 25–35 мл на 1 кг веса в сутки.
Мочеточники. Мочеточники у детей раннего возраста относительно шире, более извилисты, чем у взрослых. Стенки мочеточников снабжены плохо сформированными мышечными и эластичными волокнами.
Мочевой пузырь. У новорожденных мочевой пузырь – овальной формы и находится выше, чем у взрослых. Его слизистая оболочка полностью сформирована. С возрастом ребенка утолщаются его мышечный слой и эластические волокна. Емкость мочевого пузыря у новорожденного составляет 50 мл, в 1 год – 200 мл.
Мочеиспускательный канал. У мальчиков его длина составляет 5–6 см, у взрослых мужчин – 14–18 см.
ОСОБЕННОСТЬ МОЧЕИСПУСКАНИЯ У ДЕТЕЙ
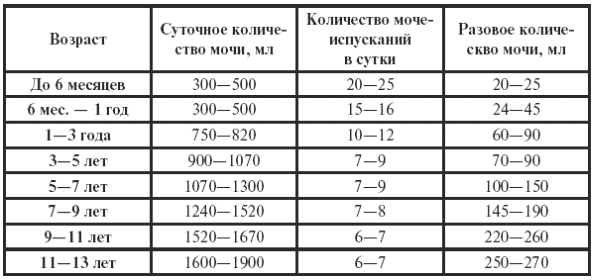
Мочеиспускание новорожденного производится благодаря врожденным спинальным рефлексам. При достижении возраста 12 месяцев полностью закрепляется условный рефлекс на мочеиспускание (см. табл. 16).
 Самым информативным показателем мочевой системы является анализ мочи. Цвет мочи в норме желтый, окраска мочи зависит от концентрации мочевых элементов. Она может меняться при приеме метиленового синего, рибофлавина и от пищевых пигментов.
Самым информативным показателем мочевой системы является анализ мочи. Цвет мочи в норме желтый, окраска мочи зависит от концентрации мочевых элементов. Она может меняться при приеме метиленового синего, рибофлавина и от пищевых пигментов.
Свежевыпущенная моча прозрачна. Мутность при стоянии мочи зависит от присутствия большого количества солей, кислотных элементов, бактерий, слизи и жира.
Моча имеет слабокислую реакцию, при искусстевенном вскармливании – слабощелочную.
Плотность мочи колеблется в пределах 1002–1030. Она зависит от количества выпитой жидкости, пищевого рациона, потоотделения. Моча у детей раннего возраста менее концентрирована (см. табл. 17).
 На величину плотности мочи влияет присутствие в ней белка, глюкозы и других веществ. Снижение относительной плотности мочи наблюдается при хронической почечной недостаточности, гипофизарной недостаточности и других заболеваниях. Увеличение плотности мочи возникает при больших потерях жидкости.
На величину плотности мочи влияет присутствие в ней белка, глюкозы и других веществ. Снижение относительной плотности мочи наблюдается при хронической почечной недостаточности, гипофизарной недостаточности и других заболеваниях. Увеличение плотности мочи возникает при больших потерях жидкости.
В осадке мочи обычно обнаруживаются 1–2 клетки плоского эпителия. При воспалительных процессах происходит увеличение этого показателя.
Клетки цилиндрического эпителия обнаруживаются в осадке мочи в единичных числах.
Эритроциты могут быть единичными: 0–1 в поле зрения, до 2-х у девочек.
Лейкоциты также обнаруживаются в нормальной моче 5–6 в поле зрения.
Единичные гиалиновые и восковидные цилиндры могут обнаруживаться у здоровых людей при физической нагрузке.
Белок в моче обнаруживается при физическом напряжении, воспалительных и хронических заболеваниях почек, когда повышается проницаемость мембранного фильтра.
Глюкоза в моче может проявляться при нарушениях углеводного обмена.
Кетонурия обнаруживается при частой рвоте, расстройствах обмена веществ.
Увеличение количества мочи (полиурия) характерно для больных сахарным диабетом, хроническим нефритом, при отхождении отеков, после лихорадочных заболеваний.
Олигурия (уменьшение количества мочи на 20–30 %) или отсутствие мочи зависят от уменьшения или полного прекращения выделения мочи почками, а также – от рефлекторного спазма и препятствия оттоку в нижних отделах почек. Причинами олигурии могут быть заболевания сердца и почек, потери жидкости при рвоте, поносе, недостаточном приеме жидкости.
Дизурия (нарушение мочеиспускания с задержкой мочи в мочевом пузыре) чаще всего связана с рефлекторным спазмом сфинктера мочевого пузыря при воспалительных заболеваниях мочевыводящих путей, поражении центральной нервной системы и других заболеваниях.
Поллакиурия (учащенное мочеиспускание) наблюдается при диабете, хронической почечной недостаточности, охлаждении.
Болезненное мочеиспускание может отмечаться при циститах и других заболеваниях мочевыводящих путей.
Наряду с общим анализом мочи производится количественное определение эритроцитов и лейкоцитов в моче. Для этого собирают суточную порцию мочи (проба Аддис-Каковского) либо 1 мл мочи (проба Нечипоренко).
Таблица 16
Количество мочи и частота мочеиспускания у детей (Папаян А. В., 1997 г.)

Свежевыпущенная моча прозрачна. Мутность при стоянии мочи зависит от присутствия большого количества солей, кислотных элементов, бактерий, слизи и жира.
Моча имеет слабокислую реакцию, при искусстевенном вскармливании – слабощелочную.
Плотность мочи колеблется в пределах 1002–1030. Она зависит от количества выпитой жидкости, пищевого рациона, потоотделения. Моча у детей раннего возраста менее концентрирована (см. табл. 17).
Таблица 17
Относительная плотность мочи (Папаян А. В., 1997 г.)

В осадке мочи обычно обнаруживаются 1–2 клетки плоского эпителия. При воспалительных процессах происходит увеличение этого показателя.
Клетки цилиндрического эпителия обнаруживаются в осадке мочи в единичных числах.
Эритроциты могут быть единичными: 0–1 в поле зрения, до 2-х у девочек.
Лейкоциты также обнаруживаются в нормальной моче 5–6 в поле зрения.
Единичные гиалиновые и восковидные цилиндры могут обнаруживаться у здоровых людей при физической нагрузке.
Белок в моче обнаруживается при физическом напряжении, воспалительных и хронических заболеваниях почек, когда повышается проницаемость мембранного фильтра.
Глюкоза в моче может проявляться при нарушениях углеводного обмена.
Кетонурия обнаруживается при частой рвоте, расстройствах обмена веществ.
Увеличение количества мочи (полиурия) характерно для больных сахарным диабетом, хроническим нефритом, при отхождении отеков, после лихорадочных заболеваний.
Олигурия (уменьшение количества мочи на 20–30 %) или отсутствие мочи зависят от уменьшения или полного прекращения выделения мочи почками, а также – от рефлекторного спазма и препятствия оттоку в нижних отделах почек. Причинами олигурии могут быть заболевания сердца и почек, потери жидкости при рвоте, поносе, недостаточном приеме жидкости.
Дизурия (нарушение мочеиспускания с задержкой мочи в мочевом пузыре) чаще всего связана с рефлекторным спазмом сфинктера мочевого пузыря при воспалительных заболеваниях мочевыводящих путей, поражении центральной нервной системы и других заболеваниях.
Поллакиурия (учащенное мочеиспускание) наблюдается при диабете, хронической почечной недостаточности, охлаждении.
Болезненное мочеиспускание может отмечаться при циститах и других заболеваниях мочевыводящих путей.
Наряду с общим анализом мочи производится количественное определение эритроцитов и лейкоцитов в моче. Для этого собирают суточную порцию мочи (проба Аддис-Каковского) либо 1 мл мочи (проба Нечипоренко).
ОСОБЕННОСТИ СБОРА МОЧИ У ДЕТЕЙ
Для обычного общего анализа собирают утреннюю порцию мочи в чистую бутылочку. Перед мочеиспусканием наружные половые органы обмывают теплой водой. Если имеются признаки воспаления половых органов, мочу получают с помощью катетера, обычно это делает врач.
Для сбора мочи у новорожденных используют специальные мочеприемники.
Катетеризация мочевого пузыря у детей раннего возраста проводится в исключительных случаях.
Проба по Зимницкому определяет количество выделяемой мочи и ее относительную плотность в течение суток. Мочу собирают через 3 ч. Особого режима питания, двигательной активности не требуется.
Суточный диурез должен составлять 2/3 принятой жидкости, из них дневной диурез – 2/3.
Для пробы заранее подготавливают емкости, на каждой из 8 емкостей ставятся норма и время. Ребенок в день исследования опорожняет мочевой пузырь в 6.00 ч утра, последующие порции собирают в пронумерованную посуду.
№ 1–9.00 ч.
№ 2-12.00 ч.
№ 3-15.00 ч.
№ 4-18.00 ч.
№ 5-21.00 ч.
№ 6-24.00 ч.
№ 7–3.00 ч.
№ 8–6.00 ч.
Ночью будят ребенка. Если в какое-то время ребенок не мочился, емкость отправляют в лабораторию пустой.
Проба Аддис-Каковского. Эта проба производится наряду с общим анализом для определения эритроцитов, лейкоцитов и цилиндров в суточной порции мочи (см. табл. 18).
 При биохимических методах исследования мочи определяются белок, желчные пигменты, желчные кислоты, уробилин, сахар, ацетон и т. д. Важное клиническое значение имеет определение солей.
При биохимических методах исследования мочи определяются белок, желчные пигменты, желчные кислоты, уробилин, сахар, ацетон и т. д. Важное клиническое значение имеет определение солей.
Бактериологическое исследование мочи. Перед исследованием проводится тщательный туалет наружных половых органов. Затем открывается стерильная пробирка или банка, и ребенок мочится, заполняя ее на 1/2 или 3/5 объема. Процедура проводится четко и быстро, чтобы флакон оставался открытым минимальное время и края его не соприкасались с нестерильными поверхностями, чтобы исключить попадание бактерий из окружающей среды. Собирается моча в середине или конце мочеиспускания.
Сбор мочи на сахар. Утром ребенку необходимо опорожнить мочевой пузырь от ночной мочи, после этого провести тщательный туалет наружных половых органов и собирать мочу в проградуированную трехлитровую банку. На ней отмечают показатели объема (100, 200, 300, 400 мл и т. д.).
После сбора отмечается суточный диурез, моча мешается стеклянной палочкой, отливают 200 мл мочи и отправляют ее на исследование.
Для сбора мочи у новорожденных используют специальные мочеприемники.
Катетеризация мочевого пузыря у детей раннего возраста проводится в исключительных случаях.
Проба по Зимницкому определяет количество выделяемой мочи и ее относительную плотность в течение суток. Мочу собирают через 3 ч. Особого режима питания, двигательной активности не требуется.
Суточный диурез должен составлять 2/3 принятой жидкости, из них дневной диурез – 2/3.
Для пробы заранее подготавливают емкости, на каждой из 8 емкостей ставятся норма и время. Ребенок в день исследования опорожняет мочевой пузырь в 6.00 ч утра, последующие порции собирают в пронумерованную посуду.
№ 1–9.00 ч.
№ 2-12.00 ч.
№ 3-15.00 ч.
№ 4-18.00 ч.
№ 5-21.00 ч.
№ 6-24.00 ч.
№ 7–3.00 ч.
№ 8–6.00 ч.
Ночью будят ребенка. Если в какое-то время ребенок не мочился, емкость отправляют в лабораторию пустой.
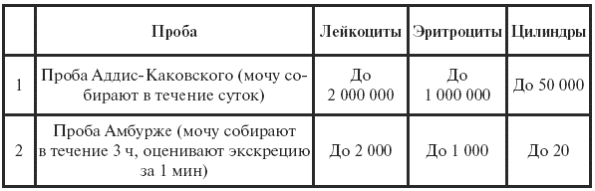
Проба Аддис-Каковского. Эта проба производится наряду с общим анализом для определения эритроцитов, лейкоцитов и цилиндров в суточной порции мочи (см. табл. 18).
Таблица 18
Оценка количественных мочевых проб (Эрман М. В., 1997 г.)

Окончание табл. 18

Бактериологическое исследование мочи. Перед исследованием проводится тщательный туалет наружных половых органов. Затем открывается стерильная пробирка или банка, и ребенок мочится, заполняя ее на 1/2 или 3/5 объема. Процедура проводится четко и быстро, чтобы флакон оставался открытым минимальное время и края его не соприкасались с нестерильными поверхностями, чтобы исключить попадание бактерий из окружающей среды. Собирается моча в середине или конце мочеиспускания.
Сбор мочи на сахар. Утром ребенку необходимо опорожнить мочевой пузырь от ночной мочи, после этого провести тщательный туалет наружных половых органов и собирать мочу в проградуированную трехлитровую банку. На ней отмечают показатели объема (100, 200, 300, 400 мл и т. д.).
После сбора отмечается суточный диурез, моча мешается стеклянной палочкой, отливают 200 мл мочи и отправляют ее на исследование.
ИНСТРУМЕНТАЛЬНЫЕ ОБСЛЕДОВАНИЯ ПРИ ЗАБОЛЕВАНИЯХ ПОЧЕК
УЗИ дает возможность оценить размеры почек и лоханок, их расположение, состояние ткани и почек.
Рентгенологические методы исследования:
1) экскреторная урография, диагностирующая пороки мочевого пузыря, уретры, почек;
2) ретроградная пиелография, исследующая состояние мочевого пузыря, мочеточников, почек.
Для исследования кровообращения почек проводится почечная ангиография.
Радиоизотопные методы исследования применяются для оценки функции, для определения динамики патологического процесса.
Биопсия почки заключается в прижизненном исследовании почечной ткани с изучением ее морфологической структуры.
Рентгенологические методы исследования:
1) экскреторная урография, диагностирующая пороки мочевого пузыря, уретры, почек;
2) ретроградная пиелография, исследующая состояние мочевого пузыря, мочеточников, почек.
Для исследования кровообращения почек проводится почечная ангиография.
Радиоизотопные методы исследования применяются для оценки функции, для определения динамики патологического процесса.
Биопсия почки заключается в прижизненном исследовании почечной ткани с изучением ее морфологической структуры.
ЧАСТЬ II
ЗАБОЛЕВАНИЯ НОВОРОЖДЕННЫХ И ДЕТЕЙ РАННЕГО ВОЗРАСТА
ГЛАВА 1. ПОВРЕЖДЕНИЯ ПРИ РОДАХ
Под травмами понимают неизбежные или предотвратимые механические повреждения плода. Они могут возникать как вследствие неправильного ведения родов, так и независимо от квалификации акушера и каких-либо неправильных действий родителей. Родовая травма – это гораздо более широкое понятие, чем акушерская травма. Травматичность акушерских пособий зависит не только от навыков акушера, но и от того, каким плод вступает в роды. Предрасполагающими факторами к развитию родовой травмы являются: макросомия, большие размеры головки плода, тазовое и другие аномальные предлежания, глубокая недоношенность, переношенность, затяжные или чрезмерно быстрые (стремительные) роды, аномалии развития плода, уменьшение размеров (последствия рахита, инфантилизма и др.) и повышенная ригидность родовых путей, акушерские пособия (наложение полостных или выходных акушерских щипцов, вакуумэкстрактора и др.). Родовые травмы чаще наблюдаются у первородящих матерей и могут возникнуть как при недоношенном, так и доношенном плоде. Различные заболевания матери могут играть существенную роль в происхождении родового травматизма. К ним относятся: токсикоз, сердечно-сосудистые болезни, перенесенные во время беременности инфекции, в особенности вирусные, различные нарушения обмена, эндокринные болезни, резус-несовместимость. Антенатальные факторы, независимо от состояния матери, могут также обусловить тяжелые роды и явления родовой травмы. Среди причин большое значение имеют врожденные дисплазии, выявляющиеся уже в эмбриональном периоде. Роды могут протекать с травмой при наличии врожденных дефектов и некоторых наследственных болезней. При оценке всех этих факторов нередко делаются ошибки, и многое из того, что обусловливает тяжелые роды, принимается как следствие тяжелых родов. Большое значение имеет патология родового акта: положение плода, продолжительность родового акта и «потужного периода», преждевременное отхождение вод. Значительное место в генезе родовых травм уделяется особенностям черепных костей плода и новорожденного. Под влиянием различных механических факторов, зависящих от расположения плода или родовых путей, и создающихся неблагоприятных условий может легко наступить надвигание черепных костей друг на друга, при этом происходит сдавление синусов и разрыв вен мозговых оболочек.
ТРАВМЫ МЯГКИХ ТКАНЕЙ
Петехии и экхимозы, ссадины на различных участках тела – самое частое проявление родовой травмы. Они могут возникать на месте предлежащей части плода в родах, наложения щипцов. Небольшие ссадины и порезы требуют только местных антисептических мероприятий – обработка спиртовыми растворами анилиновых красителей, повязка и др. Экхимозы рассасываются самостоятельно в течение нескольких дней – 1 недели жизни.
Повреждения и кровоизлияния в грудино-ключично-сосцевидную мышцу могут возникнуть при наложении щипцов, ручных пособиях, особенно в случае родов в ягодичном предлежании. В области повреждения и гематомы прощупывается небольшая, тестоватой консистенции опухоль. Иногда впервые ее диагностируют к середине-концу первой недели жизни, когда развивается кривошея – голова ребенка наклонена в сторону поврежденной мышцы, а подбородок повернут в противоположную сторону. Нередко кровоизлияние в мышцу сочетается со спинальной травмой. Гематому грудино-ключично-сосцевидной мышцы следует дифференцировать с врожденной мышечной кривошеей. Причиной последней может быть аномалия положения плода, небольшое количество околоплодных вод и давление на мышцу костной части таза матери, а иногда гематома является проявлением множественного поражения костно-мышечной системы (позвоночник, кости черепа и др.). Лечение состоит в обеспечении корригирующего положения головы (валики, которые способствуют устранению патологического наклона головы и поворота лица), использовании сухого тепла, физиотерапии (электрофорез с йодистым калием), позже – массажа. Если лечение оказалось неэффективным, то показано оперативное вмешательство, проводимое в первые 6 месяцев жизни.
Кровоизлияние под апоневроз характеризуется припухлостью тестоватой структуры, отеком теменной и затылочной областей головы. В отличие от кефалогематомы отечность распространяется за границы одной кости, а от родовой опухоли – может расти после рождения. Факторами риска являются вакуум-экстрактор и другие акушерские пособия в родах. Возможно инфицирование. При больших размерах кровоизлияния следует исключить наследственные геморрагические болезни. Необходимо выполнение рентгенограммы черепа для исключения переломов. Нередко сочетается с признаками внутричерепной родовой травмы. Кровоизлияние резорбируется через 2–3 недели.
Кефалогематома– это поднадкостничное кровоизлияние, ограниченное поверхностью одной кости черепа. Ей несвойственно побледнение кожи, типичное для подкожного кровоизлияния, и припухлость обычно появляется только через несколько часов после родов, так как кровотечение в поднадкостничной области происходит медленно. Опухоль вначале имеет упругую консистенцию, никогда не переходит на соседнюю кость, не пульсирует, безболезненная. В первые дни жизни кефалогематома может увеличиваться, на 2-3-й неделе жизни размеры ее уменьшаются, и полная резорбция наступает к 6-8-й неделе. В некоторых случаях возможно обызвествление, редко – нагноение. Причиной поднадкостничного кровоизлияния являются отслойка надкостницы при движениях головы в момент ее прорезывания, реже – трещины черепа. Поэтому всем детям с большими кефалогематомами (диаметром более 8 см) необходимо выполнение рентгенограммы черепа для исключения трещины. Дифференциальный диагноз проводят с родовой опухолью, кровоизлиянием под апоневроз, мозговыми грыжами.
Лечение. Первые 3–4 дня жизни кормить сцеженным материнским молоком из бутылочки, а далее при стабильном состоянии – приложить ребенка к груди. Небольшие кефалогематомы не требуют лечения. При кефалогематоме более 8 см проводят пункцию.
Повреждения и кровоизлияния в грудино-ключично-сосцевидную мышцу могут возникнуть при наложении щипцов, ручных пособиях, особенно в случае родов в ягодичном предлежании. В области повреждения и гематомы прощупывается небольшая, тестоватой консистенции опухоль. Иногда впервые ее диагностируют к середине-концу первой недели жизни, когда развивается кривошея – голова ребенка наклонена в сторону поврежденной мышцы, а подбородок повернут в противоположную сторону. Нередко кровоизлияние в мышцу сочетается со спинальной травмой. Гематому грудино-ключично-сосцевидной мышцы следует дифференцировать с врожденной мышечной кривошеей. Причиной последней может быть аномалия положения плода, небольшое количество околоплодных вод и давление на мышцу костной части таза матери, а иногда гематома является проявлением множественного поражения костно-мышечной системы (позвоночник, кости черепа и др.). Лечение состоит в обеспечении корригирующего положения головы (валики, которые способствуют устранению патологического наклона головы и поворота лица), использовании сухого тепла, физиотерапии (электрофорез с йодистым калием), позже – массажа. Если лечение оказалось неэффективным, то показано оперативное вмешательство, проводимое в первые 6 месяцев жизни.
Кровоизлияние под апоневроз характеризуется припухлостью тестоватой структуры, отеком теменной и затылочной областей головы. В отличие от кефалогематомы отечность распространяется за границы одной кости, а от родовой опухоли – может расти после рождения. Факторами риска являются вакуум-экстрактор и другие акушерские пособия в родах. Возможно инфицирование. При больших размерах кровоизлияния следует исключить наследственные геморрагические болезни. Необходимо выполнение рентгенограммы черепа для исключения переломов. Нередко сочетается с признаками внутричерепной родовой травмы. Кровоизлияние резорбируется через 2–3 недели.
Кефалогематома– это поднадкостничное кровоизлияние, ограниченное поверхностью одной кости черепа. Ей несвойственно побледнение кожи, типичное для подкожного кровоизлияния, и припухлость обычно появляется только через несколько часов после родов, так как кровотечение в поднадкостничной области происходит медленно. Опухоль вначале имеет упругую консистенцию, никогда не переходит на соседнюю кость, не пульсирует, безболезненная. В первые дни жизни кефалогематома может увеличиваться, на 2-3-й неделе жизни размеры ее уменьшаются, и полная резорбция наступает к 6-8-й неделе. В некоторых случаях возможно обызвествление, редко – нагноение. Причиной поднадкостничного кровоизлияния являются отслойка надкостницы при движениях головы в момент ее прорезывания, реже – трещины черепа. Поэтому всем детям с большими кефалогематомами (диаметром более 8 см) необходимо выполнение рентгенограммы черепа для исключения трещины. Дифференциальный диагноз проводят с родовой опухолью, кровоизлиянием под апоневроз, мозговыми грыжами.
Лечение. Первые 3–4 дня жизни кормить сцеженным материнским молоком из бутылочки, а далее при стабильном состоянии – приложить ребенка к груди. Небольшие кефалогематомы не требуют лечения. При кефалогематоме более 8 см проводят пункцию.
ПАРАЛИЧ ЛИЦЕВОГО НЕРВА
Встречается при повреждении наложенными выходными акушерскими щипцами периферического участка нерва и его ветвей. Характеризуется опущением и неподвижностью угла рта, его припухлостью, отсутствием носогубной складки, неплотным закрытием век на стороне поражения, асимметрией рта при крике, слезотечением. Лечение проводится при консультации с невропатологом.
РОДОВАЯ ТРАВМА СПИННОГО МОЗГА И ПЛЕЧЕВОГО СПЛЕТЕНИЯ
Родовые повреждения спинного мозга чаще всего возникают в результате действия механического фактора (растяжение позвоночника плода при тракции его за головку или тазовый конец, сгибание и вращение позвоночника вокруг продольной оси при поворотах головки во время активного ведения родов). Такие повреждения нередко сочетаются с травматическими повреждениями тел позвонков и межпозвонковых дисков. Второе место по частоте встречаемости занимают поражения спинного мозга, вызываемые действием сосудистого фактора (геморрагические и ишемические нарушения спинального кровообращения). В механизме травматического повреждения спинного мозга ведущая роль принадлежит нарушению кровообращения в бассейне позвоночных артерий с развитием ишемии в области ствола мозга, мозжечка и шейного отдела спинного мозга. При этом тяжесть неврологических расстройств зависит от объема поражения и может носить обратимый характер.
