Страница:
Однако все средства, стимулирующие моторно-эвакуаторную функцию кишечника, часто оказываются малоэффективными вследствие токсической блокады его нейромышечного аппарата при тяжелых отравлениях наркотическими средствами, ФОИ и некоторыми другими ядами.
Наиболее надежный способ очищения кишечника от токсичных веществ – промывание с помощью зондирования и введения специальных растворов – кишечный лаваж.
Лечебное действие этого метода заключается в том, что он дает возможность непосредственного очищения тонкой кишки, где при позднем промывании желудка (через 2–3 ч после отравления) депонируется значительное количество токсиканта, продолжающего поступать в кровь.
Для выполнения кишечного лаважа больному через нос вводят в желудок двухканальный силиконовый зонд (длиной около 2 м) со вставленным в него металлическим мандреном. Затем под контролем гастроскопа этот зонд проводят на расстоянии 30–60 см дистальнее связки Трейтца, после чего мандрен извлекают. Через отверстие перфузионного канала, расположенного у дистального конца зонда, вводят специальный солевой раствор, идентичный по ионному составу химусу (состав раствора представлен в табл. 5).

Навески солей растворяют дистиллированной водой в 2/3 объема, затем добавляют 150 мл 10 %-ного раствора хлорида кальция, 50 мл 25 %-ного раствора сульфата магния и дистиллированной воды до 10 л. В закрытой посуде раствор может храниться 3–4 дня. Осмотическое давление раствора – 235 мОсм/л.
При изменении концентрации раствора меняется его осмолярность (зависимость нелинейная). Если осмотическое давление раствора меньше коллоидно-осмотического давления плазмы крови, то вектор движения воды направлен из кишки в кровь. При обратном соотношении этих значений вектор движения воды направлен из крови в кишку. Для оптимизации процесса и повышения технической эффективности процедуры (по В.А. Маткевичу, 2003) целесообразно готовить более концентрированный раствор по сравнению со стандартным, т. е. доливать дистиллированную воду необходимо не до 10-литровой отметки, а до 9 литров. Интервал значений осмолярности раствора в этих случаях соответственно находится в пределах 280–260 мОсм/л.
Описание методики непрерывного кишечного лаважа (КЛ)
по В.А. Маткевичу (2003)
Процедуры КЛ технически и методически отличаются друг от друга в зависимости от показания и состояния пациента.
Больному устанавливают двухканальный назоеюнальный зонд (ЗКС-21) под эндоскопическим контролем. Подогретый до 38–40 гррС СЭР вводят с помощью насоса в один из каналов зонда со скоростью 60-200 мл/мин. Через некоторое время у больного развивается диарея; часть раствора при этом изливается по второму каналу зонда. Вместе с кишечным содержимым удаляется токсичное вещество, вызвавшее отравление. Для усиления детоксикации организма КЛ сочетают с энтеросорбцией, вводя с помощью шприца через аспирационный (широкий) канал зонда взвесь порошкообразного энтеросорбента в количестве 70-150 г. Кишечник промывают до появления энтеросорбента в промывных водах, полученных из прямой кишки, либо до светлых промывных вод, уже не содержащих яда. Общий объем используемого раствора – 30–60 л и более (до 120 л). В результате КЛ симптомы интоксикации ликвидируются.
Возможные осложнения КЛ бывают в виде травматических повреждений слизистой оболочки ЖКТ вследствие зондирования кишки (5,3 %), рвоты и аспирации (1,8 %), гипергидратации (29,2 %), при строгом соблюдении методики могут быть сведены к минимуму. Гипергидратация легко снимается при ультрафильтрации аппаратом «искусственная почка».
Этим целям лучше всего отвечают осмотические диуретики (мочевина, маннитол), клиническое применение которых было начато датским врачом Лассеном в 1960 г. Осмотический диуретик распределяется только во внеклеточном секторе, не подвергается метаболическим превращениям, полностью фильтруется через базальную мембрану клубочка, не реабсорбируется в канальцевом аппарате почки.
Маннитол – наилучший, широко применяемый осмотический диуретик. Распространяется только во внеклеточной среде, не подвергается метаболизму, не реабсорбируется канальцами почек. Объем распределения маннитола в организме составляет около 14–16 л. Растворы маннитола не раздражают интиму вен, при попадании под кожу не вызывают некрозов. Их вводят внутривенно в виде 15–20 %-ного раствора 1,0–1,5 г на 1 кг массы тела. Суточная доза составляет не более 180 г.
Мочевина – условный осмотический диуретик, распределяется во всем водном секторе организма путем свободной диффузии, не подвергается метаболизму. Препарат нетоксичен, однако высококонцентрированные растворы его повреждают интиму вен и могут быть причиной флебитов. Длительно хранящиеся растворы дают гемолиз. Применяется в виде 30 % раствора в дозе 1,0–1,5 г на 1 кг массы тела больного. При нарушении функции почек введение мочевины может резко повысить содержание азота в организме, поэтому в таких случаях она не применяется.
Фуросемид (лазикс) – сильное диуретическое (салуретическое) средство, действие которого связано с угнетением реабсорбции ионов Na+ и Cl, в меньшей степени – К+.
Эффективность диуретического действия препарата, применяемого в разовой дозе 100–150 мг, сравнима с действием осмотических диуретиков, однако при повторном его введении возможны более значительные потери электролитов, особенно калия.
Метод форсированного диуреза – достаточно универсальный способ ускоренного удаления из организма различных токсичных веществ, в том числе барбитуратов, морфина, ФОИ, хинина и пахикарпина, дихлорэтана, тяжелых металлов и других препаратов, выводимых из организма почками. Эффективность проводимой диуретической терапии значительно снижается в результате образования прочной связи многих химических веществ, попавших в организм, с белками и липидами крови. Это наблюдается, например, при отравлениях фенотиазинами, либриумом, лепонексом и др. При отравлениях токсикантами, дающими в водном растворе кислую реакцию (барбитураты, салицилаты и пр.), предварительно проводится ощелачивание крови путем внутривенного введения гидрокарбоната натрия (4 %-ный раствор 500 мл).
Форсированный диурез всегда проводится в три этапа: предварительная водная нагрузка, быстрое введение диуретика и заместительная инфузия растворов электролитов.
Рекомендуется следующая методика форсированного диуреза. Предварительно производят компенсацию развивающейся при тяжелых отравлениях гиповолемии путем внутривенного введения плазмозамещающих растворов (полиглюкин, 400 мл и 5 %-ный раствор глюкозы в объеме 1,0–1,5 л). Одновременно определяют концентрацию токсичного вещества в крови и моче, гематокрит и вводят постоянный мочевой катетер для измерения почасового диуреза. Мочевину или маннитол (15–20 %-ный раствор) вводят внутривенно струйно в количестве 1,0–1,5 г на 1 кг массы тела больного в течение 10–15 мин, затем – раствор электролитов со скоростью, равной скорости диуреза. Высокий диуретический эффект (500–800 мл/ч) сохраняется в течение 3–4 ч, после чего осмотическое равновесие восстанавливается. При необходимости весь цикл повторяется, но не более двух раз во избежание развития осмотической нефропатии. Сочетанное применение осмотических диуретиков с салуретиками (фуросемид) дает дополнительную возможность увеличить диуретический эффект в 1,5 раза. Однако высокая скорость и большой объем форсированного диуреза, достигающего 10–20 л/сутки, таят в себе потенциальную опасность быстрого вымывания из организма электролитов плазмы.
Для коррекции возможных нарушений солевого баланса вводят раствор электролитов, концентрация которых несколько больше, чем в моче, с учетом того, что часть водной нагрузки создается плазмозамещающими растворами. Оптимальный вариант такого раствора: хлорида калия – 13,5 ммоль/л и хлорида натрия – 120 ммоль/л с последующим контролем и дополнительной коррекцией при необходимости. Кроме того, на каждые 10 л выведенной мочи требуется введение 10 мл 10 % раствора хлорида кальция.
Метод форсированного диуреза иногда называют промыванием крови, поэтому связанная с ним водно-электролитная нагрузка выдвигает повышенные требования к сердечно-сосудистой системе и почкам. Строгий учет введенной и выделенной жидкости, определение гематокрита и центрального венозного давления позволяют легко контролировать водный баланс организма в процессе лечения, несмотря на высокую скорость диуреза.
Осложнения метода форсированного диуреза (гипергидратация, гипокалиемия, гипохлоремия) связаны только с нарушением техники его применения. Во избежание тромбофлебита в месте введения растворов рекомендуется использовать подключичную вену. При длительном применении осмотических диуретиков (свыше 3 суток) возможно развитие осмотического нефроза и острой почечной недостаточности. Поэтому длительность форсированного диуреза обычно ограничивают этими сроками, а осмотические диуретики комбинируют с салуретиками.
Метод форсированного диуреза противопоказан при интоксикациях, осложненных острой сердечно-сосудистой недостаточностью (стойкий коллапс, нарушение кровообращения II–III ст.), а также при нарушениях функции почек (олигурия, азотемия, повышение содержания креатинина крови более 221 ммоль/л, что связано с низким объемом фильтрации). У больных старше 50 лет эффективность метода форсированного диуреза по той же причине заметно снижена.
Эффективность этого метода детоксикации при острых отравлениях сероуглеродом (до 70 % его выделяется через легкие), хлорированными углеводородами, угарным газом доказана в клинических условиях. Однако длительная гипервентиляция приводит к развитию нарушений газового состава крови (гипокапния) и кислотно-основного состояния (дыхательный алкалоз). Поэтому под контролем указанных параметров проводится прерывистая гипервентиляция (по 15–20 мин) повторно через 1–2 ч в течение всей токсикогенной фазы отравления.
Индукторы могут применяться при отравлении веществами, ближайшие метаболиты которых отличаются значительно меньшей токсичностью, чем нативное вещество.
Ингибиторы можно использовать при отравлении такими соединениями, биотрансформация которых протекает по типу «летального синтеза», т. е. с образованием более токсичных метаболитов.
В настоящее время известно более двухсот веществ, способных влиять на активность микросомальных ферментов (цитохром Р-450).
Наиболее изученные индукторы – барбитураты, в частности фенобарбитал или бензонал и специальный венгерский препарат – зиксорин. Под влиянием этих препаратов в митохондриях печени увеличивается уровень и активность цитохрома Р-450, что обусловлено стимуляцией процессов их синтеза. Поэтому лечебное действие проявляется не сразу, а спустя 1,5–2 суток, что значительно ограничивает возможности их применения только теми видами острых отравлений, токсикогенная фаза которых развивается медленно и протекает более длительно, чем указанные выше сроки. Клиническое применение индукторов ферментативной активности показано при отравлениях (передозировке) стероидными гормонами, антикоагулянтами кумаринового ряда, контрацептивными средствами стероидной структуры, анальгетиками типа антипирина, сульфаниламидами, противоопухолевыми препаратами (цитостатиками), витамином D, а также некоторыми инсектицидами (особенно при подостром отравлении) из группы карбаминовой кислоты (диоксикарб, пиримор, севин, фурадан) и фосфорорганическими соединениями (актеллик, валексон, хлорофос).
Дозы применяемых в клинике индукторов ферментативной активности составляют: для зиксорина – по 50-100 мг на 1 кг массы тела 4 раза в день, для реамберина – 5 %-ный раствор 400 мл в вену 2–3 суток. В последние годы наиболее широко в качестве индукторов ферментативной активности используются методы химиогемотерапии с помощью инфузий гипохлорита натрия, также с этой целью можно применять ГБО и ФГТ.
В качестве ингибиторов ферментативной активности предложены многие лекарственные препараты, в частности ниаламид (ингибитор моноаминооксидазы), левомицетин, тетурам и т. д. Однако их клиническая эффективность при отравлении веществами, претерпевающими в организме летальный синтез, ограничена, так как ингибирующее действие развивается на 3-4-е сутки, когда токсикогенная фаза большинства отравлений уже на исходе.
Общая характеристика. Магнитные поля (МП) оказывают на организм сложное воздействие. Учитывая чрезвычайно малую энергию МП, применяемых в лечебных целях, важная роль принадлежит информационному фактору с реализацией ответного сигнала со стороны ЦНС и желез внутренней секреции на клеточном уровне. Кроме того, в силу резонансного эффекта происходит синхронизация колебаний нескольких групп клеток (триггерная реакция) с последующей конформационной перестройкой клеточных структур. Автоколебания, возникающие в мембранах клеток, могут оказать существенное влияние на поляризацию клеточных структур (ядер, электронов и др.) с изменением проницаемости мембран, молекулярного транспорта через них, а также функционирования белков-ферментов и течения биохимических реакций. Большое значение могут иметь процессы структурирования воды с изменением ориентации ядерных спинов водорода в ее молекулах. Изменение условий гидродинамического взаимодействия эритроцитов и возрастание их эквидистантности (пространственного разобщения) приводит к положительным сдвигам гемореологических показателей. При острых отравлениях психофармакологическими средствами, ФОИ и другими токсикантами экстракорпоральное воздействие магнитных полей на кровь, протекающую в рабочем зазоре электромагнита специального устройства (МГТ), сопровождается быстрой и значительной (на 18–59 %) дезагрегацией эритроцитов и тромбоцитов, также снижением гематокрита, СОЭ, относительной вязкости крови и плазмы. В результате существенно улучшаются основные гемодинамические показатели, что расширяет возможности искусственной (сорбционно-диализной) детоксикации организма: в процессе гемосорбции заметно возрастает темп сорбции некоторых ядов (ФОИ, амитриптилина), а также «средних молекул» (СМ) за счет их более полного контакта с сорбентом.
На фоне МГТ также улучшается иммунный статус, что сопровождается более заметными положительными сдвигами гуморального иммунитета и активацией кислородзависимой переваривающей функции нейтрофилов. Через сутки после МГТ, кроме того, заметно возрастает артериовенозная разность по кислороду. В качестве специфического биохимического эффекта МГТ имеет место быстрое восстановление активности холинэстеразы крови при отравлениях ФОИ.
Использование физико-химической гемотерапии, в том числе и магнитной, требует обязательного определения границ однократного воздействия, которые, подобно разовым дозам фармакологических препаратов, должны находиться в пределах так называемых биотропных параметров, обеспечивающих безопасность применяемого лечения и его объективный биологический эффект. При МГТ, не обладающей мощным энергетическим воздействием, учитываются такие параметры, как вид магнитного поля (постоянное, импульсное), частота импульсного магнитного поля, а также продолжительность процедуры (сеанса). Кроме того, достигается возможность более целенаправленного воздействия МГТ: постоянные магнитные поля эффективней в отношении гемореологических показателей, а импульсные активней влияют на очищение крови от эндогенных токсикантов среднемолекулярного характера, причем оптимальной частотой импульсного магнитного поля является частота, равная 100 Гц. При ней детоксикация крови от «средних молекул» при различных значениях магнитной индукции протекает наиболее устойчиво. Использование импульсных магнитных полей, следовательно, более полезно в случаях выраженного эндотоксического компонента, определяемого по высокому уровню в крови «средних молекул» и по другим тестам, что может наблюдаться, например, при позднем поступлении больных и связанными с этим большими сроками токсикогенной стадии.
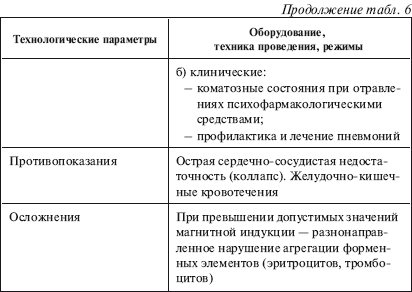
Конкретные технологические параметры МГТ приведены в табл. 6.



Ультрафиолетовая гемотерапия (УФГТ)
Общая характеристика. Лечебное действие ультрафиолетовых лучей (длина волны 100–400 нм), представляющих часть солнечного спектра, связывают с их влиянием на белки и липиды, поглощение которыми квантов излучения сопровождается образованием озона и фотоперекисей, что катализирует энзиматические реакции (перекисная теория). Полагают также, что частичная фотодеструкция (фотолизис) молекул белка и других биополимеров (липидов, полисахаридов, нуклеиновых кислот и пигментов) ведет к образованию новых биологически активных соединений – свободнорадикальных продуктов. Они являются антигенами и вызывают иммунный ответ организма (антигенная теория). При этом различают прямой эффект ультрафиолетового облучения, сопровождающий первичное повреждающее действие продуктов, образованных вследствие поглощения УФ-лучей биополимерами и активации эндо– и экзонуклеазы, и непрямой, связанный с поглощением и переносом энергии низкомолекулярными структурами, что вызывает вторичную реакцию биополимеров. В обоих случаях последующие реакции формируют биологический эффект УФ-облучения. При этом возможны и репаративные процессы (фотосинтез), так как повреждение биополимеров одновременно приводит к активации лидазы. Иммунный ответ также может быть вызван сенсибилизацией лейкоцитов УФ-лучами. Активация ферментов, кроме того, может быть обязана действию сульфгидрильных групп, интенсивно образующихся под влиянием УФ-облучения (сульфгидрильная теория). В целом физиологический эффект УФ-облучения на организм складывается из сложного взаимодействия многочисленных молекулярных клеточных и клеточно-опосредованных механизмов с участием биологически активных веществ, что, вероятно, приводит к фотоассоциации равновесных физиологических процессов.
К важнейшим эффектам УФ-облучения относят его бактерицидное действие, связанное с блокированием в вирусах и бактериях процессов репликации ДНК и синтеза информационной РНК, а также инактивацией трансформационной активности ДНК, что приводит микроорганизмы к гибели. Тем самым бактерицидность крови может быть многократно увеличена.
При острых отравлениях, отравлениях психофармакологическими средствами, ФОИ и другими ядами сочетанное проведение гемосорбции и ультрафиолетовой гемотерапии (УФГТ) сопровождается заметным снижением летальности, частоты и тяжести инфекционных осложнений, особенно пневмоний. При этом наблюдается сокращение длительности коматозного состояния, продолжительности искусственной вентиляции легких, а при отравлениях фосфорорганическими соединениями – уменьшение частоты рецидивов интоксикации. Также отмечают более раннее и стойкое (чем только при гемосорбции) улучшение некоторых показателей иммунитета, изначально измененных по типу токсической иммунной депрессии, в виде увеличения уровня в крови Т-лимфоцитов (на 30–90 %) и активности фагоцитоза, особенно метаболической. Характерное следствие УФГТ – значительное повышение функциональных резервов фагоцитарной системы, что заметно усиливает ее надежность. В результате сроки восстановления иммунограммы до изначальных значений сокращаются до 1 недели.
Наиболее надежный способ очищения кишечника от токсичных веществ – промывание с помощью зондирования и введения специальных растворов – кишечный лаваж.
Лечебное действие этого метода заключается в том, что он дает возможность непосредственного очищения тонкой кишки, где при позднем промывании желудка (через 2–3 ч после отравления) депонируется значительное количество токсиканта, продолжающего поступать в кровь.
Для выполнения кишечного лаважа больному через нос вводят в желудок двухканальный силиконовый зонд (длиной около 2 м) со вставленным в него металлическим мандреном. Затем под контролем гастроскопа этот зонд проводят на расстоянии 30–60 см дистальнее связки Трейтца, после чего мандрен извлекают. Через отверстие перфузионного канала, расположенного у дистального конца зонда, вводят специальный солевой раствор, идентичный по ионному составу химусу (состав раствора представлен в табл. 5).

Навески солей растворяют дистиллированной водой в 2/3 объема, затем добавляют 150 мл 10 %-ного раствора хлорида кальция, 50 мл 25 %-ного раствора сульфата магния и дистиллированной воды до 10 л. В закрытой посуде раствор может храниться 3–4 дня. Осмотическое давление раствора – 235 мОсм/л.
При изменении концентрации раствора меняется его осмолярность (зависимость нелинейная). Если осмотическое давление раствора меньше коллоидно-осмотического давления плазмы крови, то вектор движения воды направлен из кишки в кровь. При обратном соотношении этих значений вектор движения воды направлен из крови в кишку. Для оптимизации процесса и повышения технической эффективности процедуры (по В.А. Маткевичу, 2003) целесообразно готовить более концентрированный раствор по сравнению со стандартным, т. е. доливать дистиллированную воду необходимо не до 10-литровой отметки, а до 9 литров. Интервал значений осмолярности раствора в этих случаях соответственно находится в пределах 280–260 мОсм/л.
Описание методики непрерывного кишечного лаважа (КЛ)
по В.А. Маткевичу (2003)
Процедуры КЛ технически и методически отличаются друг от друга в зависимости от показания и состояния пациента.
Больному устанавливают двухканальный назоеюнальный зонд (ЗКС-21) под эндоскопическим контролем. Подогретый до 38–40 гррС СЭР вводят с помощью насоса в один из каналов зонда со скоростью 60-200 мл/мин. Через некоторое время у больного развивается диарея; часть раствора при этом изливается по второму каналу зонда. Вместе с кишечным содержимым удаляется токсичное вещество, вызвавшее отравление. Для усиления детоксикации организма КЛ сочетают с энтеросорбцией, вводя с помощью шприца через аспирационный (широкий) канал зонда взвесь порошкообразного энтеросорбента в количестве 70-150 г. Кишечник промывают до появления энтеросорбента в промывных водах, полученных из прямой кишки, либо до светлых промывных вод, уже не содержащих яда. Общий объем используемого раствора – 30–60 л и более (до 120 л). В результате КЛ симптомы интоксикации ликвидируются.
Возможные осложнения КЛ бывают в виде травматических повреждений слизистой оболочки ЖКТ вследствие зондирования кишки (5,3 %), рвоты и аспирации (1,8 %), гипергидратации (29,2 %), при строгом соблюдении методики могут быть сведены к минимуму. Гипергидратация легко снимается при ультрафильтрации аппаратом «искусственная почка».
Клинический пример № 13
Больная М., 47 лет,
поступила в Центр лечения острых отравлений НИИ СП им. Н.В. Склифосовского 14.04.85 г. в 02:15. Доставлена бригадой СМП из дома, где была обнаружена родственниками без сознания. Предположительно, накануне могла принять препараты снотворного действия с суицидальной целью. Врач «Скорой помощи» промыл желудок больной через зонд, начал внутривенную инфузионную терапию.
При поступлении состояние больной было крайне тяжелым: без сознания, болевая чувствительность и фотореакция зрачков отсутствовали, отмечалась гипотония скелетной мускулатуры. Кожные покровы бледные, цианоз губ, акроцианоз. Дыхание – в виде единичных поверхностных вдохов. Пульс – 80 уд/мин, АД – 110/70 мм рт. ст.
В крови больной были обнаружены барбитураты в количестве 32 мкг/мл, в моче – 68 мкг/мл. Кроме того, в моче больной были обнаружены бензодиазепины.
Диагноз: отравление снотворными препаратами III ст., нарушение дыхания по смешанному типу. Суицид.
Лечебные мероприятия: интубация трахеи, эндоскопическая санация трахеобронхиального дерева, ИВЛ. С целью детоксикации организма продолжена инфузионная терапия с последующей стимуляцией диуреза. Повторно промыт желудок через зонд. Проводилась симптоматическая терапия. С целью очищения крови больной проведена гемосорбция в течение 60 мин двумя колонками объемом 150 см3 каждая, заполненными активированным углем марки «ИГИ». Скорость потока крови через колонку составила 100 мл/мин.
В результате проведенного лечения состояние больной существенно не улучшилось: появилась лишь слабо выраженная двигательная реакция на болевые раздражения и реакция зрачков на свет.
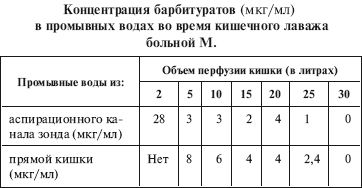
Концентрация барбитуратов в крови больной при этом снизилась до 22 мкг/мл, а через некоторое время был отмечен подъем – до уровня 43 мкг/мл. В связи с этим под эндоскопическим контролем было произведено зондирование тонкой кишки больной и начат кишечный лаваж (КЛ). В пробах жидкости, оттекавшей по аспирационному каналу зонда и дренажу, находившемуся в прямой кишке, обнаруживались барбитураты и бензодиазепины. Пробы промывных вод брали после введения через зонд 2, 5, 10, 15 и т. д. литров раствора. Объем перфузии кишки в данном случае составил 30 литров раствора. Концентрация барбитуратов в пробах промывных вод представлена в таблице.

К моменту окончания КЛ состояние больной улучшилось: глубина комы уменьшилась. Концентрация барбитуратов в крови к этому моменту снизилась на 46,5 %, но оставалась еще на довольно высоком уровне – 23 мкг/мл. В связи с этим была проведена повторная ГС в прежнем режиме. Во время ГС у больной появилась спонтанная двигательная активность, восстановилось самостоятельное дыхание, больная стала приходить в сознание. В последующее время была произведена экстубация трахеи, симптомы интоксикации разрешились, процесс выздоровления протекал гладко.
Понятно, что быстро снизить концентрацию барбитуратов в крови больной удалось лишь после КЛ. В результате активной комбинированной детоксикации организма (ГС и КЛ) больная через короткое время (7 ч) из глубокой комы пришла в сознание.
Клинический диагноз: 1. Острое отравление барбитуратами и бензодиазепинами III ст. Суицид. 2. Коматозное состояние с нарушением дыхания по смешанному типу (3б по шкале Глазго).
P.S. В данном случае имел место прием большого количества снотворных препаратов и длительная экспозиция отравления. Первый сеанс ГС позволил на короткое время снизить концентрацию токсикантов в крови, что сопровождалось некоторым улучшением состояния больной. Однако это спровоцировало возобновление резорбции токсичных веществ из желудочно-кишечного тракта (ЖКТ), повышение концентрации барбитуратов в крови до уровня, превышающего первоначальный (при поступлении в отделение) и утяжеление клинического состояния больной. Применение КЛ позволило удалить депо токсичных веществ из полости ЖКТ, уменьшить поступление этих веществ в кровь, что сопровождалось плавным снижением концентрации барбитуратов в крови и улучшением клинического состояния пациентки. В этих условиях эффект от повторного сеанса ГС оказался более выраженным, чем от первого, и достаточным, так как позволил «оборвать» токсикогенную стадию отравления. Таким образом, в данном случае было бы логичнее начать детоксикацию организма с КЛ, а затем, при необходимости, подключить метод очищения крови (ГС).
2. Метод форсированного диуреза
Форсированный диурез как метод детоксикации основан на применении препаратов, способствующих резкому возрастанию диуреза, и является наиболее распространенным методом консервативного лечения отравлений, когда выведение гидрофильных токсикантов осуществляется преимущественно почками.Этим целям лучше всего отвечают осмотические диуретики (мочевина, маннитол), клиническое применение которых было начато датским врачом Лассеном в 1960 г. Осмотический диуретик распределяется только во внеклеточном секторе, не подвергается метаболическим превращениям, полностью фильтруется через базальную мембрану клубочка, не реабсорбируется в канальцевом аппарате почки.
Маннитол – наилучший, широко применяемый осмотический диуретик. Распространяется только во внеклеточной среде, не подвергается метаболизму, не реабсорбируется канальцами почек. Объем распределения маннитола в организме составляет около 14–16 л. Растворы маннитола не раздражают интиму вен, при попадании под кожу не вызывают некрозов. Их вводят внутривенно в виде 15–20 %-ного раствора 1,0–1,5 г на 1 кг массы тела. Суточная доза составляет не более 180 г.
Мочевина – условный осмотический диуретик, распределяется во всем водном секторе организма путем свободной диффузии, не подвергается метаболизму. Препарат нетоксичен, однако высококонцентрированные растворы его повреждают интиму вен и могут быть причиной флебитов. Длительно хранящиеся растворы дают гемолиз. Применяется в виде 30 % раствора в дозе 1,0–1,5 г на 1 кг массы тела больного. При нарушении функции почек введение мочевины может резко повысить содержание азота в организме, поэтому в таких случаях она не применяется.
Фуросемид (лазикс) – сильное диуретическое (салуретическое) средство, действие которого связано с угнетением реабсорбции ионов Na+ и Cl, в меньшей степени – К+.
Эффективность диуретического действия препарата, применяемого в разовой дозе 100–150 мг, сравнима с действием осмотических диуретиков, однако при повторном его введении возможны более значительные потери электролитов, особенно калия.
Метод форсированного диуреза – достаточно универсальный способ ускоренного удаления из организма различных токсичных веществ, в том числе барбитуратов, морфина, ФОИ, хинина и пахикарпина, дихлорэтана, тяжелых металлов и других препаратов, выводимых из организма почками. Эффективность проводимой диуретической терапии значительно снижается в результате образования прочной связи многих химических веществ, попавших в организм, с белками и липидами крови. Это наблюдается, например, при отравлениях фенотиазинами, либриумом, лепонексом и др. При отравлениях токсикантами, дающими в водном растворе кислую реакцию (барбитураты, салицилаты и пр.), предварительно проводится ощелачивание крови путем внутривенного введения гидрокарбоната натрия (4 %-ный раствор 500 мл).
Форсированный диурез всегда проводится в три этапа: предварительная водная нагрузка, быстрое введение диуретика и заместительная инфузия растворов электролитов.
Рекомендуется следующая методика форсированного диуреза. Предварительно производят компенсацию развивающейся при тяжелых отравлениях гиповолемии путем внутривенного введения плазмозамещающих растворов (полиглюкин, 400 мл и 5 %-ный раствор глюкозы в объеме 1,0–1,5 л). Одновременно определяют концентрацию токсичного вещества в крови и моче, гематокрит и вводят постоянный мочевой катетер для измерения почасового диуреза. Мочевину или маннитол (15–20 %-ный раствор) вводят внутривенно струйно в количестве 1,0–1,5 г на 1 кг массы тела больного в течение 10–15 мин, затем – раствор электролитов со скоростью, равной скорости диуреза. Высокий диуретический эффект (500–800 мл/ч) сохраняется в течение 3–4 ч, после чего осмотическое равновесие восстанавливается. При необходимости весь цикл повторяется, но не более двух раз во избежание развития осмотической нефропатии. Сочетанное применение осмотических диуретиков с салуретиками (фуросемид) дает дополнительную возможность увеличить диуретический эффект в 1,5 раза. Однако высокая скорость и большой объем форсированного диуреза, достигающего 10–20 л/сутки, таят в себе потенциальную опасность быстрого вымывания из организма электролитов плазмы.
Для коррекции возможных нарушений солевого баланса вводят раствор электролитов, концентрация которых несколько больше, чем в моче, с учетом того, что часть водной нагрузки создается плазмозамещающими растворами. Оптимальный вариант такого раствора: хлорида калия – 13,5 ммоль/л и хлорида натрия – 120 ммоль/л с последующим контролем и дополнительной коррекцией при необходимости. Кроме того, на каждые 10 л выведенной мочи требуется введение 10 мл 10 % раствора хлорида кальция.
Метод форсированного диуреза иногда называют промыванием крови, поэтому связанная с ним водно-электролитная нагрузка выдвигает повышенные требования к сердечно-сосудистой системе и почкам. Строгий учет введенной и выделенной жидкости, определение гематокрита и центрального венозного давления позволяют легко контролировать водный баланс организма в процессе лечения, несмотря на высокую скорость диуреза.
Осложнения метода форсированного диуреза (гипергидратация, гипокалиемия, гипохлоремия) связаны только с нарушением техники его применения. Во избежание тромбофлебита в месте введения растворов рекомендуется использовать подключичную вену. При длительном применении осмотических диуретиков (свыше 3 суток) возможно развитие осмотического нефроза и острой почечной недостаточности. Поэтому длительность форсированного диуреза обычно ограничивают этими сроками, а осмотические диуретики комбинируют с салуретиками.
Метод форсированного диуреза противопоказан при интоксикациях, осложненных острой сердечно-сосудистой недостаточностью (стойкий коллапс, нарушение кровообращения II–III ст.), а также при нарушениях функции почек (олигурия, азотемия, повышение содержания креатинина крови более 221 ммоль/л, что связано с низким объемом фильтрации). У больных старше 50 лет эффективность метода форсированного диуреза по той же причине заметно снижена.
3. Лечебная гипервентиляция
К методам усиления естественных процессов детоксикации организма относится лечебная гипервентиляция, которая может быть обеспечена ингаляцией карбогена или подключением больного к аппарату искусственного дыхания, позволяющему повысить минутный объем дыхания (МОД) в 1,5–2 раза. Этот метод считается особенно эффективным при острых отравлениях токсичными веществами, которые в значительной степени удаляются из организма легкими.Эффективность этого метода детоксикации при острых отравлениях сероуглеродом (до 70 % его выделяется через легкие), хлорированными углеводородами, угарным газом доказана в клинических условиях. Однако длительная гипервентиляция приводит к развитию нарушений газового состава крови (гипокапния) и кислотно-основного состояния (дыхательный алкалоз). Поэтому под контролем указанных параметров проводится прерывистая гипервентиляция (по 15–20 мин) повторно через 1–2 ч в течение всей токсикогенной фазы отравления.
4. Регуляция ферментативной активности
Биотрансформация токсичных веществ – один из важнейших путей естественной детоксикации организма. При этом возможно повышение активности индукции ферментов, главным образом в микросомах печени, ответственных за метаболизм токсичных соединений, или снижение активности этих метаболитов, т. е. ингибиция, влекущее за собой замедление метаболизма. В клинической практике используются препараты-индукторы или ингибиторы ферментов, влияющие на биотрансформацию ксенобиотиков с целью снижения их токсического действия.Индукторы могут применяться при отравлении веществами, ближайшие метаболиты которых отличаются значительно меньшей токсичностью, чем нативное вещество.
Ингибиторы можно использовать при отравлении такими соединениями, биотрансформация которых протекает по типу «летального синтеза», т. е. с образованием более токсичных метаболитов.
В настоящее время известно более двухсот веществ, способных влиять на активность микросомальных ферментов (цитохром Р-450).
Наиболее изученные индукторы – барбитураты, в частности фенобарбитал или бензонал и специальный венгерский препарат – зиксорин. Под влиянием этих препаратов в митохондриях печени увеличивается уровень и активность цитохрома Р-450, что обусловлено стимуляцией процессов их синтеза. Поэтому лечебное действие проявляется не сразу, а спустя 1,5–2 суток, что значительно ограничивает возможности их применения только теми видами острых отравлений, токсикогенная фаза которых развивается медленно и протекает более длительно, чем указанные выше сроки. Клиническое применение индукторов ферментативной активности показано при отравлениях (передозировке) стероидными гормонами, антикоагулянтами кумаринового ряда, контрацептивными средствами стероидной структуры, анальгетиками типа антипирина, сульфаниламидами, противоопухолевыми препаратами (цитостатиками), витамином D, а также некоторыми инсектицидами (особенно при подостром отравлении) из группы карбаминовой кислоты (диоксикарб, пиримор, севин, фурадан) и фосфорорганическими соединениями (актеллик, валексон, хлорофос).
Дозы применяемых в клинике индукторов ферментативной активности составляют: для зиксорина – по 50-100 мг на 1 кг массы тела 4 раза в день, для реамберина – 5 %-ный раствор 400 мл в вену 2–3 суток. В последние годы наиболее широко в качестве индукторов ферментативной активности используются методы химиогемотерапии с помощью инфузий гипохлорита натрия, также с этой целью можно применять ГБО и ФГТ.
В качестве ингибиторов ферментативной активности предложены многие лекарственные препараты, в частности ниаламид (ингибитор моноаминооксидазы), левомицетин, тетурам и т. д. Однако их клиническая эффективность при отравлении веществами, претерпевающими в организме летальный синтез, ограничена, так как ингибирующее действие развивается на 3-4-е сутки, когда токсикогенная фаза большинства отравлений уже на исходе.
5. Физио– и химиогемотерапия
Магнитная гемотерапия (МГТ)Общая характеристика. Магнитные поля (МП) оказывают на организм сложное воздействие. Учитывая чрезвычайно малую энергию МП, применяемых в лечебных целях, важная роль принадлежит информационному фактору с реализацией ответного сигнала со стороны ЦНС и желез внутренней секреции на клеточном уровне. Кроме того, в силу резонансного эффекта происходит синхронизация колебаний нескольких групп клеток (триггерная реакция) с последующей конформационной перестройкой клеточных структур. Автоколебания, возникающие в мембранах клеток, могут оказать существенное влияние на поляризацию клеточных структур (ядер, электронов и др.) с изменением проницаемости мембран, молекулярного транспорта через них, а также функционирования белков-ферментов и течения биохимических реакций. Большое значение могут иметь процессы структурирования воды с изменением ориентации ядерных спинов водорода в ее молекулах. Изменение условий гидродинамического взаимодействия эритроцитов и возрастание их эквидистантности (пространственного разобщения) приводит к положительным сдвигам гемореологических показателей. При острых отравлениях психофармакологическими средствами, ФОИ и другими токсикантами экстракорпоральное воздействие магнитных полей на кровь, протекающую в рабочем зазоре электромагнита специального устройства (МГТ), сопровождается быстрой и значительной (на 18–59 %) дезагрегацией эритроцитов и тромбоцитов, также снижением гематокрита, СОЭ, относительной вязкости крови и плазмы. В результате существенно улучшаются основные гемодинамические показатели, что расширяет возможности искусственной (сорбционно-диализной) детоксикации организма: в процессе гемосорбции заметно возрастает темп сорбции некоторых ядов (ФОИ, амитриптилина), а также «средних молекул» (СМ) за счет их более полного контакта с сорбентом.
На фоне МГТ также улучшается иммунный статус, что сопровождается более заметными положительными сдвигами гуморального иммунитета и активацией кислородзависимой переваривающей функции нейтрофилов. Через сутки после МГТ, кроме того, заметно возрастает артериовенозная разность по кислороду. В качестве специфического биохимического эффекта МГТ имеет место быстрое восстановление активности холинэстеразы крови при отравлениях ФОИ.
Использование физико-химической гемотерапии, в том числе и магнитной, требует обязательного определения границ однократного воздействия, которые, подобно разовым дозам фармакологических препаратов, должны находиться в пределах так называемых биотропных параметров, обеспечивающих безопасность применяемого лечения и его объективный биологический эффект. При МГТ, не обладающей мощным энергетическим воздействием, учитываются такие параметры, как вид магнитного поля (постоянное, импульсное), частота импульсного магнитного поля, а также продолжительность процедуры (сеанса). Кроме того, достигается возможность более целенаправленного воздействия МГТ: постоянные магнитные поля эффективней в отношении гемореологических показателей, а импульсные активней влияют на очищение крови от эндогенных токсикантов среднемолекулярного характера, причем оптимальной частотой импульсного магнитного поля является частота, равная 100 Гц. При ней детоксикация крови от «средних молекул» при различных значениях магнитной индукции протекает наиболее устойчиво. Использование импульсных магнитных полей, следовательно, более полезно в случаях выраженного эндотоксического компонента, определяемого по высокому уровню в крови «средних молекул» и по другим тестам, что может наблюдаться, например, при позднем поступлении больных и связанными с этим большими сроками токсикогенной стадии.
Конкретные технологические параметры МГТ приведены в табл. 6.




Ультрафиолетовая гемотерапия (УФГТ)
Общая характеристика. Лечебное действие ультрафиолетовых лучей (длина волны 100–400 нм), представляющих часть солнечного спектра, связывают с их влиянием на белки и липиды, поглощение которыми квантов излучения сопровождается образованием озона и фотоперекисей, что катализирует энзиматические реакции (перекисная теория). Полагают также, что частичная фотодеструкция (фотолизис) молекул белка и других биополимеров (липидов, полисахаридов, нуклеиновых кислот и пигментов) ведет к образованию новых биологически активных соединений – свободнорадикальных продуктов. Они являются антигенами и вызывают иммунный ответ организма (антигенная теория). При этом различают прямой эффект ультрафиолетового облучения, сопровождающий первичное повреждающее действие продуктов, образованных вследствие поглощения УФ-лучей биополимерами и активации эндо– и экзонуклеазы, и непрямой, связанный с поглощением и переносом энергии низкомолекулярными структурами, что вызывает вторичную реакцию биополимеров. В обоих случаях последующие реакции формируют биологический эффект УФ-облучения. При этом возможны и репаративные процессы (фотосинтез), так как повреждение биополимеров одновременно приводит к активации лидазы. Иммунный ответ также может быть вызван сенсибилизацией лейкоцитов УФ-лучами. Активация ферментов, кроме того, может быть обязана действию сульфгидрильных групп, интенсивно образующихся под влиянием УФ-облучения (сульфгидрильная теория). В целом физиологический эффект УФ-облучения на организм складывается из сложного взаимодействия многочисленных молекулярных клеточных и клеточно-опосредованных механизмов с участием биологически активных веществ, что, вероятно, приводит к фотоассоциации равновесных физиологических процессов.
К важнейшим эффектам УФ-облучения относят его бактерицидное действие, связанное с блокированием в вирусах и бактериях процессов репликации ДНК и синтеза информационной РНК, а также инактивацией трансформационной активности ДНК, что приводит микроорганизмы к гибели. Тем самым бактерицидность крови может быть многократно увеличена.
При острых отравлениях, отравлениях психофармакологическими средствами, ФОИ и другими ядами сочетанное проведение гемосорбции и ультрафиолетовой гемотерапии (УФГТ) сопровождается заметным снижением летальности, частоты и тяжести инфекционных осложнений, особенно пневмоний. При этом наблюдается сокращение длительности коматозного состояния, продолжительности искусственной вентиляции легких, а при отравлениях фосфорорганическими соединениями – уменьшение частоты рецидивов интоксикации. Также отмечают более раннее и стойкое (чем только при гемосорбции) улучшение некоторых показателей иммунитета, изначально измененных по типу токсической иммунной депрессии, в виде увеличения уровня в крови Т-лимфоцитов (на 30–90 %) и активности фагоцитоза, особенно метаболической. Характерное следствие УФГТ – значительное повышение функциональных резервов фагоцитарной системы, что заметно усиливает ее надежность. В результате сроки восстановления иммунограммы до изначальных значений сокращаются до 1 недели.
