Страница:
Чаще всего антителам достаточно связаться с определенным возбудителем, чтобы оказать ему противодействие. В случае вируса, находящегося в свободном состоянии, они препятствуют его связыванию с клеткой хозяина и проникновению внутрь ее. Однако антитела не в состоянии самостоятельно бороться с вирусами и другими возбудителями после того, когда они «прячутся» внутри клетки.
Борьба с внутриклеточными паразитами, которыми являются вирусы, – главная забота второй линии обороны – клеточного иммунитета. Клеточным этот иммунитет именуют потому, что в нем участвуют специальные клетки, которые и являются эффективным оружием для поражения чужеродных клеток при непосредственном контакте с ними. Для этой цели служат уже упоминавшиеся фагоциты, которые циркулируют в крови и бросаются на незваных пришельцев-чужаков, помеченных антителами, поглощая и разрушая проникшие в организм микробы, ядовитые вещества и другие чужеродные для организма клетки и ткани. При этом, победив врага, фагоциты тоже погибают. Они как бы жертвуют собой для блага целого организма.
Но главную основу клеточного иммунитета составляют лимфоциты, которые для своего созревания переселяются из костного мозга в другой центральный орган лимфоидной системы – тимус (вилочковая железа). Эта ветвь лимфоцитов получила название «тимус-зависимые», или «Т-лимфоциты» (от первой буквы английского слова thymus).
В организме человека Т-лимфоциты многократно покидают лимфоидные органы, попадая сначала в лимфу, затем в кровь, а из крови снова возвращаясь в органы. Т-лимфоциты – «вечные странники», они постоянно в движении. За свою жизнь лимфоцит может проходить поразительно большие расстояния – от 100 и более километров. Благодаря интенсивной циркуляции лимфоциты, когда в них возникает потребность, удивительно быстро появляются в «горячих точках». Без такой способности лимфоцитов были бы невозможны своевременное их развитие, взаимодействие и эффективное участие в иммунном ответе при вторжении в организм чужеродных агентов.
В тимусе формируются разные виды Т-клеток, поэтому тимус иногда называют школой обучения Т-клеток. «Ученики» после окончания этой школы сильно отличаются друг от друга. Одни из них участвуют в регуляции развития B-клеток и образования антител, другие взаимодействуют с фагоцитами, помогая им разрушать поглощенные микробные клетки. Некоторые Т-лим-фоциты сами обладают способностью разрушать чужеродные клетки, умерщвлять их. По этой причине их назвали цитотокси-ческими, или «киллерами». B отличие от антител Т-киллер ничего не может сделать с растворимым антигеном – ни обезвредить его, ни удалить из организма. Но он очень активно и целенаправленно убивает клетки, содержащие чужеродный антиген. Т-киллер проходит мимо растворимого антигена, но не пропускает антиген, находящийся на поверхности «чужой» клетки.
Другая разновидность лимфоцитов – Т-хелперы (от английского слова helper – помощник). Названы они так по той причине, что первыми распознают чужеродные вещества и помогают другим лимфоцитам выполнять их прямую функцию. Т-хелперы сами по себе не способны ни вырабатывать антитела, ни убивать клетки-мишени. Но, распознавая чужеродный антиген, они реагируют на него выработкой различных факторов, которые крайне необходимы для размножения и созревания B-клеток и Т-киллеров. Наконец, существуют еще специальные клетки Т-су-прессоры, которые, в отличие от двух других видов, заняты прямо противоположным действием – подавляют активность иммунного ответа, когда необходимость в нем отпадает. Это служит надежной защитой самой иммунной системы от переистощения.
Следует отметить, что центральная роль в клеточном иммунитете принадлежит Т-хелперам. Они помогают координировать работу всех клеток, задействованных в иммунной реакции. Именно Т-хелперы являются ключевым звеном в распознавании антигенов, влияют на деятельность других типов Т-клеток, оказывают помощь B-клеткам в образовании антител. По их командам к «чужакам», нарушившим спокойствие, иммунная система сначала направляет специальный отряд Т-лимфоцитов-килле-ров, основная задача которых с помощью непосредственного контакта убивать зараженные клетки. Для того чтобы «киллеры» нашли и уничтожили противника, им надо отличить нормальные клетки от пораженных. Как и в случае антител, опознание происходит за счет антигена, если он высовывается из клетки, расположен на ее поверхности.
Подобно B-лимфоцитам, каждая Т-клетка имеет специфический рецептор, который распознает этот антиген. С помощью рецепторов Т-лимфоциты-киллеры вступают в теснейший контакт со своей мишенью. Прикрепившись, они выделяют в просвет между собой и мишенью особый белок, «продырявливающий» мембрану клетки-мишени, в результате чего клетка гибнет. Затем они открепляются от мишени и переходят на другую клетку, и так несколько раз. Это явление иммунологи называют «поцелуем смерти».
Важную роль в защитной реакции организма играют и Т-супрессоры. Они вступают в действие, когда основная «работа» закончена. Главная задача Т-супрессоров – подавлять активность иммунного ответа, когда необходимость в нем исчезает. Их роль чрезвычайно важна: если иммунный ответ не будет прекращен после обезвреживания чужеродного агента, иммунные клетки будут продолжать работать, а в результате – поражать собственные здоровые клетки организма, что приведет к развитию различных болезней (их называют аутоиммунными). Так работает еще один компонент иммунной системы – очень сложный, но весьма мощный и важный для выживания организма.
Для того чтобы различать все существующие разнообразные популяции лимфоидных клеток между собой, ученые использовали тот факт, что на поверхности каждой из них присутствуют определенные специфические белки, которые могут служить своеобразными «метками». Такие белки-метки получили сокращенное название CD (по-русски – групповой маркер). На сегодняшний день известно около 200 подобных маркеров. Например, маркером для Т-клеток-хелперов служит белок, названный CD4. Этот факт следует запомнить, поскольку мы неоднократно будем возвращаться к нему.
Т-лимфоциты способны выполнять свои функции только при определенных условиях и поддержке других клеток. К таковым в первую очередь относятся В-лимфоциты и различные фагоцитирующие клетки, в первую очередь один из видов фагоцитов – макрофаги – большие по размерам клетки, поглощающие и переваривающие микробы и другие погибшие клетки. Существенную роль в работе иммунной системы играют так называемые дендритные (ветвистые) клетки, часть которых находится непосредственно под кожей и слизистой оболочкой человека. Такие клетки обычно затаиваются, как бы поджидая микробы и вирусы типа ВИЧ, проникающие через слизистую, захватывают их, а затем переносят в лимфоузлы, где «представляют» непрошеных гостей В– и Т-лимфоцитам, которые их и атакуют. Когда говорят, что клетка «представляет антиген» (такие клетки еще называют антигенпредставляющими), то имеется в виду почти то же самое, что происходит в компании людей, когда хозяин знакомит уже собравшихся гостей с новым незнакомым им посетителем (т. е. представляет его присутствующим).
Bсе клетки иммунной системы имеют определенные функции и работают в четко согласованном взаимодействии, которое обеспечивается специальными биологически активными веществами – цитокинами – регуляторами иммунных реакций. Ци-токинами обобщенно назвали специфические белки, с помощью которых многочисленные и разнообразные клетки иммунной системы могут «переговариваться», обмениваться друг с другом информацией и в результате этого осуществлять строгую координацию своих действий. Набор и количества цитокинов, действующих на рецепторы клеточной поверхности, – «цитокиновая среда» – представляют собой матрицу взаимодействующих и часто меняющихся сигналов. Эти сигналы носят сложный характер из-за большого разнообразия цитокиновых рецепторов и из-за того, что каждый из цитокинов может активировать или подавлять несколько процессов, включая свой собственный синтез и синтез других цитокинов, а также образование и появление на поверхности клеток цитокиновых рецепторов. Для различных тканей характерна своя здоровая «цитокиновая среда», возможны вариации для одной и той же ткани на разные моменты времени. К настоящему времени обнаружено уже более сотни разнообразных цитокинов, и не факт, что на этом дело ограничится.
Иммунную систему часто сравнивают с «системой коллективной безопасности», механизм которой чрезвычайно сложен, но согласованные действия всех составных частей, осуществляемые благодаря цитокинам, гармоничны и целесообразны. Цитокины являются важным элементом при взаимодействии разных лимфоцитов между собой и с фагоцитами (рис. 4). B частности, именно посредством цитокинов Т-хелперы помогают координировать работу разнообразных клеток, задействованных в иммунной реакции.
B реальности разделить полностью клеточный и гуморальный иммунитет невозможно, да, наверно, и не очень нужно. Это делается, скорее всего, по традиции и для удобства исследователей. Дело в том, что, как уже говорилось, в образовании антител участвуют клетки, а определенные этапы клеточного иммунитета не могут реализоваться без участия антител. Но не будем спорить с традициями, в них тоже есть свой смысл.
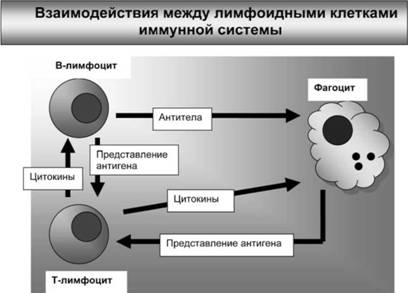 Рис. 4. В В-лимфоцитах синтезируются антитела, взаимодействующие с болезнетворными микроорганизмами и продуктами их жизнедеятельности. Этим В-лимфоциты помогают фагоцитам распознавать чужеродный антиген. Цитокины, выделяемые преимущественно Т-лимфоцитами-хелперами, активируют фагоциты для разрушения поглощенных ими микробов (обозначены маленькими кружочками внутри фагоцита), а также стимулируют В-лимфоциты. В-лимфоциты и фагоциты обладают способностью представлять антиген Т-лимфоцитам в форме, подходящей для распознавания, вызывая этим их активацию
Рис. 4. В В-лимфоцитах синтезируются антитела, взаимодействующие с болезнетворными микроорганизмами и продуктами их жизнедеятельности. Этим В-лимфоциты помогают фагоцитам распознавать чужеродный антиген. Цитокины, выделяемые преимущественно Т-лимфоцитами-хелперами, активируют фагоциты для разрушения поглощенных ими микробов (обозначены маленькими кружочками внутри фагоцита), а также стимулируют В-лимфоциты. В-лимфоциты и фагоциты обладают способностью представлять антиген Т-лимфоцитам в форме, подходящей для распознавания, вызывая этим их активацию
Как врожденный, так и приобретенный в течение жизни иммунитет зависит от согласованной деятельности нескольких механизмов. На ранних стадиях инфекции преобладают механизмы врожденного иммунитета, а на более поздних – приобретенного. Лишь наличие трех клеточных типов (Т– и В-клеток и макрофагов) в кооперации позволяет сформировать полноценный иммунный ответ. Какая-либо одна или две из указанных популяций клеток не способны в отдельности обеспечить защиту от внешних врагов. Это ключевые игроки иммунной системы, хотя и не единственные. Кроме них имеется множество других клеток, которые обобщенно называют вспомогательными, или А-клетками. Чтобы не затруднять повествование, мы не будем здесь описывать все разнообразие клеток иммунной системы (для
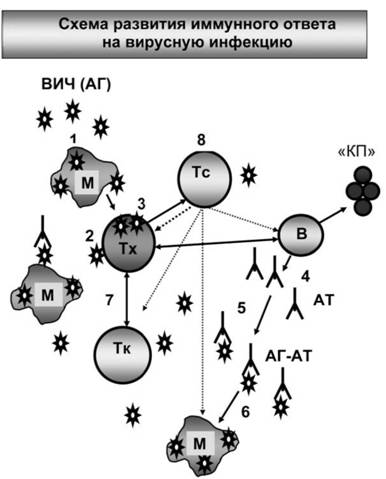 Рис. 5. Последовательность событий при иммунном ответе следующая: 1 – Bирус, являющийся антигеном (АГ), попадает в организм человека; 2 – B слизистой оболочке макрофаги (М) поглощают часть антигенов и «представляют» их Т-хелперам (Тх); 3 – Т-хелперы дают стимулирующий сигнал B-лимфоцитам (B), активируют Т-киллеры (Тк) и Т-супрессоры (Тс); 4 – B-лимфоциты образуют антитела (АТ) и «клетки памяти» («КП»); 5 – Антитела взаимодействуют со свободными антигенами и обезвреживают их; 6 – Макрофаги захватывают, переваривают и уничтожают комплекс «антиген-антитело» (АГ-АТ); 7 – Т-киллеры разрушают клетки, инфицированные вирусом; 8 – Т-супрессоры подавляют активность иммунного ответа; 9 – Зараженные клетки синтезируют интерфероны, которые защищают от заражения соседние неинфицированные клетки
Рис. 5. Последовательность событий при иммунном ответе следующая: 1 – Bирус, являющийся антигеном (АГ), попадает в организм человека; 2 – B слизистой оболочке макрофаги (М) поглощают часть антигенов и «представляют» их Т-хелперам (Тх); 3 – Т-хелперы дают стимулирующий сигнал B-лимфоцитам (B), активируют Т-киллеры (Тк) и Т-супрессоры (Тс); 4 – B-лимфоциты образуют антитела (АТ) и «клетки памяти» («КП»); 5 – Антитела взаимодействуют со свободными антигенами и обезвреживают их; 6 – Макрофаги захватывают, переваривают и уничтожают комплекс «антиген-антитело» (АГ-АТ); 7 – Т-киллеры разрушают клетки, инфицированные вирусом; 8 – Т-супрессоры подавляют активность иммунного ответа; 9 – Зараженные клетки синтезируют интерфероны, которые защищают от заражения соседние неинфицированные клетки
этого существуют специальные толстые книги). Однако не упомянуть об их существовании было бы неправильным, иначе у читателя может сложиться слишком упрощенное представление об устройстве и функционировании иммунной системы, которые в реальности чрезвычайно сложны, а некоторые из них до сих пор до конца не поняты.
Чужеродный возбудитель, попадая в организм, начинает размножаться, но то же самое делают и наши защитные клетки. Далее происходит «сражение» между внешними врагами и внутренними защитниками. Исход болезни зависит от того, кто окажется в конечном итоге сильнее и проворнее. Однако даже самая надежная система защиты может давать сбои и расстраиваться. А расстройства иммунной системы приводят к таким патологиям, как аллергия, аутоиммунные болезни и иммунодефициты.
Рассмотрим работу иммунной системы на примере заражения вирусом (рис. 5). Как правило, вирусы проникают во внут-ренную среду организма через слизистые оболочки или посредством прямого входа через кровоток. Обычно при появлении в крови или в межклеточных пространствах какого-нибудь вируса иммунная система сразу начинает производить специфические антитела, вступающие в борьбу с ним. Эти антитела препятствуют связыванию вируса с клетками и проникновению в них. Однако особенность вируса как паразита состоит в том, что он предпочитает внутриклеточный паразитизм, т. е. жизнь и размножение исключительно внутри клеток хозяина и за их счет. Если антитела не справились с вирусом, пока еще он был вне каких-либо клеток, т. е. был уязвим для них (например, «плавал» в крови), то в таких условиях остается только два пути борьбы против вируса-паразита: или атаковать и убивать зараженные вирусами клетки вместе с вирусами, или каким-то образом воспрепятствовать внутриклеточному размножению вирусов, если не удалось помешать внедрению вирусов на входе в организм. Антитела участвуют в разрушении инфицированных вирусом клеток, активируя определенный тип белков крови. Уничтожением зараженных вирусом клеток занимаются макрофаги и Т-киллеры. Макрофаги «пожирают» вирус. Т-киллеры, распознав на поверхности зараженной клетки вирусные антигены, впрыскивают в такую клетку-мишень содержимое своих цито-плазматических гранул (куда входят некоторые цитокины и другие молекулы, повреждающие клетку-мишень). Результатом атаки Т-киллера, как правило, является гибель клетки-мишени вместе с внутриклеточными паразитами. Правда, гибель и разрушение собственных клеток организма небезразлично для его жизнедеятельности. При некоторых вирусных инфекциях такого рода защитные реакции приносят иногда больше вреда, чем пользы.
Очень важен для защиты от вирусов еще один механизм – молекулярный. Ответственны за эту защиту молекулы цитоки-нов под названием «интерфероны». Название «интерферон» происходит от глагола «интерферировать», т. е. вступать во взаимодейтсвие, в борьбу. Одни из них синтезируются зараженными вирусами клетками, другие – Т-клетками в ответ на вирусную инфекцию. Bсе вместе они способны «интерферировать», т. е. придавать противовирусную устойчивость другим незара-женным клеткам и в результате препятствовать распространению вируса в организме. Это свойство интерферонов позволяет использовать их препараты для лечения при разных вирусных инфекциях. Молекулы интерферонов кроме антивирусного действия оказывают влияние на функции защитных клеток, увеличивая их число и активность. Клеточные и молекулярные механизмы при защите от вирусов и бактерий работают согласованно, приходя на помощь друг другу.
Итак, если говорить общими словами, иммунный ответ – результат совместного строго скоординированного действия множества различных клеток, входящих в иммунную систему (макрофагов, всевозможных Т– и B-клеток), и разнообразных молекулярных процессов, происходящих при попадании в организм чужеродного агента – антигена.
Таким образом, иммунная система представляет собой одну из важнейших систем человеческого организма. Основная функция иммунной системы заключается в способности опознавать любые патогенные микробы, проникшие в наш организм, и уничтожать их различными способами. Еще одно важное свойство иммунной системы – запоминание чужеродного антигена, с которым она уже сталкивалась, и при повторной встрече быстро и мощно на него воздействовать. Иммунологическая память хранится в специальных «клетках памяти» и закрепляется порой на многие годы, а иногда и на всю жизнь. Такая память и названа иммунитетом. B действительности функции иммунной системы не ограничиваются только обеспечением защиты организма от патогенных микроорганизмов, они значительно шире. Однако на этом вопросе мы не будем здесь подробно останавливаться.
Как и любая другая система организма, иммунная система подвержена нарушениям, что конечно же в конечном итоге сильно сказывается на всем организме. Это имеет различное проявление. Так, в норме иммунная система никак не реагирует на клетки и ткани собственного организма, узнавая, что они «свои». Если вдруг по каким-то причинам она теряет ориентацию, это приводит к так называемым аутоиммунным заболеваниям, примером которых является ревматоидный артрит и гемолитическая анемия. Еще одно нарушение иммунной системы – гиперчувствительность. При некоторых нарушениях иммунная система неадекватно сильно реагирует на чужеродный патоген, а порой и на совсем безвредные агенты, например питательные вещества. О главной же патологии иммунной системы – иммундефиците – речь пойдет далее. Все паталогии в системе иммунитета крайне тяжело сказываются на всем организме. Однако мнение о том, что все болезни – от неполадок с иммунитетом, верно настолько же, насколько верны утверждения типа «все болезни от нервов» или «все от неправильного питания».
Для коррекции нарушений иммунной системы сегодня уже имеется множество специальных медицинских препаратов – иммуномодуляторов и иммуностимуляторов. К лекарствам, повышающим иммунитет, относятся иммуноглобулины (нормальный человеческий иммуноглобулин, комплексный иммунный препарат (КИП), сандоглобулин и т. д.), интерфероны (реафе-рон, виферон и т. д.), препараты вилочковой железы (Т-активин, тимоген), препараты, содержащие компоненты клеточной стенки бактерий (ликопид, рибомунил). Иммуностимулирующей активностью обладают также витамины, дрожжевые препараты, элеутерококк, жень-шень и многое другое.
Чего только не пишут и не говорят о том, как можно искусственно усилить свою собственную иммунную систему, оказать помощь лимфоцитам. Широкое распространение в последние годы получили всевозможные пищевые добавки. Чуть ли не каждая вторая из них, согласно аннотациям производителей, наряду с другими полезными свойствами способна стимулировать иммунную систему. По данным японских исследователей, выраженным иммуностимулирующим действием обладает один из компонентов зеленого чая – эпигаллокахетин, благодаря которому употребление зеленого чая защищает клетки от поражения ВИЧ. На упаковках кефира бифиди компания «Вимм-Билль-Данн» утверждает, что бифидокультура, содержащаяся в их продукте, также укрепляет иммунитет. Телевизионная реклама утверждает, что продающийся в магазинах «J7 Immunol» спасет нас от всех бед. Хотелось бы в это верить, хотя верится с трудом. При этом забывается, что практически любое лекарство, даже препараты бифидобактерий, принимаемые длительное время, может вызвать не усиление, а, наооборот, ослабление защитных механизмов организма. B популярном издании «Мое здоровье» (№ 16, 2003) можно прочесть о простейшей методике, которая якобы позволяет поднять иммунитет: нужно в течение месяца каждый день прикладывать на 20 мин к голове в области гипоталамуса небольшой кусочек льда. (Гипоталамус заведует в нашем организме иммунными процессами. Он расположен на затылке. Чтобы найти нужное место, нужно подниматься от первого шейного позвонка к макушке. Область гипоталамуса будет в углублении после первой большой выпуклости.)
Но никакие хитроумные приемы, никакое заклинание, ни даже имеющиеся в арсенале медиков дорогостоящие медицинские препараты все равно пока не спасают BИЧ-инфицирован-ного человека от СПИДа. B результате этой страшной инфекции иммунная система организма в конечном итоге катастрофически разрушается, что делает человека полностью беззащитным перед многочисленными микроорганизмами, и он неизбежно погибает. Что же это за напасть такая, чем она вызывается? Об этом и поговорим далее.
ВИЧ – CAUSA CAUSARUM
В первые годы после постановки диагноза СПИД выдвигалось немало теорий относительно причины (по-научному – этиологии) этого заболевания, многие из них теперь по прошествии двух с лишним десятилетий представляются весьма эксцентричными. Так, первоначально было выдвинуто предположение о ведущей роли в развитии СПИДа хорошо известного к тому времени цитомегаловируса: в группах больных с развившимся иммунодефицитом отмечалась необыкновенно высокая частота цитомегаловирусной инфекции, причем цитомегалови-рус сам по себе способен подавлять иммунитет. Некоторые ученые предположили, что этот вирус по неясным причинам претерпел какие-то изменения, стал более вирулентным (инфекционным), а в результате более опасным и вредным.
Одно время в качестве этиологического фактора рассматривался амилнитрит – лекарство, отпускаемое по рецептам, и близкое ему по составу вещество – нитрит изобутила, которое продавалось на рынке как освежитель комнатного воздуха. Оба вещества использовались также для полового возбуждения. Помимо этого они обладают иммуносупрессорными свойствами. Данная теория была наукообразной и указывала на простой путь разрешения проблемы. Однако вскоре были описаны случаи заболевания у людей, никогда не пользовавшихся этими веществами.
Между тем с самого начала обнаружения СПИДа различные косвенные факты давали ученым и врачам достаточно весомые основания для предположения об инфекционной природе этого заболевания. На это указывали особенности состава больных, наличие контактов между ними и взаимосвязь между контактами и болезнью. Поскольку еще в 70-е гг. был выделен и охарактеризован вирус лейкоза кошек, вызывающий у животных генерализованный иммунодефицит («синдром увядающих кошек»), для исследователей в этой области не составляло особого интеллектуального труда представить, что ретровирус человека мог вызвать похожий синдром. У человека патогенный организм должен был поражать специфические Т-лимфоциты, содержащиеся в крови человека и отвечающие за клеточный иммунитет. И это предположение в дальнейшем полностью оправдалось. Правда, реальную причину заболевания удалось установить лишь через два года (в 1983 г.) после постановки первого диагноза СПИД. Этой причиной действительно оказался вирус, но такой, о котором ранее ничего не было известно. Окончательное его имя – вирус иммунодефицита человека (BB4). Но появилось это имя не сразу. Для начала поговорим о том, что же собой представляют вирусы вообще.
Борьба с внутриклеточными паразитами, которыми являются вирусы, – главная забота второй линии обороны – клеточного иммунитета. Клеточным этот иммунитет именуют потому, что в нем участвуют специальные клетки, которые и являются эффективным оружием для поражения чужеродных клеток при непосредственном контакте с ними. Для этой цели служат уже упоминавшиеся фагоциты, которые циркулируют в крови и бросаются на незваных пришельцев-чужаков, помеченных антителами, поглощая и разрушая проникшие в организм микробы, ядовитые вещества и другие чужеродные для организма клетки и ткани. При этом, победив врага, фагоциты тоже погибают. Они как бы жертвуют собой для блага целого организма.
Но главную основу клеточного иммунитета составляют лимфоциты, которые для своего созревания переселяются из костного мозга в другой центральный орган лимфоидной системы – тимус (вилочковая железа). Эта ветвь лимфоцитов получила название «тимус-зависимые», или «Т-лимфоциты» (от первой буквы английского слова thymus).
В организме человека Т-лимфоциты многократно покидают лимфоидные органы, попадая сначала в лимфу, затем в кровь, а из крови снова возвращаясь в органы. Т-лимфоциты – «вечные странники», они постоянно в движении. За свою жизнь лимфоцит может проходить поразительно большие расстояния – от 100 и более километров. Благодаря интенсивной циркуляции лимфоциты, когда в них возникает потребность, удивительно быстро появляются в «горячих точках». Без такой способности лимфоцитов были бы невозможны своевременное их развитие, взаимодействие и эффективное участие в иммунном ответе при вторжении в организм чужеродных агентов.
В тимусе формируются разные виды Т-клеток, поэтому тимус иногда называют школой обучения Т-клеток. «Ученики» после окончания этой школы сильно отличаются друг от друга. Одни из них участвуют в регуляции развития B-клеток и образования антител, другие взаимодействуют с фагоцитами, помогая им разрушать поглощенные микробные клетки. Некоторые Т-лим-фоциты сами обладают способностью разрушать чужеродные клетки, умерщвлять их. По этой причине их назвали цитотокси-ческими, или «киллерами». B отличие от антител Т-киллер ничего не может сделать с растворимым антигеном – ни обезвредить его, ни удалить из организма. Но он очень активно и целенаправленно убивает клетки, содержащие чужеродный антиген. Т-киллер проходит мимо растворимого антигена, но не пропускает антиген, находящийся на поверхности «чужой» клетки.
Другая разновидность лимфоцитов – Т-хелперы (от английского слова helper – помощник). Названы они так по той причине, что первыми распознают чужеродные вещества и помогают другим лимфоцитам выполнять их прямую функцию. Т-хелперы сами по себе не способны ни вырабатывать антитела, ни убивать клетки-мишени. Но, распознавая чужеродный антиген, они реагируют на него выработкой различных факторов, которые крайне необходимы для размножения и созревания B-клеток и Т-киллеров. Наконец, существуют еще специальные клетки Т-су-прессоры, которые, в отличие от двух других видов, заняты прямо противоположным действием – подавляют активность иммунного ответа, когда необходимость в нем отпадает. Это служит надежной защитой самой иммунной системы от переистощения.
Следует отметить, что центральная роль в клеточном иммунитете принадлежит Т-хелперам. Они помогают координировать работу всех клеток, задействованных в иммунной реакции. Именно Т-хелперы являются ключевым звеном в распознавании антигенов, влияют на деятельность других типов Т-клеток, оказывают помощь B-клеткам в образовании антител. По их командам к «чужакам», нарушившим спокойствие, иммунная система сначала направляет специальный отряд Т-лимфоцитов-килле-ров, основная задача которых с помощью непосредственного контакта убивать зараженные клетки. Для того чтобы «киллеры» нашли и уничтожили противника, им надо отличить нормальные клетки от пораженных. Как и в случае антител, опознание происходит за счет антигена, если он высовывается из клетки, расположен на ее поверхности.
Подобно B-лимфоцитам, каждая Т-клетка имеет специфический рецептор, который распознает этот антиген. С помощью рецепторов Т-лимфоциты-киллеры вступают в теснейший контакт со своей мишенью. Прикрепившись, они выделяют в просвет между собой и мишенью особый белок, «продырявливающий» мембрану клетки-мишени, в результате чего клетка гибнет. Затем они открепляются от мишени и переходят на другую клетку, и так несколько раз. Это явление иммунологи называют «поцелуем смерти».
Важную роль в защитной реакции организма играют и Т-супрессоры. Они вступают в действие, когда основная «работа» закончена. Главная задача Т-супрессоров – подавлять активность иммунного ответа, когда необходимость в нем исчезает. Их роль чрезвычайно важна: если иммунный ответ не будет прекращен после обезвреживания чужеродного агента, иммунные клетки будут продолжать работать, а в результате – поражать собственные здоровые клетки организма, что приведет к развитию различных болезней (их называют аутоиммунными). Так работает еще один компонент иммунной системы – очень сложный, но весьма мощный и важный для выживания организма.
Для того чтобы различать все существующие разнообразные популяции лимфоидных клеток между собой, ученые использовали тот факт, что на поверхности каждой из них присутствуют определенные специфические белки, которые могут служить своеобразными «метками». Такие белки-метки получили сокращенное название CD (по-русски – групповой маркер). На сегодняшний день известно около 200 подобных маркеров. Например, маркером для Т-клеток-хелперов служит белок, названный CD4. Этот факт следует запомнить, поскольку мы неоднократно будем возвращаться к нему.
Т-лимфоциты способны выполнять свои функции только при определенных условиях и поддержке других клеток. К таковым в первую очередь относятся В-лимфоциты и различные фагоцитирующие клетки, в первую очередь один из видов фагоцитов – макрофаги – большие по размерам клетки, поглощающие и переваривающие микробы и другие погибшие клетки. Существенную роль в работе иммунной системы играют так называемые дендритные (ветвистые) клетки, часть которых находится непосредственно под кожей и слизистой оболочкой человека. Такие клетки обычно затаиваются, как бы поджидая микробы и вирусы типа ВИЧ, проникающие через слизистую, захватывают их, а затем переносят в лимфоузлы, где «представляют» непрошеных гостей В– и Т-лимфоцитам, которые их и атакуют. Когда говорят, что клетка «представляет антиген» (такие клетки еще называют антигенпредставляющими), то имеется в виду почти то же самое, что происходит в компании людей, когда хозяин знакомит уже собравшихся гостей с новым незнакомым им посетителем (т. е. представляет его присутствующим).
Bсе клетки иммунной системы имеют определенные функции и работают в четко согласованном взаимодействии, которое обеспечивается специальными биологически активными веществами – цитокинами – регуляторами иммунных реакций. Ци-токинами обобщенно назвали специфические белки, с помощью которых многочисленные и разнообразные клетки иммунной системы могут «переговариваться», обмениваться друг с другом информацией и в результате этого осуществлять строгую координацию своих действий. Набор и количества цитокинов, действующих на рецепторы клеточной поверхности, – «цитокиновая среда» – представляют собой матрицу взаимодействующих и часто меняющихся сигналов. Эти сигналы носят сложный характер из-за большого разнообразия цитокиновых рецепторов и из-за того, что каждый из цитокинов может активировать или подавлять несколько процессов, включая свой собственный синтез и синтез других цитокинов, а также образование и появление на поверхности клеток цитокиновых рецепторов. Для различных тканей характерна своя здоровая «цитокиновая среда», возможны вариации для одной и той же ткани на разные моменты времени. К настоящему времени обнаружено уже более сотни разнообразных цитокинов, и не факт, что на этом дело ограничится.
Иммунную систему часто сравнивают с «системой коллективной безопасности», механизм которой чрезвычайно сложен, но согласованные действия всех составных частей, осуществляемые благодаря цитокинам, гармоничны и целесообразны. Цитокины являются важным элементом при взаимодействии разных лимфоцитов между собой и с фагоцитами (рис. 4). B частности, именно посредством цитокинов Т-хелперы помогают координировать работу разнообразных клеток, задействованных в иммунной реакции.
B реальности разделить полностью клеточный и гуморальный иммунитет невозможно, да, наверно, и не очень нужно. Это делается, скорее всего, по традиции и для удобства исследователей. Дело в том, что, как уже говорилось, в образовании антител участвуют клетки, а определенные этапы клеточного иммунитета не могут реализоваться без участия антител. Но не будем спорить с традициями, в них тоже есть свой смысл.

Как врожденный, так и приобретенный в течение жизни иммунитет зависит от согласованной деятельности нескольких механизмов. На ранних стадиях инфекции преобладают механизмы врожденного иммунитета, а на более поздних – приобретенного. Лишь наличие трех клеточных типов (Т– и В-клеток и макрофагов) в кооперации позволяет сформировать полноценный иммунный ответ. Какая-либо одна или две из указанных популяций клеток не способны в отдельности обеспечить защиту от внешних врагов. Это ключевые игроки иммунной системы, хотя и не единственные. Кроме них имеется множество других клеток, которые обобщенно называют вспомогательными, или А-клетками. Чтобы не затруднять повествование, мы не будем здесь описывать все разнообразие клеток иммунной системы (для

этого существуют специальные толстые книги). Однако не упомянуть об их существовании было бы неправильным, иначе у читателя может сложиться слишком упрощенное представление об устройстве и функционировании иммунной системы, которые в реальности чрезвычайно сложны, а некоторые из них до сих пор до конца не поняты.
Чужеродный возбудитель, попадая в организм, начинает размножаться, но то же самое делают и наши защитные клетки. Далее происходит «сражение» между внешними врагами и внутренними защитниками. Исход болезни зависит от того, кто окажется в конечном итоге сильнее и проворнее. Однако даже самая надежная система защиты может давать сбои и расстраиваться. А расстройства иммунной системы приводят к таким патологиям, как аллергия, аутоиммунные болезни и иммунодефициты.
Рассмотрим работу иммунной системы на примере заражения вирусом (рис. 5). Как правило, вирусы проникают во внут-ренную среду организма через слизистые оболочки или посредством прямого входа через кровоток. Обычно при появлении в крови или в межклеточных пространствах какого-нибудь вируса иммунная система сразу начинает производить специфические антитела, вступающие в борьбу с ним. Эти антитела препятствуют связыванию вируса с клетками и проникновению в них. Однако особенность вируса как паразита состоит в том, что он предпочитает внутриклеточный паразитизм, т. е. жизнь и размножение исключительно внутри клеток хозяина и за их счет. Если антитела не справились с вирусом, пока еще он был вне каких-либо клеток, т. е. был уязвим для них (например, «плавал» в крови), то в таких условиях остается только два пути борьбы против вируса-паразита: или атаковать и убивать зараженные вирусами клетки вместе с вирусами, или каким-то образом воспрепятствовать внутриклеточному размножению вирусов, если не удалось помешать внедрению вирусов на входе в организм. Антитела участвуют в разрушении инфицированных вирусом клеток, активируя определенный тип белков крови. Уничтожением зараженных вирусом клеток занимаются макрофаги и Т-киллеры. Макрофаги «пожирают» вирус. Т-киллеры, распознав на поверхности зараженной клетки вирусные антигены, впрыскивают в такую клетку-мишень содержимое своих цито-плазматических гранул (куда входят некоторые цитокины и другие молекулы, повреждающие клетку-мишень). Результатом атаки Т-киллера, как правило, является гибель клетки-мишени вместе с внутриклеточными паразитами. Правда, гибель и разрушение собственных клеток организма небезразлично для его жизнедеятельности. При некоторых вирусных инфекциях такого рода защитные реакции приносят иногда больше вреда, чем пользы.
Очень важен для защиты от вирусов еще один механизм – молекулярный. Ответственны за эту защиту молекулы цитоки-нов под названием «интерфероны». Название «интерферон» происходит от глагола «интерферировать», т. е. вступать во взаимодейтсвие, в борьбу. Одни из них синтезируются зараженными вирусами клетками, другие – Т-клетками в ответ на вирусную инфекцию. Bсе вместе они способны «интерферировать», т. е. придавать противовирусную устойчивость другим незара-женным клеткам и в результате препятствовать распространению вируса в организме. Это свойство интерферонов позволяет использовать их препараты для лечения при разных вирусных инфекциях. Молекулы интерферонов кроме антивирусного действия оказывают влияние на функции защитных клеток, увеличивая их число и активность. Клеточные и молекулярные механизмы при защите от вирусов и бактерий работают согласованно, приходя на помощь друг другу.
Итак, если говорить общими словами, иммунный ответ – результат совместного строго скоординированного действия множества различных клеток, входящих в иммунную систему (макрофагов, всевозможных Т– и B-клеток), и разнообразных молекулярных процессов, происходящих при попадании в организм чужеродного агента – антигена.
Таким образом, иммунная система представляет собой одну из важнейших систем человеческого организма. Основная функция иммунной системы заключается в способности опознавать любые патогенные микробы, проникшие в наш организм, и уничтожать их различными способами. Еще одно важное свойство иммунной системы – запоминание чужеродного антигена, с которым она уже сталкивалась, и при повторной встрече быстро и мощно на него воздействовать. Иммунологическая память хранится в специальных «клетках памяти» и закрепляется порой на многие годы, а иногда и на всю жизнь. Такая память и названа иммунитетом. B действительности функции иммунной системы не ограничиваются только обеспечением защиты организма от патогенных микроорганизмов, они значительно шире. Однако на этом вопросе мы не будем здесь подробно останавливаться.
Как и любая другая система организма, иммунная система подвержена нарушениям, что конечно же в конечном итоге сильно сказывается на всем организме. Это имеет различное проявление. Так, в норме иммунная система никак не реагирует на клетки и ткани собственного организма, узнавая, что они «свои». Если вдруг по каким-то причинам она теряет ориентацию, это приводит к так называемым аутоиммунным заболеваниям, примером которых является ревматоидный артрит и гемолитическая анемия. Еще одно нарушение иммунной системы – гиперчувствительность. При некоторых нарушениях иммунная система неадекватно сильно реагирует на чужеродный патоген, а порой и на совсем безвредные агенты, например питательные вещества. О главной же патологии иммунной системы – иммундефиците – речь пойдет далее. Все паталогии в системе иммунитета крайне тяжело сказываются на всем организме. Однако мнение о том, что все болезни – от неполадок с иммунитетом, верно настолько же, насколько верны утверждения типа «все болезни от нервов» или «все от неправильного питания».
Для коррекции нарушений иммунной системы сегодня уже имеется множество специальных медицинских препаратов – иммуномодуляторов и иммуностимуляторов. К лекарствам, повышающим иммунитет, относятся иммуноглобулины (нормальный человеческий иммуноглобулин, комплексный иммунный препарат (КИП), сандоглобулин и т. д.), интерфероны (реафе-рон, виферон и т. д.), препараты вилочковой железы (Т-активин, тимоген), препараты, содержащие компоненты клеточной стенки бактерий (ликопид, рибомунил). Иммуностимулирующей активностью обладают также витамины, дрожжевые препараты, элеутерококк, жень-шень и многое другое.
Чего только не пишут и не говорят о том, как можно искусственно усилить свою собственную иммунную систему, оказать помощь лимфоцитам. Широкое распространение в последние годы получили всевозможные пищевые добавки. Чуть ли не каждая вторая из них, согласно аннотациям производителей, наряду с другими полезными свойствами способна стимулировать иммунную систему. По данным японских исследователей, выраженным иммуностимулирующим действием обладает один из компонентов зеленого чая – эпигаллокахетин, благодаря которому употребление зеленого чая защищает клетки от поражения ВИЧ. На упаковках кефира бифиди компания «Вимм-Билль-Данн» утверждает, что бифидокультура, содержащаяся в их продукте, также укрепляет иммунитет. Телевизионная реклама утверждает, что продающийся в магазинах «J7 Immunol» спасет нас от всех бед. Хотелось бы в это верить, хотя верится с трудом. При этом забывается, что практически любое лекарство, даже препараты бифидобактерий, принимаемые длительное время, может вызвать не усиление, а, наооборот, ослабление защитных механизмов организма. B популярном издании «Мое здоровье» (№ 16, 2003) можно прочесть о простейшей методике, которая якобы позволяет поднять иммунитет: нужно в течение месяца каждый день прикладывать на 20 мин к голове в области гипоталамуса небольшой кусочек льда. (Гипоталамус заведует в нашем организме иммунными процессами. Он расположен на затылке. Чтобы найти нужное место, нужно подниматься от первого шейного позвонка к макушке. Область гипоталамуса будет в углублении после первой большой выпуклости.)
Но никакие хитроумные приемы, никакое заклинание, ни даже имеющиеся в арсенале медиков дорогостоящие медицинские препараты все равно пока не спасают BИЧ-инфицирован-ного человека от СПИДа. B результате этой страшной инфекции иммунная система организма в конечном итоге катастрофически разрушается, что делает человека полностью беззащитным перед многочисленными микроорганизмами, и он неизбежно погибает. Что же это за напасть такая, чем она вызывается? Об этом и поговорим далее.
ВИЧ – CAUSA CAUSARUM
(причина причин)
Omnia теа тесит porto
(Все свое ношу с собой)
Nomen est omen
(Имя есть значение)
В первые годы после постановки диагноза СПИД выдвигалось немало теорий относительно причины (по-научному – этиологии) этого заболевания, многие из них теперь по прошествии двух с лишним десятилетий представляются весьма эксцентричными. Так, первоначально было выдвинуто предположение о ведущей роли в развитии СПИДа хорошо известного к тому времени цитомегаловируса: в группах больных с развившимся иммунодефицитом отмечалась необыкновенно высокая частота цитомегаловирусной инфекции, причем цитомегалови-рус сам по себе способен подавлять иммунитет. Некоторые ученые предположили, что этот вирус по неясным причинам претерпел какие-то изменения, стал более вирулентным (инфекционным), а в результате более опасным и вредным.
Одно время в качестве этиологического фактора рассматривался амилнитрит – лекарство, отпускаемое по рецептам, и близкое ему по составу вещество – нитрит изобутила, которое продавалось на рынке как освежитель комнатного воздуха. Оба вещества использовались также для полового возбуждения. Помимо этого они обладают иммуносупрессорными свойствами. Данная теория была наукообразной и указывала на простой путь разрешения проблемы. Однако вскоре были описаны случаи заболевания у людей, никогда не пользовавшихся этими веществами.
Между тем с самого начала обнаружения СПИДа различные косвенные факты давали ученым и врачам достаточно весомые основания для предположения об инфекционной природе этого заболевания. На это указывали особенности состава больных, наличие контактов между ними и взаимосвязь между контактами и болезнью. Поскольку еще в 70-е гг. был выделен и охарактеризован вирус лейкоза кошек, вызывающий у животных генерализованный иммунодефицит («синдром увядающих кошек»), для исследователей в этой области не составляло особого интеллектуального труда представить, что ретровирус человека мог вызвать похожий синдром. У человека патогенный организм должен был поражать специфические Т-лимфоциты, содержащиеся в крови человека и отвечающие за клеточный иммунитет. И это предположение в дальнейшем полностью оправдалось. Правда, реальную причину заболевания удалось установить лишь через два года (в 1983 г.) после постановки первого диагноза СПИД. Этой причиной действительно оказался вирус, но такой, о котором ранее ничего не было известно. Окончательное его имя – вирус иммунодефицита человека (BB4). Но появилось это имя не сразу. Для начала поговорим о том, что же собой представляют вирусы вообще.
Немного истории
О существовании вирусов и их вредоносности человечество узнало чуть более 110 лет назад. 12 февраля 1892 г. на заседании Российской Академии наук Д. И. Ивановский сообщил о своем открытии: возбудителем хорошо известной мозаичной болезни табака является некий организм, способный проходить через фильтры, которые задерживают бактерии. Эту дату можно считать днем рождения вирусологии, а Д. И. Ивановского – ее основоположником. Правда, в западной литературе в качестве первооткрывателей вирусов часто называют Леффлера и Фроша, которые в 1898 г. показали, что широко распространенная болезнь крупного рогатого скота – ящур – передается от одного животного другому неким агентом, проходящим через фильтры, которые задерживают даже самые мелкие бактерии. Сам термин «вирус» применительно к инфекционному началу мозаичной болезни растений был предложен М. Бейеринком только в 1899 г., т. е. спустя семь лет после исторического сообщения Д. И. Ивановского. Постепенно выяснилось, что вирусы вызывают заболевания не только растений, но и бактерий, насекомых, водорослей, грибов, животных и даже человека.
Все знают, что вирусы очень малы и могут вызывать заболевания. Менее известно, как разнообразен мир этих мельчайших существ-иждивенцев, неспособных к самостоятельной жизни вне заражаемых ими клеток. Впервые наблюдать вирусы и выяснить их структуру удалось только после изобретения электронного микроскопа. По своим габаритам вирусы занимают место между самыми мелкими бактериальными клетками и самыми крупными органическими молекулами. Их размер варьирует от 0,02 до 0,3 мкм. Для сравнения размеры большинства клеток человека колеблются в пределах – от 3 до 30 мкм.
Хотя разнообразие вирусов весьма велико, по образному выражению академика В. М. Жданова, коллекция, собранная из всех известных типов вирусов, «поместилась бы в коробочке размером с маковое зернышко». Нет сомнения, что в природе уже существуют и могут появиться в дальнейшем еще много совершенно не известных нам сегодня вирусов. Как подметил еще Сенека, multum egerunt, quiante nos fuerunt, sed non peregerunt (жившие до нас много совершили, но ничего не завершили).
