Страница:
Долгие годы продолжался спор: вирусы – это живые существа или часть неживой природы? Невозможность существования и размножения вирусов вне клетки, их способность к самосборке и кристаллизации говорили скорее о том, что вирус ведет себя как «неживая» материя. После установления природы гена и обнаружения в вирусах генетического материала, присущего живым организмам, вирусы стали относить к живой природе. Энциклопедические словари стыдливо признают – современная наука пока не смогла понять природы этих странных созданий, мало знает о путях их эволюции. Ученые даже не смогли прийти к единому мнению: вирус – это существо или вещество? Безжалостные убийцы настолько чужды всему земному, что изучающие их специалисты иногда в отчаянии предполагают, что они попали к нам из дальнего Космоса. До сих пор сохраняет актуальность определение, данное А. Львовым: «вирусы – это вирусы».
Сегодня в оценках превалирует «дуализм». Согласно современным представлениям, вирусы лежат на границе «живого» и «неживого», это внеклеточные формы жизни, способные проникать в определенные живые клетки и размножаться только внутри них.
Генетический аппарат вирусов представлен различными формами нуклеиновых кислот, такого разнообразия нет ни у одной из других форм жизни. У всех живых организмов, кроме вирусов, генетический аппарат состоит из двунитевой молекулы дезоксири-бонуклеиновой кислоты (ДНК), а рибонуклеиновая кислота (РНК), выполняющая в нормальных клетках роль переносчика информации, всегда однонитевая. У вирусов же природа будто бы опробовала все возможные варианты устройства генетического аппарата: одно– и двунитевая РНК, одно– и двунитевая ДНК. При этом и вирусная РНК, и вирусная ДНК могут быть либо линейными, либо замкнутыми в кольцо.
Постепенно пришли к пониманию, что вирусы могут быть основной причиной многих хронических заболеваний у человека. К началу XXI в. было открыто и исследовано свыше тысячи разнообразных вирусов, вызывающих такие заболевания, как грипп, герпес, гепатит, оспа, полиомиелит, цитомегаловирусная инфекция, энцефалит, корь и др. Сколько же существует вирусов всего – не знает никто. Ведь невесть откуда постоянно появляются все новые их разновидности, порой угрожающие нам смертельной опасностью. В целом около 80 % инфекционных заболеваний, регистрируемых в настоящее время, вызывают вирусы. Первые места по массовости поражения занимают острые респираторные заболевания, грипп, вирусный гепатит, теперь к ним прибавился и СПИД.
Широко распространены вирусные заболевания и у животных. Хорошо известны эпидемии вирусов у птиц, овец, коров. В результате эпидемии вируса висны в 30—40-е гг. прошлого века исландцы были вынуждены забить более 150 тыс. животных. Вирус лейкоза птиц причинил убыток птицеводству США в 1955 г. в размере свыше 60 млн долларов. Известна широкая пораженность крупного рогатого скота вирусом лейкоза. В некоторых странах мира им заражено свыше 80 % коров и быков.
Чтобы читатель далее более четко понимал, как устроены вирусы, каковы молекулярные механизмы их взаимодействия с клеткой, необходимо сделать небольшое напоминание о том, как хранится и используется генетическая программа в обычной нормальной клетке высших организмов. Основу генетического аппарата (генома) подавляющего большинства организмов составляет высокополимерная молекула ДНК, состоящая из двух полимерных цепей, закрученных в правильную двойную спираль. B ней закодирована вся наследственная информация о формировании организма и его дальнейшем функционировании. ДНК, как из кирпичиков, строится из четырех видов молекул, которые называются нуклеотидами. Каждый нуклеотид – это одно из четырех азотистых оснований (аденин, гуанин, цито-зин или тимин, сокращенно А, Г, Ц и Т), соединенных с углеводом – дезоксирибозой и еще остатком фосфорной кислоты. Последовательность нуклеотидов в ДНК и является тем, что называют генетическим кодом, в котором зашифрованы структуры различных белков. Участок длинной молекулы ДНК, кодирующий определенный белок (иногда только РНК), получил название «ген». Однако одного наличия гена недостаточно для синтеза белка. Чтобы это произошло, требуется посредник, который обеспечивает перенос информации от ДНК, расположенной в ядре клеток, в цитоплазму, где и происходит синтез белка. Таким посредником служит другая специальная молекула – рибо-нуклеиновая кислота (РНК). В ней вместо дезоксирибозы присутствует рибоза (отсюда и название). РНК синтезируется на ДНК (процесс называется транскрипцией), а затем переходит из ядра в цитоплазму. Там на специальных «машинах» – рибосомах на этой РНК, как на матрице, и синтезируется белок (процесс синтеза белка по-научному называют трансляцией). Такая последовательность молекулярных событий получила название основной догмы молекулярной биологии.
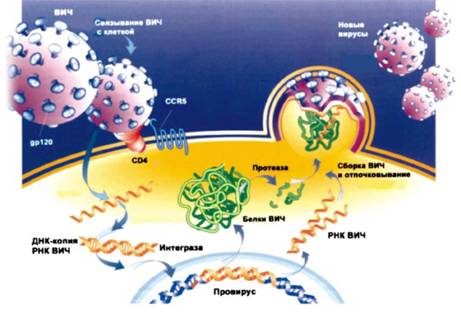 Рис. 8. Инфицируя СБ4-лимфоциты, ВИЧ осуществляет ряд превращений, в результате которых происходит его размножение и гибель клетки-хозяина. Подробности см. в тексте.
Рис. 8. Инфицируя СБ4-лимфоциты, ВИЧ осуществляет ряд превращений, в результате которых происходит его размножение и гибель клетки-хозяина. Подробности см. в тексте.
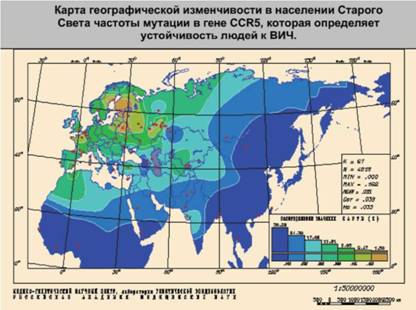 Рис. 12. Цветовой переход на карте соответствует изменению значений частоты (указан в шкале интервалов). Карта выявляет четкую клинальную изменчивость: падение частоты мутации от Северной Европы (выше 15 %) к югу и востоку. Так, если в Европе в целом частота мутации превышает 5 %, то в Африке южнее Сахары и Восточной Азии мутация практически отсутствует. (Любезно предоставлена доктором биологических наук Е. В. Балановской).
Рис. 12. Цветовой переход на карте соответствует изменению значений частоты (указан в шкале интервалов). Карта выявляет четкую клинальную изменчивость: падение частоты мутации от Северной Европы (выше 15 %) к югу и востоку. Так, если в Европе в целом частота мутации превышает 5 %, то в Африке южнее Сахары и Восточной Азии мутация практически отсутствует. (Любезно предоставлена доктором биологических наук Е. В. Балановской).
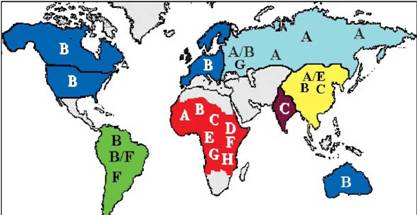 Рис. 13. Разные субтипы ВИЧ-1 неравномерно распределены по планете. Названия субтипов вирусов, превалирующих в разных регионах, обозначены заглавными латинскими буквами.
Рис. 13. Разные субтипы ВИЧ-1 неравномерно распределены по планете. Названия субтипов вирусов, превалирующих в разных регионах, обозначены заглавными латинскими буквами.
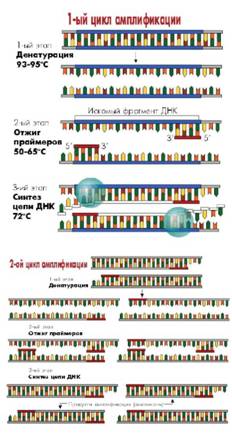 Рис. 28. Метод ПЦР весьма чувствительный, его проведение требует большой предосторожности. Необходимые пояснения см. на рисунке и в тексте.
Рис. 28. Метод ПЦР весьма чувствительный, его проведение требует большой предосторожности. Необходимые пояснения см. на рисунке и в тексте.
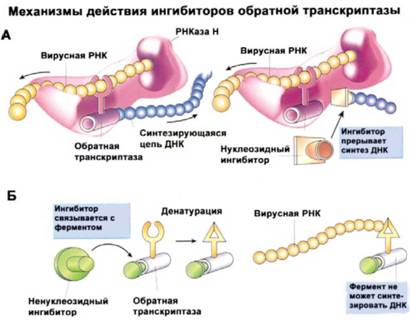 Рис. 30. Когда обратная траскриптаза синтезирует ДНК на вирусной РНК ей необходимо иметь в качестве строительного материала все четыре типа кирпичиков-нуклеотидов, из которых построена ДНК. Если встречается «кирпич», сильно отличающийся по своей форме, это останавливает всю дальнейшую работу. В качестве такого «кирпича» выступают специальные нуклеозидные ингибиторы (А). Ненуклео-зидные ингибиторы действуют по другому принципу (Б). Они специфически связываются с обратной транскриптазой и денатурируют ее. В результате фермент перестает работать и синтез ДНК-копии вирусной РНК прекращается.
Рис. 30. Когда обратная траскриптаза синтезирует ДНК на вирусной РНК ей необходимо иметь в качестве строительного материала все четыре типа кирпичиков-нуклеотидов, из которых построена ДНК. Если встречается «кирпич», сильно отличающийся по своей форме, это останавливает всю дальнейшую работу. В качестве такого «кирпича» выступают специальные нуклеозидные ингибиторы (А). Ненуклео-зидные ингибиторы действуют по другому принципу (Б). Они специфически связываются с обратной транскриптазой и денатурируют ее. В результате фермент перестает работать и синтез ДНК-копии вирусной РНК прекращается.
 Рис. 36. Красная ленточка – международный символ озабоченности проблемой СПИДа и солидарности с ВИЧ-инфицированными.
Рис. 36. Красная ленточка – международный символ озабоченности проблемой СПИДа и солидарности с ВИЧ-инфицированными.
Первоначально основная догма молекулярной биологии была сформулирована как
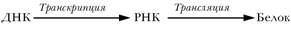 Однако детальное изучение устройства вирусов показало, что у некоторых из них геномом служит не ДНК, как обычно, а РНК. Такие необычные вирусы были названы ретровирусами (ретро – обратный). Как же реализуется генетическая информация, заложенная в РНКовом геноме? Благодаря изучению жизненного цикла ретровирусов в 1970 г. стало ясно, что основная догма требует существенного дополнения. Два американских вирусолога – Дэвид Балтимор и Ховард Мартин Темин – открыли в это время реальный механизм передачи информации от вирусной РНК к ДНК, т. е. прямо оборатное тому, что имеет место в клетках высших организмов. Такой процесс получил название обратной транскрипции, а фермент, его осуществляющий, был назван обратной транскриптазой или ревертазой. Оба первооткрывателя обратной транскриптазы получили в 1975 г. Нобелевскую премию по физиологии и медицине «за открытия, касающиеся взаимодействия между опухолевыми вирусами и генетическим материалом клетки».
Однако детальное изучение устройства вирусов показало, что у некоторых из них геномом служит не ДНК, как обычно, а РНК. Такие необычные вирусы были названы ретровирусами (ретро – обратный). Как же реализуется генетическая информация, заложенная в РНКовом геноме? Благодаря изучению жизненного цикла ретровирусов в 1970 г. стало ясно, что основная догма требует существенного дополнения. Два американских вирусолога – Дэвид Балтимор и Ховард Мартин Темин – открыли в это время реальный механизм передачи информации от вирусной РНК к ДНК, т. е. прямо оборатное тому, что имеет место в клетках высших организмов. Такой процесс получил название обратной транскрипции, а фермент, его осуществляющий, был назван обратной транскриптазой или ревертазой. Оба первооткрывателя обратной транскриптазы получили в 1975 г. Нобелевскую премию по физиологии и медицине «за открытия, касающиеся взаимодействия между опухолевыми вирусами и генетическим материалом клетки».
После этого основная догма молекулярной биологии в окончательном виде изображается сегодня следующим образом:
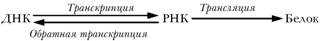 После небольшого ликбеза по устройству и работе генетического аппарата (генома) живых организмов вернемся снова к ВИЧ, который является типичным представителем ретровиру-сов. Но для начала расскажем вкраце весьма непростую историю его обнаружения.
После небольшого ликбеза по устройству и работе генетического аппарата (генома) живых организмов вернемся снова к ВИЧ, который является типичным представителем ретровиру-сов. Но для начала расскажем вкраце весьма непростую историю его обнаружения.
Таким образом, было твердо установлено, что различные типы BB4 и BBO являются главной причиной развития СПИДа у человека и его ближайших родственников – обезьян соответственно. Подобно всем другим ранее известным вирусам эти вирусы являются паразитами, которые размножаются только в живых клетках организма хозяина. При этом они оказывают патологическое действие, диаметрально противоположное действию ранее обнаруженного вируса HTLV-1. Тогда как HTLV-1 превращает нормальную Т-клетку в злокачественную и вызывает безудержное размножение Т-хелперов, и BB4, и BBO, наоборот, убивают эти клетки.
Сразу же стало ясно, что и BB4, и BBO относятся к семейству ретровирусов, но не к той подруппе, к которой относится ранее обнаруженный ретровирус HTLV–L Они принадлежат к особой подгруппе ретровирусов под названием «лентивирусы» («медленные» вирусы). Лентивирусы были довольно хорошо известны ученым еще до начала эпидемии СПИДа. Первый ленивый ретровирус был открыт в далеком 1904 г., когда французы А. Балле и А. Карре обнаружили фильтрующийся агент, вызывающий анемию у лошадей – вирус инфекционной анемии лошадей. Затем были открыты другие лентивирусные инфекции сельскохозяйственных животных. Типичными лентивирусами являются давно изученные вирус висны у овец, кошачий вирус иммунодефицита у кошек, вирус артрита у коз. Кроме сходства по своему строению эти вирусы вызывают однотипные патологии. Например, заражение овец вирусом висны приводит к длительному хроническому заболеванию, которое тянется порой до двух и более лет. Но затем, так же как и при инфицировании BB4, неизбежно наступает летальный исход.
Как уже говорилось, все ретровирусы имеют одну особенность – их генетический аппарат (геном) состоит из молекулы РНК, что отличает их от высших организмов и бактерий, у которых гены закодированы в молекулах ДНК. Поэтому, прежде чем размножиться и оказать влияние на клетки, ретровирусу требуется перевести информацию, записанную в молекуле РНК, в форму ДНК. Ретровирусы сами по себе это сделать не могут, для своего развития они используют элементы клетки, в которую проникают. По этой причине их иногда называют «молекулярными пиратами».
Как же выглядит этот страшный смертоносный пират по имени ВИЧ? В общих чертах строение ВИЧ подобно другим представителям подсемейства лентивирусов. Строение вируса оказалось не слишком сложным, но с помощью нескольких «хитроумных» механизмов, о которых мы поговорим позднее, вирус беспрепятственно проникает в организм человека и успешно там распространяется. Первоначальные данные были получены с помощью электронного микроскопа. В микроскопе вирусная частица (вирион) ВИЧ выглядит как некая шарообразная микрочастица диаметром около 100 нм, что составляет 1/10000 миллиметра (т. е. в тысячи раз меньше обыкновенной клетки), которая имеет форму икосаэдра (двадцатигранника). Для сравнения на линии длиной 1 см могут разместиться до 100 тыс. вирусных частиц, а на площади с копеечную монету – несколько десятков миллионов возбудителей.
ВИЧ представляет собой простой «футляр» (капсид), в котором хранятся две молекулы РНК (вирусный генетический аппарат) (рис. 6). Вся поверхность «футляра» покрыта шиповидными выростами, общее число которых равно 72. Поэтому обычно ВИЧ изображают похожим на противолодочную мину времен Второй мировой войны, на поверхности которой расположены белковые «грибы», служащие вирусу отмычкой для проникновения в клетку крови человека. Иногда вирус сравнивают еще с подушкой, утыканной иголками.
Наружная оболочка ВИЧ состоит из двойного слоя липидов, который происходит из мембраны клетки хозяина. «Шляпка» гриба, встроенного в мембрану, состоит из четырех молекул белка по имени gp120 (gp – сокращенно от англ. слова гликопроте-ин, а цифра – его молекулярный вес в тысячах дальтон). «Ножка» гриба формируется из четырех молекул другого гликопро-теина – gp41, которые встроены в мембрану. Так как мембрана имеет клеточное происхождение, то на ее поверхности и внутри нее сохраняется множество клеточных белков. Под наружной оболочкой располагается сердцевина вируса (кор), которая имеет форму усеченного конуса и образована двумя тысячами молекул белка р24. Внутренная поверхность мембраны выстлана так называемым матриксным белком р17. Кроме того, в коре присутствуют три фермента, которые необходимы для осуществления важнейших стадий в жизненном цикле вируса после заражения им клетки: обратная транскриптаза, интеграза и протеаза.
У ВИЧ, как и у других ретровирусов, вся генетическая информация закодирована в молекуле РНК. Внутри сердцевины
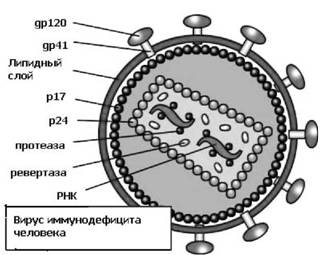 Рис. 6. Общий план строения вируса иммунодефицита человека (BB4) напоминает устройство других ретровирусов. Необходимые пояснения даны в тексте
Рис. 6. Общий план строения вируса иммунодефицита человека (BB4) напоминает устройство других ретровирусов. Необходимые пояснения даны в тексте
вируса располагаются две однонитевые молекулы вирусной РНК, связанные с двумя низкомолекулярными белками (р6 и р7). Генетический аппарат BB4-1 – его РНК – имеет длину чуть меньше 10 тыс. нуклеотидов и содержит всего девять генов (рис. 7а). Для сравнения: у человека в геноме присутствует свыше 35 тыс. генов! Строение генетического аппарата BB4-2 слегка отличается от BB4-1 (рис. 7б) и больше напоминает устройство генома BИO (рис. 7в). Примечательная особенность генов всех этих вирусов состоит в том, что они перекрываются друг с другом, т. е. одни и те же вирусные нуклеотидные последовательности РНК могут участвовать в кодировании разных белков. Достигается это за счет использования разных точек начала считывания информации с нуклеотидной последовательности ДНК и благодаря разнообразной комбинаторике отдельных фрагментов из разных участков генома. Ряд генов «разорван», т. е. белок кодируется не одной непрерывной последовательностью нук-леотидов, а двумя участками вирусной РНК, порой далеко отстоящими друг от друга. Таким образом, небольшой по размерам геном вирусов за счет использования всевозможных «хитростей» кодирует довольно большое число разнообразных белков. Для сравнения: средний размер гена, кодирующего белок у человека, составляет около 27 тыс. пар нуклеотидов (п.н.), т. е. почти в три раза превышает размер всего генома BИЧ.
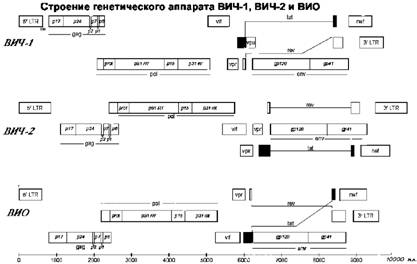 Рис. 7. Прямоугольниками на рисунке обозначены отдельные вирусные гены или их фрагменты, тонкими линиями указаны, из каких фрагментов устроены «разорванные» гены. Внутри прямоугольников дано название генов. Шкала – в парах нук-леотидов (п.н.). LTR – одинаковые концевые участки вирусного генома
Рис. 7. Прямоугольниками на рисунке обозначены отдельные вирусные гены или их фрагменты, тонкими линиями указаны, из каких фрагментов устроены «разорванные» гены. Внутри прямоугольников дано название генов. Шкала – в парах нук-леотидов (п.н.). LTR – одинаковые концевые участки вирусного генома
Теперь дадим краткую характеристику отдельных генов ВИЧ и кодируемых ими белков (табл. 1). У вируса, так же как и у всех других известных ретровирусов, имеются гены, называемые gag, env и pol, которые, однако, отличаются по размерам у ВИЧ-1 и ВИЧ-2. Первые два из них кодируют структурные белки оболочки вируса. Сначала образуются белки-предшественники, которые затем разрезаются на меньшие по размеру белки. Так, например, ген gag у ВИЧ-1 кодирует первоначально большой белок-предшественник р53. Затем этот белок расщепляется в клетке на три меньших по размерам белка (р15, р 17 и р24). Некоторые гены кодируют один белок, другие несколько. Так, единичный ген по имени pol обеспечивает вирус такими тремя специфическими белками-ферментами, как ревертаза, интеграза и протеаза.
Два других гена ВИЧ – tat и rev – кодируются разными не связанными между собой участками генома ВИЧ (такие гены иногда называют разорванными). Они обеспечивают синтез ре-гуляторных белков, которые стимулируют транскрипцию вирусной ДНК и трансляцию РНК. Продукты этих генов способны влиять на работу не только вирусных, но и клеточных генов.
Еще один регуляторный ген – ген rief – выполняет, по-видимому, много различных функций (не все они еще хорошо изучены), в частности, его продукт может понижать содержание CD4-лимфоцитов, влияет на активность Т-лимфоцитов. Продукт гена vpr ингибирует размножение клеток, важен для размножения вируса в отдельных (неделящихся) типах клеток, ген vpu необходим для «почкования» вирусных частиц, а продукт гена vif осуществляет транспорт компонентов вируса в клетке. У BИЧ-1 имеется ген, которого нет у BИЧ-2 (ген vpu), и, наоборот, у BИЧ-2 имеется один ген, которого нет у BИЧ-1 (ген vpx). Функция гена vpx BИЧ-2 пока малоизучена.
Кроме того, на концах каждой нити РНК содержатся нуклео-тидные последовательности, которые осуществляют регуляцию работы вирусных генов.
Bот, собственно, и все. Тем не менее такого короткого генетического текста, записанного всего в 9 генах, вирусу вполне достаточно, чтобы обмануть человеческую клетку, влезть в нее и воспользоваться всеми возможностями, которые в ней имеются, для достижения своих корыстных целей.
Таблица 1
Гены и кодируемые ими белки у ВИЧ-1 и ВИЧ-2
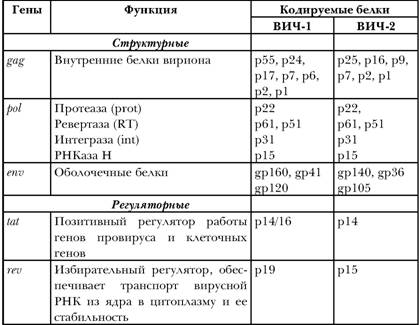
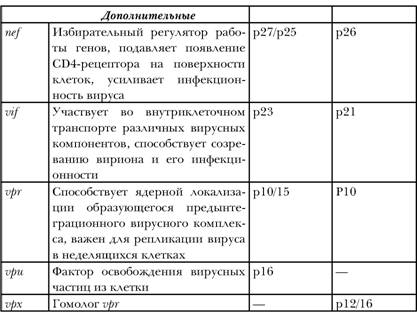 Примечание: p – (от англ. – protein), белок; gp – (от англ. – glycoprotein), гликопротеин, т. е. белок, соединенный с остатками сахара. Цифрами указан молекулярный вес белков (в тысячах дальтон)
Примечание: p – (от англ. – protein), белок; gp – (от англ. – glycoprotein), гликопротеин, т. е. белок, соединенный с остатками сахара. Цифрами указан молекулярный вес белков (в тысячах дальтон)
Если какая-нибудь маленькая песчинка попадет в наш организм и проникнет даже в кровь, она, несмотря на огромные по сравнению с вирусом размеры, ничего существенного сделать в клетке не сможет. Все дело в том, что неживая природа на владеет «генетическим языком», она не умеет разговаривать с живой и поэтому остается безмолвной. А вот вирус умеет «говорить» с клеткой, он способен без труда подложить ей свою лжепрограмму, которую клетка начинает воспринимать как свою собственную. Это подобно тому, как компьютерные вирусы, вероломно влезая в компьютеры и «говоря» с ними на общем языке, способны все испортить. Здесь также нормальная генетическая программа заменяется привнесенной извне лжепрограммой.
По мнению известного борца с компьютерными вирусами нашего бывшего соотечественника, проживающего в Америке, Е. Касперского, первый компьютерный вирус появился где-то в самом начале 70-х или даже в конце 60-х гг., хотя «вирусом» его тогда никто еще не называл. Термин «компьютерный вирус» появился позднее – официально считается, что его впервые употребил американец Ф. Коэн в 1984 г. на конференции по безопасности информации, проходившей в США. Здесь просматривается определенная аналогия с появлением ВИЧ в человеческой популяции и официальным его названием. Удивительно еще одно сходство. Компьютерные вирусы, как и ВИЧ, способны мутировать, для многих из них характерен полиморфизм. Наконец, несколько лет назад был зафиксирован случай, когда компьютерный вирус стал причиной гибели человека – в одном из госпиталей Нидерландов пациент получил летальную дозу морфия по той причине, что компьютер был заражен компьютерным вирусом и выдавал неверную информацию.
Жизненный цикл ВИЧ (круговорот вич в клетке)
Еще со школы всем нам хорошо известно такое понятие, как круговорот веществ в природе. Так вот у ВИЧ тоже есть свой круговорот, а точнее, его жизненный цикл, который связан только с человеком, с определенными его клетками. В окружающей среде без человека вирус совершенно беспомощен и быстро погибает. Если случилось бы такое, что все человечество исчезло с планеты Земля, то тут же исчез бы и ВИЧ. На сегодняшний день это единственно возможный, хотя, понятно, совершенно нереальный, чисто фантастический способ освобождения нашей планеты от ВИЧ. ВИЧ подобен огню, существующему только, если есть горючий материал, сжигающему этот материал дотла и вместе с ним погибающему.
Сейчас уже хорошо известно, как вирус проникает в клетки и как его генетическая программа реализуется в пораженном им организме. Как же ведет себя ВИЧ в своем единственно возможном месте обитания – в человеке? Общая схема поведения вируса в клетках изображена на рис. 8 (см. вклейку после с. 64). В целом эта схема сходна у всех ретровирусов, отличия здесь только в деталях, но именно эти детали и делают ВИЧ тем, что он есть – смертельно опасным.
Сегодня в оценках превалирует «дуализм». Согласно современным представлениям, вирусы лежат на границе «живого» и «неживого», это внеклеточные формы жизни, способные проникать в определенные живые клетки и размножаться только внутри них.
Генетический аппарат вирусов представлен различными формами нуклеиновых кислот, такого разнообразия нет ни у одной из других форм жизни. У всех живых организмов, кроме вирусов, генетический аппарат состоит из двунитевой молекулы дезоксири-бонуклеиновой кислоты (ДНК), а рибонуклеиновая кислота (РНК), выполняющая в нормальных клетках роль переносчика информации, всегда однонитевая. У вирусов же природа будто бы опробовала все возможные варианты устройства генетического аппарата: одно– и двунитевая РНК, одно– и двунитевая ДНК. При этом и вирусная РНК, и вирусная ДНК могут быть либо линейными, либо замкнутыми в кольцо.
Постепенно пришли к пониманию, что вирусы могут быть основной причиной многих хронических заболеваний у человека. К началу XXI в. было открыто и исследовано свыше тысячи разнообразных вирусов, вызывающих такие заболевания, как грипп, герпес, гепатит, оспа, полиомиелит, цитомегаловирусная инфекция, энцефалит, корь и др. Сколько же существует вирусов всего – не знает никто. Ведь невесть откуда постоянно появляются все новые их разновидности, порой угрожающие нам смертельной опасностью. В целом около 80 % инфекционных заболеваний, регистрируемых в настоящее время, вызывают вирусы. Первые места по массовости поражения занимают острые респираторные заболевания, грипп, вирусный гепатит, теперь к ним прибавился и СПИД.
Широко распространены вирусные заболевания и у животных. Хорошо известны эпидемии вирусов у птиц, овец, коров. В результате эпидемии вируса висны в 30—40-е гг. прошлого века исландцы были вынуждены забить более 150 тыс. животных. Вирус лейкоза птиц причинил убыток птицеводству США в 1955 г. в размере свыше 60 млн долларов. Известна широкая пораженность крупного рогатого скота вирусом лейкоза. В некоторых странах мира им заражено свыше 80 % коров и быков.
Чтобы читатель далее более четко понимал, как устроены вирусы, каковы молекулярные механизмы их взаимодействия с клеткой, необходимо сделать небольшое напоминание о том, как хранится и используется генетическая программа в обычной нормальной клетке высших организмов. Основу генетического аппарата (генома) подавляющего большинства организмов составляет высокополимерная молекула ДНК, состоящая из двух полимерных цепей, закрученных в правильную двойную спираль. B ней закодирована вся наследственная информация о формировании организма и его дальнейшем функционировании. ДНК, как из кирпичиков, строится из четырех видов молекул, которые называются нуклеотидами. Каждый нуклеотид – это одно из четырех азотистых оснований (аденин, гуанин, цито-зин или тимин, сокращенно А, Г, Ц и Т), соединенных с углеводом – дезоксирибозой и еще остатком фосфорной кислоты. Последовательность нуклеотидов в ДНК и является тем, что называют генетическим кодом, в котором зашифрованы структуры различных белков. Участок длинной молекулы ДНК, кодирующий определенный белок (иногда только РНК), получил название «ген». Однако одного наличия гена недостаточно для синтеза белка. Чтобы это произошло, требуется посредник, который обеспечивает перенос информации от ДНК, расположенной в ядре клеток, в цитоплазму, где и происходит синтез белка. Таким посредником служит другая специальная молекула – рибо-нуклеиновая кислота (РНК). В ней вместо дезоксирибозы присутствует рибоза (отсюда и название). РНК синтезируется на ДНК (процесс называется транскрипцией), а затем переходит из ядра в цитоплазму. Там на специальных «машинах» – рибосомах на этой РНК, как на матрице, и синтезируется белок (процесс синтеза белка по-научному называют трансляцией). Такая последовательность молекулярных событий получила название основной догмы молекулярной биологии.






Первоначально основная догма молекулярной биологии была сформулирована как
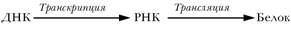
После этого основная догма молекулярной биологии в окончательном виде изображается сегодня следующим образом:
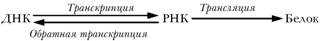
История открытияВ современной человеческой популяции наиболее распространен ВИЧ-1, известный в популярной литературе просто как ВИЧ (в англоязычной литературе – HIV). Другой вариант вируса – ВИЧ-2, обнаруживаемый главным образом в Западной Африке, хотя и очень напоминает ВИЧ-1, во многом подобен ему, тем не менее существенно отличается от последнего. Nullus simile est idem (подобное не есть то же самое). Сходство между геномами различных вариантов ВИЧ-1 и ВИЧ-2 составляет всего от 50 до 60 %. По структуре генов ВИЧ-2 более родствен возбудителю СПИД-подобного заболевания у обезьян. Он способен инфицировать разные виды приматов, порой весьма удаленные от человека на лестнице эволюции, тогда как ВИЧ-1 заражает только людей и наиболее близкородственного ему из ныне живущих приматов – шимпанзе. Кроме того, BB4-2 передается хуже, чем BB4-1, и симптомы, вызываемые им, развиваются у человека медленнее, чем при инфекции BB4-1. Можно сказать, что в целом BB4-2 более «ленивый», чем BB4-1.
Начало обнаружению вируса, вызывающего СПИД, было положено в 1981 г., когда группа ученых Национального института рака в США, руководимых известным иммунологом и вирусологом Робертом Галло, открыла возбудителя одного из видов рака человека, называемого Т-клеточным лейкозом. Это заболевание было впервые зарегистрировано в конце 70-х гг. в странах Карибского бассейна и в Южной Японии. В тяжелой форме лейкоз протекал очень быстро: больные погибали за 3–4 месяца. Возбудителем острого Т-клеточного лейкоза у человека оказался вирус, который назвали вирусом Т-клеточной лейкемии человека (по-английски сокращенно HTLV–I). По существующей классификации он был отнесен к классу ретровирусов, т. е. вирусов, у которых генетический аппарат представлен не ДНК, а РНК. Как самостоятельная группа ретровирусы известны с 1974 г., хотя отдельные представители таких вирусов у животных были открыты еще в начале прошлого века. Всех их ученые разделили на несколько подклассов. HTLV-1 стал первым обнаруженным ретровирусом человека и был отнесен к подклассу онковирусов, т. е. вирусов, вызывающих рак (отсюда приставка онко– онкологические). Некоторые разновидности HTLV–I, особенно выделенные у зеленых мартышек и шимпанзе, имели много сходного с ним. На этом основании было предположено, что вновь открытый вирус возник первоначально в Африке, где им заразились приматы Старого Света, а потом и человек тоже, а на американский континент этот ретровирус проник благодаря работорговле.
Как раз в это время (в начале 80-х гг.) в США началась эпидемия СПИДа. Вполне естественно Р. Галло предположил, что обнаруженный им HTLV–I и есть возбудитель СПИДа или его ближайший родственник. Более того, у некоторых больных СПИДом удалось обнаружить и выделить HTLV–I. Однако, как выяснилось в дальнейшем, признанный научный авторитет Р. Галло в этом случае ошибся.
Причиной СПИДа в самом деле оказался вирус, но который существенно отличался от HTLV–I. Первые публикации о возбудителе нового заболевания, связанного с тяжелым расстройством иммунной системы человека, появились в 1983 г. Специалисты лабораторий Люка Монтанье из Института Пастера в Париже и Роберта Галло из Национального института рака в Бетесде (США) под двумя разными названиями описали один и тот же вирус, вызывающий СПИД. Французские ученые из Пастеровского института в Париже во главе с Люком Монтанье опубликовали статью, в которой сообщалось о наличии у двух из 33 больных СПИДом нового ретровируса, который, в отличие от HTLV-1, не обладал способностью влиять на злокачественное перерождение Т-лимфоцитов. Авторы дали ему название LAV (вирус, ассоциированный с лимфоаденопатией). В отличие от HTLV-1 он вызывал не размножение, а, наоборот, гибель Т-лимфоцитов. Параллельно с Монта-нье в США работала группа Роберта Галло в США, которая также выделила из больных СПИДом новый ретровирус, который они назвали HTLV-3. Вскоре установили, что вирус HTLV-3 Галло и вирус LAV Монтанье – это один и тот же вирус. Поэтому новый вирус стали обозначать как HTLV-3/LAV. Поскольку каждая лаборатория, описавшая новый вариант вируса, давала свое собственное название, было решено навести в этом деле порядок. И в 1986 г. по решению подкомитета Международного комитета по таксономии вирусов вирус, выделенный Монтанье и Галло, получил окончательное название – вирус иммунодефицита человека (Human Immunodeficiency Virus, сокращенно HIV, в русской транскрипции – ВИЧ). В том же году у больного из Западной Африки был выделен еще один вариант вируса иммунодефицита человека, так появились названия ВИЧ-1 и ВИЧ-2. Сначала ВИЧ-2 обнаруживался только в одном районе, а затем был детектирован и в других регионах мира. В настоящее время ясно, что существуют по крайней мере два родственных типа возбудителя иммунодефицита человека: ВИЧ-1 и ВИЧ-2. Обычно СПИД вызывается одним из них. Вместе с тем описаны случаи одновременного существования в организме человека этих двух типов вирусов. Будучи довольно дальними родственниками, они порой успешно уживаются друг с другом.
У обезьян также были обнаружены вирусы иммунодефицита, получившие общее название Simian Immunodeficiency Virus (сокращенно SIV), по-русски – вирус иммунодефицита обезьян (ВИО). У разных видов обезьян ВИО немного отличаются, но все они по своей структуре больше напоминают один из типов ВИЧ, а именно ВИЧ-2.
Таким образом, было твердо установлено, что различные типы BB4 и BBO являются главной причиной развития СПИДа у человека и его ближайших родственников – обезьян соответственно. Подобно всем другим ранее известным вирусам эти вирусы являются паразитами, которые размножаются только в живых клетках организма хозяина. При этом они оказывают патологическое действие, диаметрально противоположное действию ранее обнаруженного вируса HTLV-1. Тогда как HTLV-1 превращает нормальную Т-клетку в злокачественную и вызывает безудержное размножение Т-хелперов, и BB4, и BBO, наоборот, убивают эти клетки.
Сразу же стало ясно, что и BB4, и BBO относятся к семейству ретровирусов, но не к той подруппе, к которой относится ранее обнаруженный ретровирус HTLV–L Они принадлежат к особой подгруппе ретровирусов под названием «лентивирусы» («медленные» вирусы). Лентивирусы были довольно хорошо известны ученым еще до начала эпидемии СПИДа. Первый ленивый ретровирус был открыт в далеком 1904 г., когда французы А. Балле и А. Карре обнаружили фильтрующийся агент, вызывающий анемию у лошадей – вирус инфекционной анемии лошадей. Затем были открыты другие лентивирусные инфекции сельскохозяйственных животных. Типичными лентивирусами являются давно изученные вирус висны у овец, кошачий вирус иммунодефицита у кошек, вирус артрита у коз. Кроме сходства по своему строению эти вирусы вызывают однотипные патологии. Например, заражение овец вирусом висны приводит к длительному хроническому заболеванию, которое тянется порой до двух и более лет. Но затем, так же как и при инфицировании BB4, неизбежно наступает летальный исход.
Как уже говорилось, все ретровирусы имеют одну особенность – их генетический аппарат (геном) состоит из молекулы РНК, что отличает их от высших организмов и бактерий, у которых гены закодированы в молекулах ДНК. Поэтому, прежде чем размножиться и оказать влияние на клетки, ретровирусу требуется перевести информацию, записанную в молекуле РНК, в форму ДНК. Ретровирусы сами по себе это сделать не могут, для своего развития они используют элементы клетки, в которую проникают. По этой причине их иногда называют «молекулярными пиратами».
Как же выглядит этот страшный смертоносный пират по имени ВИЧ? В общих чертах строение ВИЧ подобно другим представителям подсемейства лентивирусов. Строение вируса оказалось не слишком сложным, но с помощью нескольких «хитроумных» механизмов, о которых мы поговорим позднее, вирус беспрепятственно проникает в организм человека и успешно там распространяется. Первоначальные данные были получены с помощью электронного микроскопа. В микроскопе вирусная частица (вирион) ВИЧ выглядит как некая шарообразная микрочастица диаметром около 100 нм, что составляет 1/10000 миллиметра (т. е. в тысячи раз меньше обыкновенной клетки), которая имеет форму икосаэдра (двадцатигранника). Для сравнения на линии длиной 1 см могут разместиться до 100 тыс. вирусных частиц, а на площади с копеечную монету – несколько десятков миллионов возбудителей.
ВИЧ представляет собой простой «футляр» (капсид), в котором хранятся две молекулы РНК (вирусный генетический аппарат) (рис. 6). Вся поверхность «футляра» покрыта шиповидными выростами, общее число которых равно 72. Поэтому обычно ВИЧ изображают похожим на противолодочную мину времен Второй мировой войны, на поверхности которой расположены белковые «грибы», служащие вирусу отмычкой для проникновения в клетку крови человека. Иногда вирус сравнивают еще с подушкой, утыканной иголками.
Наружная оболочка ВИЧ состоит из двойного слоя липидов, который происходит из мембраны клетки хозяина. «Шляпка» гриба, встроенного в мембрану, состоит из четырех молекул белка по имени gp120 (gp – сокращенно от англ. слова гликопроте-ин, а цифра – его молекулярный вес в тысячах дальтон). «Ножка» гриба формируется из четырех молекул другого гликопро-теина – gp41, которые встроены в мембрану. Так как мембрана имеет клеточное происхождение, то на ее поверхности и внутри нее сохраняется множество клеточных белков. Под наружной оболочкой располагается сердцевина вируса (кор), которая имеет форму усеченного конуса и образована двумя тысячами молекул белка р24. Внутренная поверхность мембраны выстлана так называемым матриксным белком р17. Кроме того, в коре присутствуют три фермента, которые необходимы для осуществления важнейших стадий в жизненном цикле вируса после заражения им клетки: обратная транскриптаза, интеграза и протеаза.
У ВИЧ, как и у других ретровирусов, вся генетическая информация закодирована в молекуле РНК. Внутри сердцевины

вируса располагаются две однонитевые молекулы вирусной РНК, связанные с двумя низкомолекулярными белками (р6 и р7). Генетический аппарат BB4-1 – его РНК – имеет длину чуть меньше 10 тыс. нуклеотидов и содержит всего девять генов (рис. 7а). Для сравнения: у человека в геноме присутствует свыше 35 тыс. генов! Строение генетического аппарата BB4-2 слегка отличается от BB4-1 (рис. 7б) и больше напоминает устройство генома BИO (рис. 7в). Примечательная особенность генов всех этих вирусов состоит в том, что они перекрываются друг с другом, т. е. одни и те же вирусные нуклеотидные последовательности РНК могут участвовать в кодировании разных белков. Достигается это за счет использования разных точек начала считывания информации с нуклеотидной последовательности ДНК и благодаря разнообразной комбинаторике отдельных фрагментов из разных участков генома. Ряд генов «разорван», т. е. белок кодируется не одной непрерывной последовательностью нук-леотидов, а двумя участками вирусной РНК, порой далеко отстоящими друг от друга. Таким образом, небольшой по размерам геном вирусов за счет использования всевозможных «хитростей» кодирует довольно большое число разнообразных белков. Для сравнения: средний размер гена, кодирующего белок у человека, составляет около 27 тыс. пар нуклеотидов (п.н.), т. е. почти в три раза превышает размер всего генома BИЧ.

Теперь дадим краткую характеристику отдельных генов ВИЧ и кодируемых ими белков (табл. 1). У вируса, так же как и у всех других известных ретровирусов, имеются гены, называемые gag, env и pol, которые, однако, отличаются по размерам у ВИЧ-1 и ВИЧ-2. Первые два из них кодируют структурные белки оболочки вируса. Сначала образуются белки-предшественники, которые затем разрезаются на меньшие по размеру белки. Так, например, ген gag у ВИЧ-1 кодирует первоначально большой белок-предшественник р53. Затем этот белок расщепляется в клетке на три меньших по размерам белка (р15, р 17 и р24). Некоторые гены кодируют один белок, другие несколько. Так, единичный ген по имени pol обеспечивает вирус такими тремя специфическими белками-ферментами, как ревертаза, интеграза и протеаза.
Два других гена ВИЧ – tat и rev – кодируются разными не связанными между собой участками генома ВИЧ (такие гены иногда называют разорванными). Они обеспечивают синтез ре-гуляторных белков, которые стимулируют транскрипцию вирусной ДНК и трансляцию РНК. Продукты этих генов способны влиять на работу не только вирусных, но и клеточных генов.
Еще один регуляторный ген – ген rief – выполняет, по-видимому, много различных функций (не все они еще хорошо изучены), в частности, его продукт может понижать содержание CD4-лимфоцитов, влияет на активность Т-лимфоцитов. Продукт гена vpr ингибирует размножение клеток, важен для размножения вируса в отдельных (неделящихся) типах клеток, ген vpu необходим для «почкования» вирусных частиц, а продукт гена vif осуществляет транспорт компонентов вируса в клетке. У BИЧ-1 имеется ген, которого нет у BИЧ-2 (ген vpu), и, наоборот, у BИЧ-2 имеется один ген, которого нет у BИЧ-1 (ген vpx). Функция гена vpx BИЧ-2 пока малоизучена.
Кроме того, на концах каждой нити РНК содержатся нуклео-тидные последовательности, которые осуществляют регуляцию работы вирусных генов.
Bот, собственно, и все. Тем не менее такого короткого генетического текста, записанного всего в 9 генах, вирусу вполне достаточно, чтобы обмануть человеческую клетку, влезть в нее и воспользоваться всеми возможностями, которые в ней имеются, для достижения своих корыстных целей.
Таблица 1
Гены и кодируемые ими белки у ВИЧ-1 и ВИЧ-2


Если какая-нибудь маленькая песчинка попадет в наш организм и проникнет даже в кровь, она, несмотря на огромные по сравнению с вирусом размеры, ничего существенного сделать в клетке не сможет. Все дело в том, что неживая природа на владеет «генетическим языком», она не умеет разговаривать с живой и поэтому остается безмолвной. А вот вирус умеет «говорить» с клеткой, он способен без труда подложить ей свою лжепрограмму, которую клетка начинает воспринимать как свою собственную. Это подобно тому, как компьютерные вирусы, вероломно влезая в компьютеры и «говоря» с ними на общем языке, способны все испортить. Здесь также нормальная генетическая программа заменяется привнесенной извне лжепрограммой.
По мнению известного борца с компьютерными вирусами нашего бывшего соотечественника, проживающего в Америке, Е. Касперского, первый компьютерный вирус появился где-то в самом начале 70-х или даже в конце 60-х гг., хотя «вирусом» его тогда никто еще не называл. Термин «компьютерный вирус» появился позднее – официально считается, что его впервые употребил американец Ф. Коэн в 1984 г. на конференции по безопасности информации, проходившей в США. Здесь просматривается определенная аналогия с появлением ВИЧ в человеческой популяции и официальным его названием. Удивительно еще одно сходство. Компьютерные вирусы, как и ВИЧ, способны мутировать, для многих из них характерен полиморфизм. Наконец, несколько лет назад был зафиксирован случай, когда компьютерный вирус стал причиной гибели человека – в одном из госпиталей Нидерландов пациент получил летальную дозу морфия по той причине, что компьютер был заражен компьютерным вирусом и выдавал неверную информацию.
Жизненный цикл ВИЧ (круговорот вич в клетке)
Vices superbae
(Неумолимый круговорот судьбы)
Еще со школы всем нам хорошо известно такое понятие, как круговорот веществ в природе. Так вот у ВИЧ тоже есть свой круговорот, а точнее, его жизненный цикл, который связан только с человеком, с определенными его клетками. В окружающей среде без человека вирус совершенно беспомощен и быстро погибает. Если случилось бы такое, что все человечество исчезло с планеты Земля, то тут же исчез бы и ВИЧ. На сегодняшний день это единственно возможный, хотя, понятно, совершенно нереальный, чисто фантастический способ освобождения нашей планеты от ВИЧ. ВИЧ подобен огню, существующему только, если есть горючий материал, сжигающему этот материал дотла и вместе с ним погибающему.
Сейчас уже хорошо известно, как вирус проникает в клетки и как его генетическая программа реализуется в пораженном им организме. Как же ведет себя ВИЧ в своем единственно возможном месте обитания – в человеке? Общая схема поведения вируса в клетках изображена на рис. 8 (см. вклейку после с. 64). В целом эта схема сходна у всех ретровирусов, отличия здесь только в деталях, но именно эти детали и делают ВИЧ тем, что он есть – смертельно опасным.
