• концентрация кислорода в дыхательной смеси должна быть той минимальной, которая достаточна для коррекции гипоксемии;
• предельная безопасная для длительного использования концентрация кислорода в дыхательной смеси, по последним
данным, равна 50 %;
• токсическое влияние высоких концентраций кислорода
на легкие не имеет специфических проявлений и всплывает в виде ателектазов, гнойного трахеобронхита или респираторного дистресс-синдрома, которые в дальнейшем соотносят
с чем угодно, но не с оксигенотерапией;
• и наконец, к кислороду в полной мере относится "золотое правило" интенсивной терапии: лучший лист назначений - не тот, к которому нечего добавить, а тот, из которого нечего вычеркнуть.
Пульсоксиметрия - ключ к решению многих перечисленных выше проблем. Мониторинг оксигенации помогает не только своевременно обнаружить гипоксемию, но также установить ее причину, подобрать оптимальную концентрацию кислорода в дыхательной смеси и в нужный момент безопасно перевести больного на дыхание атмосферным воздухом.
Нормальная величина SpO2 находится в диапазоне 94-98 %, причем у пациентов молодого и среднего возраста, не имеющих легочной патологии, преобладают значения сатурации 96-98 %, а у пожилых больных чаще встречается Sp02 94-96 %, что обусловлено возрастными изменениями в легких.
У пациентов с хронической легочной патологией отмечается адаптация к более низкому уровню сатурации. Попытка искусственной "нормализации" SpO2 у таких больных может закончиться угнетением спонтанного дыхания.
При нормальном уровне SpO2 оксигенотерапия показана:
1. При выраженной острой недостаточности кровообращения или очень глубокой анемии, когда приходится надеяться даже на незначительное увеличение системного транспорта кислорода за счет до насыщения кислородом оставшихся 2-4 % гемоглобина.
2. В качестве профилактической меры при реальном риске внезапного развития гипоксемииу пациентов с нестабильным дыханием, например в раннем послеоперационном периоде или при неврологической патологии, затрагивающей дыхательный центр или дыхательную мускулатуру. В таких случаях обычно бывает достаточно повысить FiOa до 30-40 %.
К числу показаний мы не относим отравление угарным газом, при котором значение Sp02 всегда является артефактным.
Снижение Sp02 до 90-94 % расценивается как умеренная артериальная гипоксемия. Если она обнаруживается у больных, дышащих атмосферным воздухом, вопрос о необходимости оксигенотерапии решается индивидуально. Надо помнить, что неглубокую гипоксемию человек может довольно длительно переносить без печальных последствий. Исключение составляют пациенты с тяжелой анемией, недостаточностью кровообращения, нарушениями коронарного или мозгового кровотока, гиперметаболизмом.
Выраженная артериальная гипоксемия (SpO2 =85-90 %) - это следствие и признак серьезного нарушения газообмена и безусловное показание для назначения кислорода. Нормализация пульсоксиметрических параметров на фоне оксигенотерапии не отменяет необходимости выяснения причины расстройства и ее устранения с использованием приемов, рассмотренных выше.
При глубокой гипоксемии (SpO2 «85 %) оксигенотерапия служит экстренной первичной мерой коррекции и фоном для применения более сложных и требующих времени методов лечения, выбор которых определяется причиной нарушения газообмена.
Пульсоксиметрия позволяет реализовать важнейший принцип оксигенотерапии - использование кислорода в концентрации, не превышающей ту минимальную; которая требуется, чтобы удерживать SpO2 в пределах нормальных значений. После заполнения гемоглобиновой емкости артериальной крови на 98-100 % дальнейшее увеличение FiO2 становится бессмысленным, поскольку приводит лишь к незначительному приросту оксигенации крови за счет физически растворенного в ней кислорода.
Стремление увеличить количество физически растворенного в крови кислорода оправдано лишь:
• при крайне низком содержании гемоглобина;
• при выраженной недостаточности кровообращения;
• при отравлении окисью углерода;
• при необходимости денитрогенации организма.
В подавляющем большинстве случаев применение кислорода в концентрациях, превышающих минимально достаточную для практически полного насыщения гемоглобина артериальной крови (SpO2 =98-100%), не содействует сколько-нибудь заметному улучшению оксигенации тканей, но повышает риск гипероксического повреждения легких и приводит к непроизводительному расходу газа.
Пульсоксиметр измеряет степень заполнения кислородом гемоглобиновой емкости артериальной крови и потому не способен выявлять гипероксию.
После того как достигается 100 % сатурация гемоглобина (у здорового человека этого добиваются назначением 30 % кислорода), дальнейшее увеличение Fi02 приводит лишь к росту напряжения и содержания физически растворенного кислорода в крови, на который пульсоксиметр не реагирует. В подобных случаях монитор будет показывать на дисплее один и тот же, максимально возможный, уровень сатурации (Sp02 = 100 %), начиная с Fi02 - 0,3 и далее, при увеличении концентрации кислорода во вдыхаемом газе вплоть до использования чистого кислорода.
В случаях, когда пульсоксиметр отображает на индикаторе SpO2 = 100 %, врач не может быть уверен в том, что концентрация кислорода не избыточна (рис. 1.16).
Чтобы выйти из этого положения, достаточно плавно уменьшить содержание кислорода в дыхательной смеси до того уровня, при котором Sp02 составит 98-99 % или вовсе вернется в границы нормы. При снижении SpO2 со 100 до 98 % уменьшение содержания кислорода в артериальной крови столь несущественно, что в подавляющем большинстве случаев может быть произведено незаметно для здоровья больного. Зато врач приобретает надежный ориентир, помогающий отслеживать в мониторном режиме правильность дозирования кислорода. В дальнейшем регулировать FiOa нужно таким образом, чтобы поддерживать Sp02 на 1-3 % ниже 100 %. Тем самым обеспечиваются нормальное насыщение гемоглобина артериальной крови Кислородом и минимальная достаточная концентрация кислорода во вдыхаемом газе. Благодаря такому подходу не только сокращается риск ги-пероксического повреждения легких, но и экономно расходуется сжатый кислород.
При катастрофическом поражении легких, сопровождающемся массивным шунтированием крови и глубокой гипоксемией, даже вентиляция 100 % кислородом не позволяет нормализовать Sp02. В этих случаях приходится идти на вынужденный компромисс, выбирая между наименьшим допустимым уровнем SpO2 и максимально приемлемой для длительного применения концентрацией кислорода во вдуваемом газе. И если повышение Fi02 c 50 дo 100 % дает увеличение SpO2 с 75 до 78 %, задумайтесь, не слишком ли высока цена за столь незначительный результат.
Диагноз "токсическое поражение легких кислородом" практически не встречается ни в историях болезни, ни в протоколах патологоанатомического исследования, но это говорит лишь о неумении распознавать патологию, а не о ее отсутствии.
Разумеется, сказанное выше относится к многочасовой и многосуточной оксигенотерапии, в том числе и при длительной ИВЛ. При кратковременном лечении кислородом критерии к его дози-рованию не столь жестки и основная цель пульсоксиметрии состоит в предупреждении гипоксемии и своевременном прекращении оксигенотерапии.
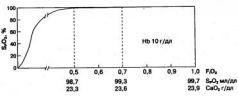 Рис. 1.16. Пример влияния FiO2 на SpO2
Рис. 1.16. Пример влияния FiO2 на SpO2
отчетливо видна нецелесообразность применения Fi02 выше 50 %
Пульсоксиметрия при ИВЛ. Обеспечение оксигенации артериальной крови - одна из основных конечных задач ИВЛ, и уже только поэтому пульсоксиметрия является обязательным методом мониторинга у пациентов, подключенных к дыхательной аппаратуре. Это требовании содержится практически во всех стандартах обеспечения безопасности пациентов.
Искусственная вентиляция легких способна влиять на все параметры пульсоксиметрии, так что умение анализировать эти изменения помогает вовремя сориентироваться в ситуации. Однако диагностические возможности метода в данном случае не ограничиваются простым контролем SpO2. ИВЛ радикальным образом изменяет работу всех звеньев процесса легочного газообмена, и в ситуациях, порожденных этим вмешательством, пульсоксиметр предоставляет богатую информацию для размышления.
ИВЛ на фоне гиповолемии. Иногда во время проведения ИВЛ наблюдается снижение амплитуды фотоплетизмограммы. Наиболее частая причина этого - уменьшение сердечного выброса из-за роста внутригрудного давления на фоне скрытой гиповолемии. Амплитуда ФПГ может снижаться даже при компенсированной гиповолемии, что, как правило, сочетается с тахикардией, возникновением дыхательных волн, а также с умеренной гипоксемией, легко уступающей повышению FiO2.
При декомпенсированной гиповолемии, приводящей к уменьшению минутного объема кровообращения и аварийному перераспределению кровотока, применение ИВЛ чревато катастрофическими последствиями для легочной и системной гемодинамики. В некоторых случаях перфузия периферии нарушается настолько сильно, что монитор не улавливает пульсацию артериол. Резкое снижение фотоплетизмограммы или ее исчезновение с дисплея монитора в таких ситуациях сопровождается сообщением "low perfusion" ("нарушение перфузии") или "low quality signal" ("сигнал низкого качества") и свидетельствует о плачевном состоянии периферического кровотока. При появлении этих симптомов (а они обычно полностью вписываются в общеклиническую картину) необходимо добиваться не только подъема артериального, и центрального венозного давления, но и нормализации пульсоксиметрического статуса.
Гиповолемия всегда сопровождается уменьшением давления в легочных капиллярах, особенно в верхних зонах легких, и повышенное альвеолярное давление при искусственном вдохе пережимает межальвеолярные сосуды, направляя кровоток в нижние отделы, вентиляция которых недостаточна для обработки возросшего потока крови. Регионарная гиповентиляция вызывает падение SpO2, что, в сочетании с малым минутным объемом кровообращения, а нередко и анемией, приводит к резкому сокращению доставки кислорода к тканям.
Экстренная мера коррекции гипоксии (помимо инфузионной и медикаментозной терапии) - временное изменение режима вентиляции, которое имеет своей целью снижение альвеолярного и внутригрудного давления и включает: (1) отказ от использования ПДКВ; (2) в отдельных случаях - применение активного выдоха с разрежением от -3 до -8 см вод. ст.;
(3) уменьшение дыхательного объема с соответствующим увеличением частоты вентиляции или (4) переход на ВЧ ИВЛ с частотой 80-100 в 1 мин и отношением вдох: выдох, равным 1: 3. Гипоксемия, обусловленная регионарной гиповентиляцией, поддается коррекции посредством повышения Fi02. Как правило, принятие этих мер позволяет добиться заметного улучшения пульсоксиметрических показателей задолго до ликвидации гиповолемии.
ИВЛ при тяжелом поражении легких. В данной ситуации, требующей применения ИВЛ, пульсоксиметр служит непрерывным поставщиком информации, важность которой трудно переоценить. Респираторному дистресс-синдрому, обширной пневмонии, аспирационному пневмониту и прочим вариантам критического поражения легких сопутствуют комплексные расстройства газообмена и кровообращения, когда выбор оптимального метода и режима ИВЛ является сложнейшей задачей, которую невозможно решать вслепую. Этот выбор подразумевает поиск компромисса между (1) необходимостью создания в течение всего дыхательного цикла повышенного внутрилегочного давления, обеспечивающего поддержание альвеол в раскрытом состоянии, и (2) стремлением причинить при этом минимальный урон объему и распределению легочного кровотока.
Увеличение пикового и среднего внутрилегочного давления способно оказать двойственное действие на сатурацию артериальной крови.
С одной стороны, высокое давление надува позволяет ввести в жесткие легкие нужный дыхательный объем и тем самым избежать гиповентиляции. Повышенное давление, в том числе и во время выдоха (ПДКВ), требуется также для расправления множественных микро- и макроателектазов и поддержания жестких легких в раскрытом состоянии в течение всего дыхательного цикла. Достижение данной цели сопровождается уменьшением гиповентиляции, шунтирования и диффузионных расстройств. Это проявляется постепенным возрастанием SpO2 и дает возможность снизить FiOa, что при длительной ИВЛ имеет большое значение. В процессе объемной ИВЛ при расправлении ателектазов происходит также падение давления вдоха на манометре респиратора, поскольку дыхательный объем начинает распределяться в возросшем объеме легочной ткани. При вентиляции с ограниченным давлением вдоха (PCV) увеличению объема функционирующей легочной ткани и повышению растяжимости легких сопутствуют самопроизвольный прирост дыхательного объема и возникновение гипервентиляции.
С другой стороны, высокое внутрилегочное давление способно вызывать компрессию капилляров в межальвеолярных перегородках, дополнительное увеличение легочного сосудистого сопротивления и уменьшение минутного объема кровообращения, что на дисплее пульсоксиметра отражается снижением амплитуды ФПГ и появлением волн, синхронных с ритмом респиратора. Поскольку сжатие капилляров высоким давлением возможно только в работающих альвеолах, кровоток, минуя их, направляется в пневмонические очаги, ателектазы и инфильтраты (рис. 1.17). Это приводит к усилению шунтирования и падению Sp02.
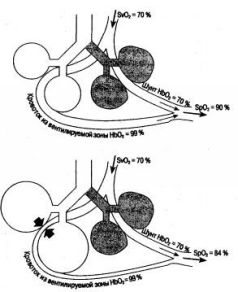 Рис. 1.17. Шунтирование крови при очаговом поражении легких (вверху) и усиление шунтирования при ИВЛ с избыточным давлением вдоха(внизу)
Рис. 1.17. Шунтирование крови при очаговом поражении легких (вверху) и усиление шунтирования при ИВЛ с избыточным давлением вдоха(внизу)
Комплексная оценка пульсоксиметрических показателей в динамике помогает ориентироваться в событиях, происходящих в пораженных легких под воздействием ИВЛ, и установить баланс между противоречивыми требованиями при выборе и последующей доработке режима вентиляции.
В рассмотренной выше ситуации тяжелого поражения легких отказ от применения ПДКВ или, тем более, использование активного выдоха недопустимы, потому что при рестриктивной патологии такие действия приводят к ателектазированию, уменьшению ФОЕ и резкому ухудшению легочного газообмена. Наиболее выгодные условия для работы правого желудочка создаются при ИВЛ с инверсией отношения вдох: выдох, благодаря которой удается снизить ПДКВ и сократить дыхательный объем за счет более выгодного распределения внутрилегочного давления в течение дыхательного цикла. Повысить выброс правого желудочка, подавленный искусственной вентиляцией, помогают инфузии добутамина (добутрекса), усиливающего сократимость миокарда. Эти действия позволяют увеличить объем кровообращения, улучшить распределение легочного кровотока и уменьшить степень артериальной гипоксемии. Результаты коррекции отчетливо прослеживаются на трендах ФПГ и SpO2.
Необходимо учитывать, что при глубокой гипоксемии и плохой перфузии периферии точность измерения SpO2 может существенно снизиться. В этих условиях данные пульсоксиметрии требуют периодического сопоставления с результатами лабораторного измерения газового состава артериальной крови.
Резкие бессистемные колебания всех параметров пульсоксиметрии наблюдаются при нарушении адаптации пациента к режиму ИВЛ. Эти артефакты бывают обусловлены движением больного, волнами венозного давления при "сопротивлении" респиратору, нарушением процесса вентиляции и повышением потребности в кислороде. Причину легко определить при взгляде на пациента и по неправильной форме ФПГ. Ориентироваться на данные пульсоксиметрии в такие моменты нельзя.
Причины внезапного падения SpO2 во время и в связи с ИВЛ:
• разгерметизация системы "пациент-респиратор";
• развитие пневмоторакса;
• смещение интубационной трубки в бронх;
• нарушение подачи кислорода;
• неисправность респиратора.
Массивное кровотечение на фоне ИВЛ сопровождается значительно более выраженными изменениями на дисплее пульсоксиметра, чем при самостоятельном дыхании. Генез и характер этих изменений, включающих и гипоксемию, обсужден выше.
Видимо, излишне напоминать о том, что принятие ответственных решений должно базироваться на достоверной информации, источником которой является пульсоксиметр, произведенный фирмой, имеющей надежную репутацию на рынке мониторов.
Пульсоксиметрия в анестезиологии
• предельная безопасная для длительного использования концентрация кислорода в дыхательной смеси, по последним
данным, равна 50 %;
• токсическое влияние высоких концентраций кислорода
на легкие не имеет специфических проявлений и всплывает в виде ателектазов, гнойного трахеобронхита или респираторного дистресс-синдрома, которые в дальнейшем соотносят
с чем угодно, но не с оксигенотерапией;
• и наконец, к кислороду в полной мере относится "золотое правило" интенсивной терапии: лучший лист назначений - не тот, к которому нечего добавить, а тот, из которого нечего вычеркнуть.
Пульсоксиметрия - ключ к решению многих перечисленных выше проблем. Мониторинг оксигенации помогает не только своевременно обнаружить гипоксемию, но также установить ее причину, подобрать оптимальную концентрацию кислорода в дыхательной смеси и в нужный момент безопасно перевести больного на дыхание атмосферным воздухом.
Нормальная величина SpO2 находится в диапазоне 94-98 %, причем у пациентов молодого и среднего возраста, не имеющих легочной патологии, преобладают значения сатурации 96-98 %, а у пожилых больных чаще встречается Sp02 94-96 %, что обусловлено возрастными изменениями в легких.
У пациентов с хронической легочной патологией отмечается адаптация к более низкому уровню сатурации. Попытка искусственной "нормализации" SpO2 у таких больных может закончиться угнетением спонтанного дыхания.
При нормальном уровне SpO2 оксигенотерапия показана:
1. При выраженной острой недостаточности кровообращения или очень глубокой анемии, когда приходится надеяться даже на незначительное увеличение системного транспорта кислорода за счет до насыщения кислородом оставшихся 2-4 % гемоглобина.
2. В качестве профилактической меры при реальном риске внезапного развития гипоксемииу пациентов с нестабильным дыханием, например в раннем послеоперационном периоде или при неврологической патологии, затрагивающей дыхательный центр или дыхательную мускулатуру. В таких случаях обычно бывает достаточно повысить FiOa до 30-40 %.
К числу показаний мы не относим отравление угарным газом, при котором значение Sp02 всегда является артефактным.
Снижение Sp02 до 90-94 % расценивается как умеренная артериальная гипоксемия. Если она обнаруживается у больных, дышащих атмосферным воздухом, вопрос о необходимости оксигенотерапии решается индивидуально. Надо помнить, что неглубокую гипоксемию человек может довольно длительно переносить без печальных последствий. Исключение составляют пациенты с тяжелой анемией, недостаточностью кровообращения, нарушениями коронарного или мозгового кровотока, гиперметаболизмом.
Выраженная артериальная гипоксемия (SpO2 =85-90 %) - это следствие и признак серьезного нарушения газообмена и безусловное показание для назначения кислорода. Нормализация пульсоксиметрических параметров на фоне оксигенотерапии не отменяет необходимости выяснения причины расстройства и ее устранения с использованием приемов, рассмотренных выше.
При глубокой гипоксемии (SpO2 «85 %) оксигенотерапия служит экстренной первичной мерой коррекции и фоном для применения более сложных и требующих времени методов лечения, выбор которых определяется причиной нарушения газообмена.
Пульсоксиметрия позволяет реализовать важнейший принцип оксигенотерапии - использование кислорода в концентрации, не превышающей ту минимальную; которая требуется, чтобы удерживать SpO2 в пределах нормальных значений. После заполнения гемоглобиновой емкости артериальной крови на 98-100 % дальнейшее увеличение FiO2 становится бессмысленным, поскольку приводит лишь к незначительному приросту оксигенации крови за счет физически растворенного в ней кислорода.
Стремление увеличить количество физически растворенного в крови кислорода оправдано лишь:
• при крайне низком содержании гемоглобина;
• при выраженной недостаточности кровообращения;
• при отравлении окисью углерода;
• при необходимости денитрогенации организма.
В подавляющем большинстве случаев применение кислорода в концентрациях, превышающих минимально достаточную для практически полного насыщения гемоглобина артериальной крови (SpO2 =98-100%), не содействует сколько-нибудь заметному улучшению оксигенации тканей, но повышает риск гипероксического повреждения легких и приводит к непроизводительному расходу газа.
Пульсоксиметр измеряет степень заполнения кислородом гемоглобиновой емкости артериальной крови и потому не способен выявлять гипероксию.
После того как достигается 100 % сатурация гемоглобина (у здорового человека этого добиваются назначением 30 % кислорода), дальнейшее увеличение Fi02 приводит лишь к росту напряжения и содержания физически растворенного кислорода в крови, на который пульсоксиметр не реагирует. В подобных случаях монитор будет показывать на дисплее один и тот же, максимально возможный, уровень сатурации (Sp02 = 100 %), начиная с Fi02 - 0,3 и далее, при увеличении концентрации кислорода во вдыхаемом газе вплоть до использования чистого кислорода.
В случаях, когда пульсоксиметр отображает на индикаторе SpO2 = 100 %, врач не может быть уверен в том, что концентрация кислорода не избыточна (рис. 1.16).
Чтобы выйти из этого положения, достаточно плавно уменьшить содержание кислорода в дыхательной смеси до того уровня, при котором Sp02 составит 98-99 % или вовсе вернется в границы нормы. При снижении SpO2 со 100 до 98 % уменьшение содержания кислорода в артериальной крови столь несущественно, что в подавляющем большинстве случаев может быть произведено незаметно для здоровья больного. Зато врач приобретает надежный ориентир, помогающий отслеживать в мониторном режиме правильность дозирования кислорода. В дальнейшем регулировать FiOa нужно таким образом, чтобы поддерживать Sp02 на 1-3 % ниже 100 %. Тем самым обеспечиваются нормальное насыщение гемоглобина артериальной крови Кислородом и минимальная достаточная концентрация кислорода во вдыхаемом газе. Благодаря такому подходу не только сокращается риск ги-пероксического повреждения легких, но и экономно расходуется сжатый кислород.
При катастрофическом поражении легких, сопровождающемся массивным шунтированием крови и глубокой гипоксемией, даже вентиляция 100 % кислородом не позволяет нормализовать Sp02. В этих случаях приходится идти на вынужденный компромисс, выбирая между наименьшим допустимым уровнем SpO2 и максимально приемлемой для длительного применения концентрацией кислорода во вдуваемом газе. И если повышение Fi02 c 50 дo 100 % дает увеличение SpO2 с 75 до 78 %, задумайтесь, не слишком ли высока цена за столь незначительный результат.
Диагноз "токсическое поражение легких кислородом" практически не встречается ни в историях болезни, ни в протоколах патологоанатомического исследования, но это говорит лишь о неумении распознавать патологию, а не о ее отсутствии.
Разумеется, сказанное выше относится к многочасовой и многосуточной оксигенотерапии, в том числе и при длительной ИВЛ. При кратковременном лечении кислородом критерии к его дози-рованию не столь жестки и основная цель пульсоксиметрии состоит в предупреждении гипоксемии и своевременном прекращении оксигенотерапии.

отчетливо видна нецелесообразность применения Fi02 выше 50 %
Пульсоксиметрия при ИВЛ. Обеспечение оксигенации артериальной крови - одна из основных конечных задач ИВЛ, и уже только поэтому пульсоксиметрия является обязательным методом мониторинга у пациентов, подключенных к дыхательной аппаратуре. Это требовании содержится практически во всех стандартах обеспечения безопасности пациентов.
Искусственная вентиляция легких способна влиять на все параметры пульсоксиметрии, так что умение анализировать эти изменения помогает вовремя сориентироваться в ситуации. Однако диагностические возможности метода в данном случае не ограничиваются простым контролем SpO2. ИВЛ радикальным образом изменяет работу всех звеньев процесса легочного газообмена, и в ситуациях, порожденных этим вмешательством, пульсоксиметр предоставляет богатую информацию для размышления.
ИВЛ на фоне гиповолемии. Иногда во время проведения ИВЛ наблюдается снижение амплитуды фотоплетизмограммы. Наиболее частая причина этого - уменьшение сердечного выброса из-за роста внутригрудного давления на фоне скрытой гиповолемии. Амплитуда ФПГ может снижаться даже при компенсированной гиповолемии, что, как правило, сочетается с тахикардией, возникновением дыхательных волн, а также с умеренной гипоксемией, легко уступающей повышению FiO2.
При декомпенсированной гиповолемии, приводящей к уменьшению минутного объема кровообращения и аварийному перераспределению кровотока, применение ИВЛ чревато катастрофическими последствиями для легочной и системной гемодинамики. В некоторых случаях перфузия периферии нарушается настолько сильно, что монитор не улавливает пульсацию артериол. Резкое снижение фотоплетизмограммы или ее исчезновение с дисплея монитора в таких ситуациях сопровождается сообщением "low perfusion" ("нарушение перфузии") или "low quality signal" ("сигнал низкого качества") и свидетельствует о плачевном состоянии периферического кровотока. При появлении этих симптомов (а они обычно полностью вписываются в общеклиническую картину) необходимо добиваться не только подъема артериального, и центрального венозного давления, но и нормализации пульсоксиметрического статуса.
Гиповолемия всегда сопровождается уменьшением давления в легочных капиллярах, особенно в верхних зонах легких, и повышенное альвеолярное давление при искусственном вдохе пережимает межальвеолярные сосуды, направляя кровоток в нижние отделы, вентиляция которых недостаточна для обработки возросшего потока крови. Регионарная гиповентиляция вызывает падение SpO2, что, в сочетании с малым минутным объемом кровообращения, а нередко и анемией, приводит к резкому сокращению доставки кислорода к тканям.
Экстренная мера коррекции гипоксии (помимо инфузионной и медикаментозной терапии) - временное изменение режима вентиляции, которое имеет своей целью снижение альвеолярного и внутригрудного давления и включает: (1) отказ от использования ПДКВ; (2) в отдельных случаях - применение активного выдоха с разрежением от -3 до -8 см вод. ст.;
(3) уменьшение дыхательного объема с соответствующим увеличением частоты вентиляции или (4) переход на ВЧ ИВЛ с частотой 80-100 в 1 мин и отношением вдох: выдох, равным 1: 3. Гипоксемия, обусловленная регионарной гиповентиляцией, поддается коррекции посредством повышения Fi02. Как правило, принятие этих мер позволяет добиться заметного улучшения пульсоксиметрических показателей задолго до ликвидации гиповолемии.
ИВЛ при тяжелом поражении легких. В данной ситуации, требующей применения ИВЛ, пульсоксиметр служит непрерывным поставщиком информации, важность которой трудно переоценить. Респираторному дистресс-синдрому, обширной пневмонии, аспирационному пневмониту и прочим вариантам критического поражения легких сопутствуют комплексные расстройства газообмена и кровообращения, когда выбор оптимального метода и режима ИВЛ является сложнейшей задачей, которую невозможно решать вслепую. Этот выбор подразумевает поиск компромисса между (1) необходимостью создания в течение всего дыхательного цикла повышенного внутрилегочного давления, обеспечивающего поддержание альвеол в раскрытом состоянии, и (2) стремлением причинить при этом минимальный урон объему и распределению легочного кровотока.
Увеличение пикового и среднего внутрилегочного давления способно оказать двойственное действие на сатурацию артериальной крови.
С одной стороны, высокое давление надува позволяет ввести в жесткие легкие нужный дыхательный объем и тем самым избежать гиповентиляции. Повышенное давление, в том числе и во время выдоха (ПДКВ), требуется также для расправления множественных микро- и макроателектазов и поддержания жестких легких в раскрытом состоянии в течение всего дыхательного цикла. Достижение данной цели сопровождается уменьшением гиповентиляции, шунтирования и диффузионных расстройств. Это проявляется постепенным возрастанием SpO2 и дает возможность снизить FiOa, что при длительной ИВЛ имеет большое значение. В процессе объемной ИВЛ при расправлении ателектазов происходит также падение давления вдоха на манометре респиратора, поскольку дыхательный объем начинает распределяться в возросшем объеме легочной ткани. При вентиляции с ограниченным давлением вдоха (PCV) увеличению объема функционирующей легочной ткани и повышению растяжимости легких сопутствуют самопроизвольный прирост дыхательного объема и возникновение гипервентиляции.
С другой стороны, высокое внутрилегочное давление способно вызывать компрессию капилляров в межальвеолярных перегородках, дополнительное увеличение легочного сосудистого сопротивления и уменьшение минутного объема кровообращения, что на дисплее пульсоксиметра отражается снижением амплитуды ФПГ и появлением волн, синхронных с ритмом респиратора. Поскольку сжатие капилляров высоким давлением возможно только в работающих альвеолах, кровоток, минуя их, направляется в пневмонические очаги, ателектазы и инфильтраты (рис. 1.17). Это приводит к усилению шунтирования и падению Sp02.

Комплексная оценка пульсоксиметрических показателей в динамике помогает ориентироваться в событиях, происходящих в пораженных легких под воздействием ИВЛ, и установить баланс между противоречивыми требованиями при выборе и последующей доработке режима вентиляции.
В рассмотренной выше ситуации тяжелого поражения легких отказ от применения ПДКВ или, тем более, использование активного выдоха недопустимы, потому что при рестриктивной патологии такие действия приводят к ателектазированию, уменьшению ФОЕ и резкому ухудшению легочного газообмена. Наиболее выгодные условия для работы правого желудочка создаются при ИВЛ с инверсией отношения вдох: выдох, благодаря которой удается снизить ПДКВ и сократить дыхательный объем за счет более выгодного распределения внутрилегочного давления в течение дыхательного цикла. Повысить выброс правого желудочка, подавленный искусственной вентиляцией, помогают инфузии добутамина (добутрекса), усиливающего сократимость миокарда. Эти действия позволяют увеличить объем кровообращения, улучшить распределение легочного кровотока и уменьшить степень артериальной гипоксемии. Результаты коррекции отчетливо прослеживаются на трендах ФПГ и SpO2.
Необходимо учитывать, что при глубокой гипоксемии и плохой перфузии периферии точность измерения SpO2 может существенно снизиться. В этих условиях данные пульсоксиметрии требуют периодического сопоставления с результатами лабораторного измерения газового состава артериальной крови.
Резкие бессистемные колебания всех параметров пульсоксиметрии наблюдаются при нарушении адаптации пациента к режиму ИВЛ. Эти артефакты бывают обусловлены движением больного, волнами венозного давления при "сопротивлении" респиратору, нарушением процесса вентиляции и повышением потребности в кислороде. Причину легко определить при взгляде на пациента и по неправильной форме ФПГ. Ориентироваться на данные пульсоксиметрии в такие моменты нельзя.
Причины внезапного падения SpO2 во время и в связи с ИВЛ:
• разгерметизация системы "пациент-респиратор";
• развитие пневмоторакса;
• смещение интубационной трубки в бронх;
• нарушение подачи кислорода;
• неисправность респиратора.
Массивное кровотечение на фоне ИВЛ сопровождается значительно более выраженными изменениями на дисплее пульсоксиметра, чем при самостоятельном дыхании. Генез и характер этих изменений, включающих и гипоксемию, обсужден выше.
Видимо, излишне напоминать о том, что принятие ответственных решений должно базироваться на достоверной информации, источником которой является пульсоксиметр, произведенный фирмой, имеющей надежную репутацию на рынке мониторов.
Пульсоксиметрия в анестезиологии
В начале 80-х годов, когда пульсоксиметрия еще только внедрялась в клиническую практику, некоторые страховые компании предусматривали специальные меры для поощрения анестезиологов, применявших пульсоксиметры в операционной, поскольку затраты на своевременное предупреждение осложнений анестезии оказывались значительно ниже, чем на их лечение.
Анестезиологическое пособие всегда сопряжено с фармакологическим и инструментальным вмешательством в работу систем дыхания и кровообращения. Разнообразные нарушения в работе этих систем могут возникать и вследствие хирургического вмешательства, например при анестезии, кровопотере, манипуляциях в рефлексогенных зонах, изменении операционного положения больного, операциях на сердце, сосудах, легких, головном мозге. Грамотно поставленный мониторинг значительно повышает своевременность и эффективность распознавания, предупреждения и коррекции осложнений у таких больных.
Благодаря высокой информативности, неинвазивности, простоте и экономичности в применении пульсоксиметрия отнесена к обязательным методам мониторинга при любой анестезии. Этот тезис, впервые приведенный в Гарвардском стандарте анестезии (1985 год), в настоящее время является общепризнанным.
В анестезиологической практике представлены все варианты расстройств кровообращения и дыхания, рассмотренные в предыдущих разделах. Основные принципы пульсоксиметрической диагностики данных расстройств приведены выше и не нуждаются в дополнительных комментариях. Вместе с тем пульсоксиметрия позволяет решать некоторые проблемы, специфичные именно для анестезиологии.
Пульсоксиметрия при общей анестезии. У большинства пациентов каждому этапу анестезиологического пособия соответствует собственная типичная динамика пульсоксиметрических показателей (рис. 1.18).
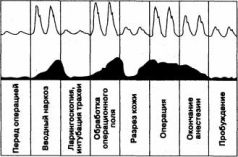 Рис. 1.18. Характерные изменения ФПГ на различных этапах общей анестезии. В верхней части - фрагменты ФПГ, в нижней - тренд амплитуды ФПГ
Рис. 1.18. Характерные изменения ФПГ на различных этапах общей анестезии. В верхней части - фрагменты ФПГ, в нижней - тренд амплитуды ФПГ
Период, непосредственно предшествующий анестезии, характеризуется психоэмоциональным стрессом, приводящим к активации симпатической системы и выбросу в кровь катехоламинов. Вот почему в этом периоде у многих больных наблюдаются периферический вазоспазм и тахикардия. Своим внешне спокойным поведением больной может ввести в заблуждение врача, но не пульсоксиметр.
Перед началом наркоза пульсоксиметр обнаруживает снижение амплитуды ФПГ и увеличение ЧСС.
При адекватной премедикации, включающей транквилизаторы и наркотические анальгетики, амплитуда ФПГ часто (но не всегда) нормализуется. Не следует забывать и о другой, вполне вероятной, причине снижения пульсовых волн - холодовой вазоконстрикции, которая имеет место в том случае, если температура в помещении некомфортная.
У пациентов с хронической дыхательной недостаточностью или тяжелым поражением головного мозга использование указанных выше препаратов чревато угнетением дыхания и уменьшением SpO2.
Вводный наркоз способствует исчезновению негативного эмоционального фона. Некоторые препараты, используемые для индукции, оказывают вазодилатирующее действие (тиопентал, дроперидол, летучие анестетики). Поэтому во время вводного наркоза происходит увеличение амплитуды ФПГ. Обычно при индукции производится преоксигенация, в процессе которой азот, содержащийся в легких, частично замещается кислородом, и Sp02 быстро поднимается до 100%.,
Ларингоскопия и интубация трахеи сопровождаются механическим раздражением мощных рефлексогенных зон и возбуждением симпатической системы, которое проявляется вазо-спазмом, артериальной гипертензией, тахикардией и, довольно часто, транзиторными нарушениями ритма сердца. В такие минуты внимание анестезиолога полностью сосредоточено на выполняемых действиях, но при просмотре трендов, хранящихся в памяти пульсоксиметра, нередко обнаруживается снижение амплитуды ФПГ и постепенное ее восстановление после завершения манипуляции. Рефлекторные реакции, возникающие при интубации трахеи, в большинстве случаев не имеют клинического значения, однако у больных с ИБС, гипертонической болезнью, аритмиями, глубокой сердечной недостаточностью, гормонально-активными опухолями, аневризмами мозговых сосудов их необходимо избегать, углубляя вводный наркоз или используя местную анестезию слизистых оболочек. Исходя из анализа трендов ФПГ, врач составляет представление об эффективности этих мер и совершенствует их.
При затянувшейся интубации трахеи пульсоксиметр дает возможность контролировать допустимую продолжительность этой манипуляции по уровню SpO2, для чего нужно установить минимальное время обновления данных на дисплее монитора (режим "fast response"), чтобы сократить промежуток от момента возникновения гипоксемии до ее регистрации монитором.
Кожный разрез зачастую выполняется до достижения стабильной глубины анестезии. Этот мощный болевой стимул приводит к выраженной периферической вазоконстрикции. Амплитуда ФПГ позволяет оценить адекватность обезболивания к непосредственному началу оперативного вмешательства. Любопытно, что снижение пульсовых волн, спровоцированное болью, на данном и последующих этапах может быть зарегистрировано даже в тех случаях, когда ЧСС и артериальное давление остаются стабильными. В настоящее время не вызывает сомнения тот факт, что боль, испытанная пациентом в ходе операции, усиливает болевой синдром в постоперационном периоде. Это положение легло в основу метода "предварительной анестезии" ("preemptive anesthesia") - инфильтрационной или регионарной блокады зоны кожного разреза, помогающей существенно уменьшить потребность в наркотических анальгетиках после операции. Наблюдение за амплитудой ФПГ служит доступным способом определения эффективности данной меры.
Снижение пульсовой волны и появление тахикардии в процессе оперативного вмешательства может свидетельствовать о недостаточной глубине анестезии, развитии гиповолемии или гипервентиляции.
Амплитуда ФПГ очень чувствительна к адекватности обезболивания: она резко снижается при возникновении боли и быстро возрастает после углубления анестезии.
Надо помнить и о такой тривиальной причине уменьшения ФПГ, как холодовая вазоконстрикция. При длительном оперативном вмешательстве в условиях общей анестезии возникает гипотермия, поэтому амплитуда ФПГ во время операции постепенно уменьшается.
Передозировка общих анестетиков сопровождается выраженной вазодилатацией и проявляется на дисплее монитора увеличением амплитуды ФПГ. Сходные признаки имеет и гиперкапния, обусловленная недостаточным объемом вентиляции или нарушением работы контура наркозного аппарата.
У пациента, находящегося под наркозом, величина SpO2 зависит от четырех факторов: концентрации кислорода в газовой смеси, минутного объема вентиляции, адекватности ОЦК и правильности положения интубационной трубки. (Обсуждение всех четырех факторов содержится выше.)
Применение надежного пульсоксиметра позволяет без риска развития гипоксемии назначать закись азота в более высоких концентрациях, чем те, которые устанавливаются ротаметрами по стандартным соотношениям N2O: О2*.
* В этих случаях крайне желательно также применение оксиметра.
В раннем послеоперационном периоде происходит восстановление самостоятельного дыхания, сознания и болевой чувствительности. На этом этапе пациент обычно неспособен к полноценному контакту с окружающими, но о появлении у него боли и неприятных ощущений можно судить по снижению амплитуды ФПГ. Для комфортного выхода из наркоза характерно наличие нормальной или незначительно сниженной амплитуды пульсовой волны.
Вторая серьезная проблема, возникающая сразу после окончания анестезии,- артериальная гипоксемия. Она редко сопровождает регионарную анестезию, но очень часто наблюдается после масочных, и особенно - интубационных наркозов. Операции на органах грудной клетки и верхнего этажа брюшной полости приводят к более выраженной и длительной послеоперационной гипоксемии, чем вмешательства на нижнем этаже брюшной полости и на конечностях. Частота и степень десатурации напрямую зависят от дозы фентанила или концентрации фторотана, применявшихся при наркозе. К факторам риска также относятся пожилой возраст больного и наличие у него ожирения.
В ближайшем посленаркозном периоде, длительность которого составляет около 20 мин, выраженная гипоксемия
(Sp02 = 85-90 %) при дыхании атмосферным воздухом отмечается в среднем у 40-60 % пациентов, глубокая гипоксемия (SpO2 «85 %) - у 10-20 %, а в остальных случаях SpO2 редко превышает 94 %.
Основные причины гипоксемии на этом этапе: (1) центральная депрессия дыхания, обусловленная действием наркотических препаратов и гипервентиляцией во время наркоза; (2) остаточная миорелаксация; (3) нарушения проходимости верхних дыхательных путей; (4) множественные микроателектазы, факт появления которых у больных во время наркоза доказан, хотя их этиология до сих пор остается неясной,
Анестезиологическое пособие всегда сопряжено с фармакологическим и инструментальным вмешательством в работу систем дыхания и кровообращения. Разнообразные нарушения в работе этих систем могут возникать и вследствие хирургического вмешательства, например при анестезии, кровопотере, манипуляциях в рефлексогенных зонах, изменении операционного положения больного, операциях на сердце, сосудах, легких, головном мозге. Грамотно поставленный мониторинг значительно повышает своевременность и эффективность распознавания, предупреждения и коррекции осложнений у таких больных.
Благодаря высокой информативности, неинвазивности, простоте и экономичности в применении пульсоксиметрия отнесена к обязательным методам мониторинга при любой анестезии. Этот тезис, впервые приведенный в Гарвардском стандарте анестезии (1985 год), в настоящее время является общепризнанным.
В анестезиологической практике представлены все варианты расстройств кровообращения и дыхания, рассмотренные в предыдущих разделах. Основные принципы пульсоксиметрической диагностики данных расстройств приведены выше и не нуждаются в дополнительных комментариях. Вместе с тем пульсоксиметрия позволяет решать некоторые проблемы, специфичные именно для анестезиологии.
Пульсоксиметрия при общей анестезии. У большинства пациентов каждому этапу анестезиологического пособия соответствует собственная типичная динамика пульсоксиметрических показателей (рис. 1.18).

Период, непосредственно предшествующий анестезии, характеризуется психоэмоциональным стрессом, приводящим к активации симпатической системы и выбросу в кровь катехоламинов. Вот почему в этом периоде у многих больных наблюдаются периферический вазоспазм и тахикардия. Своим внешне спокойным поведением больной может ввести в заблуждение врача, но не пульсоксиметр.
Перед началом наркоза пульсоксиметр обнаруживает снижение амплитуды ФПГ и увеличение ЧСС.
При адекватной премедикации, включающей транквилизаторы и наркотические анальгетики, амплитуда ФПГ часто (но не всегда) нормализуется. Не следует забывать и о другой, вполне вероятной, причине снижения пульсовых волн - холодовой вазоконстрикции, которая имеет место в том случае, если температура в помещении некомфортная.
У пациентов с хронической дыхательной недостаточностью или тяжелым поражением головного мозга использование указанных выше препаратов чревато угнетением дыхания и уменьшением SpO2.
Вводный наркоз способствует исчезновению негативного эмоционального фона. Некоторые препараты, используемые для индукции, оказывают вазодилатирующее действие (тиопентал, дроперидол, летучие анестетики). Поэтому во время вводного наркоза происходит увеличение амплитуды ФПГ. Обычно при индукции производится преоксигенация, в процессе которой азот, содержащийся в легких, частично замещается кислородом, и Sp02 быстро поднимается до 100%.,
Ларингоскопия и интубация трахеи сопровождаются механическим раздражением мощных рефлексогенных зон и возбуждением симпатической системы, которое проявляется вазо-спазмом, артериальной гипертензией, тахикардией и, довольно часто, транзиторными нарушениями ритма сердца. В такие минуты внимание анестезиолога полностью сосредоточено на выполняемых действиях, но при просмотре трендов, хранящихся в памяти пульсоксиметра, нередко обнаруживается снижение амплитуды ФПГ и постепенное ее восстановление после завершения манипуляции. Рефлекторные реакции, возникающие при интубации трахеи, в большинстве случаев не имеют клинического значения, однако у больных с ИБС, гипертонической болезнью, аритмиями, глубокой сердечной недостаточностью, гормонально-активными опухолями, аневризмами мозговых сосудов их необходимо избегать, углубляя вводный наркоз или используя местную анестезию слизистых оболочек. Исходя из анализа трендов ФПГ, врач составляет представление об эффективности этих мер и совершенствует их.
При затянувшейся интубации трахеи пульсоксиметр дает возможность контролировать допустимую продолжительность этой манипуляции по уровню SpO2, для чего нужно установить минимальное время обновления данных на дисплее монитора (режим "fast response"), чтобы сократить промежуток от момента возникновения гипоксемии до ее регистрации монитором.
Кожный разрез зачастую выполняется до достижения стабильной глубины анестезии. Этот мощный болевой стимул приводит к выраженной периферической вазоконстрикции. Амплитуда ФПГ позволяет оценить адекватность обезболивания к непосредственному началу оперативного вмешательства. Любопытно, что снижение пульсовых волн, спровоцированное болью, на данном и последующих этапах может быть зарегистрировано даже в тех случаях, когда ЧСС и артериальное давление остаются стабильными. В настоящее время не вызывает сомнения тот факт, что боль, испытанная пациентом в ходе операции, усиливает болевой синдром в постоперационном периоде. Это положение легло в основу метода "предварительной анестезии" ("preemptive anesthesia") - инфильтрационной или регионарной блокады зоны кожного разреза, помогающей существенно уменьшить потребность в наркотических анальгетиках после операции. Наблюдение за амплитудой ФПГ служит доступным способом определения эффективности данной меры.
Снижение пульсовой волны и появление тахикардии в процессе оперативного вмешательства может свидетельствовать о недостаточной глубине анестезии, развитии гиповолемии или гипервентиляции.
Амплитуда ФПГ очень чувствительна к адекватности обезболивания: она резко снижается при возникновении боли и быстро возрастает после углубления анестезии.
Надо помнить и о такой тривиальной причине уменьшения ФПГ, как холодовая вазоконстрикция. При длительном оперативном вмешательстве в условиях общей анестезии возникает гипотермия, поэтому амплитуда ФПГ во время операции постепенно уменьшается.
Передозировка общих анестетиков сопровождается выраженной вазодилатацией и проявляется на дисплее монитора увеличением амплитуды ФПГ. Сходные признаки имеет и гиперкапния, обусловленная недостаточным объемом вентиляции или нарушением работы контура наркозного аппарата.
У пациента, находящегося под наркозом, величина SpO2 зависит от четырех факторов: концентрации кислорода в газовой смеси, минутного объема вентиляции, адекватности ОЦК и правильности положения интубационной трубки. (Обсуждение всех четырех факторов содержится выше.)
Применение надежного пульсоксиметра позволяет без риска развития гипоксемии назначать закись азота в более высоких концентрациях, чем те, которые устанавливаются ротаметрами по стандартным соотношениям N2O: О2*.
* В этих случаях крайне желательно также применение оксиметра.
В раннем послеоперационном периоде происходит восстановление самостоятельного дыхания, сознания и болевой чувствительности. На этом этапе пациент обычно неспособен к полноценному контакту с окружающими, но о появлении у него боли и неприятных ощущений можно судить по снижению амплитуды ФПГ. Для комфортного выхода из наркоза характерно наличие нормальной или незначительно сниженной амплитуды пульсовой волны.
Вторая серьезная проблема, возникающая сразу после окончания анестезии,- артериальная гипоксемия. Она редко сопровождает регионарную анестезию, но очень часто наблюдается после масочных, и особенно - интубационных наркозов. Операции на органах грудной клетки и верхнего этажа брюшной полости приводят к более выраженной и длительной послеоперационной гипоксемии, чем вмешательства на нижнем этаже брюшной полости и на конечностях. Частота и степень десатурации напрямую зависят от дозы фентанила или концентрации фторотана, применявшихся при наркозе. К факторам риска также относятся пожилой возраст больного и наличие у него ожирения.
В ближайшем посленаркозном периоде, длительность которого составляет около 20 мин, выраженная гипоксемия
(Sp02 = 85-90 %) при дыхании атмосферным воздухом отмечается в среднем у 40-60 % пациентов, глубокая гипоксемия (SpO2 «85 %) - у 10-20 %, а в остальных случаях SpO2 редко превышает 94 %.
Основные причины гипоксемии на этом этапе: (1) центральная депрессия дыхания, обусловленная действием наркотических препаратов и гипервентиляцией во время наркоза; (2) остаточная миорелаксация; (3) нарушения проходимости верхних дыхательных путей; (4) множественные микроателектазы, факт появления которых у больных во время наркоза доказан, хотя их этиология до сих пор остается неясной,
