Страница:
При выраженном обострении банального хронического ларингита и его осложнениях пиогенного характера, а также для их профилактики применяют антибиотики из групп цефалоспоринов (цефтриоксон, терцеф, цефуроксим, суперо), макролидов (азитромицин, сумазид) и фторхинолинов (офлоксацин, ориферид).
В патогенезе хронического атрофического ларингита существенную роль играют локальная вторичная нутритивная недостаточность, гиповитаминоз и тканевая гипоксия. Для борьбы с этими факторами, усиливающими основной патологический процесс, рекомендуют витамины C, тиамин, рибофлавин, фолиевую, парааминобензойную, пантотеновую кислоты, витамины B1, B6, B и PP, глюкозу, АТФ, бромистый натрий с кофеином.
Хирургическое лечение некоторых форм хронического гиперпластического ларингита. К этому лечению прибегают в случаях, когда очевидна безрезультатность консервативного лечения и необходимо устранить препятствующее функциям гортани объемное образование, не подлежащее консервативному лечению (киста, папиллома, фиброма, пролапс гортанного желудочка и др.). Развитие эндоларингеальной хирургии началось после изобретения в 1854 г. М. Гарсией непрямой ларингоскопии, и уже к концу XIX в. было изобретено много хирургических инструментов для эндохирургического вмешательства на гортани (рис. 20.6).
Препятствием для развития эндохирургии гортани было неудобство, связанное с затеканием крови и слизи в трахею при попытках более радикального хирургического вмешательства. Применение отсоса несколько облегчало задачу хирурга, но не настолько, чтобы можно было оперировать в сухом поле. С изобретением в 1880 г. шотландским врачом Макъюином (Macewen W.) интубации трахеи для эндотрахеального введения наркотических газовых веществ развитие эндоларингеальной хирургии ускорилось. В XX в., в связи с развитием волоконной оптики и способа видеоэндоскопии, возник и достиг совершенства метод эндоларингеальной микрохирургии. Были разработаны и внедрены в практику оригинальные модели ларингоскопов (рис. 20.7) и самые разнообразные виды хирургического инструментария, позволяющие под большим увеличением с использованием операционного микроскопа проводить тончайшие хирургические операции практически при всех видах перечисленных гиперпластических процессов в гортани.
Приводим рекомендации по эндохирургии гортани одного из ведущих европейских специалистов в этой области Оскара Клейнзассера. Прежде всего автор советует оперировать двумя руками с использованием двух инструментов. В большинстве случаев применяют щипчики с ножницами (рис. 20.8, 1) или коагулятор с отсосом.
Щипчики предназначены только для фиксации удаляемого объекта и ни в коем случае не для срывания или скусывания ткани (рис. 20.8, 2, 3). «Стиппинг»[33], т. е. срывание полипа или сдирание отека Рейнке, является серьезной хирургической ошибкой, так как при этом может быть нанесена травма той ткани, которую необходимо сохранить, что впоследствии может привести к нарушению голоса и образованию нежелательных рубцов. Поэтому гладкое отсечение подлежащей удалению ткани с помощью острых ножниц или специального скальпеля должно стать неукоснительным правилом.
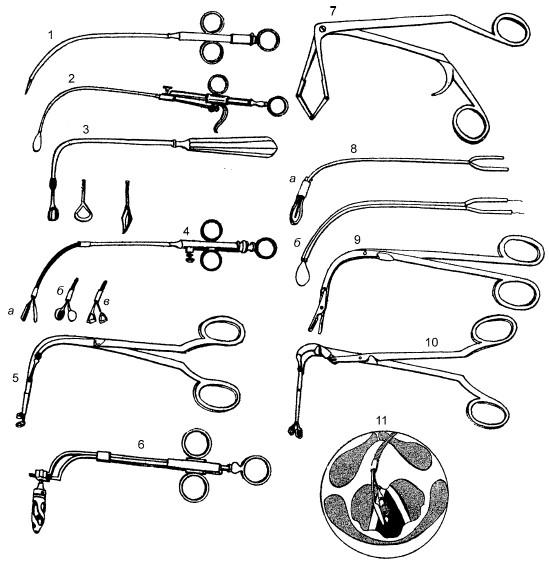
Рис. 20.6. Инструменты для эндоларингеальных операций, применявшиеся в XIX и XX вв. (по Escat E., 1908):
1 – гортанный скальпель с выдвигающимся лезвием; 2 – петля гортанная (полипотом); 3 – рукоятка-держатель и кюретки Геринга (Heryng), ромбовидная кюретка Люка (Luc); 4 – щипцы Морица Шмидта (Moritz Schmidt) со сменными наконечниками: а – щелевидный; б – ложковидный; в – стремевидный; 5 – щипцы гортанные боковые Маю (Mahu); 6 – гортанный вращающийся папиллотом Эска (Escat); 7 – гортанные шипцы Дюнда – Гранда (Dundas – Grand); 8 – гортанный электрокаутер с петлей накаливания: а – с протектором-проводником; б – без протектора-проводника; 9 – щипцы гортанные Рюолта (Ruault); 10 – щипцы гортанные вертикальные Маю (Mahu); 11 – схема операции удаления папилломы голосовой складки щипцами Морица Шмидта
Для соблюдения щадящего принципа, основного для эндоларингеальной микрохирургии, особенно на голосовых складках, О. Клейнзассер рекомендует начинающим хирургам отчетливо представлять тонкие анатомические структуры гортани и детально изучать основные патологоанатомические изменения для их дифференцирования от здоровых тканей, подлежащих сохранению. При вмешательстве на голосовой складке необходимо учитывать тот факт, что плоский эпителий лежит нефиксированным с подлежащим субстратом только над телом голосовой складки; в остальной части он прикреплен сверху и снизу к неровным поверхностям, дорсально – к голосовому отростку черпаловидного хряща, вентрально – к передней комиссуре. Следует также учитывать и строение пространства Рейнке (см. ранее). Поэтому дефекты эпителия голосовой складки, образующиеся после удаления полипов, узелков и варикозных образований, должны быть как можно меньшими, чтобы они быстро покрывались новым эпителием и пространство Рейнке вновь закрылось. При удалении небольших патологических образований, например полипов, узелков и прилипающих к эпителию небольших кист, их не следует захватывать у самого основания, а фиксировать щипчиками у края складки слизистой оболочки, подтягивать к середине голосовой щели и срезать у самого их основания (рис. 20.8, 4).

Рис. 20.7. Разновидности современных ларингофарингоскопов (по Берси и Уорду): 1 – оптика вертикального видения под углом 90°, длина тубуса 20 см, стержень инструмента овальный (10×8,5 мм), полезная длина 14 см со встроенным стекловолоконным световодом и каналом для воздухообдува против запотевания оптики; 2 – тот же ларингофарингоскоп по Берси и Уорду с предохранительным стержнем по Клейнзассеру, сменный с возможностью стерилизации; надвигается на овальный стержень; 3 – оптика вертикального видения (90°, 19 см) при 4-кратном увеличении с фокусирующим устройством: стержень инструмента D = 11 мм, полезная длина L = 14 см со встроенным стекловолоконным световодом и каналом для обдува оптики; 4 – волоконно-оптический риноларингоскоп: угол зрения 0°, угловая апертура 70°, полезная длина 25 см, наружный диаметр 3,5 мм
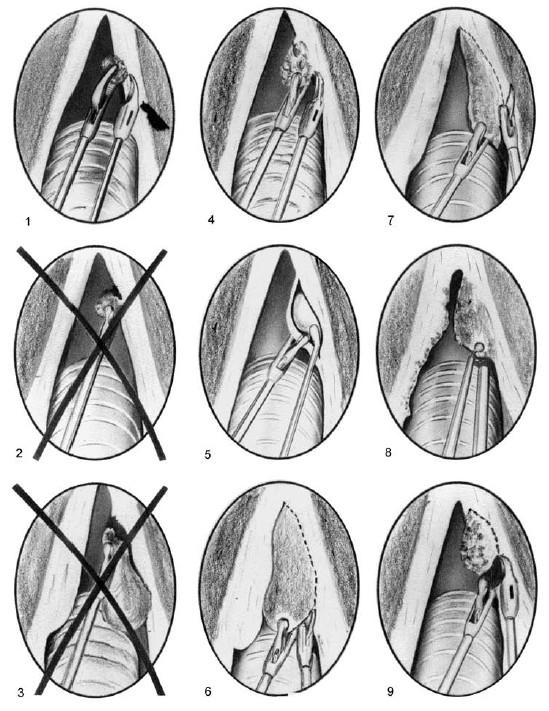
Рис. 20.8. Схематическое изображение некоторых микрохирургических приемов при эндоларингеальных вмешательствах (по О. Клейнзассеру). Объяснения в тексте
Большие кисты, располагающиеся на голосовой складке, после продольного рассечения покрывающей их слизистой оболочки без повреждения стенки кисты тщательно вылущивают миниатюрной ложечкой целиком с капсулой (рис. 20.8, 5).
При отеках Рейнке отсасывание слизи, кюретаж и резекция остатков слизистой оболочки в большинстве случаев не приводят к желаемому результату. О. Клейнзассер предостерегает от часто рекомендуемого способа «стриппинга», при котором полосу эпителия просто срывают с голосовой складки. При этой патологии автор рекомендует сначала ровно надрезать ножницами ткань вокруг удаляемой полосы эпителия (рис 20.8, 6), и только после этого удаляемый «препарат» с держащейся на нем вязкой отечной жидкостью может быть «стянут» целиком, без повреждения подлежащих тканей. Оставшийся на голосовой складке желеобразный секрет удаляется при помощи отсоса. При большом отеке Рейнке во избежание чрезмерного нарушения голосовой функции рекомендуют трехэтапное вмешательство: при первой операции лишь частично удалять патологическую ткань, а затем с интервалом в 5–6 недель завершить хирургическое лечение еще двумя аналогичными оперативными вмешательствами.
При далеко зашедшем хроническом гипертрофическом ларингите с утолщением голосовых складок целесообразно иссекать узкие полоски наиболее утолщенного эпителиального слоя и воспаленной подслизистой ткани с тем, чтобы в будущем представилась возможность ремоделировать форму голосовых складок за счет оставшегося эпителиального слоя (7).
При юношеских папилломах целесообразно применять метод их диатермокоагуляции с отсасыванием разрушенной папилломатозной ткани. Этот метод является наиболее быстрым, щадящим и почти бескровным, обеспечивая удовлетворительную функцию голосовых складок (8). Разрушение осуществляют прикосновением микрокоагулятора к наиболее выступающей части удаляемой ткани, при этом силу тока устанавливают на низком уровне, чтобы ткань при коагуляции не прожигалась, а становилась мягкой («вареной») и белой и легко удалялась без кровотечения с помощью отсоса. Такая методика не позволяет воздействовать током на недопустимую глубину и обеспечивает коагуляцию только того слоя, который необходимо удалить. Из-за дозированного воздействия термической энергии не возникает большого послеоперационного отека голосовой складки и окружающих тканей.
При предраковых изменениях ткани и небольших карциномах в настоящее время проводят, как правило, эксцизионную биопсию, а не только получение маленьких биоптатов (рис. 20.8, 9): надрезают здоровый на вид эпителий пораженной части голосовой складки, отсепаровывают эту часть в пределах здоровой ткани до самого ее основания и удаляют целиком.
Кератозы, а также преинвазивные и микроинвазивные карциномы обычно удаляются без технических трудностей и без повреждения подслизистых структур голосовых складок. Но при прорастании опухоли вглубь голосовой мышцы следует резецировать и ее в пределах здоровых тканей.
Как отмечал О. Клейнзассер, эндоларингеальная хордэктомия в руководимой им клинике Марбургского университета осуществляется в тех случаях, когда опухолью поражен только поверхностный мышечный слой. При более значительном поражении голосовой складки автор рекомендует проводить операцию наружным доступом, что обеспечивает хороший обзор и одномоментное восстановление голосовой складки и тем самым позволяет сохранить голосовую функцию.
На рис. 17 (см. цветную вклейку) представлены примеры манипуляций при микрохирургии гортани. В последнее десятилетие значительные успехи достигнуты в лазерной микрохирургии гортани (М. С. Плужников, W. J. Steiner, A. Werner и др.) с применением СО2 – лазера. На рис. 18 (см. цветную вклейку) представлен пример применения лазерной микрохирургии при удалении ангиоматозного полипа левой голосовой складки.
Хронические специфические ларингиты
Туберкулез гортани
В патогенезе хронического атрофического ларингита существенную роль играют локальная вторичная нутритивная недостаточность, гиповитаминоз и тканевая гипоксия. Для борьбы с этими факторами, усиливающими основной патологический процесс, рекомендуют витамины C, тиамин, рибофлавин, фолиевую, парааминобензойную, пантотеновую кислоты, витамины B1, B6, B и PP, глюкозу, АТФ, бромистый натрий с кофеином.
Хирургическое лечение некоторых форм хронического гиперпластического ларингита. К этому лечению прибегают в случаях, когда очевидна безрезультатность консервативного лечения и необходимо устранить препятствующее функциям гортани объемное образование, не подлежащее консервативному лечению (киста, папиллома, фиброма, пролапс гортанного желудочка и др.). Развитие эндоларингеальной хирургии началось после изобретения в 1854 г. М. Гарсией непрямой ларингоскопии, и уже к концу XIX в. было изобретено много хирургических инструментов для эндохирургического вмешательства на гортани (рис. 20.6).
Препятствием для развития эндохирургии гортани было неудобство, связанное с затеканием крови и слизи в трахею при попытках более радикального хирургического вмешательства. Применение отсоса несколько облегчало задачу хирурга, но не настолько, чтобы можно было оперировать в сухом поле. С изобретением в 1880 г. шотландским врачом Макъюином (Macewen W.) интубации трахеи для эндотрахеального введения наркотических газовых веществ развитие эндоларингеальной хирургии ускорилось. В XX в., в связи с развитием волоконной оптики и способа видеоэндоскопии, возник и достиг совершенства метод эндоларингеальной микрохирургии. Были разработаны и внедрены в практику оригинальные модели ларингоскопов (рис. 20.7) и самые разнообразные виды хирургического инструментария, позволяющие под большим увеличением с использованием операционного микроскопа проводить тончайшие хирургические операции практически при всех видах перечисленных гиперпластических процессов в гортани.
Приводим рекомендации по эндохирургии гортани одного из ведущих европейских специалистов в этой области Оскара Клейнзассера. Прежде всего автор советует оперировать двумя руками с использованием двух инструментов. В большинстве случаев применяют щипчики с ножницами (рис. 20.8, 1) или коагулятор с отсосом.
Щипчики предназначены только для фиксации удаляемого объекта и ни в коем случае не для срывания или скусывания ткани (рис. 20.8, 2, 3). «Стиппинг»[33], т. е. срывание полипа или сдирание отека Рейнке, является серьезной хирургической ошибкой, так как при этом может быть нанесена травма той ткани, которую необходимо сохранить, что впоследствии может привести к нарушению голоса и образованию нежелательных рубцов. Поэтому гладкое отсечение подлежащей удалению ткани с помощью острых ножниц или специального скальпеля должно стать неукоснительным правилом.

Рис. 20.6. Инструменты для эндоларингеальных операций, применявшиеся в XIX и XX вв. (по Escat E., 1908):
1 – гортанный скальпель с выдвигающимся лезвием; 2 – петля гортанная (полипотом); 3 – рукоятка-держатель и кюретки Геринга (Heryng), ромбовидная кюретка Люка (Luc); 4 – щипцы Морица Шмидта (Moritz Schmidt) со сменными наконечниками: а – щелевидный; б – ложковидный; в – стремевидный; 5 – щипцы гортанные боковые Маю (Mahu); 6 – гортанный вращающийся папиллотом Эска (Escat); 7 – гортанные шипцы Дюнда – Гранда (Dundas – Grand); 8 – гортанный электрокаутер с петлей накаливания: а – с протектором-проводником; б – без протектора-проводника; 9 – щипцы гортанные Рюолта (Ruault); 10 – щипцы гортанные вертикальные Маю (Mahu); 11 – схема операции удаления папилломы голосовой складки щипцами Морица Шмидта
Для соблюдения щадящего принципа, основного для эндоларингеальной микрохирургии, особенно на голосовых складках, О. Клейнзассер рекомендует начинающим хирургам отчетливо представлять тонкие анатомические структуры гортани и детально изучать основные патологоанатомические изменения для их дифференцирования от здоровых тканей, подлежащих сохранению. При вмешательстве на голосовой складке необходимо учитывать тот факт, что плоский эпителий лежит нефиксированным с подлежащим субстратом только над телом голосовой складки; в остальной части он прикреплен сверху и снизу к неровным поверхностям, дорсально – к голосовому отростку черпаловидного хряща, вентрально – к передней комиссуре. Следует также учитывать и строение пространства Рейнке (см. ранее). Поэтому дефекты эпителия голосовой складки, образующиеся после удаления полипов, узелков и варикозных образований, должны быть как можно меньшими, чтобы они быстро покрывались новым эпителием и пространство Рейнке вновь закрылось. При удалении небольших патологических образований, например полипов, узелков и прилипающих к эпителию небольших кист, их не следует захватывать у самого основания, а фиксировать щипчиками у края складки слизистой оболочки, подтягивать к середине голосовой щели и срезать у самого их основания (рис. 20.8, 4).

Рис. 20.7. Разновидности современных ларингофарингоскопов (по Берси и Уорду): 1 – оптика вертикального видения под углом 90°, длина тубуса 20 см, стержень инструмента овальный (10×8,5 мм), полезная длина 14 см со встроенным стекловолоконным световодом и каналом для воздухообдува против запотевания оптики; 2 – тот же ларингофарингоскоп по Берси и Уорду с предохранительным стержнем по Клейнзассеру, сменный с возможностью стерилизации; надвигается на овальный стержень; 3 – оптика вертикального видения (90°, 19 см) при 4-кратном увеличении с фокусирующим устройством: стержень инструмента D = 11 мм, полезная длина L = 14 см со встроенным стекловолоконным световодом и каналом для обдува оптики; 4 – волоконно-оптический риноларингоскоп: угол зрения 0°, угловая апертура 70°, полезная длина 25 см, наружный диаметр 3,5 мм

Рис. 20.8. Схематическое изображение некоторых микрохирургических приемов при эндоларингеальных вмешательствах (по О. Клейнзассеру). Объяснения в тексте
Большие кисты, располагающиеся на голосовой складке, после продольного рассечения покрывающей их слизистой оболочки без повреждения стенки кисты тщательно вылущивают миниатюрной ложечкой целиком с капсулой (рис. 20.8, 5).
При отеках Рейнке отсасывание слизи, кюретаж и резекция остатков слизистой оболочки в большинстве случаев не приводят к желаемому результату. О. Клейнзассер предостерегает от часто рекомендуемого способа «стриппинга», при котором полосу эпителия просто срывают с голосовой складки. При этой патологии автор рекомендует сначала ровно надрезать ножницами ткань вокруг удаляемой полосы эпителия (рис 20.8, 6), и только после этого удаляемый «препарат» с держащейся на нем вязкой отечной жидкостью может быть «стянут» целиком, без повреждения подлежащих тканей. Оставшийся на голосовой складке желеобразный секрет удаляется при помощи отсоса. При большом отеке Рейнке во избежание чрезмерного нарушения голосовой функции рекомендуют трехэтапное вмешательство: при первой операции лишь частично удалять патологическую ткань, а затем с интервалом в 5–6 недель завершить хирургическое лечение еще двумя аналогичными оперативными вмешательствами.
При далеко зашедшем хроническом гипертрофическом ларингите с утолщением голосовых складок целесообразно иссекать узкие полоски наиболее утолщенного эпителиального слоя и воспаленной подслизистой ткани с тем, чтобы в будущем представилась возможность ремоделировать форму голосовых складок за счет оставшегося эпителиального слоя (7).
При юношеских папилломах целесообразно применять метод их диатермокоагуляции с отсасыванием разрушенной папилломатозной ткани. Этот метод является наиболее быстрым, щадящим и почти бескровным, обеспечивая удовлетворительную функцию голосовых складок (8). Разрушение осуществляют прикосновением микрокоагулятора к наиболее выступающей части удаляемой ткани, при этом силу тока устанавливают на низком уровне, чтобы ткань при коагуляции не прожигалась, а становилась мягкой («вареной») и белой и легко удалялась без кровотечения с помощью отсоса. Такая методика не позволяет воздействовать током на недопустимую глубину и обеспечивает коагуляцию только того слоя, который необходимо удалить. Из-за дозированного воздействия термической энергии не возникает большого послеоперационного отека голосовой складки и окружающих тканей.
При предраковых изменениях ткани и небольших карциномах в настоящее время проводят, как правило, эксцизионную биопсию, а не только получение маленьких биоптатов (рис. 20.8, 9): надрезают здоровый на вид эпителий пораженной части голосовой складки, отсепаровывают эту часть в пределах здоровой ткани до самого ее основания и удаляют целиком.
Кератозы, а также преинвазивные и микроинвазивные карциномы обычно удаляются без технических трудностей и без повреждения подслизистых структур голосовых складок. Но при прорастании опухоли вглубь голосовой мышцы следует резецировать и ее в пределах здоровых тканей.
Как отмечал О. Клейнзассер, эндоларингеальная хордэктомия в руководимой им клинике Марбургского университета осуществляется в тех случаях, когда опухолью поражен только поверхностный мышечный слой. При более значительном поражении голосовой складки автор рекомендует проводить операцию наружным доступом, что обеспечивает хороший обзор и одномоментное восстановление голосовой складки и тем самым позволяет сохранить голосовую функцию.
На рис. 17 (см. цветную вклейку) представлены примеры манипуляций при микрохирургии гортани. В последнее десятилетие значительные успехи достигнуты в лазерной микрохирургии гортани (М. С. Плужников, W. J. Steiner, A. Werner и др.) с применением СО2 – лазера. На рис. 18 (см. цветную вклейку) представлен пример применения лазерной микрохирургии при удалении ангиоматозного полипа левой голосовой складки.
Хронические специфические ларингиты
Туберкулез гортани
История. Туберкулез известен с глубокой древности. По литературным данным (Эйнис В. Л., 1959), патологические изменения костей позвоночника, характерные для туберкулезного поражения, были обнаружены на скелете при раскопках под Гейдельбергом; возраст находки относят к раннему периоду каменного века (5000 лет до н. э.). Среди десяти скелетов египетских мумий, отнесенных к 2700 г. до н. э., у четырех был найден кариес позвоночника. По мнению В. Л. Эйниса, легочный туберкулез не был обнаружен при раскопках потому, что в древности при захоронении внутренности, за исключением сердца, хоронились отдельно. Первые убедительные описания проявлений легочной чахотки имеются у древних народов восточных стран. В древней Греции врачеватели были знакомы с проявлениями туберкулеза, а Изократ (390 г. до н. э.) уже говорит о заразности этого заболевания. В древнем Риме (I–II в. н. э.) Аретей, Гален и другие дают достаточно полные описания признаков легочного туберкулеза, которые господствовали на протяжении многих последующих веков. Эти сведения мы находим в трудах Авиценны, Сильвия, Фракастро и других выдающихся врачей Средневековья. В русских лечебниках второй половины XVII в. туберкулез именовали «болезнь сухотная» и «скорбь чахотная». Существенные достижения в учении о туберкулезе отмечены в XVIII–XIX вв. в области патологической анатомии этого заболевания, (G. L. Bayle, R. T. H. Laennec, S. F. Broussais, K. Rokitansky, W. Addison, J. Cohnheim), когда были открыты его основные патоморфологические проявления. Однако, хотя уже была доказана заразность заболевания, все еще оставался неизвестным его возбудитель. В 1882 г. выдающийся немецкий бактериолог, один из основоположников современной микробиологии Роберт Кох [R. Koch (18431910)] сообщил об открытии им возбудителя туберкулеза. В его докладе в Берлинском физиологическом обществе были подробно охарактеризованы морфология туберкулезных палочек, способы их обнаружения и свойства.[34] В России к середине XIX в. Н. И. Пирогов описал генерализованные формы, острый милиарный туберкулез, туберкулез легких, костей и суставов.
Этапом огромной важности явилось открытие французским ученым Гереном (C. Guerin) в 1921–1926 гг. противотуберкулезной профилактической вакцинации введением ослабленной культуры микобактерий туберкулеза бычьего типа (вакцина BCG). Большую роль в диагностике туберкулеза сыграли труды австрийского патолога и педиатра К. Пирке (Pirquet von C., 1874–1929), открывшего в 1907 г. диагностическую кожную пробу на туберкулез (туберкулинодиагностика). Перечисленные труды, наряду с открытием в 1895 г. Х-лучей великим немецким физиком В. К. Рентгеном (Rontgen W. K., 1845–1923), дали возможность клинически дифференцировать изменения в органах и прежде всего в легких, пищеварительном тракте и костях. Однако успехи в диагностике и других областях проблемы туберкулеза в течение всего XIX в. тормозились отсутствием этиологического лечения. В течение XIX в. врач располагал главным образом гигиено-диетическими методами лечения туберкулезной инфекции. Принципы санаторно-курортного лечения разрабатывались за рубежом (H. Brehmer) и в России (В. А. Манассеин, Г. А. Захарьин, В. А. Воробьев и др.).
Основой в новейшем направлении антибиотической терапии туберкулеза стали теоретические соображения И. И. Мечникова об антагонизме микробов. В 1943–1944 гг. С. Ваксман, А. Шац и Е. Бьюжи (S. A. Vaksman, A. Schatz, E. Bugie) открыли стрептомицин – мощный противотуберкулезный антибиотик. В дальнейшем были синтезированы такие химиотерапевтические противотуберкулезные препараты, как ПАСК, изониазид, фтивазид и др. Развивалось также и хирургическое направление в лечении туберкулеза (Ф. Р. Киевский, П. И. Дьяконов, А. Н. Бакулев, П. А. Куприянов, L. Brauer, M. Vilms и др.).
Возбудитель туберкулеза относится к обширной группе микобактерий, родственных низшим растительным организмам – лучистым грибкам, или актиномицетам. VI Всесоюзный съезд фтизиатров (1957) рекомендовал придерживаться следующей терминологии: микобактерия туберкулеза, или туберкулезные палочки (БК – бактерии Коха).
Источники заражения. Главным из них является больной человек, все его выделения могут служить источником заражения. Наибольшее значение имеет мокрота больного туберкулезом легких и ВДП, высохшая в пыль и распространяющаяся в атмосфере (теория Коха – Корнета). По Флюгге, главным источником заражения является воздушно-капельная инфекция, распространяющаяся при кашле, разговоре, чихании. Источником заражения может быть рогатый скот: инфекция передается через молоко больных туберкулезом животных.
Входными воротами инфекции у человека могут быть кожа, слизистые оболочки и альвеолярный легочный эпителий. Местом вхождения БК может быть лимфаденоидная ткань глотки, конъюнктива глаз, слизистой оболочки половых органов. Туберкулезная инфекция распространяется лимфогенным и гематогенным путем, а также per continuitatem.
Лекарственная устойчивость микобактерий туберкулеза обусловлена широким применением химиотерапевтических препаратов. Уже в 1961 г. 60 % штаммов БК были устойчивы к стрептомицину, 66 % – к фтивазиду, 32 % – к ПАСК.
Возникновение устойчивых форм бактерии Коха обусловлено более или менее продолжительным воздействием на них суббактериостатических доз препарата. В настоящее время устойчивость БК к специфическим препаратам существенно снижается благодаря комбинированному применению их с синтетическими противотуберкулезными лекарственными средствами, иммуномодуляторами, витаминотерапией и рационально подобранными пищевыми добавками.
Патогенез туберкулезной инфекции сложен и зависит от многообразия условий, в которых взаимодействуют возбудитель и организм. Инфицирование далеко не всегда сопровождается развитием туберкулезного процесса. В. А. Манассеин[35] в патогенезе туберкулеза придавал большое значение общей сопротивляемости организма. Это положение привлекло внимание фтизиатров к изучению реактивности организма, аллергии и иммунитета, что углубило познания о туберкулезе и позволило утверждать, что, казалось бы, ранее смертельное заболевание излечимо. Ведущую роль в возникновении туберкулеза играют неблагоприятные условия жизни и снижение сопротивляемости организма. Имеются данные о наследственной предрасположенности к заболеванию.
В развитии туберкулеза выделяют первичный и вторичный периоды. Для первичного туберкулеза характерна высокая чувствительность тканей к микобактериям и их токсинам. В этот период в месте внедрения инфекции может возникнуть первичный очаг (первичный аффект), в ответ на который в связи с сенсибилизацией организма развивается специфический процесс по ходу лимфатических сосудов и в лимфоузлах с образованием первичного комплекса, чаще в легких и внутригрудных лимфоузлах. В процессе формирования очагов первичного туберкулеза наблюдается бактериемия, что может вести к лимфогенной и гематогенной диссеминации с образованием туберкулезных очагов в различных органах – легких, ВДП, костях, почках и др. Бактериемия приводит к возрастанию иммунной активности организма.
По современным представлениям, иммунитет при туберкулезе зависит от наличия в организме живых микобактерий, а также от функций иммунокомпетентных клеток; клеточный иммунитет выступает ведущим звеном в формировании сопротивляемости к туберкулезной инфекции.
Классификация. В соответствии с клинической классификацией, принятой в нашей стране, выделяют: туберкулезную интоксикацию у детей и подростков, туберкулез органов дыхания, туберкулез других органов и систем (внелегочный туберкулез). К туберкулезу органов дыхания, помимо туберкулеза легких, относят туберкулез гортани, трахеи и бронхов, которые будут нами рассмотрены далее.
Особенности клинических проявлений. Синдром общей интоксикации может быть разной степени выраженности. В его основе лежит размножение бактерий, их диссеминация и действие туберкулезного токсина. По выраженности локальных изменений можно выделить ограниченные очаги (малые формы) поражений, распространенные изменения без деструкции, в том числе с поражением нескольких органов, прогрессирующий деструктивный процесс. Ранее часто встречались такие формы, как туберкулезная казеозная пневмония, милиарный туберкулез и туберкулезный менингит, а также генерализованные формы с множественным поражением различных органов. И хотя сейчас эти формы туберкулеза встречаются значительно реже, проблема первичного и вторичного туберкулеза остается актуальной, особенно для закрытых коллективов.
Вторичный туберкулез протекает длительно, волнообразно, со сменой периодов обострения и затихания. Локальные проявления первичного туберкулеза (туберкулез гортани, бронхов, глотки и других ЛОР-органов) выявляются в основном у невакцинированных детей, у детей и подростков с явлениями иммунодепрессивных и иммунодефицитных состояний[36]. У лиц пожилого и старческого возраста симптомы туберкулеза наблюдаются на фоне возрастных изменений в различных органах и системах (в первую очередь в ВДП и бронхолегочной системе), а также сопутствующих заболеваний.
Отрицательно влияют на клиническое течение туберкулеза беременность, особенно ранняя, и послеродовый период. Однако у матерей, больных туберкулезом, рождаются полноценные, практически здоровые дети. Они, как правило, не инфицированы и их необходимо вакцинировать БЦЖ.
В нашей стране в начале XXI в. актуальность туберкулезной инфекции значительно возросла, инфицирование резко увеличивается, и, по опубликованным данным, ежегодно от этой инфекции в России погибает около 30 тыс. человек.
Этиопатогенез туберкулеза гортани. Первичный туберкулез гортани встречается редко, чаще это вторичный процесс при первичной локализации инфекции в легких с поражением внутригрудных лимфоузлов. Нередко туберкулезу гортани сопутствует туберкулез трахеи и бронхов, туберкулезный плеврит и туберкулез другой локализации (носа, глотки, небных миндалин, костная, суставная, кожная формы туберкулеза). Вторичный туберкулез гортани, наряду с туберкулезом трахеи и бронхов, является самым частым и грозным осложнением туберкулеза легких. Частота возникновения туберкулеза гортани и тяжесть клинического течения находятся в прямой зависимости от длительности и формы заболевания. По Рюеди (A. Ruedi), туберкулез гортани встречается у 10 % больных начальной формой туберкулеза легких, у 30 % лиц с длительным течением процесса и в 70 % – на аутопсии умерших от туберкулеза легких. Туберкулез гортани чаще встречается у больных с экссудативными, открытыми и активными формами туберкулеза легких и реже – при продуктивных формах.
Иногда при первичном туберкулезе легких или при застарелых инактивных, ранее не распознанных очагах первыми признаками общей туберкулезной инфекции могут явиться симптомы поражения гортани, что дает повод к соответствующему обследованию больного и выявлению или первичного очага, или активизации дремлющей туберкулезной инфекции. Значительно чаще болеют мужчины в возрасте 20–40 лет. У женщин туберкулез гортани встречается чаще во время беременности или спустя короткое время после родов. Дети болеют реже, а в возрасте менее 10 лет – очень редко.
Обычно в клиническом течении между туберкулезом гортани и легких существует определенный параллелизм, который проявляется одними и теми же экссудативными или продуктивными явлениями. Однако в ряде случаев такой параллелизм не наблюдается: либо обостряется туберкулез гортани и редуцируется туберкулез легких, либо наоборот. У многих больных нет соответствия между количеством инфицированной мокроты, выделяемой из легочного очага, и частотой или формой туберкулезного поражения гортани. Это свидетельствует о наличии либо отсутствии индивидуальной предрасположенности больного туберкулезом легких к заболеванию туберкулезом гортани. Вероятно, речь идет о качестве так называемого местного иммунитета, либо находящегося в активном состоянии, либо подавленного внешними вредными факторами. Например, доказано, что туберкулезом легких, вторичным и первичным туберкулезом гортани болеют преимущественно курильщики, алкоголики и лица, профессии которых связаны с наличием во вдыхаемом воздухе вредных агентов, снижающих сопротивляемость инфекции слизистой оболочки ВДП и легких.
Инфицирование гортани происходит или канальным путем, при котором инфекция проникает в слизистые из выделяемой из легочного очага мокроты, или, что значительно чаще, – гематогенным путем. Гематогенная диссеминация наблюдается при закрытых и милиарных формах туберкулеза. Наличие банальных ларингитов способствует внедрению БК в слизистую оболочку гортани. Поражения гортани чаще всего находятся на той же стороне, что и первичный очаг в легких. Это объясняется тем, что инфицирование гортани произошло лимфогенным путем из лимфатических узлов трахеи и бронхов одноименной стороны. Другое объяснение гомолатерального поражения гортани заключается в действии мерцательного эпителия, который доставляет инфекцию со своей стороны на ту же сторону в гортань. Это объяснение подтверждает канальный механизм локального гомолатерального поражения гортани либо в области «задней комиссуры», в межчерпаловидном пространстве или монолатерально, в то время как при гематогенном пути очаги туберкулезной инфекции могут возникать беспорядочно по всей поверхности гортани, захватывая и ее преддверие.
Этапом огромной важности явилось открытие французским ученым Гереном (C. Guerin) в 1921–1926 гг. противотуберкулезной профилактической вакцинации введением ослабленной культуры микобактерий туберкулеза бычьего типа (вакцина BCG). Большую роль в диагностике туберкулеза сыграли труды австрийского патолога и педиатра К. Пирке (Pirquet von C., 1874–1929), открывшего в 1907 г. диагностическую кожную пробу на туберкулез (туберкулинодиагностика). Перечисленные труды, наряду с открытием в 1895 г. Х-лучей великим немецким физиком В. К. Рентгеном (Rontgen W. K., 1845–1923), дали возможность клинически дифференцировать изменения в органах и прежде всего в легких, пищеварительном тракте и костях. Однако успехи в диагностике и других областях проблемы туберкулеза в течение всего XIX в. тормозились отсутствием этиологического лечения. В течение XIX в. врач располагал главным образом гигиено-диетическими методами лечения туберкулезной инфекции. Принципы санаторно-курортного лечения разрабатывались за рубежом (H. Brehmer) и в России (В. А. Манассеин, Г. А. Захарьин, В. А. Воробьев и др.).
Основой в новейшем направлении антибиотической терапии туберкулеза стали теоретические соображения И. И. Мечникова об антагонизме микробов. В 1943–1944 гг. С. Ваксман, А. Шац и Е. Бьюжи (S. A. Vaksman, A. Schatz, E. Bugie) открыли стрептомицин – мощный противотуберкулезный антибиотик. В дальнейшем были синтезированы такие химиотерапевтические противотуберкулезные препараты, как ПАСК, изониазид, фтивазид и др. Развивалось также и хирургическое направление в лечении туберкулеза (Ф. Р. Киевский, П. И. Дьяконов, А. Н. Бакулев, П. А. Куприянов, L. Brauer, M. Vilms и др.).
Возбудитель туберкулеза относится к обширной группе микобактерий, родственных низшим растительным организмам – лучистым грибкам, или актиномицетам. VI Всесоюзный съезд фтизиатров (1957) рекомендовал придерживаться следующей терминологии: микобактерия туберкулеза, или туберкулезные палочки (БК – бактерии Коха).
Источники заражения. Главным из них является больной человек, все его выделения могут служить источником заражения. Наибольшее значение имеет мокрота больного туберкулезом легких и ВДП, высохшая в пыль и распространяющаяся в атмосфере (теория Коха – Корнета). По Флюгге, главным источником заражения является воздушно-капельная инфекция, распространяющаяся при кашле, разговоре, чихании. Источником заражения может быть рогатый скот: инфекция передается через молоко больных туберкулезом животных.
Входными воротами инфекции у человека могут быть кожа, слизистые оболочки и альвеолярный легочный эпителий. Местом вхождения БК может быть лимфаденоидная ткань глотки, конъюнктива глаз, слизистой оболочки половых органов. Туберкулезная инфекция распространяется лимфогенным и гематогенным путем, а также per continuitatem.
Лекарственная устойчивость микобактерий туберкулеза обусловлена широким применением химиотерапевтических препаратов. Уже в 1961 г. 60 % штаммов БК были устойчивы к стрептомицину, 66 % – к фтивазиду, 32 % – к ПАСК.
Возникновение устойчивых форм бактерии Коха обусловлено более или менее продолжительным воздействием на них суббактериостатических доз препарата. В настоящее время устойчивость БК к специфическим препаратам существенно снижается благодаря комбинированному применению их с синтетическими противотуберкулезными лекарственными средствами, иммуномодуляторами, витаминотерапией и рационально подобранными пищевыми добавками.
Патогенез туберкулезной инфекции сложен и зависит от многообразия условий, в которых взаимодействуют возбудитель и организм. Инфицирование далеко не всегда сопровождается развитием туберкулезного процесса. В. А. Манассеин[35] в патогенезе туберкулеза придавал большое значение общей сопротивляемости организма. Это положение привлекло внимание фтизиатров к изучению реактивности организма, аллергии и иммунитета, что углубило познания о туберкулезе и позволило утверждать, что, казалось бы, ранее смертельное заболевание излечимо. Ведущую роль в возникновении туберкулеза играют неблагоприятные условия жизни и снижение сопротивляемости организма. Имеются данные о наследственной предрасположенности к заболеванию.
В развитии туберкулеза выделяют первичный и вторичный периоды. Для первичного туберкулеза характерна высокая чувствительность тканей к микобактериям и их токсинам. В этот период в месте внедрения инфекции может возникнуть первичный очаг (первичный аффект), в ответ на который в связи с сенсибилизацией организма развивается специфический процесс по ходу лимфатических сосудов и в лимфоузлах с образованием первичного комплекса, чаще в легких и внутригрудных лимфоузлах. В процессе формирования очагов первичного туберкулеза наблюдается бактериемия, что может вести к лимфогенной и гематогенной диссеминации с образованием туберкулезных очагов в различных органах – легких, ВДП, костях, почках и др. Бактериемия приводит к возрастанию иммунной активности организма.
По современным представлениям, иммунитет при туберкулезе зависит от наличия в организме живых микобактерий, а также от функций иммунокомпетентных клеток; клеточный иммунитет выступает ведущим звеном в формировании сопротивляемости к туберкулезной инфекции.
Классификация. В соответствии с клинической классификацией, принятой в нашей стране, выделяют: туберкулезную интоксикацию у детей и подростков, туберкулез органов дыхания, туберкулез других органов и систем (внелегочный туберкулез). К туберкулезу органов дыхания, помимо туберкулеза легких, относят туберкулез гортани, трахеи и бронхов, которые будут нами рассмотрены далее.
Особенности клинических проявлений. Синдром общей интоксикации может быть разной степени выраженности. В его основе лежит размножение бактерий, их диссеминация и действие туберкулезного токсина. По выраженности локальных изменений можно выделить ограниченные очаги (малые формы) поражений, распространенные изменения без деструкции, в том числе с поражением нескольких органов, прогрессирующий деструктивный процесс. Ранее часто встречались такие формы, как туберкулезная казеозная пневмония, милиарный туберкулез и туберкулезный менингит, а также генерализованные формы с множественным поражением различных органов. И хотя сейчас эти формы туберкулеза встречаются значительно реже, проблема первичного и вторичного туберкулеза остается актуальной, особенно для закрытых коллективов.
Вторичный туберкулез протекает длительно, волнообразно, со сменой периодов обострения и затихания. Локальные проявления первичного туберкулеза (туберкулез гортани, бронхов, глотки и других ЛОР-органов) выявляются в основном у невакцинированных детей, у детей и подростков с явлениями иммунодепрессивных и иммунодефицитных состояний[36]. У лиц пожилого и старческого возраста симптомы туберкулеза наблюдаются на фоне возрастных изменений в различных органах и системах (в первую очередь в ВДП и бронхолегочной системе), а также сопутствующих заболеваний.
Отрицательно влияют на клиническое течение туберкулеза беременность, особенно ранняя, и послеродовый период. Однако у матерей, больных туберкулезом, рождаются полноценные, практически здоровые дети. Они, как правило, не инфицированы и их необходимо вакцинировать БЦЖ.
В нашей стране в начале XXI в. актуальность туберкулезной инфекции значительно возросла, инфицирование резко увеличивается, и, по опубликованным данным, ежегодно от этой инфекции в России погибает около 30 тыс. человек.
Этиопатогенез туберкулеза гортани. Первичный туберкулез гортани встречается редко, чаще это вторичный процесс при первичной локализации инфекции в легких с поражением внутригрудных лимфоузлов. Нередко туберкулезу гортани сопутствует туберкулез трахеи и бронхов, туберкулезный плеврит и туберкулез другой локализации (носа, глотки, небных миндалин, костная, суставная, кожная формы туберкулеза). Вторичный туберкулез гортани, наряду с туберкулезом трахеи и бронхов, является самым частым и грозным осложнением туберкулеза легких. Частота возникновения туберкулеза гортани и тяжесть клинического течения находятся в прямой зависимости от длительности и формы заболевания. По Рюеди (A. Ruedi), туберкулез гортани встречается у 10 % больных начальной формой туберкулеза легких, у 30 % лиц с длительным течением процесса и в 70 % – на аутопсии умерших от туберкулеза легких. Туберкулез гортани чаще встречается у больных с экссудативными, открытыми и активными формами туберкулеза легких и реже – при продуктивных формах.
Иногда при первичном туберкулезе легких или при застарелых инактивных, ранее не распознанных очагах первыми признаками общей туберкулезной инфекции могут явиться симптомы поражения гортани, что дает повод к соответствующему обследованию больного и выявлению или первичного очага, или активизации дремлющей туберкулезной инфекции. Значительно чаще болеют мужчины в возрасте 20–40 лет. У женщин туберкулез гортани встречается чаще во время беременности или спустя короткое время после родов. Дети болеют реже, а в возрасте менее 10 лет – очень редко.
Обычно в клиническом течении между туберкулезом гортани и легких существует определенный параллелизм, который проявляется одними и теми же экссудативными или продуктивными явлениями. Однако в ряде случаев такой параллелизм не наблюдается: либо обостряется туберкулез гортани и редуцируется туберкулез легких, либо наоборот. У многих больных нет соответствия между количеством инфицированной мокроты, выделяемой из легочного очага, и частотой или формой туберкулезного поражения гортани. Это свидетельствует о наличии либо отсутствии индивидуальной предрасположенности больного туберкулезом легких к заболеванию туберкулезом гортани. Вероятно, речь идет о качестве так называемого местного иммунитета, либо находящегося в активном состоянии, либо подавленного внешними вредными факторами. Например, доказано, что туберкулезом легких, вторичным и первичным туберкулезом гортани болеют преимущественно курильщики, алкоголики и лица, профессии которых связаны с наличием во вдыхаемом воздухе вредных агентов, снижающих сопротивляемость инфекции слизистой оболочки ВДП и легких.
Инфицирование гортани происходит или канальным путем, при котором инфекция проникает в слизистые из выделяемой из легочного очага мокроты, или, что значительно чаще, – гематогенным путем. Гематогенная диссеминация наблюдается при закрытых и милиарных формах туберкулеза. Наличие банальных ларингитов способствует внедрению БК в слизистую оболочку гортани. Поражения гортани чаще всего находятся на той же стороне, что и первичный очаг в легких. Это объясняется тем, что инфицирование гортани произошло лимфогенным путем из лимфатических узлов трахеи и бронхов одноименной стороны. Другое объяснение гомолатерального поражения гортани заключается в действии мерцательного эпителия, который доставляет инфекцию со своей стороны на ту же сторону в гортань. Это объяснение подтверждает канальный механизм локального гомолатерального поражения гортани либо в области «задней комиссуры», в межчерпаловидном пространстве или монолатерально, в то время как при гематогенном пути очаги туберкулезной инфекции могут возникать беспорядочно по всей поверхности гортани, захватывая и ее преддверие.
