Страница:
Фосфора окислы
). Различают ортофосфорную кислоту (обычно называемую фосфорной кислотой) и конденсированные Ф. к. Наиболее изучена и важна ортофосфорная кислота H
3PO
4, образующаяся при растворении P
4O
10(или P
2O
5) в воде.">Фосфорные кислоты
)
;2) взаимодействие ортофосфорной кислоты с гидроокисями, аммиаком, хлоридами или карбонатами, например:
H 3PO 4+ MH 3= NH 4H 2PO 4
H 3PO 4+ KCl = KH 2PO 4– HCl
Труднорастворимые ортофосфаты тяжелых металлов (например, Ag, Cu) образуются в результате обменных реакций, например:
2Na 2HPO 4+ 3AgNO 3= Ag 3PO 4+ 3NaNO 3+ NaH 2PO 4
Полимерные Ф. различных структурных типов могут быть описаны формулами: линейные полифосфаты Me n + 2P n O 3 n+ 1, или
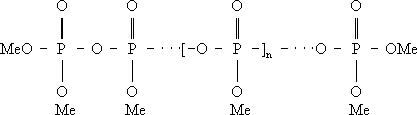
кольцевые метафосфаты Me n P n O 3 n, или
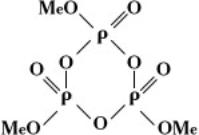
(где n– степень полимеризации).
Свойства полимерных Ф. зависят от характера катиона, строения фосфат-аниона, степени полимеризации, структуры фосфата и др. Так, например, растворимость линейных полифосфатов, как правило, падает с увеличением степени полимеризации, но может быть увеличена путём модифицирования полифосфатов, например изменением скорости охлаждения расплава.
Получают полимерные Ф. (линейные и кольцевые) в основном термической дегидратацией одно- и двухзамещённых ортофосфатов или нейтрализацией соответствующих поли- или мета- (циклических) фосфорных кислот:
H n + 2P n O 3 n+ 1+ nNH 3= (NH 4) n H 2P n O 3 n+ 1
(иногда эти процессы совмещаются, как, например, при высокотемпературной аммонизации ортофосфорной кислоты для получения полифосфатов аммония). В промышленных масштабах эти способы используют для получения пиро-, триполифосфатов натрия (соответственно Na 4P 2O 7, Na 5P 3O 10) и в меньшей степени – калия, а также полимерных метафосфатов (натрий-фосфатные стекла, метафосфат калия и др.).
Из циклических метафосфатов наиболее изучены тримета-, тетрамета-, гексамета- и октаметафосфаты.
Ультрафосфаты – соединения общей формулы Me nR P n O n (5 + R)/2, где R = Me 2O/P 2O 5, как правило, аморфные, стеклообразные вещества, гигроскопичные, легко гидролизующиеся на воздухе с образованием поли- и метафосфатов. Последние в присутствии большого количества воды могут гидролизоваться за счёт полного расщепления Р–О–Р-связей вплоть до ортофосфатов. Выделенные в кристаллическом виде ультрафосфаты кальция, магния, марганца и некоторых лантаноидов, как правило, не гигроскопичны. Ультрафосфаты образуются в результате термической дегидратации смеси ортофосфатов с фосфорными кислотами или с фосфорным ангидридом, т. е. при наличии условия
О < Me 2O/P 2O 5< 1.
Ф. кальция, аммония, калия и др. широко применяются в качестве фосфорных удобрений.В 70-е гг. 20 в. выросло производство кормовых фосфатов [например, обесфторенные Ф., преципитат,динатрийфосфат, фосфаты мочевины – H 3PO 4Ч(NH 2) 2CO и др.]. Ф. натрия и калия (особенно триполифосфаты) применяют в качестве компонентов жидких и порошкообразных моющих средств и поверхностно-активных веществ при буровых работах, в цементной, текстильной промышленности при подготовке шерсти, хлопка к белению и крашению. Ф. используют в пищевой промышленности в качестве рыхлителей теста, например (NH 4) 2HPO 4. Некотоpые Ф. (например, BPO 4) применяют в качестве катализаторов в реакциях органического синтеза. Ф. преимущественно щелочных металлов входят в состав эмалей, глазурей, стекол, огнестойких материалов (как антипирены ) ,а также мягких абразивов; они используются при фосфатировании металлов (Mg, Fe, Zn). Кристаллы однозамещённых фосфатов калия, аммония применяются как сегнетоэлектрики и пьезоэлектрические материалы.Ф. используются в фармацевтической промышленности при изготовлении лекарственных препаратов (например, фосфакол, АТФ – аденозинтрифосфат и др.), зубных паст и порошков.
Л. В. Кубасова.
Из эфиров фосфорных кислот наиболее известны одно-, двух- и трёхзамещённые ортофосфаты, соответственно ROP (O)(OH) 2, (RO) 2P (O) OH и (KO) 3PO (где R – алкил, арил или гетероциклический остаток). Получаются при взаимодействии POCl 3со спиртами:
POCl 3+ 3ROH ® (RO) 3PO
POCl 3+ 2ROH ® (RO) 2P (O) Cl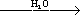 (RO)
2P (O) OH
(RO)
2P (O) OH
и др. способами.
Применяются как пестициды, присадкик маслам, экстрагенты и т.д. Некоторые органические Ф. ( нуклеиновые кислоты, аденозинфосфорные кислоты) выполняют важные функции в живых организмах.
Э. Е. Нифантьев.
Лит.:Продан Е. А., Продан Л. И., Ермоленко Н. Ф., Триполифосфаты и их применение, Минск, 1969; см. также лит. при ст. Фосфор .
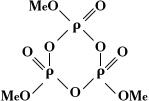 Фосфаты.
Фосфаты.
фосфорных кислот,см. в ст.
Фосфаты.
H 3PO 4+ MH 3= NH 4H 2PO 4
H 3PO 4+ KCl = KH 2PO 4– HCl
Труднорастворимые ортофосфаты тяжелых металлов (например, Ag, Cu) образуются в результате обменных реакций, например:
2Na 2HPO 4+ 3AgNO 3= Ag 3PO 4+ 3NaNO 3+ NaH 2PO 4
Полимерные Ф. различных структурных типов могут быть описаны формулами: линейные полифосфаты Me n + 2P n O 3 n+ 1, или
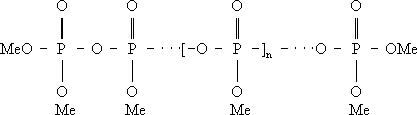
кольцевые метафосфаты Me n P n O 3 n, или

(где n– степень полимеризации).
Свойства полимерных Ф. зависят от характера катиона, строения фосфат-аниона, степени полимеризации, структуры фосфата и др. Так, например, растворимость линейных полифосфатов, как правило, падает с увеличением степени полимеризации, но может быть увеличена путём модифицирования полифосфатов, например изменением скорости охлаждения расплава.
Получают полимерные Ф. (линейные и кольцевые) в основном термической дегидратацией одно- и двухзамещённых ортофосфатов или нейтрализацией соответствующих поли- или мета- (циклических) фосфорных кислот:
H n + 2P n O 3 n+ 1+ nNH 3= (NH 4) n H 2P n O 3 n+ 1
(иногда эти процессы совмещаются, как, например, при высокотемпературной аммонизации ортофосфорной кислоты для получения полифосфатов аммония). В промышленных масштабах эти способы используют для получения пиро-, триполифосфатов натрия (соответственно Na 4P 2O 7, Na 5P 3O 10) и в меньшей степени – калия, а также полимерных метафосфатов (натрий-фосфатные стекла, метафосфат калия и др.).
Из циклических метафосфатов наиболее изучены тримета-, тетрамета-, гексамета- и октаметафосфаты.
Ультрафосфаты – соединения общей формулы Me nR P n O n (5 + R)/2, где R = Me 2O/P 2O 5, как правило, аморфные, стеклообразные вещества, гигроскопичные, легко гидролизующиеся на воздухе с образованием поли- и метафосфатов. Последние в присутствии большого количества воды могут гидролизоваться за счёт полного расщепления Р–О–Р-связей вплоть до ортофосфатов. Выделенные в кристаллическом виде ультрафосфаты кальция, магния, марганца и некоторых лантаноидов, как правило, не гигроскопичны. Ультрафосфаты образуются в результате термической дегидратации смеси ортофосфатов с фосфорными кислотами или с фосфорным ангидридом, т. е. при наличии условия
О < Me 2O/P 2O 5< 1.
Ф. кальция, аммония, калия и др. широко применяются в качестве фосфорных удобрений.В 70-е гг. 20 в. выросло производство кормовых фосфатов [например, обесфторенные Ф., преципитат,динатрийфосфат, фосфаты мочевины – H 3PO 4Ч(NH 2) 2CO и др.]. Ф. натрия и калия (особенно триполифосфаты) применяют в качестве компонентов жидких и порошкообразных моющих средств и поверхностно-активных веществ при буровых работах, в цементной, текстильной промышленности при подготовке шерсти, хлопка к белению и крашению. Ф. используют в пищевой промышленности в качестве рыхлителей теста, например (NH 4) 2HPO 4. Некотоpые Ф. (например, BPO 4) применяют в качестве катализаторов в реакциях органического синтеза. Ф. преимущественно щелочных металлов входят в состав эмалей, глазурей, стекол, огнестойких материалов (как антипирены ) ,а также мягких абразивов; они используются при фосфатировании металлов (Mg, Fe, Zn). Кристаллы однозамещённых фосфатов калия, аммония применяются как сегнетоэлектрики и пьезоэлектрические материалы.Ф. используются в фармацевтической промышленности при изготовлении лекарственных препаратов (например, фосфакол, АТФ – аденозинтрифосфат и др.), зубных паст и порошков.
Л. В. Кубасова.
Из эфиров фосфорных кислот наиболее известны одно-, двух- и трёхзамещённые ортофосфаты, соответственно ROP (O)(OH) 2, (RO) 2P (O) OH и (KO) 3PO (где R – алкил, арил или гетероциклический остаток). Получаются при взаимодействии POCl 3со спиртами:
POCl 3+ 3ROH ® (RO) 3PO
POCl 3+ 2ROH ® (RO) 2P (O) Cl
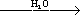 (RO)
2P (O) OH
(RO)
2P (O) OHи др. способами.
Применяются как пестициды, присадкик маслам, экстрагенты и т.д. Некоторые органические Ф. ( нуклеиновые кислоты, аденозинфосфорные кислоты) выполняют важные функции в живых организмах.
Э. Е. Нифантьев.
Лит.:Продан Е. А., Продан Л. И., Ермоленко Н. Ф., Триполифосфаты и их применение, Минск, 1969; см. также лит. при ст. Фосфор .

